Spis treści:
Ulotka dołączona do opakowania: informacja dla użytkownika
Biotum, 1 g, proszek do sporządzania roztworu do wstrzykiwań lub infuzji Biotum, 2 g, proszek do sporządzania roztworu do wstrzykiwań lub infuzji
Ceftazidimum
Należy uważnie zapoznać się z treścią ulotki przed zażyciem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać.
W razie jakichkolwiek wątpliwości należy zwrócić się do lekarza lub pielęgniarki.
Lek ten przepisano ściśle określonej osobie. Nie należy go przekazywać innym. Lek może zaszkodzić innej osobie, nawet jeśli objawy jej choroby są takie same.
Jeśli u pacjenta wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy
niepożądane niewymienione w tej ulotce, należy powiedzieć o tym lekarzowi lub pielęgniarce. Patrz punkt 4.
Spis treści ulotki
Co to jest lek Biotum i w jakim celu się go stosuje
dolnych dróg oddechowych, w tym płuc
płuc i oskrzeli u pacjentów z mukowiscydozą
mózgu (zapalenie opon mózgowo-rdzeniowych)
ucha
dróg moczowych
skóry i tkanek miękkich
jamy brzusznej i powłok brzusznych (zapalenie otrzewnej)
kości i stawów.
Biotum można również stosować:
w zapobieganiu zakażeniom podczas przezcewkowej resekcji gruczołu krokowego u mężczyzn
w leczeniu pacjentów z małą liczbą białych krwinek (neutropenia), mających gorączkę z powodu zakażenia bakteryjnego.
Biotum jest antybiotykiem stosowanym u dorosłych i dzieci (w tym u noworodków). Działa on bakteriobójczo na bakterie wywołujące zakażenia. Należy do grupy leków zwanych cefalosporynami.
Biotum stosuje się w leczeniu ciężkich zakażeń bakteryjnych:
Informacje ważne przed zastosowaniem leku Biotum Kiedy nie stosować leku Biotum
Jeśli pacjent ma uczulenie na ceftazydym lub którykolwiek z pozostałych składników tego leku (wymienionych w punkcie 6).
Jeśli u pacjenta kiedykolwiek występowała ciężka reakcja alergiczna na jakikolwiek inny antybiotyk (penicyliny, monobaktamy i karbapenemy), ponieważ pacjent może być również uczulony na Biotum.
Jeśli pacjent przypuszcza, że dotyczą go opisane powyżej okoliczności, powinien
poinformować o tym lekarza prowadzącego przed rozpoczęciem leczenia lekiem Biotum. Nie podawać pacjentowi leku Biotum.
Ostrzeżenia i środki ostrożności
Przed rozpoczęciem stosowania leku Biotum należy omówić to z lekarzem lub pielęgniarką.
Należy zwracać uwagę, czy w czasie stosowania leku Biotum u pacjenta nie występują szczególne objawy, takie jak reakcje alergiczne, zaburzenia układu nerwowego i zaburzenia żołądka i jelit, w tym biegunka. Zmniejszy to ryzyko możliwych problemów. Patrz „Objawy, na które należy zwrócić
uwagę” w punkcie 4. Jeśli u pacjenta kiedykolwiek występowała reakcja alergiczna na inne antybiotyki, może on być uczulony również na Biotum.
Badania krwi i moczu
Biotum może zmieniać wyniki badania zawartości (stężenia) cukru w moczu oraz badań krwi, znanych jako test Coombs’a. Jeśli pacjent ma mieć wykonywane takie badania:
Należy poinformować osobę pobierającą próbki, że pacjent przyjmował lek Biotum.
Biotum a inne leki
Należy powiedzieć lekarzowi o wszystkich lekach stosowanych przez pacjenta obecnie lub ostatnio, a także o lekach, które pacjent planuje stosować.
Pacjent nie powinien przyjmować leku Biotum bez konsultacji z lekarzem prowadzącym, jeśli przyjmuje także:
antybiotyk zwany chloramfenikolem
antybiotyk z grupy zwanej aminoglikozydami, tj. gentamycynę, tobramycynę
tabletki moczopędne zawierające furosemid.
Jeśli opisane powyżej okoliczności dotyczą pacjenta, należy poinformować o tym lekarza prowadzącego.
Ciąża i karmienie piersią
Jeśli pacjentka jest w ciąży lub karmi piersią, przypuszcza że może być w ciąży, lub gdy planuje mieć dziecko, powinna poradzić się lekarza przed zastosowaniem tego leku.
Lekarz prowadzący oceni, czy wynikające z przyjmowania leku Biotum podczas ciąży i karmienia piersią korzyści dla pacjentki przeważają zagrożenia dla dziecka.
Prowadzenie pojazdów i obsługiwanie maszyn
Biotum może powodować działania niepożądane wpływające na zdolność prowadzenia pojazdów,
takie jak zawroty głowy. Pacjent nie powinien prowadzić pojazdów ani obsługiwać maszyn, chyba że ma pewność, że nie wystąpiły u niego te działania niepożądane.
Biotum zawiera sód
Każda fiolka 1 g zawiera 60 mg sodu. Odpowiada to 3% maksymalnej zalecanej dobowej dawki sodu w diecie u osób dorosłych.
Każda fiolka 2 g zawiera 120 mg sodu. Odpowiada to 6% maksymalnej zalecanej dobowej dawki sodu w diecie u osób dorosłych.
Lek zawiera 60 mg sodu (głównego składnika soli kuchennej) w każdym gramie proszku. Odpowiada to 3% maksymalnej zalecanej dobowej dawki sodu w diecie u osób dorosłych.
Należy to wziąć pod uwagę u pacjentów ze zmniejszoną czynnością nerek i u pacjentów kontrolujących zawartość sodu w diecie.
Przygotowanie leku do podania - patrz punkt: „Informacje przeznaczone wyłącznie dla fachowego personelu medycznego” na końcu ulotki. Obliczając całkowitą zawartość sodu w przygotowanym
rozcieńczeniu leku należy uwzględnić sód pochodzący z rozcieńczalnika. W celu uzyskania dokładnej informacji dotyczącej zawartości sodu w roztworze wykorzystanym do rozcieńczenia leku, należy
zapoznać się z ulotką dla pacjenta stosowanego rozcieńczalnika.
Jak stosować lek Biotum
Możliwe działania niepożądane
Ciężka reakcja alergiczna. Objawami są: wypukła, swędząca wysypka, obrzęk, czasami twarzy lub ust, który może spowodować trudności w oddychaniu.
Wysypka na skórze, mogąca przebiegać z pęcherzykami i wyglądać jak małe tarcze (ciemna plamka w środku otoczona jaśniejszą obwódką z ciemnym pierścieniem wokół krawędzi).
Rozsiana wysypka na skórze, w obrębie której mogą wystąpić pęcherzyki i złuszczanie skóry. (Może być objawem zespołu Stevensa-Johnsona lub toksycznego martwiczego oddzielania się naskórka).
Zaburzenia układu nerwowego: drżenia, drgawki i czasami śpiączka. Zaburzenia te
występowały u pacjentów, którym podano zbyt duże dawki, szczególnie u pacjentów z chorymi nerkami.
Skórna reakcja polekowa przebiegająca z zajęciem narządów wewnętrznych (rzadko występująca, ciężka reakcja nadwrażliwości - zespół DRESS): silna wysypka z występującymi jednocześnie takimi objawami, jak: gorączka, zmęczenie, obrzęk twarzy lub węzłów chłonnych, zwiększenie liczby eozynofilów (rodzaj białych krwinek), zaburzenia czynności wątroby, nerek lub płuc.
Jeśli u pacjenta wystąpi którykolwiek z tych objawów, należy natychmiast skontaktować się z lekarzem lub pielęgniarką.
Częste działania niepożądane
Mogą wystąpić nie częściej niż u 1 na 10 pacjentów:
biegunka
obrzęk i zaczerwienienie wzdłuż żyły
czerwona wypukła wysypka na skórze, która może swędzieć
ból, pieczenie, obrzęk lub stan zapalny w miejscu wstrzyknięcia.
Jeśli którykolwiek z powyższych objawów niepokoi pacjenta, powinien powiedzieć o tym lekarzowi prowadzącemu.
Częste działania niepożądane mogące ujawnić się w wynikach badań krwi:
zwiększenie liczby jednego rodzaju białych krwinek (eozynofilia)
zwiększenie liczby płytek krwi, które biorą udział w procesie krzepnięcia krwi
zwiększenie aktywności enzymów wątrobowych.
Niezbyt częste działania niepożądane
Mogą wystąpić nie częściej niż u 1 na 100 pacjentów:
zapalenie jelit, które może powodować ból lub biegunkę, mogącą zawierać krew
pleśniawki - zakażenia grzybicze jamy ustnej lub pochwy
ból głowy
zawroty głowy
ból brzucha
nudności lub wymioty
gorączka i dreszcze.
Należy powiedzieć lekarzowi prowadzącemu, jeśli u pacjenta wystąpił którykolwiek z powyższych objawów.
Niezbyt częste działania niepożądane mogące ujawnić się w wynikach badań krwi:
zmniejszenie liczby krwinek białych
zmniejszenie liczby płytek krwi (komórek biorących udział w krzepnięciu krwi)
zwiększenie stężenia mocznika, azotu mocznikowego lub kreatyniny w surowicy krwi.
Bardzo rzadkie działania niepożądane
Mogą wystąpić nie częściej niż u 1 na 10 000 pacjentów:
zapalenie lub niewydolność nerek.
Inne działania niepożądane
Inne działania niepożądane, które wystąpiły u małej liczby pacjentów, ale dokładna częstość ich występowania jest nieznana:
mrowienie
nieprzyjemny smak w ustach
zażółcenie białkówek oczu i skóry.
Inne działania niepożądane mogące ujawnić się w wynikach badań krwi:
krwinki czerwone rozpadają się zbyt szybko
zwiększenie liczby jednego rodzaju krwinek białych we krwi
znacznego stopnia zmniejszenie liczby krwinek białych.
Odnotowano rzadkie przypadki ciężkich reakcji nadwrażliwości z silną wysypką, którym może towarzyszyć gorączka, zmęczenie, obrzęk twarzy lub gruczołów chłonnych, wzrost eozynofilów (rodzaj białych krwinek), wpływające na wątrobę, nerki i płuca (reakcja nazywana DRESS).
Zgłaszanie działań niepożądanych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione w tej ulotce, należy powiedzieć o tym lekarzowi, farmaceucie lub pielęgniarce. Działania niepożądane można zgłaszać bezpośrednio do Departamentu Monitorowania Niepożądanych Działań Produktów
Leczniczych Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych
Al. Jerozolimskie 181C 02-222 Warszawa
Tel.: + 48 22 49 21 301
Faks: + 48 22 49 21 309
Strona internetowa: https://smz.ezdrowie.gov.pl
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Dzięki zgłaszaniu działań niepożądanych można będzie zgromadzić więcej informacji na temat bezpieczeństwa stosowania leku.
Jak przechowywać lek Biotum
Zawartość opakowania i inne informacje
Substancją czynną leku jest ceftazydym. Każda fiolka zawiera 1 g lub 2 g ceftazydymu w postaci pięciowodzianu buforowanego węglanem sodu.
Pozostały składnik to: węglan sodu.
Ten lek należy zawsze stosować zgodnie z zaleceniami lekarza. W razie wątpliwości należy zwrócić się do lekarza.
Biotum jest zwykle podawany przez lekarza lub pielęgniarkę. Może być podawany w kroplówce
(infuzja dożylna) lub jako wstrzyknięcie bezpośrednio do żyły lub wstrzyknięcie domięśniowe. Biotum przygotowuje lekarz lub pielęgniarka z użyciem wody do wstrzykiwań lub innego odpowiedniego płynu infuzyjnego.
Zwykle stosowana dawka
Lekarz prowadzący zdecyduje o odpowiedniej dla pacjenta dawce leku Biotum, biorąc pod uwagę ciężkość i rodzaj zakażenia, przyjmowanie przez pacjenta jakichkolwiek innych antybiotyków, jego masę ciała, wiek oraz prawidłowość pracy nerek.
Noworodki i niemowlęta (w wieku 0-2 miesięcy)
Na każdy 1 kg masy ciała niemowlęcia, podaje się w ciągu doby od 25 mg do 60 mg leku Biotum w dwóch dawkach podzielonych.
Niemowlęta (w wieku powyżej 2 miesięcy) i dzieci o masie ciała mniejszej niż 40 kg
Na każdy kg masy ciała niemowlęcia lub dziecka podaje się w ciągu doby od 100 mg do 150 mg leku Biotum w trzech dawkach podzielonych. Maksymalnie 6 g na dobę.
Dorośli i młodzież o masie ciała 40 kg lub więcej
Od 1g do 2 g leku Biotum trzy razy na dobę. Maksymalnie 9 g na dobę.
Pacjenci w wieku powyżej 65 lat
Dawka dobowa zazwyczaj nie powinna być większa niż 3 g na dobę, szczególnie u pacjentów w wieku powyżej 80 lat.
Pacjenci z chorymi nerkami
Pacjent może otrzymać dawkę inną niż zwykle stosowana. Lekarz lub pielęgniarka zdecyduje jaką dawkę leku Biotum, w zależności o ciężkości choroby nerek, należy podać pacjentowi. Lekarz będzie uważnie obserwował pacjenta i może zlecić wykonywanie u pacjenta częstszych badań czynności nerek.
Zastosowanie większej niż zalecana dawki leku Biotum
W razie przypadkowego zastosowania większej dawki leku Biotum, niż została przepisana należy natychmiast skontaktować się z lekarzem prowadzącym lub udać do najbliższego szpitala.
Pominięcie zastosowania leku Biotum
Jeśli pacjent nie przyjął wstrzyknięcia, należy podać je najszybciej jak to możliwe.
Nie należy stosować dawki podwójnej (dwa wstrzyknięcia w tym samym czasie) w celu uzupełnienia pominiętej dawki, lecz zastosować kolejną dawkę o zwykłej porze.
Przerwanie stosowania leku Biotum
Nie należy zaprzestawać przyjmowania dawek Biotum bez zalecenia lekarza.
W razie jakichkolwiek dalszych wątpliwości związanych ze stosowaniem tego leku należy zwrócić się do lekarza lub pielęgniarki.
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
Objawy, na które należy zwrócić uwagę
Opisane niżej ciężkie objawy niepożądane wystąpiły u małej liczby osób, ale ich dokładna częstość jest nieznana (częstość nie może być określona na podstawie dostępnych danych).
Lek należy przechowywać w temperaturze do 25°C. Chronić od światła.
Przygotowany roztwór można przechowywać 24 godziny w lodówce, tj. w temperaturze od 2°C do 8°C.
Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Nie stosować tego leku po upływie terminu ważności zamieszczonego na opakowaniu. Termin ważności oznacza ostatni dzień podanego miesiąca.
Zapis na opakowaniu po skrócie EXP oznacza termin ważności, a po skrócie Lot oznacza numer serii.
Leków nie należy wyrzucać do kanalizacji ani domowych pojemników na odpadki. Należy zapytać farmaceutę, jak usunąć leki, których się już nie używa. Takie postępowanie pomoże chronić środowisko.
Co zawiera lek Biotum
Jak wygląda lek Biotum i co zawiera opakowanie
Biały lub prawie biały krystaliczny proszek umieszczony w szklanej fiolce, zamkniętej gumowym korkiem i zabezpieczonej aluminiowym wieczkiem, w tekturowym pudełku.
Opakowanie zawiera 1 fiolkę.
Podmiot odpowiedzialny i wytwórca Podmiot odpowiedzialny:
Zakłady Farmaceutyczne POLPHARMA SA ul. Pelplińska 19
83-200 Starogard Gdański
Wytwórca:
Zakłady Farmaceutyczne POLPHARMA SA ul. Pelplińska 19
83-200 Starogard Gdański
Zakłady Farmaceutyczne POLPHARMA SA Oddział Produkcyjny w Duchnicach
ul. Ożarowska 28/30
05-850 Ożarów Mazowiecki
W celu uzyskania bardziej szczegółowych informacji dotyczących tego leku należy zwrócić się do miejscowego przedstawiciela podmiotu odpowiedzialnego.
POLPHARMA Biuro Handlowe Sp. z o.o. ul. Bobrowiecka 6
00-728 Warszawa
tel. 22 364 61 01
Data ostatniej aktualizacji ulotki:
Informacje przeznaczone wyłącznie dla fachowego personelu medycznego
Biotum, 1 g, proszek do sporządzania roztworu do wstrzykiwań lub infuzji Biotum, 2 g, proszek do sporządzania roztworu do wstrzykiwań lub infuzji Ceftazidimum
Ciśnienie w fiolkach leku Biotum każdej wielkości jest mniejsze od atmosferycznego. Podczas rozpuszczania proszku ciśnienie zwiększa się wskutek uwalniania dwutlenku węgla. Można
zignorować małe pęcherzyki dwutlenku węgla znajdujące się w przygotowanym roztworze.
Instrukcja dotycząca przygotowania leku do stosowania
Należy zapoznać się z tabelą dodawanych objętości i uzyskiwanych stężeń, co może być przydatne, gdy potrzebne są dawki częściowe.
Zawartość fiolki | Droga podania | Objętość rozpuszczalnika do dodania [ml] | Przybliżone stężenie ceftazydymu [mg/ml] |
1 g | wstrzyknięcie domięśniowe | 3 ml | 260 |
wstrzyknięcie dożylne | 10 ml | 90 | |
infuzja dożylna | 50 ml* | 20 | |
2 g | wstrzyknięcie dożylne | 10 ml | 170 |
infuzja dożylna | 50 ml* | 40 |
* Uwaga. Dodawać należy dwustopniowo
Zabarwienie roztworu od jasnożółtego do bursztynowego zależy od stężenia, rodzaju rozpuszczalnika i warunków przechowywania. Jeśli spełnione są zalecane warunki, zmienność zabarwienia roztworu nie wpływa niekorzystnie na skuteczność działania produktu.
Do przygotowania roztworów do infuzji dożylnych o stężeniu ceftazydymu pomiędzy 1 mg/ml a 40 mg/ml stosuje się:
9 mg/ml (0,9%) roztwór chlorku sodu do wstrzykiwań
M/6 roztwór mleczanu sodu do wstrzykiwań
wieloskładnikowy roztwór mleczanu sodu do wstrzykiwań (Roztwór Hartmanna)
5% roztwór glukozy do wstrzykiwań
0,225% roztwór chlorku sodu z 5% roztworem glukozy do wstrzykiwań
0,45% roztwór chlorku sodu z 5% roztworem glukozy do wstrzykiwań
0,9% roztwór chlorku sodu z 5% roztworem glukozy do wstrzykiwań
0,18% roztwór chlorku sodu z 4% roztworem glukozy do wstrzykiwań
10% roztwór glukozy do wstrzykiwań
10% roztwór dekstranu 40 w 0,9% roztworze chlorku sodu do wstrzykiwań
10% roztwór dekstranu 40 w 5% roztworze glukozy do wstrzykiwań
6% roztwór dekstranu 70 w 0,9% roztworze chlorku sodu
6% roztwór dekstranu 70 w 5% roztworze glukozy do wstrzykiwań.
Ceftazydym w stężeniach pomiędzy 0,05 mg/ml a 0,25 mg/ml jest zgodny z płynem do dializy otrzewnowej (mleczanowym).
Ceftazydym do wstrzyknięć domięśniowych można rozpuścić w roztworze zawierającym 0,5% lub 1% chlorowodorku lidokainy do wstrzykiwań.
Sporządzanie roztworu do szybkiego wstrzyknięcia
Przebić igłą korek i wstrzyknąć do fiolki zalecaną objętość rozpuszczalnika. W celu nakłucia korka należy użyć igły o średnicy nie większej niż 0,8 mm (21 G w skali Gauge [G]). Igłę należy wbić
w centralnie wyznaczonym polu pod kątem 90°, zgodnie z poniższym schematem:
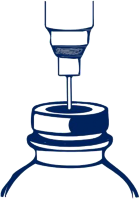
Podciśnienie wewnątrz fiolki może ułatwić wniknięcie rozpuszczalnika. Wycofać igłę ze strzykawką.
Potrząsać aż do rozpuszczenia: uwalnia się dwutlenek węgla i w ciągu 1 do 2 minut uzyskuje się klarowny roztwór.
Odwrócić fiolkę. Utrzymując tłok strzykawki w pozycji w pełni wciśniętej, przebić igłą korek fiolki i pobrać całą objętość roztworu do strzykawki (podwyższone ciśnienie w fiolce ułatwi tę czynność).
Igłę należy utrzymać wewnątrz roztworu, aby uniknąć zassania powietrza. Roztwór pobrany do strzykawki może zawierać małe pęcherzyki dwutlenku węgla.
Te roztwory można podać bezpośrednio do żyły lub do zestawu do infuzji dożylnych, jeśli pacjent otrzymuje płyny dożylnie. Ceftazydym wykazuje zgodność z najczęściej używanymi płynami dożylnymi.
Sporządzanie roztworu do infuzji dożylnych z ceftazydymu w standardowej fiolce (zestaw typu mini-bag lub burette)
Sporządzić używając w sumie 50 ml (dla fiolek 1 g i 2 g) zgodnego rozpuszczalnika, dodawanego w DWÓCH etapach, jak opisano poniżej:
Przebić igłą korek i wstrzyknąć 10 ml rozpuszczalnika do fiolki 1 g i 2 g.
Usunąć igłę i wstrząsać fiolką aż do uzyskania klarownego roztworu.
Nie wprowadzać igły odbarczającej zanim lek rozpuści się całkowicie. Wprowadzić igłę odbarczającą przez korek w celu zmniejszenia nadciśnienia wewnątrz fiolki.
Przemieścić roztwór do końcowego zbiornika (zestaw mini-bag lub burette), uzyskując całkowitą objętość nie mniejszą niż 50 ml i podawać w infuzji dożylnej przez 15 do 30 minut.
Uwaga: w celu zapewnienia jałowości leku ważne jest, aby nie wkłuwać igły odbarczającej przez korek fiolki przed całkowitym rozpuszczeniem leku.











