Spis treści:
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA
Wilate 500, 500 j.m. VWF / 500 j.m. FVIII, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań
Wilate 1000, 1000 j.m. VWF / 1000 j.m. FVIII, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań
Ludzki czynnik von Willebranda / ludzki VIII czynnik krzepnięcia
Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać.
W razie jakichkolwiek wątpliwości należy zwrócić się do lekarza lub farmaceuty.
Lek ten przepisano ściśle określonej osobie. Nie należy go przekazywać innym. Lek może zaszkodzić innej osobie, nawet jeśli objawy jej choroby są takie same.
Jeśli u pacjenta wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione w tej ulotce, należy powiedzieć o tym lekarzowi lub farmaceucie. Patrz punkt 4.
Spis treści ulotki:
Kiedy nie stosować Wilate
jeśli pacjent ma uczulenie (nadwrażliwość) na ludzki czynnik von Willebranda, VIII czynnik krzepnięcia, lub którykolwiek z pozostałych składników tego leku (wymienionych w punkcie 6).
Ostrzeżenia i środki ostrożności
Przed rozpoczęciem stosowania Wilate należy omówić to z lekarzem lub farmaceutą.
Wilate, jak każdy lek, który jest wytwarzany z ludzkiej krwi (zawierający białka) i wstrzykiwany jest do naczynia (podawany dożylnie) może wywoływać reakcje alergiczne. Należy zwrócić uwagę na wczesne objawy reakcji alergicznych (nadwrażliwości) takich jak: pokrzywka, wysypka skórna, uczucie ucisku w klatce piersiowej, świszczący oddech, spadek ciśnienia krwi lub anafilaksja (gdy którykolwiek lub wszystkie objawy pojawiają się gwałtownie i są nasilone). W przypadku wystąpienia tych objawów należy natychmiast zaprzestać stosowania leku i skontaktować się z lekarzem.
W przypadku leków wytwarzanych z ludzkiej krwi lub osocza stosuje się odpowiednie metody zapobiegające przeniesieniu zakażeń na pacjentów. Obejmują one: ścisłą selekcję dawców krwi i osocza w celu wyeliminowania nosicieli zakażeń, badanie poszczególnych donacji i puli osocza w kierunku specyficznych markerów wirusowych/infekcji, a także włączenie do procesu produkcji metod mających na celu inaktywację lub usuwanie wirusów. Pomimo tego, w przypadku podawania leków otrzymywanych z ludzkiej krwi lub osocza, nie można całkowicie wykluczyć przeniesienia czynnika zakaźnego. Dotyczy to także nieznanych lub nowo pojawiających się wirusów oraz innych typów zakażeń.
Zastosowane metody są uważane za skuteczne w stosunku do wirusów otoczkowych takich jak: ludzki wirus upośledzenia odporności (HIV), wirus zapalenia wątroby typu B i wirus zapalenia wątroby typu C oraz do bezotoczkowego wirusa zapalenia wątroby typu A. Zastosowane metody mogą mieć ograniczoną skuteczność w stosunku do wirusów bezotoczkowych takich jak parwowirus B19.
Zakażenie parwowirusem B19 może być groźne u kobiet w ciąży (zakażenie płodu) oraz u pacjentów z zaburzeniami odporności lub pacjentów z pewnymi typami niedokrwistości (np. niedokrwistość sierpowatokrwinkowa lub w stanach nieprawidłowego rozpadu krwinek czerwonych krwi).
Stanowczo zaleca się, aby przy każdorazowym podawaniu pacjentowi Wilate odnotować nazwę i numer serii produktu w celu zachowania zapisu użytych serii.
Szczepienia przeciwko zapaleniu wątroby typu A i B mogą być zalecone przez lekarza w przypadku regularnego lub powtarzanego stosowania otrzymywanych z osocza czynnika von Willebranda i czynnika VIII.
Choroba von Willebranda (VWD)
Patrz punkt 4 (choroba von Willebranda (VWD)) w celu zapoznania się z działaniami niepożądanymi związanymi z leczeniem choroby von Willebranda.
Hemofilia A
Tworzenie inhibitorów (przeciwciał) jest znanym powikłaniem, które może występować w trakcie leczenia wszystkimi lekami zawierającymi czynnik VIII. Inhibitory te, zwłaszcza przy wysokich stężeniach, przerywają prawidłowe leczenie i pacjent będzie uważnie monitorowany pod kątem wytwarzania tych inhibitorów. Jeżeli krwawienie u pacjenta nie jest prawidłowo kontrolowane przy użyciu leku Wilate, należy natychmiast powiedzieć o tym lekarzowi.
Patrz punkt 4 (Hemofilia A) w celu zapoznania się z działaniami niepożądanymi związanymi z leczeniem hemofilii A.
Wilate a inne leki
Należy powiedzieć lekarzowi lub farmaceucie o wszystkich lekach stosowanych przez pacjenta obecnie lub ostatnio, a także o lekach, które pacjent planuje stosować.
Nie stwierdzono występowania interakcji Wilate z innymi lekami. Mimo to, należy poinformować lekarza o stosowaniu lub ostatnio przyjmowanych innych lekach (włączając w to leki dostępne bez recepty).
Nie należy mieszać Wilate z innymi lekami podczas wstrzykiwania.
Ciąża, karmienie piersią i wpływ na płodność
Jeśli pacjentka jest w ciąży lub karmi piersią, przypuszcza że może być w ciąży lub gdy planuje mieć dziecko, powinna poradzić się lekarza lub farmaceuty przed zastosowaniem tego leku.
Wilate zawiera sód
Ten lek zawiera do 58,7 mg sodu (głównego składnika soli kuchennej) na fiolkę 500 j.m. czynnika von Willebranda i czynnika VIII i do 117,3 mg sodu na fiolkę 1000 j.m. czynnika von Willebranda i czynnika VIII na fiolkę. Odpowiada to, odpowiednio, 2,94% i 5,87% maksymalnej zalecanej dobowej dawki sodu w diecie u osób dorosłych.
Dawkowanie
Niezbyt często: mogą wystąpić do 1 na 100 użytkowników
Jak wygląda Wilate i co zawiera opakowanie
Wilate 500, 500 j.m. VWF i 500 j.m. FVIII, występuje w postaci proszku i rozpuszczalnika do sporządzania roztworu do wstrzykiwań zawierającego nominalnie 500 j.m. ludzkiego
czynnika von Willebranda i 500 j.m. ludzkiego VIII czynnika krzepnięcia w fiolce. Produkt zawiera około 100 j.m. ludzkiego czynnika von Willebranda i 100 j.m. ludzkiego VIII czynnika krzepnięcia po rozpuszczeniu w 5 ml wody do wstrzykiwań z 0,1% Polisorbatem 80 (rozpuszczalnik)
Wilate 1000, 1000 j.m. VWF i 1000 j.m. FVIII, występuje w postaci proszku i rozpuszczalnika do sporządzania roztworu do wstrzykiwań zawierającego nominalnie 1000 j.m. ludzkiego czynnika von Willebranda i 1000 j.m. ludzkiego VIII czynnika krzepnięcia w fiolce. Produkt zawiera około 100 j.m. ludzkiego czynnika von Willebranda i 100 j.m. ludzkiego VIII czynnika krzepnięcia po rozpuszczeniu w 10 ml wody do wstrzykiwań z 0,1% Polisorbatem 80 (rozpuszczalnik)
Zawartość opakowania
1 fiolka z liofilizowanym proszkiem 1 fiolka z rozpuszczalnikiem
opakowanie ze sprzętem do wstrzyknięcia dożylnego (1 zestaw do transferu, 1 zestaw do infuzji, 1 strzykawka jednorazowego użytku)
waciki nasączone alkoholem
Podmiot odpowiedzialny i wytwórca
Octapharma (IP) SPRL Allée de la Recherche 65 1070 Anderlecht
Belgia
W celu uzyskania bardziej szczegółowych informacji na temat tego produktu leczniczego, należy zwrócić się do lokalnego przedstawiciela podmiotu odpowiedzialnego.
Octapharma Poland Sp. z o.o. ul. Domaniewska 39a
02-672 Warszawa Polska
tel.+48 22 489 52 28
fax +48 22 489 52 29
Wytwórca
Octapharma Pharmazeutika Produktionsges.m.b.H. Oberlaaerstr. 235
A-1100 Wiedeń Austria
Data zatwierdzenia ulotki: 03/2021
Ten produkt leczniczy jest dopuszczony do obrotu w krajach członkowskich Europejskiego Obszaru Gospodarczego pod następującymi nazwami:
Austria, Belgia, Bułgaria, Chorwacja, Cypr, Czechy, Estonia, Niemcy, Węgry, Irlandia, Włochy, Łotwa, Litwa, Luksemburg, Malta, Holandia, Polska, Portugalia, Rumunia, Słowenia, Słowacja, Hiszpania, Wielka Brytania: Wilate 500/ Wilate 1000
Finlandia, Norwegia, Szwecja: Wilate
Dania: Wilnativ
Francja: Eqwilate 500/ Eqwilate 1000
Instrukcja stosowania w domu
Należy przeczytać wszystkie instrukcje i dokładnie ich przestrzegać!
Nie stosować produktu Wilate po upływie terminu ważności zamieszczonego na etykiecie.
Podczas opisanej poniżej procedury należy zachować warunki jałowe!
Przed podaniem należy sprawdzić wzrokowo, czy przygotowany roztwór produkt nie zawiera cząsteczek stałych ani przebarwień.
Roztwór powinien być przejrzysty lub lekko opalizujący. Nie używać roztworów, które są mętne lub zawierają cząstki stałe.
Przygotowany roztwór zużyć niezwłocznie w celu zapobiegnięcia skażeniu mikrobiologicznemu.
Używać wyłącznie dostarczonego zestawu do wstrzykiwań. Stosowanie innego sprzętu do wstrzykiwań/infuzji może powodować dodatkowe zagrożenia i niepowodzenie leczenia.
Nie używać produktu bezpośrednio z lodówki. Pozostawić rozpuszczalnik i proszek w zamkniętych fiolkach aż do uzyskania temperatury pokojowej.
Usunąć wieczka z obu fiolek i wyczyścić gumowe korki jednym z dołączonych wacików nasączonych alkoholem.
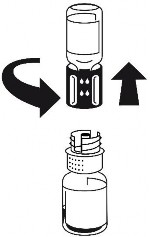
Zestaw do transferu jest przedstawiony na ryc. 1. Umieścić fiolkę z rozpuszczalnikiem na płaskiej powierzchni i mocno przytrzymać. Wziąć zestaw do transferu i obrócić do góry dnem. Umieścić niebieską część zestawu do transferu na górze fiolki z rozpuszczalnikiem i mocno wcisnąć aż do zatrzaśnięcia (ryc. 2 + 3). Nie obracać podczas podłączania.
Rozpuszczalnik
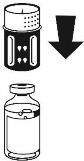
Rozpuszczalnik
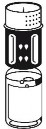
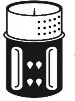
Adapter fiolki
z proszkiem
Adapter fiolki
z rozpuszczalnikiem (niebieska część)
ryc. 1 ryc. 2 ryc. 3
Powder
rozpuszczalnik
proszek
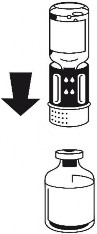

Umieścić fiolkę z proszkiem na płaskiej powierzchni i mocno przytrzymać. Wziąć fiolkę z rozpuszczalnikiem z podłączonym zestawem do transferu i obrócić ją do góry dnem. Umieścić białą część zestawu na górze fiolki z proszkiem i mocno wcisnąć aż do zatrzaśnięcia (ryc. 4). Nie obracać podczas podłączania. Rozpuszczalnik przepływa automatycznie do fiolki z proszkiem.
Fig. 4
ryc. 4
proszek
rozpuszczalnik


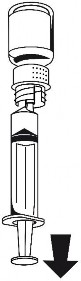
Z nadal podłączonymi obiema fiolkami delikatnie obracać fiolką z proszkiem aż produkt będzie rozpuszczony. Rozpuszczanie jest zakończone w mniej niż 10 minut w temperaturze pokojowej. Podczas przygotowania może powstać nieznaczna piana. Rozkręcić zestaw do transferu na dwie części (ryc. 5). Piana zniknie.
Podłączyć strzykawkę do białej części zestawu do transferu. Obrócić fiolkę do góry dnem i pobrać roztwór do strzykawki (ryc. 6).
Roztwór w strzykawce powinien być przejrzysty lub lekko opalizujący.
Po przeniesieniu roztworu mocno przytrzymać tłok strzykawki (trzymając w dół) i wyjąć strzykawkę z zestawu do transferu (ryc. 7).
Wyrzucić pustą fiolkę z rozpuszczalnikiem razem z białą częścią zestawu do transferu.
proszek
proszek
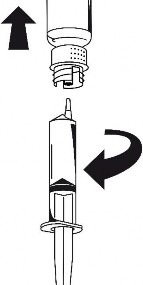
ryc. 6 ryc. 7
Oczyścić wybrane miejsce wstrzyknięcia jednym z dołączonych wacików nasączonych alkoholem.
Podłączyć dostarczony zestaw do infuzji do strzykawki.
Wprowadzić igłę do wybranej żyły. W przypadku użycia opaski uciskowej w celu uwidocznienia żyły należy rozluźnić opaskę przed rozpoczęciem wstrzykiwania produktu Wilate.
Krew nie może przedostać się do strzykawki z powodu ryzyka wytworzenia się skrzepów fibryny.
Roztwór wstrzykiwać powoli do żyły, nie szybciej niż 2-3 ml na minutę.
Dawka i częstość podawania powinny być ustalone przez lekarza indywidualnie dla każdego pacjenta. Należy zawsze stosować Wilate zgodnie z zaleceniami lekarza. Należy skonsultować się z lekarzem lub farmaceutą w przypadku jakichkolwiek wątpliwości.
Zastosowanie większej niż zalecana dawki Wilate
Nie obserwowano objawów przedawkowania ludzkiego czynnika von Willebranda lub czynnika
VIII. Jednakże nie powinno się przekraczać zalecanej dawki.
Pominięcie zastosowania Wilate
Nie należy stosować podwójnej dawki w celu uzupełnienia pominiętej dawki.
Należy skonsultować się z lekarzem lub farmaceutą w przypadku innych pytań dotyczących sposobu użycia preparatu.
Rzadko: mogą wystąpić do 1 na 1 000 użytkowników
Bardzo rzadko: mogą wystąpić do 1 na 10 000 użytkowników
Nie ma wystarczających danych, aby zalecać podawanie Wilate u wcześniej nieleczonych pacjentów.
Doświadczenie w leczeniu dzieci poniżej 6 roku życia produktem Wilate jest ograniczone.
Informacje związane z ochroną przeciwko czynnikom wirusowym patrz punkt 2 (Ostrzeżenia i środki ostrożności).
Zgłaszanie działań niepożądanych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione w ulotce, należy powiedzieć o tym lekarzowi, lub farmaceucie lub pielęgniarce. Działania niepożądane można zgłaszać bezpośrednio (szczegóły poniżej). Dzięki zgłaszaniu działań niepożądanych można będzie zgromadzić więcej informacji na temat bezpieczeństwa stosowania leku.
Departament Monitorowania Niepożądanych Działań Produktów Leczniczych Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych
Al. Jerozolimskie 181C 02-222 Warszawa
Tel.: + 48 22 49 21 301
Faks: + 48 22 49 21 309
Liofilizowany proszek: biały lub jasno żółty proszek lub zbrylona masa. Roztwór po rozpuszczeniu: powinien być przejrzysty lub lekko opalizujący.
Wilate jest dostarczany jako proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań. Dostępny jest w 2 wielkościach opakowania:
Instrukcja przygotowania roztworu:
proszek
Wyrzucić pustą fiolkę z rozpuszczalnikiem razem z niebieską częścią zestawu do transferu.
ryc. 5
Instrukcja wykonywania wstrzyknięcia:
Jako środek ostrożności należy przed wstrzyknięciem i w czasie wstrzyknięcia zbadać tętno. W przypadku znacznego zwiększenia częstości tętna należy zmniejszyć szybkość wstrzykiwania lub przerwać podawanie leku na krótki czas.
W przypadku używania więcej niż jednej fiolki proszku Wilate do jednego cyklu leczenia możliwe jest ponowne zastosowanie tej samej igły i strzykawki. Zestaw do transferu jest przeznaczony wyłącznie do jednorazowego użycia.
Wszelkie resztki niewykorzystanego roztworu czy zużytych materiałów należy usunąć w sposób zgodny z lokalnymi przepisami.
Nie wolno mieszać lub wstrzykiwać (stosując ten sam zestaw do infuzji) Wilate z innymi produktami leczniczymi.
Należy podawać tylko przy pomocy dostarczonego zestawu do infuzji. Używanie innego zestawu do wstrzykiwań lub infuzji może powodować dodatkowe ryzyko i niepowodzenie leczenia (czynnik von Willebranda i czynnik VIII mogą adsorbować do wewnętrznej powierzchni niektórych zestawów infuzyjnych).










