Spis treści:
- NAZWA PRODUKTU LECZNICZEGO
- SKŁAD JAKOŚCIOWY I ILOŚCIOWY
- POSTAĆ FARMACEUTYCZNA
- SZCZEGÓŁOWE DANE KLINICZNE
- WŁAŚCIWOŚCI FARMAKOLOGICZNE
- DANE FARMACEUTYCZNE
- PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU
- NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
- DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU I DATA PRZEDŁUŻENIA POZWOLENIA
- DATA ZATWIERDZENIA LUB CZĘŚCIOWEJ ZMIANY TEKSTU CHARAKTERYSTYKI PRODUKTU LECZNICZEGO
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
NAZWA PRODUKTU LECZNICZEGO
SKŁAD JAKOŚCIOWY I ILOŚCIOWY
POSTAĆ FARMACEUTYCZNA
SZCZEGÓŁOWE DANE KLINICZNE
Wskazania do stosowania
Dawkowanie i sposób podawania
Przeciwwskazania
Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania
Interakcje z innymi produktami leczniczymi i inne rodzaje interakcji
Wpływ na płodność, ciążę i laktację
Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn
Działania niepożądane
Przedawkowanie
WŁAŚCIWOŚCI FARMAKOLOGICZNE
Właściwości farmakodynamiczne
Właściwości farmakokinetyczne
Przedkliniczne dane o bezpieczeństwie
DANE FARMACEUTYCZNE
Wykaz substancji pomocniczych
Niezgodności farmaceutyczne
Okres ważności
Specjalne środki ostrożności podczas przechowywania
Rodzaj i zawartość opakowania
Specjalne środki ostrożności dotyczące usuwania i przygotowania produktu leczniczego do stosowania
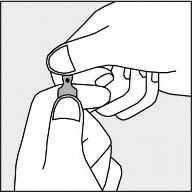
Aby otworzyć ampułkę należy trzymać ją pionowo, w obu dłoniach, kolorową kropką do siebie - patrz rysunek 2. Górną część ampułki należy uchwycić w taki sposób, aby kciuk znajdował się powyżej kolorowej kropki.
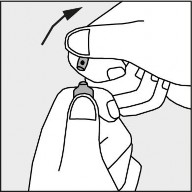
Nacisnąć zgodnie ze strzałką umieszczoną na rysunku 3.
PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU
NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU I DATA PRZEDŁUŻENIA POZWOLENIA
DATA ZATWIERDZENIA LUB CZĘŚCIOWEJ ZMIANY TEKSTU CHARAKTERYSTYKI PRODUKTU LECZNICZEGO
MORPHINI SULFAS WZF 0,1% SPINAL, 1 mg/ml, roztwór do wstrzykiwań
Każdy ml roztworu zawiera 1 mg morfiny siarczanu (Morphini sulfas). Substancja pomocnicza o znanym działaniu:
sód - produkt zawiera 0,154 mmol (3,54 mg) sodu w każdym ml roztworu. Pełny wykaz substancji pomocniczych, patrz punkt 6.1.
Roztwór do wstrzykiwań
Bezbarwny lub prawie bezbarwny, przezroczysty płyn
Morfina bez środków konserwujących wskazana jest do stosowania dożylnego, zewnątrzoponowego i podpajęczynówkowego w leczeniu bólów o dużym nasileniu, nieustępujących po podaniu nieopioidowych leków przeciwbólowych.
Zastosowanie podania zewnątrzoponowego i podpajęczynówkowego zapewnia długotrwałe działanie przeciwbólowe, pozbawione zaburzeń czucia, zaburzeń ruchowych oraz zaburzeń układu
współczulnego.
Sposób podawania
Produkt nie zawiera środków konserwujących i można go stosować dożylnie, zewnątrzoponowo i podpajęczynówkowo.
Ze względu na większe ryzyko wystąpienia wczesnych oraz późnych działań niepożądanych po podaniu podpajęczynówkowym morfiny, należy, jeśli to możliwe, stosować podanie
zewnątrzoponowe. Wstrzyknięcia zewnątrzoponowe i podpajęczynówkowe zaleca się wykonywać w odcinku lędźwiowym kręgosłupa.
Produkt może być stosowany zewnątrzoponowo i podpajęczynówkowo, wyłącznie przez
doświadczonego lekarza, dobrze znającego technikę oraz działania niepożądane związane z tą drogą podania. Po podaniu zewnątrzoponowym lub podpajęczynówkowym, pacjenta należy obserwować przez 24 godziny od podania ostatniej dawki produktu, ze względu na ryzyko wystąpienia
zahamowania ośrodka oddechowego (zarówno wczesnego jak i późnego). Należy zapewnić dostęp do aparatury resuscytacyjnej, tlenu i specyficznego antidotum - chlorowodorku naloksonu. Zahamowanie ośrodka oddechowego lub inne działania niepożądane mogą również wystąpić po niezamierzonym podaniu podpajęczynówkowym lub dożylnym zbyt dużej dawki (podpajęczynówkowo stosuje się 1/10 dawki zewnątrzoponowej).
Przed zewnątrzoponowym podaniem morfiny konieczne jest sprawdzenie prawidłowego położenia igły lub cewnika. W celu wykluczenia obecności igły lub cewnika w naczyniu lub przestrzeni
podpajęczynówkowej należy dokonać aspiracji i sprawdzić czy w strzykawce nie pojawiła się krew lub płyn mózgowo-rdzeniowy.
U pacjentów z bólem przewlekłym, leczonych morfiną podawaną zewnątrzoponowo lub podpajęczynówkowo, po rozpoczęciu terapii w warunkach szpitalnych, leczenie może być
kontynuowane ambulatoryjnie lub w domu. Nadzór nad stosowaniem morfiny może prowadzić lekarz lub pielęgniarka. U pacjentów leczonych w ośrodkach opieki paliatywno-hospicyjnej oraz w domu, powinna być prowadzona dokumentacja, uwzględniająca występowanie działań niepożądanych oraz postępowanie w przypadku ich wystąpienia.
Przerwanie leczenia
Wystąpienie zespołu abstynencyjnego może zostać przyspieszone, jeśli nagle zaprzestanie się podawania leku opioidowego. Dlatego przed planowanym odstawieniem leku, jego dawkę należy zmniejszać stopniowo.
Dawkowanie
Dawkowanie ustala się indywidualnie, uwzględniając wskazania kliniczne, rodzaj bólu (ostry czy przewlekły), stosowane dotychczas leki przeciwbólowe, stan pacjenta.
Podanie dożylne – dawka początkowa u dorosłych wynosi od 2 mg do 10 mg/70 kg mc. Brak danych dotyczących stosowania produktu u pacjentów w wieku poniżej 18 lat.
Podanie zewnątrzoponowe – u dorosłych dawka początkowa 5 mg, podana we wstrzyknięciu w odcinku lędźwiowym kręgosłupa, może zapewnić działanie przeciwbólowe przez 24 godziny. Jeżeli działanie przeciwbólowe nie zostanie osiągnięte w ciągu 1 godziny, można z zachowaniem ostrożności podać dawkę uzupełniającą 1 mg do 2 mg.
Nie należy stosować dawki większej niż 10 mg na dobę.
We wlewie ciągłym stosuje się dawkę początkową – 2 mg do 4 mg na dobę. Jeśli dawka początkowa jest niewystarczająca, można podać dawkę uzupełniającą 1 mg do 2 mg.
Podanie zewnątrzoponowe w odcinku piersiowym kręgosłupa nawet dawki 1 mg do 2 mg może spowodować wystąpienie wczesnych lub późnych objawów zahamowania ośrodka oddechowego. U osób w wieku podeszłym oraz wyniszczonych produkt należy stosować szczególnie ostrożnie.
Dawki mniejsze niż 5 mg mogą zapewnić wystarczające działanie przeciwbólowe przez 24 godziny.
Podanie podpajęczynówkowe – u dorosłych pojedyncza dawka 0,2 mg do 1 mg, podana we wstrzyknięciu może zapewnić działanie przeciwbólowe przez 24 godziny. Nie należy stosować podpajęczynówkowo więcej niż 1 ml roztworu.
Zaleca się podawanie produktu wyłącznie w odcinku lędźwiowym kręgosłupa.
Nie zaleca się powtarzania wstrzyknięcia podpajęczynówkowego. Ciągły wlew dożylny
chlorowodorku naloksonu w dawce 0,6 mg/h przez 24 godziny po podaniu podpajęczynówkowym zmniejsza możliwość wystąpienia działań niepożądanych.
Jeżeli działanie przeciwbólowe jest niewystarczające należy rozważyć inne drogi podania produktu, ponieważ możliwość powtarzania wstrzyknięć podpajęczynówkowych jest ograniczona.
U osób w wieku podeszłym oraz wyniszczonych produkt należy stosować szczególnie ostrożnie. Zazwyczaj wystarczające jest zmniejszenie dawki.
Nie ustalono bezpieczeństwa stosowania morfiny zewnątrzoponowo i podpajęczynówkowo u dzieci.
Nadwrażliwość na morfinę lub inne opioidowe leki przeciwbólowe.
Ostry napad astmy oskrzelowej lub choroba obturacyjna górnych dróg oddechowych.
Ogólne przeciwwskazania do stosowania produktu podpajęczynówkowo i zewnątrzoponowo, np. stan zapalny w miejscu wkłucia, jednoczesne leczenie lekami przeciwzakrzepowymi, skaza krwotoczna
i inne stany kliniczne, które mogą stanowić przeciwwskazanie do zastosowania zewnątrzoponowej lub podpajęczynówkowej drogi podawania morfiny.
Ostrzeżenia dotyczące podania podpajęczynówkowego i zewnątrzoponowego morfiny
Produkt może być stosowany zewnątrzoponowo i podpajęczynówkowo wyłącznie przez lekarza posiadającego doświadczenie w podawaniu zewnątrzoponowym i podpajęczynówkowym leków oraz znającego metody postępowania w przypadku wystąpienia działań niepożądanych, np. zahamowania ośrodka oddechowego. Podczas stosowania produktu Morphini sulfas WZF 0,1% Spinal należy
zapewnić dostęp do sprzętu do resuscytacji krążeniowo-oddechowej oraz do tlenu i naloksonu. Pacjenci, którym podano morfinę zewnątrzoponowo lub podpajęczynówkowo, muszą przez 24 godziny pozostawać pod ścisłym nadzorem wyszkolonego personelu medycznego ze względu na możliwość wystąpienia objawów zahamowania ośrodka oddechowego. Podanie podpajęczynówkowe obarczone jest większym ryzykiem wystąpienia zahamowania oddychania niż podanie
zewnątrzoponowe. Zaleca się ograniczenie stosowania produktu do odcinka lędźwiowego kręgosłupa.
Wzmożone napięcie mięśni gładkich, które występuje po przeniknięciu do krążenia ogólnego
znaczących ilości morfiny podanej zewnątrzoponowo lub podpajęczynówkowo pacjentom poddanym zabiegom chirurgicznym w obrębie dróg żółciowych lub osobom z zaburzeniami czynności dróg
żółciowych może wywołać kolkę żółciową.
Ostrzeżenia dotyczące podania dożylnego morfiny
Morphini sulfas WZF 0,1% Spinal należy stosować z zachowaniem szczególnej ostrożności
u pacjentów w podeszłym wieku, wyniszczonych, po urazach głowy, w przypadku zwiększonego
ciśnienia śródczaszkowego lub śródgałkowego. Zwężenie źrenic wywołane podaniem morfiny może utrudniać diagnostykę pacjentów z patologią śródczaszkową.
Bardzo starannej obserwacji wymagają pacjenci ze zmniejszoną rezerwą oddechową (np. rozedmą płuc, kifoskoliozą, znaczną otyłością).
Zastosowanie dużych dawek morfiny może wywołać drgawki. Z tego powodu produkt należy stosować ostrożnie u pacjentów z padaczką lub drgawkami w wywiadzie.
Zwiększone napięcie mięśni gładkich występujące po zastosowaniu morfiny, może spowodować wystąpienie kolki wątrobowej lub nerkowej oraz trudności w oddawaniu moczu. U chorych
z przerostem gruczołu krokowego morfina może spowodować zatrzymanie moczu, wymagające stałego cewnikowania.
U pacjentów z zaburzeniami metabolicznymi, zaburzoną czynnością wątroby lub nerek oraz niedoczynnością tarczycy eliminacja morfiny jest opóźniona. Podawanie morfiny w tej grupie pacjentów wymaga zachowania szczególnej ostrożności.
U pacjentów ze zmniejszoną objętością krwi krążącej, zaburzeniami czynności serca oraz leczonych lekami adrenolitycznymi istnieje ryzyko wystąpienia hipotonii ortostatycznej.
U pacjentów z przewlekłą obturacyjną chorobą płuc oraz u pacjentów w ostrym napadzie astmy oskrzelowej podanie morfiny może spowodować ostrą niewydolność oddechową.
Ostry zespół klatki piersiowej (ACS, ang. acute chest syndrome) u pacjentów z niedokrwistością sierpowatokrwinkową
Ze względu na możliwe powiązanie między ostrym zespołem klatki piersiowej a podawaniem morfiny pacjentom z niedokrwistością sierpowatokrwinkową otrzymującym morfinę w czasie kryzysu naczyniowo-okluzyjnego, należy uważnie obserwować, czy nie występują u nich objawy ostrego
zespołu klatki piersiowej.
Niewydolność nadnerczy
Opioidowe leki przeciwbólowe mogą spowodować nieodwracalną niewydolność nadnerczy
i konieczność obserwowania pacjenta oraz zastosowania terapii zastępczej glikokortykosteroidami.
Objawy niewydolności nadnerczy mogą obejmować np. nudności, wymioty, utratę apetytu, zmęczenie, osłabienie, zawroty głowy lub niskie ciśnienie krwi.
Zmniejszone wydzielanie hormonów płciowych i zwiększone wydzielanie prolaktyny
Długotrwałe stosowanie opioidowych leków przeciwbólowych może wiązać się ze zmniejszeniem wydzielania hormonów płciowych i zwiększeniem wydzielania prolaktyny. Objawy obejmują
zmniejszenie popędu seksualnego, impotencję lub brak miesiączki.
W trakcie leczenia, zwłaszcza podczas stosowania w dużych dawkach, może wystąpić hiperalgezja, która nie reaguje na dalsze zwiększenie dawki morfiny. Może być konieczne zmniejszenie dawki morfiny lub zmiana leku opioidowego.
Ryzyko związane z jednoczesnym stosowaniem leków uspokajających, np. benzodiazepin lub leków pochodnych:
Jednoczesne stosowanie leku Morphini sulfas WZF 0,1% Spinal i leków uspokajających,
np. benzodiazepin lub leków pochodnych, może prowadzić do wystąpienia nadmiernego uspokojenia, depresji oddechowej, śpiączki lub śmierci. Z tego względu leczenie skojarzone z takimi lekami uspokajającymi należy stosować wyłącznie u pacjentów, u których nie są dostępne alternatywne metody leczenia. Jeśli zostanie podjęta decyzja o stosowaniu leku Morphini sulfas WZF 0,1% Spinal w skojarzeniu z lekami uspokajającymi, należy podać najmniejszą skuteczną dawkę, a czas leczenia powinien być możliwie jak najkrótszy.
Należy uważnie obserwować, czy u pacjenta nie występują objawy związane z depresją oddechową
i nadmierne uspokojenie. W tym kontekście zdecydowanie zaleca się poinformowanie pacjentów i ich opiekunów o możliwości wystąpienia takich objawów (patrz punkt 4.5).
Potencjał nadużycia morfiny jest podobny jak w przypadku innych silnych leków opioidowych, dlatego morfinę należy stosować ze szczególną ostrożnością u pacjentów, którzy w przeszłości nadużywali alkoholu lub leków.
Uzależnienie i zespół odstawienny (abstynencyjny)
Stosowanie opioidowych leków przeciwbólowych może prowadzić do rozwoju fizycznego i (lub) psychicznego uzależnienia bądź tolerancji. Związane z tym ryzyko wzrasta w miarę stosowania leku oraz podczas stosowania w większych dawkach. Objawy można ograniczyć poprzez dostosowanie dawki lub postaci leku oraz stopniowe odstawianie morfiny. Informacje na temat poszczególnych objawów - patrz punkt 4.8.
Ryfampicyna może zmniejszać stężenie morfiny w osoczu. Należy obserwować działanie przeciwbólowe morfiny oraz odpowiednio dostosować dawkowanie morfiny w trakcie i po zakończeniu leczenia ryfampicyną.
Doustna terapia przeciwpłytkowa inhibitorem P2Y12
W pierwszym dniu leczenia skojarzonego inhibitorem P2Y12 i morfiną obserwowano zmniejszenie skuteczności leczenia inhibitorem P2Y12 (patrz punkt 4.5).
Produkt leczniczy zawiera 7,08 mg sodu na amp./2 ml co odpowiada 0,354% zalecanej przez WHO maksymalnej 2 g dobowej dawki sodu u osób dorosłych.
Leki uspokajające, np. benzodiazepiny lub leki pochodne:
Jednoczesne stosowanie leków opioidowych i leków uspokajających, np. benzodiazepin lub leków pochodnych, zwiększa ryzyko wystąpienia nadmiernego uspokojenia, depresji oddechowej, śpiączki lub śmierci na skutek addytywnego działania depresyjnego na OUN. Należy ograniczyć dawkę leku i czas trwania leczenia skojarzonego (patrz punkt 4.4).
Działanie morfiny mogą nasilać leki działające hamująco na ośrodkowy układ nerwowy, tj. leki uspokajające, przeciwhistaminowe, psychotropowe (np. inhibitory monoaminooksydazy, pochodne fenotiazyny, butyrofenonu oraz trójpierścieniowe leki przeciwdepresyjne) oraz alkohol.
Neuroleptyki stosowane w premedykacji i w okresie śródoperacyjnym mogą nasilać hamujące działanie morfiny na ośrodek oddechowy.
U pacjentów z ostrym zespołem wieńcowym leczonych morfiną obserwowano opóźnioną
i zmniejszoną ekspozycję na doustną terapię przeciwpłytkową inhibitorem P2Y12. Interakcja ta, może być związana ze zmniejszoną ruchliwością przewodu pokarmowego i dotyczyć innych opioidów.
Znaczenie kliniczne nie jest znane, jednak dane wskazują na możliwość zmniejszenia skuteczności inhibitora P2Y12 u pacjentów otrzymujących jednocześnie morfinę i inhibitor P2Y12 (patrz punkt 4.4). U pacjentów z ostrym zespołem wieńcowym, u których nie można wstrzymać podawania morfiny, a szybkie hamowanie P2Y12 uznaje się za kluczowe, można rozważyć zastosowanie pozajelitowego inhibitora P2Y12.
Ciąża
Nie wykazano teratogennego działania siarczanu morfiny po podaniu szczurom 35 mg/kg mc. na dobę (dawka 35 razy większa od dawki zwykle stosowanej u ludzi), natomiast odnotowano zwiększenie śmiertelności i zahamowanie wzrostu młodych osobników po zastosowaniu dawki większej niż
10 mg/kg mc. na dobę (dawka 10 razy większa od dawki zwykle stosowanej u ludzi).
Nie wiadomo, czy morfina stosowana u kobiet w ciąży może wpływać na zdolność do rozrodu
i powodować uszkodzenia płodu. Stosowanie produktu u kobiet ciężarnych wymaga zachowania szczególnej ostrożności. Morfina może być stosowana u kobiet w ciąży wyłącznie w przypadku zdecydowanej konieczności.
U noworodków urodzonych przez matki stosujące morfinę długotrwale w czasie ciąży mogą wystąpić objawy zespołu odstawiennego.
Należy obserwować, czy u noworodków, których matki przyjmowały w trakcie ciąży opioidowe leki przeciwbólowe, nie występują objawy noworodkowego zespołu odstawiennego (abstynencyjnego). Leczenie może obejmować zastosowanie leków opioidowych oraz leczenie objawowe.
Okres porodu
Morfina podana dożylnie łatwo przenika do krążenia płodowego i może powodować zaburzenia oddychania u noworodka. Hamuje czynność skurczową macicy, wydłużając czas trwania porodu. Z tego powodu nie zaleca się stosowania morfiny dożylnie w celu łagodzenia bólu podczas porodu.
Morfina podana zewnątrzoponowo lub podpajęczynówkowo łatwo przenika przez łożysko, co może powodować wystąpienie zaburzeń oddychania u noworodka. Badania kliniczne wykazały, że morfina podana zewnątrzoponowo podczas porodu łagodzi ból porodowy w niewielkim stopniu lub nie działa przeciwbólowo.
Karmienie piersią
Morfina przenika do mleka kobiet karmiących piersią. Nie ustalono, jaki wpływ wywiera morfina zawarta w mleku kobiecym na karmione przez nią niemowlę.
Płodność
W badaniach na zwierzętach wykazano, że morfina może powodować zmniejszenie płodności (patrz punkt 5.3 Przedkliniczne dane dotyczące bezpieczeństwa stosowania).
Morfina zaburza sprawność psychofizyczną. Podczas stosowania produktu nie należy prowadzić pojazdów i obsługiwać maszyn.
Działania niepożądane podano według klasyfikacji układ/narząd i częstości: często (≥1/100 do <1/10), nieznana (częstość nie może być określona na podstawie dostępnych danych).
Zaburzenia układu immunologicznego Częstość nieznana:
Reakcje anafilaktoidalne.
Zaburzenia psychiczne Częstość nieznana:
Nastrój dysforyczny, niepokój, psychozy (po zastosowaniu dużych dawek morfiny). Euforia, stany lękowe.
Uzależnienie - psychiczne i fizyczne (po długotrwałym stosowaniu morfiny, niezależnie od drogi podania) - po nagłym odstawieniu może prowadzić do wystąpienia objawów zespołu odstawiennego. Jednak u chorych, otrzymujących morfinę ze wskazań medycznych uzależnienie jest rzadkością.
Zaburzenia układu nerwowego Częstość nieznana:
Drgawki.
Bóle głowy, zawroty głowy.
Allodynia, hiperalgezja (patrz punkt 4.4), nadmierna potliwość.
Duże dawki morfiny mogą powodować pobudzenie ośrodkowego układu nerwowego.
Zaburzenia serca i zaburzenia naczyniowe
Małe dawki morfiny nie mają dużego wpływu na układ sercowo-naczyniowy, duże natomiast mogą działać pobudzająco. Jest to związane z pobudzeniem aktywności układu współczulnego
i zwiększeniem stężenia katecholamin we krwi.
Zaburzenia układu oddechowego, klatki piersiowej i śródpiersia:
Częstość nieznana:
Zahamowanie ośrodka oddechowego - najpoważniejsze działanie niepożądane, które może wystąpić po podaniu morfiny dożylnie, zewnątrzoponowo albo podpajęczynówkowo.
Po jednorazowym podaniu morfiny zewnątrzoponowo lub podpajęczynówkowo może wystąpić
wczesne lub późne (do 24 godzin) zahamowanie ośrodka oddechowego. Objawy takie obserwowano częściej po podaniu podpajęczynówkowym niż zewnątrzoponowym i podczas stosowania dawek większych niż zwykle zalecane. Zahamowanie czynności oddechowej może wymagać interwencji
lekarza. W związku z opóźnionym działaniem morfiny na ośrodkowy układ nerwowy, zbyt szybkie podanie dożylne może spowodować wystąpienie objawów przedawkowania.
Zniesienie odruchu kaszlu.
Zaburzenia żołądka i jelit Częstość nieznana:
Suchość w ustach.
Nudności, wymioty, zaparcia.
Zaburzenia skóry i tkanki podskórnej
Świąd – może wystąpić często po podaniu zewnątrzoponowym lub podpajęczynówkowym pojedynczej dawki morfiny, nie tylko w miejscu wstrzyknięcia. Występowanie świądu po podaniu morfiny zewnątrzoponowo lub podpajęczynówkowo we wlewie ciągłym jest sporadycznie odnotowywane w literaturze; nie wyjaśniono przyczyn występowania tych reakcji. Świąd może zostać zniesiony przez dożylne podawanie małej dawki naloksonu (0,2 mg).
Pokrzywka, bąbel pokrzywkowy i (lub) miejscowe podrażnienia tkanek - reakcje związane z wydzielaniem histaminy.
Zaburzenia nerek i dróg moczowych:
Zatrzymanie moczu – występuje często i może utrzymywać się przez 10 do 20 godzin po
pojedynczym zewnątrzoponowym i podpajęczynówkowym podaniu produktu i jest działaniem niepożądanym, którego można się spodziewać przede wszystkim u mężczyzn (u kobiet występuje
rzadziej). Również często odnotowywano w literaturze występowanie zatrzymania moczu podczas kilku dni hospitalizacji z powodu rozpoczęcia ciągłego podawania morfiny podpajęczynówkowo lub zewnątrzoponowo. U pacjentów, u których wystąpi zatrzymanie moczu należy zastosować leczenie z użyciem leków cholinomimetycznych i (lub) cewnikowanie pęcherza moczowego.
Zatrzymanie moczu może zostać zniesione przez dożylne podawanie małej dawki naloksonu (0,2 mg). Skąpomocz.
Zaburzenia ogólne i stany w miejscu podania Częstość nieznana:
Zespół odstawienny (abstynencyjny).
Uzależnienie od leku i zespół odstawienny (abstynencyjny)
Stosowanie opioidowych leków przeciwbólowych może prowadzić do rozwoju fizycznego i (lub) psychicznego uzależnienia bądź tolerancji. Wystąpienie zespołu abstynencyjnego może zostać
przyspieszone, jeśli nagle zaprzestanie się podawania leku opioidowego lub antagonistów receptorów opioidowych, a czasami może do niego dojść między kolejnymi dawkami. Informacje dotyczące postępowania - patrz punkt 4.4.
Fizjologiczne objawy odstawienia obejmują: bóle ciała, drgawki, zespół niespokojnych nóg, biegunka, kolka brzuszna, nudności, objawy grypopodobne, tachykardia i rozszerzenie źrenic. Do objawów psychicznych należą: nastrój dysforyczny, niepokój i drażliwość. U osób uzależnionych od leków
często występuje „głód lekowy”.
U niektórych pacjentów podczas leczenia może rozwinąć się tolerancja na morfinę, dlatego może być konieczne podawanie coraz większych dawek dla uzyskania tego samego działania przeciwbólowego. Zaburzenia ośrodka termoregulacji.
Zgłaszanie podejrzewanych działań niepożądanych
Po dopuszczeniu produktu leczniczego do obrotu istotne jest zgłaszanie podejrzewanych działań
niepożądanych. Umożliwia to nieprzerwane monitorowanie stosunku korzyści do ryzyka stosowania produktu leczniczego. Osoby należące do fachowego personelu medycznego powinny zgłaszać wszelkie podejrzewane działania niepożądane za pośrednictwem Departamentu Monitorowania
Niepożądanych Działań Produktów Leczniczych Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych
Al. Jerozolimskie 181C 02-222 Warszawa
Tel.: + 48 22 49 21 301
Faks: + 48 22 49 21 309
Strona internetowa: https://smz.ezdrowie.gov.pl
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Do wystąpienia objawów przedawkowania morfiny może dojść w wyniku podania zbyt dużej dawki produktu, niezamierzonego podania podpajęczynówkowego lub jednoczesnego stosowania innych opioidowych leków przeciwbólowych.
Objawami przedawkowania są: zahamowanie oddychania - niewydolność układu oddechowego może prowadzić do śmierci, senność przechodząca w śpiączkę, zwężone, niereagujące na światło (szpilkowate) źrenice. Zahamowanie czynności układu oddechowego może wystąpić do 24 godzin po podaniu podpajęczynówkowym i spowodować niedotlenienie narządów i tkanek.
Może wystąpić zachłystowe zapalenie płuc.
Należy zastosować oddech wspomagany lub zastępczy, podać tlen. Specyficzną odtrutką jest nalokson. Ponieważ czas działania naloksonu jest krótszy niż morfiny podanej zewnątrzoponowo lub podpajęczynówkowo, należy stosować powtarzane wstrzyknięcia lub ciągły wlew dożylny, aby
zapobiec nawrotowi objawów zatrucia. Jednocześnie należy prowadzić ogólne leczenie objawowe, zabezpieczyć pacjenta przed utratą ciepła i uzupełniać płyny.
Grupa farmakoterapeutyczna: leki przeciwbólowe; naturalne alkaloidy opium Kod ATC: N02AA01
Morfina jest alkaloidem opium. Jest silnym opioidowym lekiem przeciwbólowym, skutecznym
w leczeniu bólów pochodzenia nocyceptywnego. Działa poprzez receptory opioidowe rozmieszczone w ośrodkowym układzie nerwowym. Szczególne powinowactwo wykazuje do receptorów mi (μ).
Zastosowanie drogi zewnątrzoponowej lub podpajęczynówkowej zapewnia długotrwałe działanie przeciwbólowe bez zaburzenia czynności motorycznych, czucia i czynności układu współczulnego.
Morfina działa przeciwbólowo poprzez ośrodkowy układ nerwowy oraz na narządy zawierające
mięśnie gładkie, wywołując także senność, zmiany nastroju, obniżenie temperatury ciała, zależne od dawki zahamowanie czynności oddechowej. Działanie przeciwbólowe powodowane jest również przez modyfikację uwalniania substancji neuroprzekaźnikowych z włókien nerwowych aferentnych. Do migracji i zwiększonej koncentracji receptorów opioidowych dochodzi w tkankach zmienionych zapalnie, co wpływa na obwodowe działanie przeciwbólowe morfiny.
Morfina wywiera też działania obwodowe: rozszerza naczynia krwionośne, zwiększa napięcie mięśniówki gładkiej przewodu pokarmowego i dróg moczowych. Działanie to może powodować opóźnienie opróżniania żołądka, przedłużenie przebywania treści pokarmowej w żołądku,
zahamowanie perystaltyki jelit, zaparcia, zwiększenie ciśnienia w drogach żółciowych, zaburzenia oddawania moczu. Morfina hamuje czynność wydzielniczą kory nadnerczy pod wpływem czynników stresowych. Nie wpływa natomiast na mięśnie gładkie naczyń krwionośnych i macicy.
Morfina nie wpływa na odruchy ścięgniste (np. rzepkowy oraz ze ścięgna Achillesa) oraz
autonomiczne. Opioidowe leki przeciwbólowe mogą powodować uwalnianie histaminy, co u pacjentów z astmą może wywołać skurcz oskrzeli.
Wchłanianie
Morfina podana zewnątrzoponowo, szybko przenika do krążenia ogólnego. Wchłanianie jest tak szybkie, że zależność stężenia od czasu w osoczu jest bardzo zbliżona do wartości uzyskanych po podaniu dożylnym i domięśniowym.
Stężenie we krwi
Po podaniu dożylnym maksymalne stężenie morfiny w surowicy występuje po 30 sekundach, a po 15- 30 minutach w płynie mózgowo-rdzeniowym. Maksymalne działanie przeciwbólowe występuje po
30-45 minutach od podania.
Po podaniu zewnątrzoponowym i podpajęczynówkowym maksymalne stężenie morfiny w surowicy występuje po 30 minutach i zmniejsza się do bardzo małych wartości w okresie 2-4 godzin. Działanie przeciwbólowe występuje po 15-60 minutach od podania i utrzymuje się do 24 godzin, dlatego wystarczające jest podawanie morfiny 1 lub 2 razy na dobę.
Okres półtrwania
Okres półtrwania wynosi odpowiednio 2-2,5 godziny po podaniu doustnym i 1,5-2 godzin po podaniu parenteralnym.
Dystrybucja
Około 30% morfiny wiąże się z białkami surowicy. Niezwiązana część morfiny ulega szybkiej redystrybucji do tkanek.
Metabolizm
W wątrobie morfina ulega przemianom do 6-glukuronianu morfiny (aktywna postać) oraz 3-glukuronianu morfiny (postać nieaktywna).
Eliminacja
Około 90% podanej morfiny jest wydalane w czasie 24 godzin z moczem, a 10% w postaci glukuronianów z kałem. W niewydolności nerek dochodzi do kumulacji metabolitów, co może powodować wystąpienie objawów niepożądanych.
Szczegółowe dane na temat farmakokinetyki morfiny podanej zewnątrzoponowo i podpajęczynówkowo
Morfina podana do przestrzeni zewnątrzoponowej szybko przenika do krążenia ogólnego.
Wchłanianie jest tak szybkie, że zależność stężenia od czasu w osoczu jest bardzo zbliżona do
wartości uzyskanych po podaniu dożylnym i domięśniowym. Po podaniu 3 mg morfiny maksymalne stężenie w osoczu wynosi średnio 33-40 ng/ml (zakres 5-62 ng/ml) i jest osiągane w ciągu 10 do
15 minut. Okres półtrwania w fazie eliminacji wynosi od 39 do 249 minut (średnio 90+/- 34,3 min) i choć krótszy, rząd wielkości jest zbliżony do wartości odnotowywanych po podaniu dożylnym lub domięśniowym (1,5 do 4,5 godzin).
Po zewnątrzoponowym podaniu morfiny w dawce 2 do 6 mg pacjentom po zabiegu chirurgicznym, stężenie morfiny w płynie mózgowo-rdzeniowym jest 50 do 250 razy większe niż stężenie stwierdzane w osoczu. Stężenie morfiny stwierdzane w płynie mózgowo-rdzeniowym przewyższa stężenie stwierdzane w osoczu tylko przez 15 minut i jest możliwe do oznaczenia przez 20 godzin po podaniu 2 mg morfiny zewnątrzoponowo. Około 4% dawki podanej zewnątrzoponowo przenika do płynu mózgowo-rdzeniowego. Koresponduje to ze względnie minimalną skuteczną dawką morfiny (5 mg i 0,25 mg) podawaną zewnątrzoponowo lub podpajęczynówkowo. Dane dotyczące morfiny
w odniesieniu do płynu mózgowo-rdzeniowego wynikają z fazy eliminacji (t 0,5 – ok. 1,5 godziny)
i późniejszej fazy eliminacji wynoszącej około 6 godzin. Morfina przenika przez oponę twardą powoli z okresem połowicznego wchłaniania średnio 22 minuty. Maksymalne stężenie w płynie mózgowo- rdzeniowym morfiny występowało w ciągu 60-90 minut po iniekcji. Minimalne skuteczne stężenie
w płynie mózgowo-rdzeniowym w przypadku pooperacyjnej analgezji wynosiło 150 ng/ml (zakres 1- 380 ng/ml).
Po podaniu podpajęczynówkowym morfina przenika barierę krew-mózg i w wyniku tego, małe dawki morfiny podane tą drogą wywołują porównywalne działanie przeciwbólowe jak po podaniu
zewnątrzoponowym. Po wstrzyknięciu morfiny w bolusie jednorazowej dawki morfiny, szybka faza dystrybucji trwająca 15-30 minut i okres półtrwania w płynie mózgowo-rdzeniowym wynosi 42-136 minut (90 +/- 16 minut). Biorąc pod uwagę ograniczone dane wydaje się, że obecność morfiny
w płynie mózgowo-rdzeniowym od 15 minut po podaniu podpajęczynówkowym do końca trwającej 6 godzin obserwacji jest wypadkową faz dystrybucji i eliminacji. Stężenie morfiny w płynie mózgowo-rdzeniowym po podaniu jednorazowej dawki 0,3 mg morfiny wynosi średnio 332+/-137 ng/ml w 6 godzin. Objętość dystrybucji morfiny podanej podpajęczynówkowo wynosi około 22+/-8 ml.
Zależność maksymalnego stężenia w osoczu od czasu jest podobna (5-10 minut) zarówno po podaniu morfiny w bolusie zewnątrzoponowo, jak i podpajęczynówkowo. Maksymalne stężenie morfiny
w osoczu po podaniu podpajęczynówkowym 0,3 mg morfiny wynosiło poniżej 7,8 ng/ml. Minimalne stężenie morfiny, które działało przeciwbólowo podczas podawania metodą PCA wynosiło 20-
40 ng/ml, co sugeruje, że działanie przeciwbólowe wynikające z redystrybucji systemowej było minimalne przez pierwsze 30-60 minut po podaniu zewnątrzoponowym i niedostrzegalne po podpajęczynówkowym podaniu morfiny.
Nie prowadzono badań na zwierzętach dotyczących działania rakotwórczego i mutagennego morfiny.
U samców szczurów stwierdzono zmniejszenie płodności i uszkodzenia chromosomów w gametach.
Sodu chlorek
Woda do wstrzykiwań
Wykazano niezgodność fizykochemiczną (powstawanie osadów) między roztworami siarczanu morfiny i 5-fluorouracylu.
Morfina tworzy nierozpuszczalne kompleksy z heparyną. Nie należy mieszać morfiny z heparyną w jednym roztworze.
2 lata
Przechowywać ampułki w opakowaniu oryginalnym w celu ochrony przed światłem. Nie zamrażać.
Ampułki ze szkła bezbarwnego w tekturowym pudełku 10 ampułek o pojemności 2 ml
Produktu Morphini sulfas WZF 0,1% Spinal nie należy wyjaławiać termicznie. Produkt nie zawiera środków konserwujących.
Nie stosować w przypadku widocznej zmiany barwy.
Instrukcja otwierania ampułki
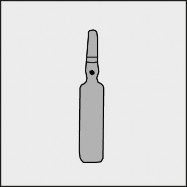
Przed otwarciem ampułki należy upewnić się, że cały roztwór znajduje się w dolnej części ampułki. Można delikatnie potrząsnąć ampułką lub postukać w nią palcem, aby ułatwić spłynięcie roztworu.
Na każdej ampułce umieszczono kolorową kropkę (patrz rysunek 1.) jako oznaczenie znajdującego się poniżej niej punktu nacięcia.
Ampułki są przeznaczone wyłącznie do jednorazowego użytku, należy je otwierać bezpośrednio przed użyciem. Pozostałą zawartość niezużytego produktu należy zniszczyć zgodnie z obowiązującymi przepisami.
Rysunek 1.
Rysunek 2.
Rysunek 3.
Warszawskie Zakłady Farmaceutyczne Polfa S.A. ul. Karolkowa 22/24; 01-207 Warszawa
Pozwolenie nr 10401
Data wydania pierwszego pozwolenia na dopuszczenie do obrotu: 15.04.2004 r. Data ostatniego przedłużenia pozwolenia: 20.01.2014 r.











