Spis treści:
- NAZWA PRODUKTU LECZNICZEGO
- SKŁAD JAKOŚCIOWY I ILOŚCIOWY
- POSTAĆ FARMACEUTYCZNA
- SZCZEGÓŁOWE DANE KLINICZNE
- WŁAŚCIWOŚCI FARMAKOLOGICZNE
- DANE FARMACEUTYCZNE
- PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO
- NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
- DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU I DATA PRZEDŁUŻENIA POZWOLENIA
- DATA ZATWIERDZENIA LUB CZĘŚCIOWEJ ZMIANY TEKSTU CHARAKTERYSTYKI
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
NAZWA PRODUKTU LECZNICZEGO
SKŁAD JAKOŚCIOWY I ILOŚCIOWY
POSTAĆ FARMACEUTYCZNA
SZCZEGÓŁOWE DANE KLINICZNE
Wskazania do stosowania
Dawkowanie i sposób podawania
pacjenci niedożywieni lub źle odżywieni;
z ciężkimi lub niedostatecznie wyrównanymi zaburzeniami endokrynologicznymi (niedoczynność przysadki, niedoczynność tarczycy, niewydolność nadnerczy);
po zaprzestaniu długotrwałego leczenia i (lub) leczenia dużymi dawkami kortykosteroidów;
z ciężkimi chorobami tętnic (ciężka choroba wieńcowa, ciężka niewydolność tętnicy szyjnej, choroba naczyń obwodowych).
Zaleca się stosowanie minimalnej dobowej dawki początkowej 30 mg.
Dzieci i młodzież
Nie ustalono bezpieczeństwa stosowania i skuteczności produktu Diamicron 30 mg u dzieci i młodzieży.
Brak danych dotyczących stosowania u dzieci.
Przeciwwskazania
nadwrażliwości na gliklazyd lub na którąkolwiek substancję pomocniczą wymienioną w punkcie 6.1, inne pochodne sulfonylomocznika, sulfonamidy;
cukrzycy typu 1;
stanu przedśpiączkowego i śpiączki cukrzycowej, ketozy i kwasicy cukrzycowej;
ciężkiej niewydolności nerek lub wątroby: w tych przypadkach zaleca się zastosowanie insuliny;
leczenia mikonazolem (patrz punkt 4.5);
laktacji (patrz punkt 4.6).
Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania
brak współpracy ze strony pacjenta (zwłaszcza u osób w podeszłym wieku);
niedożywienie, nieregularne pory spożywania posiłków, opuszczanie posiłków, okresy poszczenia lub
zmiany w diecie;
brak równowagi pomiędzy wysiłkiem fizycznym a podażą węglowodanów;
niewydolność nerek;
ciężka niewydolność wątroby;
przedawkowanie produktu Diamicron 30 mg;
niektóre zaburzenia endokrynologiczne: zaburzenia czynności tarczycy, niedoczynność przysadki oraz niewydolność nadnerczy;
równoczesne podawanie pewnych leków (patrz punkt 4.5).
Niewydolność nerek i wątroby: farmakokinetyka i (lub) farmakodynamika gliklazydu może być zmieniona u pacjentów z niewydolnością wątroby lub ciężką niewydolnością nerek.
U tych pacjentów hipoglikemia może się przedłużać, co może wymagać odpowiedniego postępowania.
Informowanie pacjenta
Ryzyko hipoglikemii, jej objawy (patrz punkt 4.8), leczenie i czynniki predysponujące do jej wystąpienia, należy wyjaśnić pacjentowi oraz członkom jego rodziny.
Pacjent powinien być poinformowany o istotnej roli, jaką spełniają zalecenia dietetyczne, regularne uprawianie ćwiczeń oraz regularne oznaczanie stężenia glukozy we krwi.
Słaba kontrola glikemii: kontrolę glikemii u pacjentów otrzymujących leki przeciwcukrzycowe może zaburzać: stosowanie preparatów zawierających ziele dziurawca zwyczajnego (Hypericum perforatum)(patrz punkt 4.5), gorączka, uraz, infekcja lub zabieg chirurgiczny. W niektórych przypadkach może być konieczne podanie insuliny.
Skuteczność działania hipoglikemizującego jakiegokolwiek doustnego leku przeciwcukrzycowego, w tym gliklazydu, z czasem ulega osłabieniu u wielu pacjentów: może to wynikać ze stopniowego nasilenia się cukrzycy lub ze zmniejszenia reakcji na leczenie. Zjawisko to, znane jest jako wtórne niepowodzenie terapeutyczne, w odróżnieniu od pierwotnego, kiedy to substancja czynna jest nieskuteczna w leczeniu pierwszego rzutu. Przed stwierdzeniem wystąpienia u pacjenta wtórnego niepowodzenia terapeutycznego należy rozważyć odpowiednie dostosowanie dawki oraz opracowanie diety.
Zaburzenia stężenia glukozy we krwi
U pacjentów z cukrzycą leczonych jednocześnie fluorochinolonami, zwłaszcza w podeszłym wieku, zgłaszano zaburzenia stężenia glukozy we krwi, w tym hipoglikemię i hiperglikemię. U wszystkich pacjentów stosujących w tym samym czasie Diamicron 30 mg i fluorochinolony zaleca się staranne monitorowanie stężenia glukozy we krwi.
Badania laboratoryjne: oznaczanie stężeń glikozylowanej hemoglobiny (lub pomiar glukozy w osoczu na czczo) zaleca się do oceny kontroli glikemii. Użyteczna jest również samokontrola stężenia glukozy we krwi.
Stosowanie pochodnych sulfonylomocznika u pacjentów z niedoborem dehydrogenazy glukozo-6-fosforano- wej może prowadzić do rozwoju niedokrwistości hemolitycznej. Ponieważ gliklazyd należy do pochodnych sulfonylomocznika, u pacjentów z niedoborem dehydrogenazy glukozo-6-fosforanowej należy zachować ostrożność i rozważyć zastosowanie leczenia lekami, nie będącymi pochodnymi
sulfonylomocznika.
Pacjenci z porfirią
U pacjentów z porfirią opisano przypadki zaostrzenia porfirii po zastosowaniu niektórych innych leków pochodnych sulfonylomocznika.
Interakcje z innymi produktami leczniczymi i inne rodzaje interakcji
Mikonazol (stosowany ogólnie, żel do stosowania w jamie ustnej): nasila działanie hipoglikemizujące z możliwością wywołania objawów hipoglikemii, lub nawet śpiączki.
Równoczesne stosowanie niezalecane
Fenylbutazon (stosowany ogólne): nasila działanie hipoglikemizujące pochodnych sulfonylomocznika (rozerwanie połączeń z białkami osocza i (lub) zmniejszenie ich wydalania).
Jest zalecane zastosowanie innego leku przeciwzapalnego, o ryzyku należy poinformować pacjenta
i podkreślić istotną rolę samokontroli.
W razie konieczności należy dostosować dawkę w trakcie i po zakończeniu leczenia lekiem
przeciwzapalnym.
Alkohol: nasila działanie hipoglikemizujące (przez blokowanie reakcji kompensacyjnych), co może pro-
wadzić do wystąpienia śpiączki hipoglikemicznej.
Należy unikać spożywania alkoholu lub leków zawierających alkohol.
Równoczesne stosowanie z ostrożnością
Nasilenie działania zmniejszającego stężenie glukozy we krwi i w niektórych przypadkach hipoglikemia może wystąpić podczas jednoczesnego przyjmowania następujących preparatów: inne leki przeciwcukrzycowe (insulina, akarboza, metformina, tiazolidynediony, inhibitory peptydazy dipeptydylowej IV, agoniści receptora GLP-1), leki blokujące receptory adrenergiczne,
flukonazol, inhibitory konwertazy angiotensyny (kaptopryl, enalapryl), leki blokujące receptory H2, inhibitory MAO, sulfonamidy, klarytromycyna i niesteroidowe leki przeciwzapalne.
Następujące produkty mogą zwiększać stężenie glukozy we krwi
Równoczesne stosowanie niezalecane
Danazol: wpływ diabetogenny danazolu.
Jeżeli zastosowania tej substancji czynnej nie można uniknąć, pacjenta należy ostrzec i podkreślić znaczenie kontroli stężenia glukozy we krwi i w moczu. W razie konieczności należy dostosować dawkę gliklazydu w trakcie i po zakończeniu leczenia danazolem.
Równoczesne stosowanie z ostrożnością
Chlorpromazyna (lek neuroleptyczny): duże dawki (> 100 mg/dobę) zwiększają stężenie glukozy we
krwi (zmniejszenie wydzielania insuliny).
Należy uprzedzić pacjenta i podkreślić istotność monitorowania stężenia glukozy we krwi. Może być konieczne dostosowanie dawki przeciwcukrzycowej substancji czynnej podczas i po zakończeniu
leczenia lekiem neuroleptycznym.
Glikokortykosteroidy (podane ogólnie i miejscowo: preparaty dostawowe, na skórę i doodbytnicze) oraz tetrakozaktyd: zwiększenie stężenia glukozy we krwi z możliwą kwasicą ketonową (zmniejszona tolerancja na węglowodany spowodowana przez glikokortykosteroidy). Należy uprzedzić pacjenta
i podkreślić istotność monitorowania stężenia glukozy we krwi, zwłaszcza na początku leczenia. Może być konieczne dostosowanie dawki przeciwcukrzycowej substancji czynnej podczas i po zakończeniu leczenia glikokortykosteroidami.
Rytodryna, salbutamol, terbutalina (dożylnie)
Zwiększenie stężenia glukozy następuje w związku z pobudzeniem receptorów beta-2. Należy podkreślić istotność monitorowania stężenia glukozy we krwi. W razie konieczności należy zastosować insulinoterapię.
Preparaty zawierające ziele dziurawca zwyczajnego (Hypericum perforatum)
Wpływ na płodność, ciążę i laktację
Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn
Działania niepożądane
zaburzenia skóry i tkanki podskórnej: wysypka, świąd, pokrzywka, obrzęk naczynioruchowy, rumień, wykwity plamkowo-grudkowe, odczyny pęcherzowe (takie jak zespół Stevensa-Johnsona, martwica toksyczno-rozpływna naskórka i autoimmunologiczne choroby pęcherzowe) i wyjątkowo wysypka polekowa z eozynofilią oraz objawami ogólnymi (DRESS, ang. Drug Rush with Eosinophilia and Systemic Symptoms).
zaburzenia krwi i układu chłonnego: zmiany w obrazie hematologicznym krwi występują rzadko; mogą one obejmować: niedokrwistość, leukopenię, małopłytkowość, granulocytopenię. Zmiany te przemijają po zaprzestaniu leczenia.
zaburzenia wątroby i dróg żółciowych: zwiększona aktywność enzymów wątrobowych (AspAT, AlAT, fosfatazy zasadowej), zapalenie wątroby (odosobnione przypadki). Należy przerwać leczenie w przypadku pojawienia się żółtaczki cholestatycznej.
Objawy te zazwyczaj przemijają po odstawieniu leku.
zaburzenia oka: przemijające zaburzenia widzenia mogą pojawiać się szczególnie na początku leczenia na skutek zmian stężeń glukozy we krwi.
działania niepożądane danej grupy leków:
Przedawkowanie
WŁAŚCIWOŚCI FARMAKOLOGICZNE
częściowe hamowanie agregacji i adhezji płytek przez zmniejszenie aktywności markerów płytek krwi (-tromboglobulina, tromboksan B2).
wpływ na aktywność fibrynolityczną śródbłonka naczyń przez zwiększenie aktywności tkankowego
Właściwości farmakokinetyczne
Przedkliniczne dane o bezpieczeństwie
DANE FARMACEUTYCZNE
Wykaz substancji pomocniczych
Niezgodności farmaceutyczne
Okres ważności
Specjalne środki ostrożności podczas przechowywania
Rodzaj i zawartość opakowania
Specjalne środki ostrożności dotyczące usuwania
PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO
NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU I DATA PRZEDŁUŻENIA POZWOLENIA
DATA ZATWIERDZENIA LUB CZĘŚCIOWEJ ZMIANY TEKSTU CHARAKTERYSTYKI
DIAMICRON 30 mg
30 mg, tabletki o zmodyfikowanym uwalnianiu
Jedna tabletka zawiera 30 mg gliklazydu (Gliclazidum).
Pełny wykaz substancji pomocniczych, patrz punkt 6.1.
Tabletka o zmodyfikowanym uwalnianiu.
Biała, podłużna tabletka z wytłoczeniem „DIA 30” z jednej strony i „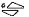 ” z drugiej strony.
” z drugiej strony.
Cukrzyca insulinoniezależna (typ 2) u osób dorosłych, kiedy przestrzeganie diety, ćwiczenia fizyczne oraz zmniejszenie masy ciała nie wystarczają do utrzymania prawidłowego stężenia glukozy we krwi.
Dawkowanie
Dawka dobowa wynosi od 1 tabletki do 4 tabletek na dobę, tj. od 30 do 120 mg przyjmowanych doustnie,
jednorazowo, w porze śniadania.
Tabletki (tabletkę) należy połykać w całości.
W przypadku pominięcia jednej dawki nie należy jej zwiększać w dniu następnym.
Podobnie jak w przypadku innych leków o działaniu hipoglikemizującym, dawka powinna być dostosowana indywidualnie w zależności od reakcji pacjenta (stężenie glukozy we krwi, HbA1c).
Dawka początkowa
Zalecana dawka początkowa wynosi 30 mg na dobę.
Jeśli stężenie glukozy we krwi jest skutecznie kontrolowane, dawka ta może być stosowana jako leczenie podtrzymujące.
Jeśli stężenie glukozy we krwi nie jest odpowiednio kontrolowane, dawkę można stopniowo zwiększyć do 60 mg, 90 mg lub 120 mg na dobę. Nie powinno się zwiększać dawki częściej, niż co najmniej po upływie 1 miesiąca, z wyjątkiem pacjentów, u których stężenie glukozy we krwi nie uległo zmniejszeniu po dwóch tygodniach leczenia. W takich przypadkach, dawkę można zwiększyć pod koniec drugiego tygodnia leczenia.
Maksymalna, zalecana dawka dobowa to 120 mg.
Zamiana tabletek produktu zawierającego 80 mg gliklazydu na produkt Diamicron 30 mg, tabletki o zmodyfikowanym uwalnianiu
1 tabletka produktu zawierającego 80 mg gliklazydu jest porównywalna z 1 tabletką produktu Diamicron 30 mg. Zmiana może być przeprowadzona pod warunkiem monitorowania parametrów krwi.
Zamiana innego, doustnego leku przeciwcukrzycowego na produkt Diamicron 30 mg
Diamicron 30 mg może być stosowany w celu zastąpienia innego, doustnego leku przeciwcukrzycowego. Podczas zamiany na produkt Diamicron 30 mg należy wziąć pod uwagę dawkę oraz okres półtrwania uprzednio stosowanego leku przeciwcukrzycowego.
Zastosowanie okresu przejściowego nie jest konieczne.
Należy zastosować dawkę początkową 30 mg i tak ją modyfikować, aby była dostosowana do reakcji stężenia glukozy we krwi danego pacjenta, tak jak to przedstawiono powyżej.
W razie zmiany z innych hipoglikemizujących pochodnych sulfonylomocznika o przedłużonym okresie półtrwania może być konieczna kilkudniowa przerwa w leczeniu, aby zapobiec wystąpieniu efektu addycyjnego dwóch preparatów, który może powodować hipoglikemię.
Schemat dawkowania w takich sytuacjach powinien być taki sam jak na początku stosowania produktu Diamicron 30 mg, tzn. leczenie należy rozpocząć od dawki 30 mg na dobę, a następnie ją zwiększać
w zależności od reakcji metabolicznej pacjenta.
Leczenie skojarzone z innymi lekami przeciwcukrzycowymi
Diamicron 30 mg może być stosowany z biguanidami, inhibitorami alfa-glukozydazy lub insuliną.
U pacjentów ze stężeniem glukozy we krwi niedostatecznie kontrolowanym z użyciem produktu Diamicron 30 mg leczenie skojarzone z insuliną powinno być wprowadzone pod ścisłą opieką medyczną.
Szczególne grupy pacjentów
Pacjenci w podeszłym wieku
Produkt Diamicron 30 mg należy stosować zgodnie z tymi samymi zasadami dawkowania, jakie są zalecane u pacjentów poniżej 65 lat.
Zaburzenie czynności nerek
U pacjentów z łagodną i umiarkowaną niewydolnością nerek powinny być zastosowane takie same zasady
dawkowania jak u pacjentów z prawidłową czynnością nerek. Pacjenci ci powinni pozostawać pod obserwacją. Dane te zostały potwierdzone w badaniach klinicznych.
Pacjenci z ryzykiem wystąpienia hipoglikemii:
Ten produkt leczniczy jest przeciwwskazany w przypadku:
Hipoglikemia
To leczenie powinno być stosowane jedynie u pacjentów regularnie odżywiających się (dotyczy śniadania). Jest ważne, aby regularnie spożywać węglowodany ze względu na zwiększone ryzyko hipoglikemii, jeśli posiłek jest przyjęty późno, jeśli spożyta jest nieodpowiednia ilość pokarmu lub posiłek zawiera mało węglowodanów. Hipoglikemia częściej pojawia się podczas stosowania diet niskokalorycznych,
w następstwie długotrwałego lub forsownego wysiłku fizycznego, picia alkoholu lub w przypadku, gdy
zastosowano leczenie skojarzone lekami przeciwcukrzycowymi.
Hipoglikemia może wystąpić w następstwie stosowania pochodnych sulfonylomocznika (patrz punkt 4.8). Niektóre przypadki ciężkiej i przedłużonej hipoglikemii mogą wymagać leczenia szpitalnego i podawania glukozy przez kilka dni.
Aby zmniejszyć ryzyko hipoglikemii, należy ostrożnie dobierać pacjentów oraz ustalać dawkę, a pacjentów należy odpowiednio poinformować.
Czynniki zwiększające ryzyko wystąpienia hipoglikemii:
Następujące produkty zazwyczaj zwiększają ryzyko hipoglikemii
Równoczesne stosowanie przeciwwskazane
Ziele dziurawca zwyczajnego (Hypericum perforatum) zmniejsza ekspozycję na gliklazyd. Należy podkreślić znaczenie monitorowania stężenia glukozy we krwi.
Następujące produkty mogą powodować zaburzenia stężenia glukozy we krwi
Równoczesne stosowanie wymagające ostrożności podczas stosowania
- Fluorochinolony: w przypadku jednoczesnego stosowania produktu Diamicron 30 mg i fluorochino- lonów należy ostrzec pacjenta o ryzyku zaburzenia stężeń glukozy we krwi i należy podkreślić zna- czenie monitorowania stężenia glukozy we krwi.
Równoczesne stosowanie po rozważeniu ryzyka
- Leki przeciwzakrzepowe (np. warfaryna). Pochodne sulfonylomocznika mogą nasilać działanie przeciwzakrzepowe podczas jednoczesnego leczenia. Może być konieczna zmiana leku przeciwzakrzepowego.
Ciąża
Brak danych lub istnieją tylko ograniczone dane (mniej niż 300 kobiet w ciąży) dotyczące stosowania gliklazydu u kobiet w ciąży, aczkolwiek istnieją nieliczne dane dotyczące innych pochodnych sulfonylomocznika.
W badaniach na zwierzętach gliklazyd nie wykazywał działania teratogennego (patrz punkt 5.3).
W celu zachowania ostrożności zaleca się unikanie stosowania gliklazydu podczas ciąży.
Normoglikemię należy uzyskać przed poczęciem, w celu zmniejszenia niebezpieczeństwa wystąpienia wad wrodzonych u płodu w wyniku niewyrównanej cukrzycy u matki.
Stosowanie doustnych leków hipoglikemizujących jest niewłaściwe. Lekiem pierwszego wyboru
w leczeniu cukrzycy u kobiet w ciąży jest insulina.
Zaleca się odstawienie doustnych leków hipoglikemizujących i rozpoczęcie insulinoterapii przed próbą zajścia w ciążę, lub niezwłocznie po jej stwierdzeniu.
Karmienie piersią
Nie wiadomo, czy gliklazyd lub jego metabolity przenikają do mleka ludzkiego. Zważywszy na niebezpieczeństwo wystąpienia hipoglikemii u noworodka stosowanie leku jest zatem przeciwwskazane u kobiet karmiących piersią. Nie można wykluczyć zagrożenia dla noworodków lub dzieci.
Płodność
Nie odnotowano wpływu na płodność albo zdolność do rozrodu u samców lub samic szczurów (patrz punkt 5.3).
Produkt Diamicron 30 mg nie ma lub ma znikomy wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn. Jednakże należy poinformować pacjenta o ryzyku wystąpienia hipoglikemii i jej objawach oraz zachowania ostrożności w czasie prowadzenia pojazdów i obsługiwania maszyn, zwłaszcza na początku leczenia.
Na podstawie doświadczenia ze stosowaniem gliklazydu donoszono o następujących działaniach niepożądanych.
Najczęstszym działaniem niepożądanym gliklazydu jest hipoglikemia.
Tak jak w przypadku innych pochodnych sulfonylomocznika leczenie produktem Diamicron 30 mg może powodować hipoglikemię, jeśli posiłki są nieregularne, a zwłaszcza, gdy są pomijane.
Możliwe objawy hipoglikemii to: ból głowy, silny głód, nudności, wymioty, zmęczenie, zaburzenia snu, pobudzenie, agresja, osłabiona koncentracja, zaburzenia świadomości oraz spowolnienie reakcji, depresja, uczucie splątania, zaburzenia widzenia i mowy, afazja, drżenie, niedowład, zaburzenia czucia, zawroty głowy, uczucie bezsilności, utrata samokontroli, majaczenie, drgawki, płytki oddech, bradykardia, senność i utrata świadomości, co może prowadzić do śpiączki oraz zgonu.
Dodatkowo mogą być obserwowane objawy pobudzenia adrenergicznego, takie jak: pocenie się, wilgotność skóry, niepokój, tachykardia, nadciśnienie, kołatanie serca, dławica piersiowa oraz zaburzenia rytmu serca. Zazwyczaj objawy ustępują po podaniu węglowodanów (cukier). Należy jednak pamiętać, że sztuczne substancje słodzące nie wywołują żadnego efektu. Doświadczenia z innymi pochodnymi sulfonylomocznika pokazują, że hipoglikemia może wystąpić ponownie nawet, jeśli pomiary początkowo wskazują
na skuteczność leczenia.
W przypadku ciężkiej lub długotrwałej hipoglikemii, nawet jeśli jest okresowo kontrolowana poprzez spożycie cukru, niezwłocznie należy rozpocząć leczenie lub nawet może być konieczna hospitalizacja.
Donoszono o zaburzeniach żołądkowo–jelitowych, takich jak: ból brzucha, nudności, wymioty, niestrawność, biegunka oraz zaparcia: można ich uniknąć lub można je zminimalizować przyjmując gliklazyd w trakcie śniadania.
Następujące działania niepożądane są rzadziej obserwowane:
Tak jak po innych pochodnych sulfonylomocznika obserwowano następujące zdarzenia niepożądane: przypadki erytrocytopenii, agranulocytozy, niedokrwistości hemolitycznej, pancytopenii, alergicznego zapalenia naczyń, hiponatremii, zwiększenia aktywności enzymów wątrobowych, a nawet zaburzenia czynności wątroby (np. z zastojem żółci i żółtaczką) oraz zapalenie wątroby, które przemijało po odstawieniu pochodnej sulfonylomocznika lub
w odosobnionych przypadkach prowadziło do zagrażającej życiu niewydolności wątroby.
Zgłaszanie podejrzewanych działań niepożądanych
Po dopuszczeniu produktu leczniczego do obrotu istotne jest zgłaszanie podejrzewanych działań niepożądanych. Umożliwia to nieprzerwane monitorowanie stosunku korzyści do ryzyka stosowania produktu leczniczego. Osoby należące do fachowego personelu medycznego powinny zgłaszać wszelkie podejrzewane działania niepożądane za pośrednictwem Departamentu Monitorowania Niepożądanych Działań Produktów Leczniczych Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych
Al. Jerozolimskie 181C 02-222 Warszawa
Tel.: + 48 22 49 21 301
Faks: + 48 22 49 21 309
Strona internetowa: https://smz.ezdrowie.gov.pl
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Przedawkowanie pochodnych sulfonylomocznika może wywołać hipoglikemię.
Nieznaczne objawy hipoglikemii, bez utraty przytomności lub objawów neurologicznych muszą być
korygowane poprzez podanie węglowodanów, dostosowanie dawki i (lub) zmianę diety.
Pacjent powinien być pod ścisłą obserwacją aż do momentu, gdy lekarz nie upewni się, że zagrożenie minęło.
Ciężkie objawy hipoglikemii ze śpiączką, drgawkami lub innymi zaburzeniami neurologicznymi muszą być leczone w ramach natychmiastowej pomocy medycznej z niezwłoczną hospitalizacją włącznie.
W razie rozpoznania lub podejrzenia śpiączki hipoglikemicznej należy podać pacjentowi w szybkim wlewie dożylnym 50 ml hipertonicznego roztworu glukozy (20-30%). Następnie należy podać we wlewie ciągłym 10% roztwór glukozy wystarczający do utrzymania stężenia glukozy we krwi powyżej 1 g/l. Pacjenci powinni być pod ścisłą obserwacją i w zależności od późniejszego stanu lekarz zadecyduje, czy dalsza obserwacja jest konieczna. Dializa nie jest skuteczna u pacjentów ze względu na silne wiązanie się gliklazydu z białkami osocza.
5.1. Właściwości farmakodynamiczne
Grupa farmakoterapeutyczna: sulfonamidy, pochodne mocznika. kod ATC: A10BB09
Mechanizm działania
Gliklazyd jest substancją czynną, doustną, hipoglikemizującą pochodną sulfonylomocznika, o działaniu przeciwcukrzycowym, różni się od innych pochodnych heterocyklicznym pierścieniem z wbudowanym atomem azotu.
Gliklazyd zmniejsza stężenie glukozy we krwi pobudzając wydzielanie insuliny przez komórki beta wysp Langerhansa. Zwiększone poposiłkowe wydzielanie insuliny i białka C w trzustce utrzymuje się nawet po dwóch latach leczenia.
Poza działaniem na metabolizm, gliklazyd wpływa również na naczynia krwionośne.
Działanie farmakodynamiczne
Wpływ na uwalnianie insuliny
W cukrzycy typu 2, gliklazyd przywraca wczesny wzrost wydzielania insuliny w obecności glukozy oraz nasila drugą fazę wydzielania insuliny.
Znamienny wzrost wydzielania insuliny jest obserwowany jako odpowiedź na stymulację indukowaną pokarmem lub glukozą.
Wpływ na naczynia krwionośne
Gliklazyd zmniejsza proces formowania się mikrozakrzepów w dwóch mechanizmach, które mogą leżeć u podstaw powikłań cukrzycy przez:
aktywatora plazminogenu (tPA).
Wchłanianie
Po podaniu doustnym stężenie leku w osoczu zwiększa się stopniowo przez 6 godzin, a następnie pozostaje na niezmienionym poziomie pomiędzy szóstą a dwunastą godziną. Różnice międzyosobnicze są nieznaczne. Wchłanianie gliklazydu jest całkowite. Posiłek nie wpływa na szybkość ani na stopień wchłaniania.
Dystrybucja
Wiązanie z białkami osocza wynosi ok. 95%. Objętość dystrybucji wynosi około 30 l. Jednorazowa dawka dobowa produktu Diamicron 30 mg umożliwia utrzymanie stężenia gliklazydu w osoczu przez ponad 24 godziny.
Metabolizm
Gliklazyd jest metabolizowany głównie w wątrobie i wydalany z moczem, przy czym wykrywa się w moczu zaledwie 1% w postaci niezmienionej. Nie wykryto żadnego czynnego metabolitu w osoczu.
Eliminacja
Okres półtrwania w fazie eliminacji gliklazydu wynosi od 12 do 20 godzin.
Liniowość lub nieliniowość
Związek pomiędzy podaną dawką do 120 mg, a powierzchnią pod krzywą stężeń w funkcji czasu jest
liniowy.
Szczególne grupy pacjentów
Pacjenci w podeszłym wieku
Nie zaobserwowano żadnych klinicznie znaczących zmian parametrów farmakokinetycznych u pacjentów w podeszłym wieku.
Przedkliniczne dane o bezpieczeństwie na podstawie konwencjonalnych badań toksyczności
i genotoksyczności z zastosowaniem powtórzonej dawki wykazały brak istotnego zagrożenia dla ludzi. Długoterminowe badania dotyczące wpływu rakotwórczego nie zostały przeprowadzone.
W badaniach na zwierzętach nie zaobserwowano zmian o podłożu teratogennym, natomiast mała masa ciała płodów była obserwowana u zwierząt otrzymujących 25 razy większą dawkę niż maksymalna dawka terapeutyczna zalecana do stosowania u ludzi. W badaniach na zwierzętach, po podaniu gliklazydu, nie obserwowano wpływu na płodność lub zdolność do rozrodu.
Wapnia wodorofosforan dwuwodny Maltodekstryna
Hypromeloza 100 cP
Hypromeloza 4000 cP Magnezu stearynian
Krzemionka koloidalna bezwodna
Nie dotyczy.
3 lata.
Brak specjalnych zaleceń dotyczących przechowywania produktu leczniczego.
7, 10, 14, 20, 28, 30, 56, 60, 84, 90, 100, 100 (opakowanie podzielone na pojedyncze dawki), 112, 120, 180 lub 500 tabletek w blistrach z folii PVC/Aluminium, pakowanych w tekturowe pudełka.
Nie wszystkie wielkości opakowań muszą znajdować się w obrocie.
Bez specjalnych wymagań.
OBROTU
Les Laboratoires Servier 50, rue Carnot
92284 Suresnes cedex Francja
Pozwolenie nr 11420
Data wydania pierwszego pozwolenia na dopuszczenie do obrotu: 6 kwietnia 2005 r. Data ostatniego przedłużenia pozwolenia: 14 lipca 2010 r.
PRODUKTU LECZNICZEGO
17/02/2020











