Spis treści:
- NAZWA PRODUKTU LECZNICZEGO
- SKŁAD JAKOŚCIOWY I ILOŚCIOWY
- POSTAĆ FARMACEUTYCZNA
- SZCZEGÓŁOWE DANE KLINICZNE
- WŁAŚCIWOŚCI FARMAKOLOGICZNE
- DANE FARMACEUTYCZNE
- PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU
- NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
- DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU I DATA PRZEDŁUŻENIA POZWOLENIA
- DATA ZATWIERDZENIA LUB CZĘŚCIOWEJ ZMIANY TEKSTU CHARAKTERYSTYKI PRODUKTU LECZNICZEGO
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
NAZWA PRODUKTU LECZNICZEGO
SKŁAD JAKOŚCIOWY I ILOŚCIOWY
POSTAĆ FARMACEUTYCZNA
SZCZEGÓŁOWE DANE KLINICZNE
Wskazania do stosowania
Dawkowanie i sposób podawania
Przeciwwskazania
Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania
Interakcje z innymi produktami leczniczymi i inne rodzaje interakcji
Wpływ na płodność, ciążę i laktację
Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn
Działania niepożądane
Przedawkowanie
WŁAŚCIWOŚCI FARMAKOLOGICZNE
Właściwości farmakodynamiczne
Właściwości farmakokinetyczne
Przedkliniczne dane o bezpieczeństwie
DANE FARMACEUTYCZNE
Wykaz substancji pomocniczych
Niezgodności farmaceutyczne
czy są rozpuszczalne i stabilne w wodzie w pH produktu leczniczego Aqua pro iniectione Kabi,
czy są ze sobą zgodne farmaceutycznie.
Okres ważności
Specjalne środki ostrożności podczas przechowywania
Rodzaj i zawartość opakowania
Specjalne środki ostrożności dotyczące usuwania i przygotowania produktu leczniczego do stosowania
PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU
NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU I DATA PRZEDŁUŻENIA POZWOLENIA
DATA ZATWIERDZENIA LUB CZĘŚCIOWEJ ZMIANY TEKSTU CHARAKTERYSTYKI PRODUKTU LECZNICZEGO
Aqua pro iniectione Kabi, rozpuszczalnik do sporządzania leków parenteralnych
Woda do wstrzykiwań 1 g na 1 ml pH 4,5 - 7,0
Pełny wykaz substancji pomocniczych, patrz punkt 6.1.
Rozpuszczalnik do sporządzania leków parenteralnych Przezroczysty i bezbarwny roztwór
Jałowa woda do wstrzykiwań służy jako środek do rozcieńczania lub rozpuszczania odpowiednich produktów leczniczych do stosowania parenteralnego.
Dawkowanie
Podawana ilość zależy od rodzaju dodanego produktu leczniczego.
Szybkość podawania zależy od schematu dawkowania przepisanego produktu leczniczego.
Po odpowiednim przygotowaniu roztworu z dodawanymi produktami leczniczymi, dawka zwykle zależy od wieku, masy ciała i stanu klinicznego pacjenta oraz wyników badań laboratoryjnych.
Sposób podawania
Roztwór przeznaczony jest do rozpuszczania i podawania produktów leczniczych.
Właściwa objętość i droga podania zależą od zasad użycia dodawanych produktów leczniczych.
Woda do wstrzykiwań nie powinna być podawana sama.
Należy wziąć pod uwagę przeciwwskazania do stosowania dodawanych produktów leczniczych.
Woda do wstrzykiwań jest hipotoniczna i nie należy jej podawać samej.
Nie należy jej stosować do dożylnego wstrzyknięcia bez doprowadzenia (w przybliżeniu) do izotonii za pomocą odpowiedniej substancji rozpuszczonej.
Jeśli woda do wstrzykiwań jest używana do rozcieńczania roztworów hipertonicznych, należy stosować odpowiednie rozcieńczenie, aby otrzymać roztwór zbliżony do izotonii.
Infuzja dużych objętości hipotonicznych roztworów z zastosowaniem jałowej wody do wstrzykiwań jako rozpuszczalnika może prowadzić do hemolizy.
W przypadku podawania dużych objętości produktu leczniczego, należy systematycznie sprawdzać równowagę jonową.
Nie są znane.
Należy wziąć pod uwagę możliwe kliniczne interakcje pomiędzy różnymi rozpuszczanymi produktami leczniczymi.
Ryzyko stosowania u kobiet w okresie ciąży i podczas karmienia piersią zależy od rodzaju dodawanych produktów leczniczych.
Nie dotyczy.
Podanie dożylne samej wody do wstrzykiwań może wywołać hemolizę.
Możliwość wystąpienia innych działań niepożądanych zależy od rodzaju dodawanego produktu leczniczego.
Zgłaszanie podejrzewanych działań niepożądanych
Po dopuszczeniu produktu leczniczego do obrotu istotne jest zgłaszanie podejrzewanych działań niepożądanych. Umożliwia to nieprzerwane monitorowanie stosunku korzyści do ryzyka stosowania produktu leczniczego. Osoby należące do fachowego personelu medycznego powinny zgłaszać wszelkie podejrzewane działania niepożądane za pośrednictwem Departamentu Monitorowania Niepożądanych Działań Produktów Leczniczych Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych
Al. Jerozolimskie 181C 02-222 Warszawa
tel.: + 48 22 49 21 301
faks: + 48 22 49 21 309
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Infuzja dużych objętości hipotonicznych roztworów z zastosowaniem jałowej wody do wstrzykiwań jako rozpuszczalnika może prowadzić do hemolizy.
Oznaki i objawy przedawkowania zależą od rodzaju dodawanego produktu leczniczego. W razie przypadkowego przedawkowania należy przerwać leczenie i obserwować pacjenta w celu wykrycia objawów przedmiotowych lub podmiotowych związanych z podawanym produktem leczniczym.
Grupa farmakoterapeutyczna: rozpuszczalniki i środki rozcieńczające, w tym roztwory do przepłukiwań, kod ATC:V07AB.
Ponieważ woda do wstrzykiwań jest tylko nośnikiem dla dodanych produktów leczniczych, właściwości farmakodynamiczne zależą od rodzaju dodanego produktu leczniczego.
Ponieważ woda do wstrzykiwań jest tylko nośnikiem dla dodanych produktów leczniczych, właściwości farmakokinetyczne zależą od rodzaju dodanego produktu leczniczego.
Ponieważ woda do wstrzykiwań jest tylko nośnikiem dla dodanych produktów leczniczych, przedkliniczne dane o bezpieczeństwie używanych roztworów zależą od rodzaju dodanego produktu leczniczego.
Brak.
Dodawane produkty lecznicze mogą wykazywać niezgodności farmaceutyczne. Nie należy dodawać produktów leczniczych niezgodnych farmaceutycznie.
Przed dodaniem produktów leczniczych należy sprawdzić:
W przypadku braku badań na zgodność farmaceutyczną, tego produktu leczniczego nie należy mieszać z innymi produktami leczniczymi.
Ampułki zawierające 5 ml, 10 ml i 20 ml: 2 lata.
Okres ważności po pierwszym otwarciu: należy zużyć natychmiast.
Brak specjalnych zaleceń dotyczących przechowywania produktu leczniczego. Przechowywać ampułkę w opakowaniu zewnętrznym.
Ampułki z polietylenu o niskiej gęstości (LDPE). Dostępne opakowania:
20 ampułek po 5 ml
50 ampułek po 5 ml
20 ampułek po 10 ml
50 ampułek po 10 ml
20 ampułek po 20 ml.
Nie wszystkie wielkości opakowań muszą znajdować się w obrocie.
Wyrzucić po jednorazowym użyciu. Wyrzucić niezużytą część roztworu.
Używać tylko jeśli roztwór jest przezroczysty, bez widocznych cząstek, a opakowanie nieuszkodzone. Konieczne jest staranne i ostrożne mieszanie z każdym dodatkiem, z zachowaniem jałowości.
Roztwór zawierający dodane produkty lecznicze powinien być użyty natychmiast po przygotowaniu, chyba że przygotowanie przeprowadzono w kontrolowanych i zwalidowanych warunkach aseptycznych.
Instrukcja obsługi
Oderwać jedną ampułkę przekręcając ją w kierunku przeciwnym do pozostałych, nie dotykając końcówki i szyjki ampułki (1). Wstrząsnąć ampułkę jednym ruchem jak pokazano poniżej, w celu usunięcia roztworu z końcówki ampułki (2). Aby otworzyć ampułkę należy przekręcić jej końcówkę w przeciwnym kierunku do pozostałej części ampułki aż do linii odłamania końcówki (3). Połączyć ampułkę ze strzykawką typu Luer lub Luer-Lock jak pokazano na rysunku (4).
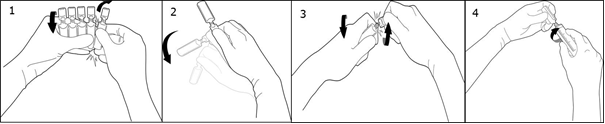
Nie ma konieczności używania igły. Stosować zawsze po rozcieńczeniu.
Fresenius Kabi Polska Sp. z o.o. Al. Jerozolimskie 134
02-305 Warszawa
Pozwolenie nr 16015
Data wydania pierwszego pozwolenia na dopuszczenie do obrotu: 07.10.2009 r. Data ostatniego przedłużenia pozwolenia: 07.12.2011 r.
02.12.2015 r.










