Spis treści:
- NAZWA PRODUKTU LECZNICZEGO
- SKŁAD JAKOŚCIOWY I ILOŚCIOWY
- POSTAĆ FARMACEUTYCZNA
- SZCZEGÓŁOWE DANE KLINICZNE
- WŁAŚCIWOŚCI FARMAKOLOGICZNE
- DANE FARMACEUTYCZNE
- PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU
- NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
- DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU I DATA PRZEDŁUŻENIA POZWOLENIA
- DATA ZATWIERDZENIA LUB CZĘŚCIOWEJ ZMIANY TEKSTU
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
NAZWA PRODUKTU LECZNICZEGO
SKŁAD JAKOŚCIOWY I ILOŚCIOWY
POSTAĆ FARMACEUTYCZNA
SZCZEGÓŁOWE DANE KLINICZNE
Wskazania do stosowania
Dawkowanie i sposób podawania
Jeśli w poprzedzającym miesiącu nie stosowano antykoncepcji hormonalnej
Przyjmowanie tabletek należy rozpocząć w 1. dniu naturalnego cyklu miesiączkowego (tj. w pierwszym dniu krwawienia).
Zmiana ze złożonego hormonalnego środka antykoncepcyjnego (złożonego doustnego środka antykoncepcyjnego (ang. combined oral contraceptive, COC), systemu terapeutycznego dopochwowego lub systemu transdermalnego, plastra)
Kobieta powinna rozpocząć stosowanie produktu leczniczego Vixpo w następnym dniu po przyjęciu ostatniej tabletki aktywnej (ostatnia tabletka zawierająca substancje czynne) poprzednio stosowanego złożonego doustnego środka antykoncepcyjnego, ale najpóźniej w dniu następującym po zwyczajowej przerwie, w czasie której nie przyjmuje się tabletek lub przyjmuje się tabletki placebo poprzedniego COC. W przypadku stosowania systemu terapeutycznego dopochwowego lub systemu transdermalnego, plastra kobieta powinna zacząć przyjmować produkt leczniczy Vixpo w dniu usunięcia poprzedniego środka antykoncepcyjnego, ale najpóźniej w dniu, na który przypadałoby kolejne zastosowanie poprzednio stosowanego produktu.
Zmiana z metody wyłącznie progestagenowej (tabletki zawierające wyłącznie progestagen, iniekcje, implant lub system domaciczny (ang. IUS) uwalniający progestagen)
Kobieta może rozpocząć stosowanie produktu leczniczego Vixpo po stosowaniu tabletek zawierających wyłącznie progestagen w dowolnym dniu (jeśli stosowała implant lub IUS - w dniu jego usunięcia, a jeśli iniekcje - w dniu, w którym powinna zostać podana następna iniekcja). W tych wszystkich przypadkach pacjentce należy jednak doradzić, aby stosowała dodatkowo mechaniczną metodę antykoncepcji w ciągu pierwszych 7 dni przyjmowania tabletek.
Po poronieniu w pierwszym trymestrze ciąży
Kobieta może rozpocząć przyjmowanie tabletek natychmiast. W tym przypadku nie jest konieczne stosowanie dodatkowych metod antykoncepcyjnych.
Po porodzie lub poronieniu w drugim trymestrze ciąży
Kobiecie należy poradzić, aby rozpoczęła stosowanie produktu w 21. do 28. dnia po porodzie lub poronieniu w drugim trymestrze ciąży. Jeżeli pacjentka rozpoczyna stosowanie produktu leczniczego później, należy jej doradzić, aby stosowała dodatkowo mechaniczną metodę antykoncepcji w ciągu pierwszych 7 dni przyjmowania tabletek. Jeżeli jednak doszło już do stosunku, przed rozpoczęciem stosowania złożonego doustnego środka antykoncepcyjnego należy wykluczyć ciążę lub odczekać do pierwszego krwawienia.
Informacje dla kobiet karmiących piersią podano w punkcie 4.6.
Postępowanie w przypadku pominięcia przyjęcia tabletek
Tabletki placebo z ostatniego (czwartego) rzędu blistra mogą zostać pominięte. Należy je jednak usunąć, aby uniknąć przypadkowego wydłużenia okresu stosowania tabletek placebo.
Poniższe zalecenia dotyczą pominięcia tabletki zawierającej substancje czynne:
Jeśli opóźnienie w przyjęciu tabletki jest mniejsze niż 24 godziny, skuteczność antykoncepcyjna jest zachowana. Kobieta powinna przyjąć pominiętą tabletkę, gdy tylko sobie o tym przypomni, a kolejne tabletki powinna przyjmować o zwykłej porze.
Jeśli od czasu przyjęcia którejkolwiek tabletki minęło więcej niż 24 godziny, ochrona antykoncepcyjna może być zmniejszona.
W przypadku pominięcia tabletek należy postępować zgodnie z następującymi dwiema podstawowymi zasadami:
Zalecenia w przypadku zaburzeń żołądkowo-jelitowych
W przypadku wystąpienia ciężkich zaburzeń żołądkowo-jelitowych (np. wymioty i biegunka) wchłanianie produktu może nie być całkowite i należy stosować dodatkowe metody antykoncepcyjne. W razie wystąpienia wymiotów w ciągu 3-4 godzin po przyjęciu tabletki zawierającej substancję czynną należy zastosować nową (dodatkową) tabletkę tak szybko jak to możliwe. Jeżeli jest to możliwe, nową tabletkę należy przyjąć przed upływem 24 godzin od zwykłej pory przyjęcia tabletki. Jeżeli upłynie więcej niż
24 godziny, należy zastosować zalecenia dotyczące pominięcia tabletki, patrz punkt 4.2 „Postępowanie
w przypadku pominięcia przyjęcia tabletek”. Jeżeli kobieta nie chce zmieniać dotychczasowego schematu stosowania tabletek, powinna przyjąć dodatkową(-e) tabletkę(-i) z innego blistra.
Jak opóźnić wystąpienie krwawienia z odstawienia
Aby opóźnić wystąpienie miesiączki, kobieta powinna rozpocząć stosowanie tabletek z następnego blistra produktu Vixpo, bez przyjmowania tabletek placebo z bieżącego opakowania. Stosowanie tabletek można kontynuować tak długo, jak długo jest to potrzebne, aż do zakończenia aktywnych tabletek z drugiego opakowania. W czasie wydłużonego cyklu może wystąpić krwawienie śródcykliczne lub plamienie. Do regularnego przyjmowania produktu Vixpo należy powrócić po zastosowaniu tabletek placebo.
Jeżeli pacjentka chce zmienić dzień wystąpienia miesiączki na inny dzień tygodnia niż w stosowanym obecnie schemacie, można jej zalecić, aby skróciła następny okres stosowania tabletek placebo o dowolną liczbę dni. Im krótszy ten okres, tym większe ryzyko, że nie wystąpi krwawienie z odstawienia i będą występowały krwawienia śródcykliczne lub plamienie w trakcie stosowania tabletek z następnego opakowania (podobnie jak w przypadku opóźniania miesiączki).
Dodatkowe informacje dotyczące szczególnych populacji
Dzieci i młodzież
Produkt leczniczy Vixpo jest wskazany tylko po rozpoczęciu miesiączkowania.
Pacjentki w podeszłym wieku
Produkt leczniczy Vixpo nie jest wskazany do stosowania po menopauzie.
Pacjentki z zaburzeniami czynności wątroby
Produkt leczniczy Vixpo jest przeciwwskazany u kobiet z ciężkimi chorobami wątroby (patrz punkty 4.3
i 5.2).
Pacjentki z zaburzeniami czynności nerek
Produkt leczniczy Vixpo jest przeciwwskazany u kobiet z ciężką niewydolnością nerek lub ostrą niewydolnością nerek (patrz punkty 4.3 i 5.2).
Sposób podawania Podanie doustne.
Przeciwwskazania
Nadwrażliwość na substancje czynne lub na którąkolwiek substancję pomocniczą wymienioną
w punkcie 6.1.
Występowanie lub ryzyko żylnej choroby zakrzepowo-zatorowej (ang. venous thromboembolism, VTE)
Żylna choroba zakrzepowo-zatorowa - czynna (leczona przeciwzakrzepowymi produktami leczniczymi) lub przebyta żylna choroba zakrzepowo-zatorowa, np. zakrzepica żył głębokich (ang. deep venous thrombosis, DVT), zatorowość płucna (ang. pulmonary embolism, PE).
Znana dziedziczna lub nabyta predyspozycja do występowania żylnej choroby zakrzepowo- zatorowej np. oporność na aktywne białko C (ang. activated protein C, APC) (w tym czynnik V Leiden), niedobór antytrombiny III, niedobór białka C, niedobór białka S.
Rozległy zabieg operacyjny związany z długotrwałym unieruchomieniem (patrz punkt 4.4).
Wysokie ryzyko żylnej choroby zakrzepowo-zatorowej wskutek występowania wielu czynników ryzyka (patrz punkt 4.4).
Występowanie lub ryzyko tętniczych zaburzeń zakrzepowo-zatorowych (ang. arterial thromboembolism, ATE)
Tętnicze zaburzenia zakrzepowo-zatorowe - czynne lub przebyte (np. zawał mięśnia sercowego) lub objawy prodromalne (np. dławica piersiowa).
Choroby naczyń mózgowych - czynny udar, przebyty udar lub objawy prodromalne
w wywiadzie (np. przemijający napad niedokrwienny, ang. transient ischaemic attack, TIA).
Stwierdzona dziedziczna lub nabyta skłonność do występowania tętniczych zaburzeń zakrzepowo-zatorowych np. hiperhomocysteinemia i obecność przeciwciał antyfosfolipidowych (przeciwciała antykardiolipinowe, antykoagulant toczniowy).
Migrena z ogniskowymi objawami neurologicznymi w wywiadzie.
Wysokie ryzyko zaburzeń zakrzepowo-zatorowych tętnic z powodu występowania wielu czynników ryzyka (patrz punkt 4.4) lub występowania jednego z poważnych czynników ryzyka, takich jak:
cukrzyca z powikłaniami naczyniowymi
ciężkie nadciśnienie tętnicze
ciężka dyslipoproteinemia.
Ciężka choroba wątroby obecnie lub w wywiadzie, do czasu powrotu wyników prób czynnościowych wątroby do wartości prawidłowych.
Ciężka lub ostra niewydolność nerek.
Obecne lub przebyte nowotwory wątroby (łagodne lub złośliwe).
Występowanie lub podejrzenie złośliwego nowotworu zależnego od steroidów płciowych (np. narządów płciowych lub piersi).
Krwawienie z pochwy o nieustalonej etiologii.
Produkt leczniczy Vixpo jest przeciwwskazany do jednoczesnego stosowania z produktami leczniczymi zawierającymi ombitaswir z parytaprewirem i rytonawirem, dazabuwir, z produktami leczniczymi zawierającymi glekaprewir z pibrentaswirem oraz sofosbuwir z welpataswirem i woksylaprewirem (patrz punkt 4.5).
Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania Ostrzeżenia
Żylna choroba zakrzepowo-zatorowa może być śmiertelna w 1-2% przypadków.
Liczba przypadków żylnej choroby zakrzepowo-zatorowej przypadających na 10 000 kobiet
w okresie roku
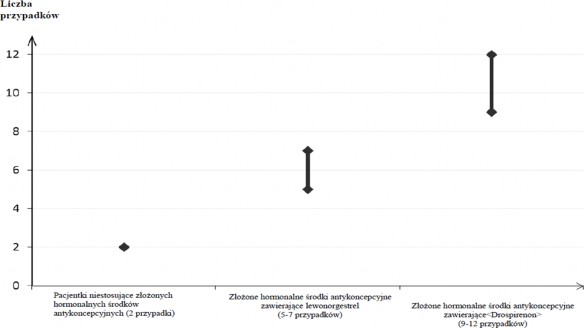
U pacjentek stosujących złożone hormonalne środki antykoncepcyjne niezwykle rzadko zgłaszano przypadki zakrzepicy w innych naczyniach krwionośnych, np. wątrobowych, krezkowych, nerkowych lub w żyłach i tętnicach siatkówki.
Czynniki ryzyka żylnej choroby zakrzepowo-zatorowej
Ryzyko żylnych powikłań zakrzepowo-zatorowych u pacjentek stosujących złożone hormonalne środki antykoncepcyjne może znacząco wzrosnąć w przypadku występowania dodatkowych czynników ryzyka, szczególnie, jeśli występuje kilka czynników ryzyka jednocześnie (patrz tabela).
Stosowanie produktu leczniczego Vixpo jest przeciwwskazane, jeśli u pacjentki występuje jednocześnie kilka czynników ryzyka, zwiększających ryzyko zakrzepicy żylnej (patrz punkt 4.3). Jeśli u kobiety wstępuje więcej niż jeden czynnik ryzyka, możliwe jest, że zwiększenie ryzyka jest większe niż suma pojedynczych czynników - w tym przypadku należy ocenić całkowite ryzyko żylnej choroby zakrzepowo- zatorowej. Jeśli ocena stosunku korzyści do ryzyka jest negatywna, nie należy przepisywać złożonych hormonalnych środków antykoncepcyjnych (patrz punkt 4.3).
Tabela: Czynniki ryzyka żylnej choroby zakrzepowo-zatorowej
Czynnik ryzyka
Uwagi
Otyłość (wskaźnik masy ciała (BMI) powyżej 30 kg/m2)
Ryzyko istotnie zwiększa się ze wzrostem BMI. Jest to szczególnie istotne do oceny, jeśli występują również inne czynniki ryzyka.
Długotrwałe unieruchomienie, rozległy zabieg operacyjny, jakikolwiek zabieg operacyjny w obrębie kończyn dolnych lub
miednicy, zabieg neurochirurgiczny lub poważny uraz.
W powyższych sytuacjach zaleca się przerwanie stosowania tabletek na co najmniej 4 tygodnie przed planowanym zabiegiem chirurgicznym i nie wznawianie stosowania produktu przed upływem dwóch tygodni od czasu powrotu do sprawności ruchowej. Należy stosować inną metodę antykoncepcji, aby uniknąć niezamierzonego zajścia w ciążę.
Należy rozważyć leczenie przeciwzakrzepowe, jeśli stosowania produktu leczniczego Vixpo nie przerwano odpowiednio wcześnie.
Uwaga: tymczasowe unieruchomienie, w tym podróż samolotem >4 godzin może również stanowić czynnik ryzyka żylnej choroby zakrzepowo-zatorowej, szczególnie u kobiet ze współistniejącymi innymi czynnikami
ryzyka.
Dodatni wywiad rodzinny (występowanie żylnych zaburzeń zakrzepowo-zatorowych u rodzeństwa bądź rodziców, szczególnie
w stosunkowo młodym wieku, np. przed 50. rokiem życia).
Jeśli podejrzewa się predyspozycję genetyczną, przed podjęciem decyzji o stosowaniu złożonego hormonalnego środka antykoncepcyjnego kobieta powinna zostać skierowana na konsultację
u specjalisty.
Inne schorzenia związane z żylną chorobą zakrzepowo-zatorową.
Nowotwór, toczeń rumieniowaty układowy, zespół hemolityczno-mocznicowy, przewlekłe zapalne choroby jelit (np. choroba Leśniowskiego-Crohna lub wrzodziejące zapalenie jelita grubego) oraz
niedokrwistość sierpowata.
Wiek
Szczególnie w wieku powyżej 35 lat.
Nie osiągnięto konsensusu, co do możliwej roli żylaków oraz zakrzepowego zapalenia żył powierzchniowych na wystąpienie lub progresję żylnej choroby zakrzepowo-zatorowej.
Należy uwzględnić zwiększone ryzyko wystąpienia choroby zakrzepowo-zatorowej w ciąży oraz
w szczególności w 6-tygodniowym okresie poporodowym (patrz punkt 4.6 „Wpływ na płodność, ciążę
i laktację”).
Objawy żylnej choroby zakrzepowo-zatorowej (zakrzepicy żył głębokich oraz zatorowości płucnej)
Należy poinformować pacjentkę, że w razie wystąpienia następujących objawów należy natychmiast zgłosić się do lekarza i powiedzieć personelowi medycznemu, że stosuje się złożone hormonalne środki antykoncepcyjne.
Objawy zakrzepicy żył głębokich (ang. deep vein thrombosis, DVT) mogą obejmować:
obrzęk nogi i/lub stopy lub obrzęk wzdłuż żyły w nodze;
ból lub tkliwość w nodze, które mogą być odczuwane wyłącznie w czasie stania lub chodzenia;
zwiększona temperatura w zmienionej chorobowo nodze; czerwona lub przebarwiona skóra nogi.
Objawy zatorowości płucnej (ang. pulmonary embolism, PE) mogą obejmować:
nagły napad niewyjaśnionego spłycenia oddechu lub przyspieszenia oddechu;
nagły napad kaszlu, który może być połączony z krwiopluciem;
ostry ból w klatce piersiowej;
ciężkie zamroczenie lub zawroty głowy;
przyspieszone lub nieregularne bicie serca.
Niektóre z tych objawów (np. „spłycenie oddechu”, „kaszel”) są niespecyficzne i mogą być niepoprawnie zinterpretowane jako występujące częściej lub mniej poważne stany (np. zakażenia układu oddechowego). Inne objawy zamknięcia naczyń mogą obejmować: nagły ból, obrzęk oraz lekko niebieskie przebarwienie kończyn.
Jeżeli zamknięcie naczynia wystąpi w oku, objawy mogą obejmować bezbolesne zaburzenia widzenia, które mogą przekształcić się w utratę widzenia. W niektórych przypadkach utrata widzenia może nastąpić niemal natychmiast.
Ryzyko tętniczych zaburzeń zakrzepowo-zatorowych
Badania epidemiologiczne wykazały związek pomiędzy stosowaniem złożonych hormonalnych środków antykoncepcyjnych a zwiększonym ryzykiem tętniczych zaburzeń zakrzepowo-zatorowych (zawału mięśnia sercowego) lub incydentów naczyniowo-mózgowych (np. przemijającego napadu niedokrwiennego, udaru). Przypadki tętniczych zaburzeń zakrzepowo-zatorowych mogą być śmiertelne.
Czynniki ryzyka tętniczych zaburzeń zakrzepowo-zatorowych
Ryzyko wystąpienia tętniczych powikłań zakrzepowo-zatorowych lub napadów naczyniowo-mózgowych u pacjentek stosujących złożone hormonalne środki antykoncepcyjne jest zwiększone u kobiet, u których występują czynniki ryzyka (patrz tabela). Stosowanie produktu leczniczego Vixpo jest przeciwwskazane, jeżeli u pacjentki występuje jeden poważny lub jednocześnie kilka czynników ryzyka tętniczych zaburzeń zakrzepowo-zatorowych, które stawiają pacjentkę w grupie wysokiego ryzyka zakrzepicy tętniczej (patrz punkt 4.3). Jeśli u kobiety wstępuje więcej niż jeden czynnik ryzyka, możliwe jest, że zwiększenie ryzyka jest większe niż suma pojedynczych czynników - w tym przypadku należy ocenić całkowite ryzyko. Jeśli ocena stosunku korzyści do ryzyka jest negatywna, nie należy przepisywać złożonych hormonalnych środków antykoncepcyjnych (patrz punkt 4.3).
Tabela: Czynniki ryzyka tętniczych zaburzeń zakrzepowo-zatorowych
Czynnik ryzyka
Uwagi
Wiek
Szczególnie w wieku powyżej 35 lat.
Palenie
Należy dokładnie pouczyć kobiety, aby nie paliły, jeśli zamierzają stosować złożone hormonalne środki antykoncepcyjne. Kobiety w wieku powyżej 35 lat, które nie zaprzestały palenia, należy dokładnie pouczyć, aby stosowały inną metodę antykoncepcji.
Nadciśnienie tętnicze
Otyłość (wskaźnik masy ciała (BMI) powyżej 30 kg/m2)
Ryzyko istotnie wzrasta wraz ze wzrostem BMI.
Jest to szczególnie ważne dla kobiet, u których występują również inne czynniki ryzyka.
Dodatni wywiad rodzinny (występowanie tętniczych zaburzeń zakrzepowo- zatorowych u rodzeństwa bądź rodziców, szczególnie w stosunkowo młodym
wieku, np. przed 50. rokiem życia).
Jeśli podejrzewa się predyspozycję genetyczną, przed podjęciem decyzji o stosowaniu złożonego hormonalnego środka antykoncepcyjnego kobieta powinna zostać skierowana na konsultację u specjalisty.
Migrena
Zwiększenie częstości występowania lub nasilenia migreny w trakcie stosowania złożonych hormonalnych środków antykoncepcyjnych (która może zapowiadać wystąpienie incydentu naczyniowo-mózgowego) może być powodem do natychmiastowego przerwania stosowania.
Inne schorzenia związane ze zdarzeniami niepożądanymi w obrębie naczyń
Cukrzyca, hiperhomocysteinemia, wady zastawkowe serca, migotanie przedsionków, dyslipoproteinemia oraz toczeń rumieniowaty układowy.
Objawy tętniczych zaburzeń zakrzepowo-zatorowych
Należy poinformować pacjentkę, że w razie wystąpienia następujących objawów należy natychmiast zgłosić się do lekarza i powiedzieć personelowi medycznemu, że stosuje się złożone hormonalne środki antykoncepcyjne.
Objawy napadu naczyniowo-mózgowego mogą obejmować:
nagłe zdrętwienie lub osłabienie twarzy, rąk lub nóg, szczególnie po jednej stronie ciała;
nagłe trudności z chodzeniem, zawroty głowy, utratę równowagi lub koordynacji;
nagłe splątanie, trudności z mówieniem lub rozumieniem;
nagłe zaburzenia widzenia w jednym oku lub obydwu oczach;
nagłe, ciężkie lub długotrwałe bóle głowy bez przyczyny;
utratę przytomności lub omdlenie z drgawkami lub bez drgawek.
Przejściowe objawy sugerujące, że zdarzenie jest przemijającym napadem niedokrwiennym (ang.
transient ischaemic attack, TIA).
Objawy zawału serca (ang. myocardial infarction, MI) mogą być następujące:
ból, uczucie dyskomfortu, ociężałość, uczucie ściskania lub pełności w klatce piersiowej, ramieniu lub poniżej mostka;
uczucie dyskomfortu promieniujące do pleców, szczęki, gardła, ramienia, żołądka;
uczucie pełności, niestrawności lub zadławienia;
pocenie się, mdłości, wymioty lub zawroty głowy;
skrajne osłabienie, niepokój lub spłycenie oddechu;
przyspieszone lub nieregularne bicie serca.
Nowotwory
W niektórych badaniach epidemiologicznych obserwowano zwiększone ryzyko raka szyjki macicy
u kobiet długotrwale (powyżej 5 lat) stosujących COC, ale nie wiadomo, do jakiego stopnia na wyniki te wpływa zachowanie seksualne oraz inne czynniki, takie jak zakażenie wirusem brodawczaka ludzkiego (HPV).
Metaanaliza 54 badań epidemiologicznych wykazała, że u kobiet obecnie stosujących złożone doustne środki antykoncepcyjne występuje nieznacznie zwiększone (RR=1,24) względne ryzyko rozpoznania raka piersi. To zwiększone ryzyko stopniowo zanika w ciągu 10 lat po zaprzestaniu stosowania COC. Ponieważ rak piersi występuje rzadko u kobiet w wieku poniżej 40 lat, zwiększenie liczby rozpoznanych przypadków raka piersi w grupie kobiet przyjmujących obecnie i ostatnio COC jest niewielkie w stosunku
do całkowitego ryzyka wystąpienia raka piersi. Badania te nie dostarczają dowodów na istnienie związku przyczynowego. Obserwowany wzorzec zwiększenia ryzyka może wynikać z wcześniejszego rozpoznania raka piersi u kobiet stosujących COC, z działania biologicznego COC lub z obu tych czynników.
Rozpoznane przypadki raka piersi u kobiet kiedykolwiek wcześniej lub aktualnie stosujących złożone doustne środki antykoncepcyjne wykazują zwykle mniejszy stan zaawansowania klinicznego niż u kobiet nigdy niestosujących złożonych doustnych środków antykoncepcyjnych.
U kobiet stosujących COC rzadko zgłaszano występowanie nowotworów łagodnych wątroby, a jeszcze rzadziej nowotworów złośliwych wątroby. Nowotwory te w pojedynczych przypadkach prowadziły do zagrażających życiu krwawień do jamy brzusznej. Jeśli u kobiet stosujących COC wystąpi silny ból
w nadbrzuszu, powiększenie wątroby lub jeśli wystąpią objawy wskazujące na krwawienia do jamy brzusznej, w rozpoznaniu różnicowym należy wziąć pod uwagę nowotwór wątroby.
Stosowanie COC w większych dawkach (50 μg etynyloestradiolu) zmniejsza ryzyko wystąpienia raka jajnika lub endometrium. Nie potwierdzono, czy dotyczy to również COC zawierających mniejsze dawki.
Inne stany kliniczne
Składnik progestagenowy produktu leczniczego Vixpo jest antagonistą aldosteronu o właściwościach oszczędzających potas. W większości przypadków nie należy spodziewać się wzrostu stężenia potasu we krwi. Jednakże w badaniu klinicznym u niektórych pacjentek z łagodnymi lub umiarkowanymi
zaburzeniami czynności nerek, stosujących jednocześnie produkty lecznicze oszczędzające potas, stężenie potasu w surowicy nieznacznie, w zakresie nieistotnym wzrosło w trakcie przyjmowania drospirenonu.
Dlatego też zaleca się kontrolę stężenia potasu w surowicy podczas pierwszego cyklu leczenia u pacjentek z niewydolnością nerek oraz stężeniem potasu przed rozpoczęciem stosowania produktu w pobliżu górnej granicy wartości uznawanych za prawidłowe, a szczególnie podczas jednoczesnego stosowania produktów leczniczych oszczędzających potas. Patrz także punkt 4.5.
U kobiet z hipertriglicerydemią lub dodatnim wywiadem rodzinnym w kierunku hipertriglicerydemii podczas stosowania COC może występować zwiększone ryzyko zapalenia trzustki.
Mimo że u wielu kobiet stosujących COC zgłaszano nieznaczny wzrost ciśnienia tętniczego, rzadko było to zwiększenie ciśnienia istotne klinicznie. Tylko w tych rzadkich przypadkach uzasadnione jest natychmiastowe zaprzestanie stosowania COC. Jeżeli podczas stosowania COC u kobiety z wcześniej występującym nadciśnieniem tętniczym stwierdza się stale zwiększone wartości ciśnienia tętniczego lub znaczne zwiększenie ciśnienia tętniczego nieodpowiadające właściwie na leczenie przeciwnadciśnieniowe, konieczne jest odstawienie COC. W uzasadnionych przypadkach po uzyskaniu prawidłowych wartości ciśnienia tętniczego na skutek leczenia przeciwnadciśnieniowego można ponownie rozpocząć stosowanie COC.
Zgłaszano wystąpienie lub pogorszenie w czasie ciąży lub podczas stosowania COC następujących stanów chorobowych, chociaż nie dowiedziono związku ich występowania ze stosowaniem COC: żółtaczka i (lub) świąd związany z zastojem żółci, kamica żółciowa, porfiria, toczeń rumieniowaty układowy, zespół hemolityczno-mocznicowy, pląsawica Sydenhama, opryszczka ciężarnych, ubytek słuchu związany z otosklerozą.
Egzogenne estrogeny mogą wywoływać lub nasilać objawy dziedzicznego lub nabytego obrzęku naczynioruchowego.
Ostre lub przewlekłe zaburzenia czynności wątroby mogą powodować konieczność przerwania stosowania COC do czasu powrotu wskaźników czynności wątroby do wartości prawidłowych. Nawrót żółtaczki cholestatycznej i (lub) świądu związanego z zastojem żółci, które uprzednio występowały
w czasie ciąży bądź podczas poprzedniego stosowania hormonów płciowych, wymagają zaprzestania stosowania COC.
Mimo że COC mogą wpływać na insulinooporność tkanek obwodowych oraz na tolerancję glukozy, nie ma dowodów na konieczność zmiany schematu leczenia cukrzycy u diabetyczek stosujących COC
o niskiej zawartości estrogenów (<0,05 mg etynyloestradiolu). Należy jednak starannie monitorować stan kobiet chorych na cukrzycę, szczególnie w początkowym okresie stosowania COC.
Opisywano pogorszenie przebiegu padaczki, choroby Leśniowskiego-Crohna oraz wrzodziejącego zapalenia jelita grubego podczas stosowania COC.
Sporadycznie może wystąpić ostuda, zwłaszcza u pacjentek z ostudą w czasie ciąży w wywiadzie. Pacjentki ze skłonnością do występowania ostudy powinny podczas stosowania COC unikać ekspozycji na słońce lub promieniowanie ultrafioletowe.
Obniżony nastrój i depresja to dobrze znane działania niepożądane stosowania hormonalnych środków antykoncepcyjnych (patrz punkt 4.8). Depresja może mieć ciężki przebieg i jest dobrze znanym czynnikiem ryzyka zachowań samobójczych i samobójstw. Jeśli u pacjentki wystąpią zmiany nastroju lub objawy depresji, również krótko po rozpoczęciu leczenia, zaleca się, aby skonsultowała się z lekarzem.
Badanie lekarskie lub konsultacja
Przed przystąpieniem do pierwszego lub powtórnego stosowania produktu leczniczego Vixpo należy zebrać pełny wywiad lekarski (w tym wywiad rodzinny) oraz wykluczyć ciążę. Należy wykonać pomiar ciśnienia tętniczego oraz badanie przedmiotowe, z uwzględnieniem przeciwwskazań (patrz punkt 4.3)
i specjalnych ostrzeżeń (patrz punkt 4.4). Ważne jest zwrócenie uwagi kobiety na informacje dotyczące zakrzepicy żył i tętnic, w tym na ryzyko stosowania produktu leczniczego Vixpo w porównaniu z innymi złożonymi hormonalnymi środkami antykoncepcyjnymi, objawy żylnej choroby zakrzepowo-zatorowej oraz zaburzeń zakrzepowo-zatorowych tętnic, znane czynniki ryzyka oraz co należy robić w przypadku podejrzenia zakrzepicy.
Należy również polecić kobietom dokładne przeczytanie ulotki i stosowanie się do znajdujących się w niej zaleceń. Częstość i rodzaj badań powinny zostać dobrane na podstawie przyjętych zaleceń praktyki
i dostosowane do każdej pacjentki.
Należy poinformować kobiety, że hormonalne środki antykoncepcyjne nie chronią przed zakażeniem wirusem HIV (AIDS) oraz innym chorobami przenoszonymi drogą płciową.
Zmniejszenie skuteczności
Skuteczność COC może być zmniejszona w przypadku np. pominięcia tabletek aktywnych (patrz
punkt 4.2), zaburzeń żołądkowo-jelitowych podczas przyjmowania tabletek aktywnych (patrz punkt 4.2) lub jednoczesnego stosowania innych leków (patrz punkt 4.5).
Zmniejszona kontrola cyklu
W związku ze stosowaniem wszystkich COC mogą wystąpić nieregularne krwawienia (plamienie lub krwawienie śródcykliczne), zwłaszcza w pierwszych miesiącach przyjmowania tabletek. Dlatego ocena nieregularnych krwawień ma znaczenie dopiero po upływie okresu adaptacyjnego trwającego około trzy cykle.
Jeśli nieregularne krwawienia nadal utrzymują się lub występują po poprzednio regularnych cyklach, należy rozważyć niehormonalne przyczyny i przeprowadzić odpowiednie badania diagnostyczne, aby wykluczyć nowotwory złośliwe lub ciążę. Mogą one obejmować łyżeczkowanie.
U niektórych kobiet w czasie przyjmowania tabletek placebo nie wystąpi krwawienie z odstawienia. Jeżeli COC przyjmowano zgodnie z zaleceniami opisanymi w punkcie 4.2, jest mało prawdopodobne, że kobieta jest w ciąży. Jeżeli jednak COC nie był przyjmowany zgodnie z tymi wskazówkami w okresie poprzedzającym pierwszy brak wystąpienia krwawienia z odstawienia lub jeśli nie wystąpiły dwa kolejne krwawienia z odstawienia, przed kontynuowaniem stosowania COC należy wykluczyć ciążę.
Vixpo zawiera laktozę i sód
Każda różowa tabletka zawiera 44 mg laktozy jednowodnej, każda biała tabletka zawiera 89,5 mg laktozy
bezwodnej.
Pacjentki z rzadko występującą dziedziczną nietolerancją galaktozy, brakiem laktazy lub zespołem złego wchłaniania glukozy-galaktozy nie powinny stosować tego produktu.
Produkt zawiera mniej niż 1 mmol (23 mg) sodu na tabletkę, to znaczy produkt uznaje się za „wolny od sodu”.
Interakcje z innymi produktami leczniczymi i inne rodzaje interakcji
Wpływ innych produktów leczniczych na działanie produktu Vixpo
Mogą wystąpić interakcje z produktami leczniczymi indukującymi enzymy mikrosomalne w postaci zwiększenia klirensu hormonów płciowych, co może prowadzić do krwawienia śródcyklicznego i (lub) braku skuteczności antykoncepcyjnej.
Postępowanie
Indukcja enzymów może wystąpić po kilku dniach leczenia. Maksymalna indukcja enzymatyczna jest zazwyczaj widoczna w ciągu kilku tygodni. Po zakończeniu leczenia indukcja enzymatyczna może utrzymywać się przez około 4 tygodnie.
Leczenie krótkoterminowe
Kobiety leczone produktami leczniczymi indukującymi enzymy mikrosomalne powinny stosować tymczasowo mechaniczną lub inną metodę antykoncepcji oprócz złożonego doustnego środka antykoncepcyjnego. Dodatkowe metody muszą być stosowane podczas całego okresu terapii skojarzonej oraz przez 28 dni po zakończeniu leczenia. Jeśli leczenie to trwa dłużej niż koniec przyjmowania tabletek zawierających substancje czynne z bieżącego opakowania złożonego doustnego środka antykoncepcyjnego, należy pominąć tabletki placebo i rozpocząć przyjmowanie tabletek z następnego opakowania.
Leczenie długoterminowe
Kobiety przyjmujące przez dłuższy czas leki indukujące enzymy wątrobowe powinny stosować inną skuteczną, niehormonalną metodę antykoncepcji.
W piśmiennictwie opisano następujące interakcje.
Produkty lecznicze zwiększające klirens złożonych doustnych środków antykoncepcyjnych (zmniejszające skuteczność poprzez indukcję enzymów) np.:
barbiturany, bozentan, karbamazepina, fenytoina, prymidon, ryfampicyna i leki stosowane w leczeniu zakażeń wirusem HIV (rytonawir, newirapina, efawirenz) i prawdopodobnie także felbamat, gryzeofulwina, okskarbazepina, topiramat oraz leki roślinne zawierające dziurawiec zwyczajny (Hypericum perforatum).
Produkty lecznicze wywierające wpływ na klirens złożonych doustnych środków antykoncepcyjnych: Równoczesne stosowanie złożonych doustnych środków antykoncepcyjnych z inhibitorami proteazy HIV i nienukleozydowymi inhibitorami odwrotnej transkryptazy, włączając połączenie z inhibitorami HCV, może zwiększać lub zmniejszać stężenie estrogenów lub progestagenów w osoczu.
W niektórych przypadkach zmiany te mogą mieć znaczenie kliniczne.
Dlatego też, zalecając równoczesne stosowanie produktów leczniczych przeciwko HIV/HCV należy wziąć pod uwagę możliwe interakcje oraz odpowiednie zalecenia. W przypadku jakichkolwiek wątpliwości,
u kobiet podczas terapii inhibitorami proteazy lub nienukleozydowymi inhibitorami odwrotnej transkryptazy należy stosować dodatkową, mechaniczną metodę antykoncepcji.
Produkty lecznicze zmniejszające klirens złożonych doustnych produktów antykoncepcyjnych (inhibitory enzymów):
Znaczenie kliniczne potencjalnych interakcji z inhibitorami enzymu pozostaje nieznane.
Jednoczesne stosowanie silnych inhibitorów CYP3A4 może zwiększać stężenie estrogenów lub progestagenów lub obu substancji w osoczu.
W wielodawkowym badaniu z zastosowaniem połączenia drospirenonu (3mg na dobę) i etynyloestradiolu (0,02 mg na dobę) dodanie silnego inhibitora CYP3A4 - ketokonazolu przez 10 dni spowodowało wzrost AUC (0-24h) drospirenonu i etynyloestradiolu odpowiednio 2,7- i 1,4-krotnie.
Dawka etorykoksybu wynosząca 60 do 120 mg na dobę, podawana równocześnie ze złożoną antykoncepcją doustną zawierającą 0,035 mg etynyloestradiolu, spowodowała zwiększenie stężenia etynyloestradiolu w osoczu od 1,4- do 1,6-krotnie.
Wpływ produktu Vixpo na działanie innych produktów leczniczych
Doustne środki antykoncepcyjne mogą wpływać na metabolizm niektórych innych substancji czynnych. Stężenia osoczowe i tkankowe mogą się odpowiednio albo zwiększyć (np. cyklosporyna), albo zmniejszyć (np. lamotrygina).
Na podstawie badań interakcji in vivo w grupie ochotniczek leczonych omeprazolem, symwastatyną lub midazolamem jako substratami markerowymi stwierdzono, że klinicznie istotna interakcja drospirenonu w dawce 3 mg z innymi substancjami czynnymi metabolizowanymi przy udziale cytochromu P450 jest mało prawdopodobna.
Dane kliniczne sugerują, że etynyloestradiol spowalnia klirens substratów CYP1A2, co prowadzi do niewielkiego (np. teofilina) lub umiarkowanego (np. tyzanidyna) zwiększenia ich stężenia w osoczu.
Inne rodzaje interakcji
Nie wykazano istotnego wpływu na stężenie potasu w surowicy podczas jednoczesnego stosowania drospirenonu oraz inhibitorów konwertazy angiotensyny (ang. ACE) lub niesteroidowych leków przeciwzapalnych (NLPZ) u pacjentek bez niewydolności nerek. Niemniej jednak nie prowadzono badań dotyczących jednoczesnego stosowania produktu Vixpo z antagonistami aldosteronu lub lekami moczopędnymi oszczędzającymi potas. W takim przypadku podczas pierwszego cyklu leczenia należy oznaczyć stężenie potasu w surowicy. Patrz także punkt 4.4.
Badania laboratoryjne
Stosowanie steroidów antykoncepcyjnych może wpływać na wyniki niektórych badań laboratoryjnych, w tym na: parametry biochemiczne czynności wątroby, tarczycy, nadnerczy i nerek, stężenia białek osoczowych (nośnikowych), np. globuliny wiążącej kortykosteroidy oraz stężenia frakcji lipidów/lipoprotein, parametry metabolizmu węglowodanów i wskaźniki krzepnięcia oraz fibrynolizy. Zmiany te zazwyczaj pozostają w zakresie wartości prawidłowych. Drospirenon powoduje zwiększenie aktywności reninowej osocza i, przez niewielkie działanie przeciwmineralokortykosteroidowe, zwiększenie stężenia aldosteronu w osoczu.
Interakcje farmakodynamiczne
Podczas badań klinicznych u pacjentów leczonych z powodu zakażenia wirusem zapalenia wątroby typu C (HCV) produktami leczniczymi zawierającymi ombitaswir z parytaprewirem i rytonawirem oraz dazabuwir z rybawiryną lub bez, zwiększenie aktywności aminotransferaz (AlAT) do wartości ponad pięciokrotnie większych niż górna granica normy występowało znacząco częściej u kobiet stosujących produkty lecznicze zawierające etynyloestradiol, takie jak złożone hormonalne produkty antykoncepcyjne.
Dodatkowo, również u pacjentów leczonych glekaprewirem z pibrentaswirem lub sofosbuwirem
z welpataswirem i woksylaprewirem, obserwowano zwiększenie aktywności AlAT u kobiet stosujących leki zawierające etynyloestradiol, takie jak złożone hormonalne środki antykoncepcyjne (patrz punkt 4.3). Dlatego pacjentka przyjmująca produkt leczniczy Vixpo musi zmienić metodę antykoncepcji na alternatywną (np. antykoncepcja zawierająca wyłącznie progestagen lub metody niehormonalne) przed rozpoczęciem leczenia za pomocą tych połączeń. Produkt leczniczy Vixpo można zastosować ponownie po 2 tygodniach po zakończeniu leczenia za pomocą wcześniej opisanych połączeń.
Wpływ na płodność, ciążę i laktację
Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn
Działania niepożądane
żylne zaburzenia zakrzepowo-zatorowe;
tętnicze zaburzenia zakrzepowo-zatorowe;
nadciśnienie tętnicze;
nowotwory wątroby;
wystąpienie lub pogorszenie stanów chorobowych, dla których związek ze stosowaniem COC nie jest jednoznaczny: choroba Leśniowskiego-Crohna, wrzodziejące zapalenie jelita grubego, padaczka, mięśniak macicy, porfiria, toczeń rumieniowaty układowy, opryszczka ciężarnych, pląsawica Sydenhama, zespół hemolityczno-mocznicowy, żółtaczka cholestatyczna;
ostuda;
ostre lub przewlekłe zaburzenia czynności wątroby mogą powodować konieczność przerwania stosowania COC do czasu powrotu wskaźników czynności wątroby do wartości prawidłowych.
Raka piersi rozpoznaje się nieznacznie częściej w grupie kobiet stosujących złożone doustne środki antykoncepcyjne. Ponieważ rak piersi występuje rzadko u kobiet w wieku poniżej 40 lat, wzrost liczby zdiagnozowanych przypadków jest niewielki w porównaniu do całkowitego ryzyka wystąpienia raka piersi. Związek przyczynowy ze stosowaniem COC nie jest znany. Dalsze informacje, patrz punkty 4.3 i 4.4.
Interakcje
Interakcje pomiędzy doustnymi środkami antykoncepcyjnymi a innymi produktami leczniczymi (induktorami enzymatycznymi) mogą prowadzić do krwawienia śródcyklicznego i (lub) braku skuteczności antykoncepcyjnej (patrz punkt 4.5).
Zgłaszanie podejrzewanych działań niepożądanych
Po dopuszczeniu produktu leczniczego do obrotu istotne jest zgłaszanie podejrzewanych działań niepożądanych. Umożliwia to nieprzerwane monitorowanie stosunku korzyści do ryzyka stosowania produktu leczniczego. Osoby należące do fachowego personelu medycznego powinny zgłaszać wszelkie podejrzewane działania niepożądane za pośrednictwem Departamentu Monitorowania Niepożądanych Działań Produktów Leczniczych Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych
i Produktów Biobójczych Al. Jerozolimskie 181C 02-222 Warszawa
Tel.: + 48 22 49 21 301
Faks: + 48 22 49 21 309
Strona internetowa: https://smz.ezdrowie.gov.pl
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Przedawkowanie
Vixpo, 3 mg + 0,02 mg, tabletki powlekane
24 tabletki powlekane barwy różowej, zawierające substancję czynną.
Każda tabletka powlekana zawiera 0,02 mg etynyloestradiolu i 3 mg drospirenonu.
Substancja pomocnicza o znanym działaniu: laktoza jednowodna.
Każda tabletka powlekana zawiera 44 mg laktozy jednowodnej.
4 tabletki powlekane placebo barwy białej: tabletki te nie zawierają substancji czynnych. Substancja pomocnicza o znanym działaniu: laktoza bezwodna.
Każda tabletka powlekana zawiera 89,5 mg laktozy bezwodnej.
Pełny wykaz substancji pomocniczych, patrz punkt 6.1.
Tabletka powlekana
Tabletka zawierająca substancję czynną to różowa, okrągła tabletka powlekana o średnicy 5,7 mm.
Tabletka placebo to biała, okrągła tabletka powlekana o średnicy 5,7 mm.
Doustna antykoncepcja.
Decyzja o przepisaniu produktu leczniczego Vixpo powinna zostać podjęta na podstawie indywidualnej oceny czynników ryzyka u kobiety, zwłaszcza ryzyka żylnej choroby zakrzepowo-zatorowej oraz ryzyka żylnej choroby zakrzepowo-zatorowej związanego ze stosowaniem produktu leczniczego Vixpo,
w odniesieniu do innych złożonych hormonalnych środków antykoncepcyjnych (ang. combined hormonal contraceptives, CHCs) (patrz punkty 4.3 i 4.4).
Dawkowanie
Jak stosować produkt leczniczy Vixpo
Tabletki należy przyjmować codziennie, mniej więcej o tej samej porze dnia, w kolejności wskazanej
na blistrze, popijając w razie potrzeby niewielką ilością płynu. Nie należy robić przerw w stosowaniu
tabletek. Przez 28 kolejnych dni należy przyjmować jedną tabletkę na dobę. Każde kolejne opakowanie należy rozpoczynać następnego dnia po przyjęciu ostatniej tabletki z poprzedniego opakowania.
Krwawienie z odstawienia rozpoczyna się przeważnie w 2.-3. dniu po rozpoczęciu przyjmowania tabletek placebo (ostatni rząd) i może nie zakończyć się przed rozpoczęciem następnego opakowania.
Jak rozpoczynać stosowanie produktu leczniczego Vixpo
Złożonych hormonalnych środków antykoncepcyjnych nie należy stosować w wymienionych poniżej przypadkach. Jeżeli którykolwiek z nich wystąpi po raz pierwszy w czasie stosowania CHC, produkt ten należy natychmiast odstawić.
Jeśli występuje którykolwiek z poniższych stanów lub czynników ryzyka, należy omówić z pacjentką zasadność stosowania produktu leczniczego Vixpo.
W razie pogorszenia lub wystąpienia po raz pierwszy któregokolwiek z wymienionych stanów lub czynników ryzyka kobieta powinna zgłosić się do lekarza prowadzącego, który zadecyduje, czy konieczne jest przerwanie stosowania produktu leczniczego Vixpo.
W przypadku podejrzenia lub potwierdzenia wystąpienia żylnej choroby zakrzepowo-zatorowej lub tętniczych zaburzeń zakrzepowo-zatorowych, stosowanie złożonych hormonalnych środków antykoncepcyjnych należy przerwać.
W przypadku rozpoczęcia stosowania leków przeciwzakrzepowych, należy zastosować alternatywną antykoncepcję, ze względu na działanie teratogenne leków przeciwzakrzepowych (kumaryny).
Zaburzenia układu krążenia
Ryzyko żylnej choroby zakrzepowo-zatorowej
Stosowanie jakichkolwiek złożonych hormonalnych środków antykoncepcyjnych (CHC) wiąże się ze zwiększonym ryzykiem żylnej choroby zakrzepowo-zatorowej w porównaniu do sytuacji, gdy terapia nie jest stosowana. Stosowanie produktów zawierających lewonorgestrel, norgestymat lub noretysteron jest związane z najmniejszym ryzykiem żylnej choroby zakrzepowo-zatorowej. Stosowanie innych produktów, takich jak produkt leczniczy Vixpo może być związane z dwukrotnie większym ryzykiem. Decyzja o zastosowaniu produktu spoza grupy najmniejszego ryzyka żylnej choroby zakrzepowo-zatorowej powinna zostać podjęta wyłącznie po rozmowie z pacjentką, w celu zapewnienia, że rozumie ona ryzyko żylnej choroby zakrzepowo-zatorowej związane z produktem leczniczym Vixpo, jak obecne czynniki ryzyka wpływają na to ryzyko oraz, że ryzyko żylnej choroby zakrzepowo-zatorowej jest największe w pierwszym roku stosowania. Istnieją pewne dowody, świadczące, że ryzyko zwiększa się, gdy złożone hormonalne środki antykoncepcyjne są przyjmowane ponownie po przerwie w stosowaniu wynoszącej 4 tygodnie lub więcej.
U około 2 na 10 000 kobiet, które nie stosują złożonych hormonalnych środków antykoncepcyjnych i nie są w ciąży, w okresie roku rozwinie się żylna choroba zakrzepowo-zatorowa. Jakkolwiek, ryzyko to może być znacznie wyższe, w zależności od czynników ryzyka występujących u danej pacjentki (patrz poniżej).
Szacuje się1, że spośród 10 000 kobiet, które stosują złożone hormonalne środki antykoncepcyjne zawierające drospirenon, u około 9 do 12 kobiet w okresie roku rozwinie się żylna choroba zakrzepowo- zatorowa, w porównaniu do około 62 kobiet stosujących złożone hormonalne środki antykoncepcyjne zawierające lewonorgestrel.
W obydwu sytuacjach, liczba przypadków żylnej choroby zakrzepowo-zatorowej przypadających na okres roku jest mniejsza niż oczekiwana liczba przypadków u kobiet w ciąży lub w okresie poporodowym.
Uwaga: należy zapoznać się z informacjami dotyczącymi jednocześnie stosowanych produktów leczniczych, aby rozpoznać możliwe interakcje.
Ciąża
Produkt leczniczy Vixpo nie jest wskazany do stosowania w okresie ciąży.
Jeżeli kobieta zajdzie w ciążę w trakcie stosowania produktu, produkt należy natychmiast odstawić. Obszerne badania epidemiologiczne nie ujawniły ani podwyższonego ryzyka urodzenia dziecka z wadami wrodzonymi przez pacjentki stosujące COC przed zajściem w ciążę, ani teratogennego wpływu COC na płód w przypadku nieumyślnego ich stosowania w ciąży.
W badaniach na zwierzętach stwierdzono działania niepożądane w okresie ciąży i laktacji (patrz punkt 5.3). Na podstawie tych danych, pochodzących z badań na zwierzętach, nie można wykluczyć działań niepożądanych ze względu na działanie hormonalne substancji czynnych. Jednakże ogólne
doświadczenie dotyczące stosowania COC w okresie ciąży nie wskazuje na występowanie rzeczywistych działań niepożądanych u ludzi.
Dostępne dane dotyczące stosowania produktu w okresie ciąży są zbyt ograniczone, by dopuszczać wnioski dotyczące niekorzystnego wpływu produktu na ciążę oraz stan zdrowia płodu lub noworodka. Brak dotychczas dostępnych odpowiednich danych epidemiologicznych.
Podejmując decyzję o ponownym rozpoczęciu stosowania Vixpo należy wziąć pod uwagę zwiększone ryzyko żylnej choroby zakrzepowo-zatorowej u kobiet w okresie poporodowym (patrz punkty 4.2 i 4.4).
Karmienie piersią
COC mogą wpływać na laktację, zmniejszając ilość i zmieniając skład mleka kobiecego. Dlatego też na ogół nie należy zalecać ich stosowania do czasu całkowitego odstawienia dziecka od piersi. Niewielkie
ilości steroidów antykoncepcyjnych i (lub) ich metabolitów mogą wydzielać się z mlekiem kobiet stosujących COC. Takie ilości mogą wpływać na dziecko.
Płodność
Produkt leczniczy Vixpo jest wskazany w zapobieganiu ciąży. Informacje dotyczące płodności, patrz punkt 5.1.
Nie przeprowadzono badań dotyczących wpływu na zdolność prowadzenia pojazdów i obsługiwania maszyn. U kobiet stosujących COC nie obserwowano wpływu na zdolność prowadzenia pojazdów
i obsługiwania maszyn.
Ciężkie działania niepożądane występujące u pacjentek stosujących złożone doustne środki antykoncepcyjne, patrz również punkt 4.4.
U kobiet przyjmujących produkt leczniczy Vixpo opisywano następujące działania niepożądane. Poniższa tabela przedstawia działania niepożądane według klasyfikacji układów i narządów MedDRA (ang. MedDRA SOC). Częstość określono na podstawie danych z badań klinicznych. Do opisania pewnych działań i ich synonimów oraz stanów pokrewnych zastosowano najbardziej odpowiednie nazewnictwo MedDRA.
Działania niepożądane związane ze stosowaniem produktu leczniczego Vixpo jako doustnego środka antykoncepcyjnego lub w leczeniu umiarkowanej postaci trądziku pospolitego według klasyfikacji układów i narządów MedDRA i terminów MedDRA.
Klasyfikacja układów i narządów (MedDRA wersja 9.1) | Często (≥1/100 do <1/10) | Niezbyt często (≥1/1000 do <1/100) | Rzadko (≥1/10 000 do <1/1000) | Częstość nieznana (nie może być określona na podstawie dostępnych danych) |
Zakażenia i zarażenia pasożytnicze | Kandydoza | |||
Zaburzenia krwi i układu chłonnego | Niedokrwistość Trombocytemia | |||
Zaburzenia układu immunologicznego | Reakcja alergiczna | Nadwrażliwość Nasilenie objawów dziedzicznego lub nabytego obrzęku naczynioruchowego | ||
Zaburzenia endokrynologiczne | Zaburzenia endokrynologiczne | |||
Zaburzenia metabolizmu i odżywiania | Zwiększone łaknienie Jadłowstręt Hiperkaliemia Hiponatremia |
Zaburzenia psychiczne | Chwiejność emocjonalna | Depresja Nerwowość Senność | Brak orgazmu Bezsenność | |
Zaburzenia układu nerwowego | Bóle głowy | Zawroty głowy pochodzenia ośrodkowego Parestezje | Zawroty głowy pochodzenia błędnikowego Drżenie | |
Zaburzenia oka | Zapalenie spojówek Suchość oczu Zaburzenia oczu | |||
Zaburzenia serca | Tachykardia | |||
Zaburzenia naczyniowe | Migrena Żylaki Nadciśnienie tętnicze | Zapalenie żyły Zaburzenia naczyniowe Krwawienie z nosa Omdlenia Żylna choroba zakrzepowo- zatorowa Tętnicze zaburzenia zakrzepowo- zatorowe | ||
Zaburzenia żołądka i jelit | Nudności | Ból brzucha Wymioty Niestrawność Wzdęcia Zapalenie błony śluzowej żołądka Biegunka | Powiększony brzuch Zaburzenia żołądkowo-jelitowe Uczucie pełności w brzuchu Przepuklina rozworu przełykowego Kandydoza jamy ustnej Zaparcia Suchość w jamie ustnej | |
Zaburzenia wątroby i dróg żółciowych | Ból woreczka żółciowego Zapalenie woreczka żółciowego | |||
Zaburzenia skóry i tkanki podskórnej | Trądzik Świąd Wysypka | Ostuda Egzema Wypadanie włosów Trądzikowe zapalenie skóry Suchość skóry Rumień guzowaty Nadmierne owłosienie Zaburzenia skóry Rozstępy na skórze Kontaktowe zapalenie skóry | Rumień wielopostaciowy |
Zapalenie skóry wywołane nadwrażliwością na światło Guzki na skórze | ||||
Zaburzenia mięśniowo- szkieletowe i tkanki łącznej | Bóle pleców Bóle kończyn Skurcze mięśni | |||
Zaburzenia układu rozrodczego i piersi | Ból piersi Krwotok maciczny* Brak miesiączki | Kandydoza pochwy Ból w obrębie miednicy Powiększenie piersi Dysplazja włóknisto- torbielowata piersi Krwawienie z macicy lub pochwy* Wydzielina z pochwy Uderzenia gorąca Zapalenie pochwy Zaburzenia cyklu miesiączkowego Bolesne miesiączkowanie Skąpe miesiączki Krwotok miesiączkowy Suchość pochwy Podejrzany wynik rozmazu w klasyfikacji Papanicolau Zmniejszenie libido | Bolesne stosunki płciowe Zapalenie sromu i pochwy Krwawienie po stosunku Krwawienie z odstawienia Torbiele w piersiach Rozrost piersi Nowotwory piersi Polipy szyjki macicy Atrofia endometrium Torbiele jajników Powiększenie macicy | |
Zaburzenia ogólne i stany w miejscu podania | Astenia Wzmożone pocenie Obrzęk (obrzęk ogólny, obrzęk obwodowy, obrzęk twarzy) | Złe samopoczucie | ||
Badania diagnostyczne | Zwiększenie masy ciała | Zmniejszenie masy ciała |
*Nieregularności w krwawieniu zazwyczaj ustępują podczas dłuższego stosowania produktu leczniczego.
Opis wybranych działań niepożądanych
U kobiet stosujących złożone hormonalne środki antykoncepcyjne odnotowano zwiększone ryzyko zakrzepicy żył i tętnic oraz zdarzeń zakrzepowo-zatorowych, w tym zawału serca, udaru, przemijającego
napadu niedokrwiennego, zakrzepicy żylnej oraz zatorowości płucnej, zostały one szerzej omówione
w punkcie 4.4.
U kobiet stosujących COC obserwowano następujące ciężkie działania niepożądane, które zostały omówione w punkcie 4.4:
Jak dotąd nie opisano przypadków przedawkowania produktu. Na podstawie doświadczeń ogólnych, dotyczących przedawkowania innych złożonych doustnych środków antykoncepcyjnych wiadomo, że w przypadku przedawkowania tabletek aktywnych mogą wystąpić następujące objawy: nudności,
wymioty oraz krwawienie z odstawienia. Krwawienie z odstawienia może wystąpić nawet u dziewcząt przed pierwszą miesiączką, jeśli omyłkowo przyjęły ten produkt leczniczy. Brak antidotum; dalsze leczenie powinno być objawowe.
WŁAŚCIWOŚCI FARMAKOLOGICZNE
Właściwości farmakodynamiczne
Właściwości farmakokinetyczne Drospirenon
Przedkliniczne dane o bezpieczeństwie
DANE FARMACEUTYCZNE
Wykaz substancji pomocniczych
Rdzeń tabletki:
Laktoza jednowodna
Skrobia żelowana kukurydziana Powidon K30 (E1201) Kroskarmeloza sodowa Polisorbat 80
Magnezu stearynian (E572)
Otoczka tabletki:
Alkohol poliwinylowy częściowo hydrolizowany Tytanu dwutlenek (E171)
Makrogol 3350 Talk
Żelaza tlenek żółty (E172) Żelaza tlenek czerwony (E172) Żelaza tlenek czarny (E172)
Powlekane tabletki placebo (białe):
Rdzeń tabletki:
Laktoza bezwodna Powidon K30 (E1201) Magnezu stearynian (E572)
Otoczka tabletki:
Niezgodności farmaceutyczne
Okres ważności
lata
Specjalne środki ostrożności podczas przechowywania
Rodzaj i zawartość opakowania
Specjalne środki ostrożności dotyczące usuwania
PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU
NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU I DATA PRZEDŁUŻENIA POZWOLENIA
DATA ZATWIERDZENIA LUB CZĘŚCIOWEJ ZMIANY TEKSTU
Grupa farmakoterapeutyczna: progestageny i estrogeny, dawki stałe, kod ATC: G03AA12 Wskaźnik Pearla dla niepowodzenia metody: 0,41 (górny dwustronny przedział ufności 95%: 0,85).
Ogólny wskaźnik Pearla (niepowodzenie metody + błąd pacjentki): 0,80 (górny dwustronny przedział ufności 95%: 1,30).
Mechanizm działania
Działanie antykoncepcyjne produktu Vixpo jest wynikiem interakcji różnych czynników, z których najważniejsze jest zahamowanie owulacji i zmiany w endometrium.
Działanie farmakodynamiczne
Schemat 24-dniowy wykazał lepszą supresję rozwoju pęcherzyków w badaniu hamowania owulacji przeprowadzonym w 3 cyklach miesiączkowych, porównującym drospirenon 3 mg + etynyloestradiol 0,02 mg w schemacie 21-dniowym i 24-dniowym. Po świadomym zastosowaniu błędnego dawkowania w trzecim cyklu miesiączkowym wykazano większy odsetek czynności owulacyjnej u kobiet stosujących schemat 21-dniowy w porównaniu do kobiet stosujących schemat 24-dniowy. Po zakończeniu leczenia, aktywność jajników wróciła do poziomu sprzed leczenia u 91,8% kobiet stosujących schemat 24-dniowy.
Skuteczność kliniczna i bezpieczeństwo stosowania
Vixpo to złożony doustny środek antykoncepcyjny, zawierający etynyloestradiol oraz progestagen - drospirenon. W dawkach terapeutycznych drospirenon wykazuje również działanie przeciwandrogenne oraz niewielkie przeciwmineralokortykosteroidowe. Nie wykazuje właściwości estrogennych, glikokortykosteroidowych oraz przeciwglikokortykosteroidowych. W związku z tym profil farmakologiczny drospirenonu jest podobny do naturalnego hormonu progesteronu.
Wyniki badań klinicznych wskazują na to, że ze względu na słabe właściwości przeciwmineralokortykosteroidowe produkt Vixpo ma słabe działanie przeciwmineralokortykosteroidowe.
Przeprowadzono dwa wieloośrodkowe, podwójnie ślepe, randomizowane badania kliniczne kontrolowane placebo w celu określenia bezpieczeństwa i skuteczności stosowania produktu u kobiet z umiarkowanym trądzikiem pospolitym.
Po 6 miesiącach leczenia produktem zawierającym etynyloestradiol i drospirenon, w porównaniu
z placebo stwierdzono statystycznie znamienne zmniejszenie liczby zmian zapalnych o 15,6% (49,3% wobec 33,7%), zmniejszenie zmian niezapalnych o 18,5% (40,6% wobec 22,1%) oraz zmniejszenie
o 16,5% liczby wszystkich zmian (44,6% wobec 28,1%). Ponadto większy procent osób badanych, 11,8% (18,6% wobec 6,8%) wykazywał się „czystą” skórą lub „prawie czystą” skórą według skali ISGA (ang. Investigator’s Static Global Assessment).
Wchłanianie
Drospirenon podany doustnie jest szybko i prawie całkowicie wchłaniany. Maksymalne stężenie substancji czynnej w surowicy wynoszące około 38 ng/ml występuje po około 1-2 godzinach po przyjęciu pojedynczej dawki. Biodostępność wynosi od 76% do 85%. Jednoczesne spożycie pokarmu nie wpływa na dostępność biologiczną drospirenonu.
Dystrybucja
Po podaniu doustnym stężenie drospirenonu w surowicy zmniejsza się z końcowym okresem półtrwania wynoszącym 31 godzin.
Drospirenon wiąże się z albuminami w osoczu; nie wiąże się z globuliną wiążącą hormony płciowe
(ang. SHBG) ani z globuliną wiążącą kortykosteroidy (ang. CBG). Tylko 3-5% całkowitej ilości substancji czynnej w surowicy występuje w postaci wolnego steroidu. Zwiększenie stężenia SHBG indukowane etynyloestradiolem nie wpływa na wiązanie drospirenonu z białkami. Średnia pozorna objętość dystrybucji drospirenonu wynosi 3,7±1,2 l/kg.
Metabolizm
Drospirenon po podaniu doustnym jest w znacznym stopniu metabolizowany. Główne metabolity
w osoczu to: kwasowa postać drospirenonu powstająca na skutek otwarcia pierścienia laktonowego oraz 3-siarczan 4,5-dihydrodrospirenonu, uzyskiwany poprzez redukcję i następnie sulfatację. Drospirenon podlega także metabolizmowi oksydacyjnemu katalizowanemu przez CYP4A4.
In vitro drospirenon, w stopniu niewielkim do umiarkowanego, hamuje enzymy cytochromu P450: CYP1A1, CYP2C9, CYP2C19 i CYP3A4.
Eliminacja
Klirens metaboliczny drospirenonu w surowicy wynosi 1,5±0,2 ml/min/kg. Jedynie śladowe ilości drospirenonu są wydalane w postaci niezmienionej. Metabolity drospirenonu są wydalane z kałem
i moczem w stosunku około 1,2-1,4. Okres półtrwania wydalania metabolitów z moczem oraz kałem wynosi około 40 godzin.
Warunki stanu stacjonarnego
Podczas cyklu stosowania leku maksymalne stężenie drospirenonu w surowicy w stanie stacjonarnym wynoszące około 70 ng/ml osiągano po około 8 dniach leczenia. Stężenie drospirenonu w surowicy charakteryzuje się kumulacją przy współczynniku równym w przybliżeniu 3, jako skutek proporcji końcowego okresu półtrwania i odstępu między dawkami.
Szczególne grupy pacjentów
Wpływ zaburzeń czynności nerek
Stężenia drospirenonu w surowicy w stanie stacjonarnym u kobiet z łagodnymi zaburzeniami czynności nerek (klirens kreatyniny CLcr = 50-80 ml/min) były porównywalne do stężeń u kobiet z prawidłową czynnością nerek. Stężenie drospirenonu w surowicy kobiet z umiarkowanymi zaburzeniami czynności nerek (CLcr = 30-50 ml/min) było średnio o 37% większe w porównaniu do stężeń u kobiet z prawidłową czynnością nerek. Drospirenon był również dobrze tolerowany u kobiet z łagodnymi lub umiarkowanymi zaburzeniami czynności nerek. Stosowanie drospirenonu nie wywierało żadnego klinicznie istotnego wpływu na stężenie potasu w surowicy.
Wpływ zaburzeń czynności wątroby
W badaniu z zastosowaniem pojedynczych dawek, u ochotników z umiarkowanymi zaburzeniami czynności wątroby stwierdzono zmniejszenie klirensu po podaniu doustnym (CL/F) o około 50% w porównaniu do osób z prawidłową czynnością wątroby. Obserwowane zmniejszenie klirensu
drospirenonu u ochotniczek z umiarkowanymi zaburzeniami czynności wątroby nie przekłada się na żadną widoczną różnicę stężenia potasu w surowicy. Nawet w przypadku współistniejącej cukrzycy oraz leczenia skojarzonego ze spironolaktonem (dwa czynniki zwiększające ryzyko hiperkaliemii) nie obserwowano zwiększenia stężenia potasu w surowicy ponad górną granicę normy. Można wnioskować, że drospirenon jest dobrze tolerowany przez pacjentki z łagodnymi lub umiarkowanymi zaburzeniami czynności wątroby (stopień B w skali Childa-Pugha).
Grupy etniczne
Nie obserwowano istotnych klinicznie różnic we właściwościach farmakokinetycznych drospirenonu oraz etynyloestradiolu pomiędzy Japonkami a kobietami rasy kaukaskiej.
Etynyloestradiol
Wchłanianie
Etynyloestradiol podany doustnie jest szybko i całkowicie wchłaniany. Maksymalne stężenie w surowicy wynoszące około 33 pg/ml występuje w ciągu 1-2 godzin po doustnym podaniu pojedynczej dawki.
Bezwzględna biodostępność wynosi około 60% z uwagi na efekt pierwszego przejścia oraz koniugację przed przejściem substancji do krążenia. Jednoczesne spożycie pokarmu spowodowało zmniejszenie biodostępności etynyloestradiolu u około 25% badanych osób, podczas gdy u pozostałych osób nie obserwowano żadnych zmian.
Dystrybucja
Stężenie etynyloestradiolu w surowicy ulega zmniejszeniu w dwóch fazach; końcowa faza dyspozycji charakteryzuje się okresem półtrwania wynoszącym około 24 godzin. Etynyloestradiol podlega silnemu, nieswoistemu wiązaniu przez albuminę (około 98,5%) i indukuje zwiększenie stężenia SHBG oraz globuliny wiążącej kortykosteroidy (ang. CBG) w surowicy. Oznaczona pozorna objętość dystrybucji wynosi 5 l/kg.
Metabolizm
Etynyloestradiol w znacznym stopniu ulega metabolizmowi pierwszego przejścia w jelicie i wątrobie. Etynyloestradiol jest głównie metabolizowany na drodze hydroksylacji pierścienia aromatycznego, jednak powstaje również wiele metabolitów hydroksylowanych i metylowanych, występujących w postaci wolnej oraz ulegających sprzęganiu i tworzących glukuronidy i siarczany. Klirens metaboliczny etynyloestradiolu w surowicy wynosi około 5 ml/min/kg.
In vitro, etynyloestradiol jest odwracalnym inhibitorem enzymów CYP2C19, CYP1A1 i CYP1A2 jak również nieodwracalnym inhibitorem CYP3A4/5, CYP2C8 i CYP2J2.
Eliminacja
Etynyloestradiol nie jest wydalany w znaczącym stopniu w postaci niezmienionej. Metabolity etynyloestradiolu są wydalane z moczem i żółcią w stosunku 4:6. Okres półtrwania wydalania metabolitów wynosi około jednego dnia.
Warunki stanu stacjonarnego
Stan stacjonarny ustala się w drugiej połowie cyklu leczenia; kumulacja etynyloestradiolu w surowicy charakteryzuje się współczynnikiem równym w przybliżeniu 2,0 do 2,3.
W badaniach na zwierzętach laboratoryjnych stwierdzono, że działania drospirenonu oraz etynyloestradiolu były ograniczone do związanych ze znanym działaniem farmakologicznym. Szczególnie w badaniu toksyczności w procesie reprodukcji stwierdzono działanie toksyczne wobec zarodków
i płodów u zwierząt; uznaje się, że działanie to jest swoiste dla każdego gatunku. U szczurów otrzymujących dawki przekraczające dawki przyjmowane z produktem odnotowano wpływ na różnicowanie płciowe płodów szczurów; tego efektu nie obserwowano u małp. Badania oceny ryzyka dla środowiska wykazały, że etynyloestradiol i drospirenon stwarzają potencjalne ryzyko dla środowiska wodnego (patrz punkt 6.6).
Powlekane tabletki aktywne (różowe):
Alkohol poliwinylowy częściowo hydrolizowany Tytanu dwutlenek (E171)
Makrogol 3350 Talk
Nie dotyczy.
Brak specjalnych zaleceń dotyczących przechowywania produktu leczniczego.
Przezroczyste do częściowo nieprzezroczystych blistry PVC/PVdC/Aluminium. Każdy blister zawiera
24 różowe powlekane tabletki aktywne i 4 białe powlekane tabletki placebo.
Wielkości opakowań:
1 x 28 tabletek powlekanych
3 x 28 tabletek powlekanych
6 x 28 tabletek powlekanych
13 x 28 tabletek powlekanych
Nie wszystkie wielkości opakowań muszą znajdować się w obrocie.
Ten produkt leczniczy może stanowić zagrożenie dla środowiska (patrz punkt 5.3). Wszelkie niewykorzystane resztki produktu leczniczego lub jego odpady należy usunąć zgodnie z lokalnymi przepisami.
Zakłady Farmaceutyczne POLPHARMA S.A.
ul. Pelplińska 19, 83-200 Starogard Gdański
Pozwolenie nr 21016
Data wydania pierwszego pozwolenia na dopuszczenie do obrotu: 01.03.2013 r. Data przedłużenia pozwolenia na dopuszczenie do obrotu: 26.03.2018 r.
CHARAKTERYSTYKI PRODUKTU LECZNICZEGO
25.10.2022 r.











