Spis treści:
- NAZWA PRODUKTU LECZNICZEGO
- SKŁAD JAKOŚCIOWY I ILOŚCIOWY
- POSTAĆ FARMACEUTYCZNA
- SZCZEGÓŁOWE DANE KLINICZNE
- WŁAŚCIWOŚCI FARMAKOLOGICZNE
- DANE FARMACEUTYCZNE
- PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU
- NUMER(Y) POZWOLENIA NA DOPUSZCZENIE DO OBROTU
- DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU / DATA PRZEDŁUŻENIA POZWOLENIA
- DATA ZATWIERDZENIA LUB CZĘŚCIOWEJ ZMIANY TEKSTU CHARAKTERYSTYKI PRODUKTU LECZNICZEGO
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
NAZWA PRODUKTU LECZNICZEGO
SKŁAD JAKOŚCIOWY I ILOŚCIOWY
POSTAĆ FARMACEUTYCZNA
SZCZEGÓŁOWE DANE KLINICZNE
Wskazania do stosowania
Przeciwwskazania
Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania
Interakcje z innymi produktami leczniczymi i inne rodzaje interakcji
Wpływ na płodność, ciążę i laktację
działanie toksyczne na układ krążenia i oddechowy (z przedwczesnym zamknięciem przewodu tętniczego i nadciśnieniem płucnym);
zaburzenia czynności nerek, mogące przekształcać się w niewydolność nerek z małowodziem; matkę i noworodka, pod koniec ciąży, na:
możliwe wydłużenie czasu krwawienia, działanie antyagregacyjne ujawniające się nawet po bardzo małych dawkach;
zahamowanie skurczów macicy, skutkujące opóźnionym lub wydłużonym porodem.
Wpływ na zdolność prowadzenia pojazdów obsługiwania maszyn
Działania niepożądane
Bardzo często ( 1/10)
- Często (≥1/100 do <1/10)
Niezbyt często (≥1/1 000 do <1/100)
- Rzadko (≥1/10 000 do <1/1 000)
Bardzo rzadko (<1/10 000)
Częstość nieznana (nie można ocenić na podstawie dostępnych danych).
Przedawkowanie
WŁAŚCIWOŚCI FARMAKOLOGICZNE
Właściwości farmakodynamiczne
Właściwości farmakokinetyczne
DANE FARMACEUTYCZNE
Wykaz substancji pomocniczych
Niezgodności farmaceutyczne
Okres ważności
Specjalne środki ostrożności dotyczące przechowywania
Rodzaj i zawartość opakowania
Szczególne środki ostrożności dotyczące usuwania
PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU
NUMER(Y) POZWOLENIA NA DOPUSZCZENIE DO OBROTU
DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU / DATA PRZEDŁUŻENIA POZWOLENIA
DATA ZATWIERDZENIA LUB CZĘŚCIOWEJ ZMIANY TEKSTU CHARAKTERYSTYKI PRODUKTU LECZNICZEGO
Nalgesin Mini, 220 mg, tabletki powlekane
Każda tabletka powlekana zawiera 220 mg naproksenu sodowego (Naproxenum natricum), co odpowiada 200 mg naproksenu.
Pełny wykaz substancji pomocniczych, patrz punkt 6.1.
Tabletki powlekane; owalne, lekko obustronnie wypukłe, jasnoszroniebieskie z metalowym połyskiem: grubość tabletki: 4,2 mm - 4,6 mm, długość tabletki : 13,5 mm - 13,8 mm.
Nalgesin Mini 220 mg tabletki powlekane wskazany jest u dorosłych i dzieci powyżej 16 lat w:
– krótkotrwałym leczeniu objawowym dolegliwości bólowych o małym i umiarkowanym nasileniu, takich jak: ból głowy, ból zęba, bolesne miesiączkowanie, bóle stawowe, bóle mięśniowe).
4.2. Dawkowanie i sposób podawania
Dawkowanie
Przyjmowanie produktu w najmniejszej dawce skutecznej przez najkrótszy okres konieczny do łagodzenia objawów zmniejsza ryzyko działań niepożądanych (patrz punkt 4.4).
Dorośli i młodzież w wieku powyżej 16 lat z masą ciała powyżej 50 kg.
Zalecana dawka dla osób dorosłych i młodzieży w wieku powyżej 16 lat z masą ciała powyżej 50 kg to 1 tabletka powlekana co 8-12 godzin.
Zamiennie można stosować dawkę dwóch tabletek powlekanych, a następnie, w razie konieczności, jednej tabletki po 8–12 godzinach.
Maksymalna dawka dobowa to 3 tabletki powlekane.
Czas trwania leczenia wynosi 7 dni. Jeżeli ból nie ustępuje lub występują nowe objawy, pacjent powinien zgłosić się do lekarza.
Pacjenci w podeszłym wieku
Maksymalna dawka dla pacjentów w podeszłym wieku to 2 tabletki powlekane na dobę, w dwóch dawkach podzielonych.
Produkt leczniczy należy stosować ostrożnie u pacjentów w podeszłym wieku ze względu na ryzyko przedawkowania (patrz punkt 4.4). Najmniejszą możliwą dawkę należy stosować w jak najkrótszym czasie leczenia, ponieważ pacjenci w podeszłym wieku są bardziej podatni na działania niepożądane.
Pacjenci z zaburzeniami czynności nerek
Maksymalna dawka dla pacjentów z zaburzeniami czynności nerek to 2 tabletki powlekane na dobę, w dwóch dawkach.
Produkt leczniczy należy stosować z zachowaniem ostrożności u pacjentów z zaburzeniami czynności nerek (patrz punkt 4.3 i 4.4). U pacjentów z klirensem kreatyniny powyżej 30 ml/min. wymagane jest zmniejszenie dawki w celu uniknięcia kumulacji metabolitów. Nie zaleca się stosowania naproksenu sodowego u pacjentów z klirensem kreatyniny poniżej 30 ml/minutę (patrz punkty 4.3 i 4.4).
Pacjenci z zaburzeniami czynności wątroby
Maksymalna dawka dla pacjentów z zaburzeniami czynności wątroby to 2 tabletki powlekane na dobę, w dwóch dawkach.
Produkt leczniczy należy stosować z zachowaniem ostrożności u pacjentów z zaburzeniem czynności wątroby (patrz punkt 4.4). U tych pacjentów konieczne jest zmniejszenie dawki z powodu ryzyka przedawkowania. Nie zaleca się stosowania naproksenu sodowego u pacjentów z ciężkimi
zaburzeniami czynności wątroby (patrz punkty 4.3 i 4.4).
Dzieci i młodzież
Dawkowanie w przypadku dzieci powyżej 16 lat o wadze ciała powyżej 50 kg jest takie samo, jak u osób dorosłych.
Nie należy stosować produktu leczniczego Nalgesin Mini u dzieci i młodzieży poniżej 16 lat, ponieważ nie jest możliwe dawkowanie w oparciu o wagę ciała.
Nie ustalono bezpieczeństwa stosowania i skuteczności produktu Nalgesin Mini u dzieci poniżej 2 lat. Sposób podawania
Tabletki należy połykać w całości, popijając odpowiednią ilością płynu, w trakcie lub po posiłkach. Pacjenci o wrażliwym żołądku powinni zażywać tabletki podczas posiłków.
Nadwrażliwość na substancję czynną lub którąkolwiek z substancji pomocniczych wymienionych w punkcie 6.1.
Skurcz oskrzeli w wywiadzie, astma, polipy w nosie, zapalenie błony śluzowej nosa, pokrzywka,
reakcje anafilaktyczne lub anafilaktoidalne związane ze stosowaniem kwasu acetylosalicylowego lub innych niesteroidowych leków przeciwzapalnych (NLPZ).
Czynna lub nawracająca w wywiadzie choroba wrzodowa żołądka i (lub) dwunastnicy lub krwawienia (dwa lub więcej wyraźne epizody potwierdzonego owrzodzenia lub krwawienia).
Krwawienie lub perforacja przewodu pokarmowego w wywiadzie, związane z wcześniejszym leczeniem NLPZ.
Ciężkie zaburzenia czynności wątroby. Ciężkie zaburzenia czynności nerek.
Ciężka niewydolność serca.
Ostatni trymestr ciąży (patrz punkt 4.6).
Krwawienie naczyniowo-mózgowe lub inne czynne krwawienia. Dzieci w wieku poniżej 2 lat.
Przyjmowanie produktu w najmniejszej skutecznej dawce przez najkrótszy okres konieczny do
łagodzenia objawów zmniejsza ryzyko działań niepożądanych (patrz punkt 4.2 i punkt wpływ na układ pokarmowy i sercowo naczyniowy)
Należy unikać jednoczesnego stosowania leku Nalgesin Mini z NLPZ, w tym selektywnych inhibitorów cyklooksygenazy-2.
Naproksen sodowy hamuje agregację płytek krwi i może wydłużyć czas krwawienia. Pacjenci, u których stwierdzono zaburzenia krzepnięcia lub którzy otrzymują leki wpływające na krzepnięcie krwi powinni być dokładnie obserwowani podczas przyjmowania produktu Nalgesin Mini.
Należy monitorować parametry nerek i wątroby podczas leczenia Nalgesin Mini, szczególnie u osób podeszłym wieku, u pacjentów z przewlekłą zastoinową niewydolnością serca lub przewlekłą niewydolnością nerek oraz u pacjentów w trakcie leczenia moczopędnego.
Osoby w podeszłym wieku
U osób w podeszłym wieku częściej występują reakcje niepożądane po podaniu NLPZ,
w szczególności krwawienie z przewodu pokarmowego lub perforacja, które to zdarzenia mogą prowadzić do zgonu (patrz punkt 4.2).
Krwawienie, owrzodzenie i perforacja przewodu pokarmowego
Krwawienie, owrzodzenie lub perforację przewodu pokarmowego mogące zakończyć się zgonem, opisywano po zastosowaniu wszystkich NLPZ, w każdym momencie leczenia, z towarzyszącymi objawami ostrzegawczymi lub poważnymi zdarzeniami dotyczącymi przewodu pokarmowego
w wywiadzie lub bez. Ryzyko krwawienia, owrzodzenia lub perforacji przewodu pokarmowego wzrasta wraz z większymi dawkami NLPZ, u pacjentów z owrzodzeniem w wywiadzie, szczególnie
jeśli było ono powikłane krwotokiem lub perforacją (patrz punkt 4.3) oraz u osób w podeszłym wieku. U pacjentów tych leczenie należy rozpoczynać od najmniejszej dostępnej dawki. U tych pacjentów oraz u pacjentów wymagających skojarzonego stosowania małych dawek aspiryny lub innych leków zwiększających ryzyko wystąpienia reakcji układu pokarmowego należy rozważyć leczenie skojarzone z lekami osłonowymi (np. mizoprostol lub inhibitory pompy protonowej) (patrz poniżej
i punkt 4.5).
Pacjentom, u których występowało działanie toksyczne dotyczące przewodu pokarmowego
w wywiadzie, szczególnie osobom w podeszłym wieku, zaleca się zgłaszanie wszelkich niepokojących objawów brzusznych (zwłaszcza krwawienia z przewodu pokarmowego), w szczególności
w początkowych etapach leczenia.
Należy zachować ostrożność u pacjentów otrzymujących leki mogące zwiększać ryzyko owrzodzenia lub krwawienia, takie jak doustne kortykosteroidy, leki przeciwzakrzepowe, np. warfaryna, selektywne inhibitory zwrotnego wychwytu serotoniny lub leki przeciwpłytkowe, np. aspiryna (patrz punkt 4.5).
Jeśli u pacjenta stosującego naproksen wystąpi krwawienie lub owrzodzenie przewodu pokarmowego, należy odstawić produkt leczniczy.
Należy zachować ostrożność podczas stosowania NLPZ u pacjentów z chorobami przewodu
pokarmowego w wywiadzie (wrzodziejące zapalenie jelita grubego, choroba Crohna), ponieważ ich stan może ulec pogorszeniu (patrz punkt 4.8 – Działania niepożądane).
Wpływ na układ sercowo-naczyniowy i naczynia mózgowe
Wymagane ( konsultacje z lekarzem lub farmaceutą) jest zachowanie ostrożności przed rozpoczęciem leczenia u pacjentów z nadciśnieniem tętniczym w wywiadzie i (lub) niewydolnością serca, gdyż w związku z leczeniem NLPZ opisywano zatrzymywanie płynów, nadciśnienie tętnicze oraz obrzęki.
Z badań klinicznych i danych epidemiologicznych wynika, że przyjmowanie niektórych NLPZ (szczególnie w dużych dawkach przez długi okres) może być związane z niewielkim zwiększeniem ryzyka incydentów zakrzepowych tętnic (np. zawał serca lub udar). Mimo, że z danych wynika, iż przyjmowanie naproksenu (w dawce dobowej 1000 mg) może być związane z małym ryzykiem,
jednak całkowicie ryzyka tego nie można wykluczyć. Nie ma wystarczających danych pozwalających
na wyciągnięcie jednoznacznych wniosków odnośnie wpływu małych dawek naproksenu 600 mg/dobę na ryzyko powstawania zakrzepów.
Reakcje skórne
Ciężkie reakcje skórne, niektóre z nich śmiertelne, włączając złuszczające zapalenie skóry, zespół Stevensa-Johnsona i toksyczne martwicze oddzielanie się naskórka, były bardzo rzadko zgłaszane w związku ze stosowaniem leków z grupy NLPZ. Wydaje się, że pacjenci są najbardziej narażeni na tego typu reakcje na wczesnym etapie leczenia, przy czym ujawnienie reakcji w większości przypadków następuje w ciągu pierwszego miesiąca leczenia. Należy zaprzestać stosowania naproksenu po wystąpieniu wysypki skórnej, uszkodzenia błony śluzowej lub innych objawów nadwrażliwości.
Środki ostrożności związane z płodnością
Istnieją dowody na to, że leki hamujące cyklooksygenazę / syntezę prostaglandyn mogą powodować zaburzenia płodności u kobiet przez wpływ na owulację. Działanie to jest przemijające i ustępuje po zakończeniu terapii.
Reakcje anafilaktyczne (anafilaktoidalne)
Reakcje nadwrażliwości (w tym anafilaktoidalne) mogą wystąpić u pacjentów zarówno ·z nadwrażliwością w wywiadzie na kwas acetylosalicylowy, inne niesteroidowe leki przeciwzapalne lub preparaty zawierające naproksen sodowy, jak i u pacjentów, u których taka nadwrażliwość wcześniej nie występowała.
Objawy te mogą pojawić się również u osób z obrzękiem naczynioruchowym, reakcjami bronchospastycznymi (np. astmą oskrzelową), nieżytem nosa, polipami nosa, chorobami alergicznymi, przewlekłymi zaburzeniami układu oddechowego lub wrażliwością na kwas acetylosalicylowy·w wywiadzie. Ma to również zastosowanie do pacjentów ze stwierdzoną alergią (objawiającą się, między innymi: reakcjami skórnymi, świądem lub wysypką) na naproksen sodowy lub inne NLPZ. Reakcje
anafilaktoidalne, w tym anafilaksja, mogą przynieść skutek śmiertelny.
Zaburzenia czynności wątroby
Produkt leczniczy należy stosować z zachowaniem ostrożności u pacjentów z zaburzeniami czynności wątroby (patrz punkty 4.2 i 4.3). U osób z przewlekłą alkoholową chorobą wątroby oraz prawdopodobnie z innymi postaciami marskości całkowite stężenie soli sodowej naproksenu w osoczu ulega zmniejszeniu, lecz stężenie frakcji wolnej zwiększa się. U tych pacjentów należy stosować najmniejsze skuteczne dawki produktu leczniczego.
Zaburzenia czynności nerek
Naproksen sodowy oraz jej metabolity wydalane są głównie przez nerki na drodze przesączania
kłębuszkowego, toteż należy zachować ostrożność w stosowaniu soli sodowej naproksenu u pacjentów z niewydolnością nerek (patrz punkt 4.2). U pacjentów z zaburzeniami czynności nerek należy kontrolować klirens kreatyniny podczas leczenia. Nie zaleca się stosowania soli sodowej naproksenu ·u pacjentów z klirensem kreatyniny poniżej 30 ml/min. (patrz punkt 4.3).
Dzieci i młodzież
Nie należy stosować produktu leczniczego Nalgesin Mini u dzieci i młodzieży poniżej 16 lat, ponieważ nie jest możliwe dawkowanie w oparciu o wagę ciała.
Substancje pomocnicze
Ten produkt leczniczy zawiera mniej niż 1 mmol sodu (23 mg) w jednej tabletce, a więc można powiedzieć, że zasadniczo „nie zawiera sodu”.
Następujące połączenia nie są zalecane:
Leki przeciwzakrzepowe
NLPZ mogą nasilać działanie leków przeciwzakrzepowych, takich jak warfaryna (patrz punkt 4.4).
Kwas acetylosalicylowy
Kliniczne dane farmakodynamiczne wskazują, że jednoczesne (w tym samym dniu) przyjmowanie naproksenu przez okres dłuższy niż jeden dzień, osłabia wpływ małych dawek kwasu
acetylosalicylowego na aktywność płytek krwi, co może trwać do kilku dni po zaprzestaniu stosowania naproksenu. Znaczenie kliniczne tego działania nie jest znane.
Leki przeciwpłytkowe i selektywne inhibitory zwrotnego wychwytu serotoniny (SSRI)
Podczas równoczesnego stosowania NLPZ istnieje zwiększone ryzyko krwawienia z przewodu pokarmowego (patrz punkt 4.4).
Kortykosteroidy
Podczas równoczesnego stosowania NLPZ istnieje zwiększone ryzyko owrzodzenia lub krwawienia z przewodu pokarmowego (patrz punkt 4.4).
Lit
Stężenie litu w osoczu może sie zwiększyć podczas równoczesnego stosowania naproksenu sodowego. Podczas jednoczesnego stosowania należy kontrolować stężenie litu w osoczu i dostosować odpowiednią dawkę.
Zachowanie szczególnej ostrożności jest zalecane w przypadku następujących połączeń: Inne NLPZ, w tym inhibitory COX-2;
Jednoczesne stosowanie dwóch lub więcej NLZ zwiększa ryzyko uszkodzenia układu pokarmowego
(patrz punkt 4.4).
Leki moczopędne, inhibitory konwertazy angiotensyny oraz antagoniści receptora angiotensyny II
NLPZ mogą zmniejszać działanie leków moczopędnych oraz innych leków przeciwnadciśnieniowych.
U niektórych pacjentów z zaburzeniem czynności nerek (np. pacjenci odwodnieni lub osoby
w podeszłym wieku z zaburzoną czynnością nerek), jednoczesne stosowanie inhibitorów konwertazy angiotensyny (ACE) lub antagonistów receptora angiotensyny II oraz leków hamujących
cyklooksygenazę może doprowadzić do dalszego pogorszenia czynności nerek, w tym do wystąpienia ostrej niewydolności nerek, która jest jednak zwykle odwracalna. Powyższe interakcje należy mieć na uwadze u pacjentów stosujących naproksen równocześnie z inhibitorami ACE oraz antagonistami
receptora angiotensyny II. Dlatego też takie połączenia należy stosować z zachowaniem ostrożności, szczególnie u osób w podeszłym wieku. Pacjentów należy odpowiednio nawodnić oraz monitorować czynność nerek po rozpoczęciu leczenia skojarzonego oraz okresowo w trakcie trwania terapii.
Zydowudyna
Badania in vitro pokazały, że równoczesne stosowanie naproksenu sodowego i zydowudyny zwiększa stężenie zydowudyny w osoczu i może zwiększać toksyczność hematologiczną.
Furosemid
Naproksen sodowy może zmniejszać natriuretyczne działanie furosemidu.
Pochodne hydantoiny lub pochodne sulfonylomocznika
Naproksen sodowy niemal całkowicie wiąże się z białkami osocza, toteż należy zachować ostrożność podczas równoczesnego stosowania pochodnych hydantoiny lub pochodnych sulfonylomocznika, ponieważ leki te również wiążą się z białkami osocza. Pacjenci przyjmujący jednocześnie naproksen i hydantoinę, sulfonamidy lub pochodne sulfonylomocznika, powinni być w razie potrzeby obserwowani pod kątem dostosowania dawki.
Metotreksat
Naproksen sodowy zmniejsza kanalikową sekrecję metotreksatu, toteż działanie toksyczne metotreksatu może zwiększać się podczas równoczesnego podawania obu leków.
Probenecyd
Podczas równoczesnego stosowania probenecydu biologiczny okres półtrwania naproksenu sodowego ulega wydłużeniu, a jego stężenie w osoczu wzrasta.
Cyklosporyna
Równoczesne stosowanie cyklosporyny może zwiększać ryzyko zaburzeń czynności nerek.
Badania laboratoryjne
Sugeruje się, że podawanie naproksenu sodowego należy przerwać 48 godzin przed wykonaniem badania czynności nadnerczy, ponieważ naproksen może zaburzać wyniki niektórych testów na oznaczenie steroidów 17-ketogennych. Naproksen sodowy może również zaburzać niektóre oznaczenia kwasu 5-hydroksyindolooctowego w moczu.
Pokarm
Pokarm może opóźniać wchłanianie naproksenu sodowego.
Alkohol
Spożywanie alkoholu może zwiększyć ryzyko wystąpienia krwotoku z przewodu pokarmowego, związanego ze stosowaniem NLPZ.
Dzieci i młodzież
Badania dotyczące interakcji prowadzone były jedynie u osób dorosłych.
Ciąża:
Hamowanie syntezy prostaglandyn może mieć niekorzystny wpływ na przebieg ciąży i (lub) rozwój
embrionalny lub płodowy. Dane epidemiologiczne sugerują zwiększenie częstości poronień, wad serca i wytrzewienia po zastosowaniu inhibitora syntezy prostaglandyn we wczesnej ciąży. Ryzyko
bezwzględne wad układu sercowo-naczyniowego zwiększyło się z wartości poniżej 1% do około 1,5%. Uważa się, że ryzyko wzrasta wraz z dawką i czasem trwania leczenia.
Wykazano, że u zwierząt podanie inhibitora syntezy prostaglandyn powoduje zwiększenie częstości przed- i poimplantacyjnych strat ciąż oraz obumarcia zarodka i płodu. Ponadto u zwierząt otrzymujących inhibitor syntezy prostaglandyn w okresie organogenezy opisywano zwiększoną
częstość występowania różnorodnych wad rozwojowych, w tym wad układu sercowo-naczyniowego. W pierwszym i drugim trymestrze ciąży nie należy stosować naproksenu sodowego, o ile nie jest to wyraźnie konieczne. Jeśli naproksen sodowy stosowany jest u kobiety planującej ciążę lub w
pierwszym bądź drugim trymestrze ciąży, należy stosować jak najmniejszą dawkę przez jak najkrótszy możliwy okres.
W trzecim trymestrze ciąży podanie inhibitorów syntezy prostaglandyn może narażać płód na:
W związku z powyższym naproksen sodowy jest przeciwwskazany w trzecim trymestrze ciąży.
Karmienie piersią
Nie zaleca się stosowania produktu Nalgesin Mini podczas karmienia piersią ponieważ naproxen sodowy przenika do mleka matki.
Płodność
Istnieją dowody na to, że leki hamujące cyklooksygenazę/syntezę prostaglandyn mogą powodować zaburzenia płodności u kobiet przez wpływ na owulację. Działanie to jest przemijające i ustępuje po zakończeniu terapii.
Nalgesin Mini nie ma wpływu lub ma nieznaczny wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn. Zawroty głowy, senność, zmęczenie i zaburzenia widzenia są możliwymi działaniami niepożądanymi stosowania NLPZ. W przypadku wystąpienia takich objawów nie należy prowadzić pojazdów i obsługiwać maszyn.
Podsumowanie profilu bezpieczeństwa
Wyniki badań klinicznych wykazują, że łączna liczba wszystkich zdarzeń niepożądanych, związanych ze stosowaniem soli sodowej naproksenu w pojedynczej małej dawce (1 tabletka), w pojedynczej dużej dawce (2 tabletki) oraz w kilku dawkach, jest porównywalna z liczbą zdarzeń niepożądanych po zażyciu placebo. Ból głowy (4,9%), nudności (4,4%), zawroty głowy (2,0%), wymioty (1,8%) oraz niestrawność (1,9%) należą do najczęściej zgłaszanych efektów niepożądanych (występujących ·u więcej niż 1 na 100 pacjentów). Poważne reakcje alergiczne występują bardzo rzadko.
Lista działań niepożądanych podano w tabeli.
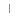
Często | Niezbyt często | Rzadko | Bardzo rzadko | Częstość nieznana | |
Zaburzenia krwi i układu chłonnego | granulocytopenia trombocytopenia niedokrwistość aplastyczna, niedokrwistość hemolityczna | ||||
Zaburzenia układu immunologicznego | reakcje alergiczne (w tym obrzęk twarzy, obrzęk naczynioruchowy | ||||
Zaburzenia psychiczne | zaburzenia snu pobudzenie | ||||
Zaburzenia układu nerwowego | bóle głowy, zawroty głowy, senność | reakcje przypominające zapalenie opon mózgowych |
Zaburzenia oka | zaburzenia widzenia | ||||
Zaburzenia ucha i błędnika | szumy uszne, zaburzenia słuchu | ||||
Zaburzenia serca | tachykardia obrzęk, nadciśnienie tetnicze, zastoinowa niewydolność serca | ||||
Zaburzenia naczyniowe | siniaki | ||||
Zaburzenia układu oddechowego, klatki piersiowej i śródpiersia | duszność astma | ||||
Zaburzenia żołądka i jelit | nudności niestrawność zgaga wymioty ból żołądka wzdęcie z oddawaniem gazów, ból brzucha | Biegunka, zaparcia | choroba wrzodowa perforacja przewodu pokarmowego krwawienie z przewodu pokarmowego krwawe wymioty smoliste stolce wrzodziejące zapalenie błony śluzowej jamy ustnej ostre zapalenie jelita grubego postęp Choroby Crohna | zapalenie jelita grubego zapalenie błony śluzowej jamy ustnej | zapalenie błony śluzowej żołądka |
Zaburzenia wątroby i dróg żółciowych | żółtaczka zapalenie wątroby nieprawidłowe wyniki badań czynnościowych wątroby, | ||||
Zaburzenia skóry i tkanki podskórnej | wysypki skórne, świąd | nadwrażliwość na światło, łysienie wysypka pęcherzykowo- pęcherzowe, takie jak |
Zespół Stevensa- Johnsona i toksyczne martwicze oddzielanie się naskórka | |||||
Zaburzenia nerek i dróg moczowych | zaburzenia czynności nerek | ||||
Zaburzenia ogólne i stany w miejscu podania | dreszcze obrzęki obwodowe |
Opis wybranych działań niepożądanych
Zaburzenia żołądka i jelit
Najczęściej obserwowane działania niepożądane dotyczą przewodu pokarmowego. Mogą występować owrzodzenia, perforacja czy krwawienie z przewodu pokarmowego, niekiedy zakończone zgonem,
w szczególności u osób w podeszłym wieku (patrz punkt 4.4). Po podaniu produktu leczniczego opisywano występowanie nudności, wymiotów, biegunki, zaparcia, niestrawności, bólu brzucha, smolistych stolców, krwawych wymiotów, wrzodziejącego zapalenia błony śluzowej jamy ustnej, zaostrzenia zapalenia jelita grubego i choroby Crohna (patrz punkt 4.4). Rzadziej obserwowano zapalenie błony śluzowej żołądka. Ryzyko krwawienia z przewodu pokarmowego jest zależne od dawki i czasu trwania leczenia.
Zaburzenia serca
W związku z leczeniem NLPZ zgłaszano występowanie obrzęków, nadciśnienia tętniczego i niewydolności serca.
Z badań klinicznych i danych epidemiologicznych wynika, że przyjmowanie niektórych NLPZ (szczególnie w dużych dawkach i w leczeniu długotrwałym) mogą być związane ze zwiększonym ryzykiem zakrzepicy tętniczej (np. zawał serca lub udar) (patrz punkt 4.4).
Zaburzenia skóry i tkanki podskórnej
Bardzo rzadko zgłaszano reakcje pęcherzowe, w tym zespół Stevensa-Johnsona i toksyczne martwicze oddzielanie się naskórka.
Zaburzenia układu immunologicznego
Jak w przypadku innych NLPZ, reakcje alergiczne o charakterze anafilaktycznym lub
anafilaktoidalnym mogą wystąpić zarówno u pacjentów, którzy zażywali wcześniej produkty lecznicze należące do tej grupy, jak i u tych, którzy nie mieli z nimi kontaktu. Typowe objawy reakcji
anafilaktycznej obejmują: ciężkie i nagłe niedociśnienie tętnicze, przyspieszanie lub zwalnianie
czynności serca, wyjątkowe zmęczenie lub osłabienie, lęk, pobudzenie, utratę przytomności, trudności w oddychaniu lub przełykaniu, świąd, pokrzywkę z towarzyszeniem obrzęku naczynioruchowego lub bez obrzęku, zaczerwienienie skóry, nudności, wymioty, skurczowe bóle brzucha, biegunkę.
Dzieci i młodzież
Uważa się, że częstość, rodzaj i nasilenie reakcji niepożądanych u dzieci są takie same, jak ·u dorosłych.
Zgłaszanie podejrzewanych działań niepożądanych
Po dopuszczeniu produktu leczniczego do obrotu istotne jest zgłaszanie podejrzewanych działań
niepożądanych. Umożliwia to nieprzerwane monitorowanie stosunku korzyści do ryzyka stosowania produktu leczniczego. Osoby należące do fachowego personelu medycznego powinny zgłaszać
wszelkie podejrzewane działania niepożądane za pośrednictwem Departamentu Monitorowania Niepożądanych Działań Produktów Leczniczych Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych, Al. Jerozolimskie 181C, 02-222 Warszawa, tel.: + 48 22 49 21 301, faks: + 48 22 49 21 309, e-mail: ndl@urpl.gov.pl
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Objawy
Przypadkowe lub celowe zażycie dużych ilości naproksenu sodowego może spowodować wystąpienie bólu brzucha, nudności, wymiotów, zawrotów głowy, szumów usznych, drażliwości, a w cięższych przypadkach również krwawych wymiotów, smolistych stolców, zaburzeń świadomości, zaburzeń oddychania, drgawek i niewydolności nerek.
Postępowanie
Zaleca się opróżnienie żołądka oraz zastosowanie standardowych działań wspomagających.
Niezwłoczne podanie (przed upływem godziny od zażycia) odpowiedniej ilości węgla aktywowanego może ograniczyć wchłanianie produktu leczniczego.
Dzieci i młodzież
Objawy oraz postępowanie w przypadku przedawkowania są takie same, jak u osób dorosłych.
Grupa farmakoterapeutyczna: Niesteroidowe leki przeciwzapalne i przeciwreumatyczne. Kod ATC: M01AE02.
Mechanizm działania
Naproksen sodowy jest niesteroidowym lekiem przeciwzapalnym o działaniu przeciwbólowym
i przeciwgorączkowym. Mechanizm działania polega na hamowaniu aktywności cyklooksygenazy, enzymu biorącego udział w syntezie prostaglandyn. W rezultacie dochodzi do zmniejszenia stężenia prostaglandyn w różnych płynach i tkankach organizmu.
Działania farmakodynamiczne
Naproksen sodowy wykazuje właściwości przeciwzapalne, przeciwbólowe i przeciwgorączkowe. Uważa się, że zahamowanie syntezy prostaglandyn wpływa pośrednio lub bezpośrednio na większość efektów farmakologicznych naproksenu sodowego, jak również innych NLPZ. Tak jak w przypadku innych NLPZ, naproksen sodowy jest silnym inhibitorem drugiej fazy agregacji płytek krwi in vitro.
Skuteczność kliniczna i bezpieczeństwo stosowania
Bezpieczeństwo stosowania oraz skuteczność naproksenu, jako leku OTC, została oceniona w kilkunastu randomizowanych, przeprowadzanych metodą podwójnie ślepej próby, kontrolowanych za pomocą placebo, porównawczych badań klinicznych z wykorzystaniem różnych modeli bólu, w tym ekstrakcji zębów, bólu pooperacyjnego, bólów miesiączkowych, bólu mięśni oraz bólu stawów w przebiegu zapalenia kostno-stawowego. Wszystkie badania kliniczne wykazały skuteczność przeciwbólową oraz znaczące złagodzenie bólu, przewyższające placebo oraz porównywalne z ibuprofenem i acetaminofenem.
Wchłanianie
Po podaniu doustnym naproksen sodowy ulega hydrolizie w kwaśnym soku żołądkowym. Po uwolnieniu mikrocząsteczki naproksenu są szybko rozpuszczane w jelicie cienkim. Powoduje to szybsze i całkowite wchłanianie naproksenu; dlatego też efektywne przeciwbólowo stężenie w osoczu osiągane jest w krótszym czasie. Maksymalne stężenie naproksenu w osoczu osiągane jest po upływie około godziny od podania.
Pokarm zmniejsza szybkość wchłaniania, jednak nie ogranicza jego zakresu. Ze względu na długi okres półtrwania działanie przeciwbólowe utrzymuje się do 12 godzin. Stan stacjonarny osiągany jest po podaniu do 5 dawek, tj. w ciągu 2–3 dni.
Dystrybucja
Po zastosowaniu standardowego dawkowania stężenie naproksenu w osoczu waha się od 23 mg/l do 49 mg/l.
Po osiągnięciu stężeń do 50 mg/l, 99% naproksenu ulega związaniu z białkami osocza. Po osiągnięciu większych stężeń frakcja wolna substancji czynnej zwiększa się.
Metabolizm
Około 70% substancji czynnej ulega wydaleniu w postaci niezmienionej metabolicznie; 60% związane jest z kwasem glukuronowym lub z innymi substancjami sprzęgającymi. Pozostałe 30% naproksenu metabolizowane jest do nieaktywnego 6-demetylonaproksenu.
Wydalanie
Około 95% naproksenu wydalane jest w moczu, a 5% w kale.
Biologiczny okres półtrwania naproksenu wynosi 12 do 15 godzin i nie zależy od dawkowania i stężenia naproksenu w osoczu. Klirens kreatyniny zależy od stężenia naproksenu w osoczu,
prawdopodobnie z powodu zwiększonej frakcji wolnej substancji czynnej po osiągnięciu większych stężeń w osoczu.
Liniowość / nieliniowość
Stężenie naproksenu w osoczu zwiększa się proporcjonalnie do wielkości dawki: do 500 mg. Dla
większych dawek ten wzrost jest mniej proporcjonalny, ze względu na nasycenie wiązania naproksenu przez białka osocza, klirens kreatyniny również się zwiększa.
Zaburzenia czynności nerek
Wydalanie naproksenu zmniejsza się w przypadku ciężkiej choroby nerek, jednak w przypadku stosowania dawek terapeutycznych nie odnotowano znaczącej kumulacji.
Zaburzenia czynności wątroby
U pacjentów z poważnymi zaburzeniami czynności wątroby wzrasta stężenie niezwiązanej postaci naproksenu w osoczu.
Osoby w podeszłym wieku
Stężenie niezwiązanej postaci naproksenu w osoczu jest podwyższone, chociaż poziom całkowitego stężenia w osoczu nie ulega zmianie.
Dzieci i młodzież
Uważa się, że parametry farmakokinetyczne są takie same, jak u dorosłych.
5.3. Przedkliniczne dane o bezpieczeństwie
Wyniki badań toksykologicznych pokazały względnie małą toksyczność naproksenu sodowego: działania niepożądane dotyczą głównie przewodu pokarmowego.
Po podaniu doustnym, wartość LD50 wyniosła około 0,5 g/kg masy ciała u szczurów i więcej niż 1,0 g/kg masy ciała u myszy, chomików i psów. Badania toksykologiczne wykazały, że myszy, króliki, małpy i świnie tolerują dobrze dawki wielokrotne naproksenu sodowego; działanie toksyczne jest wyraźniej zaznaczone u szczurów, a szczególnie u psów. Podobnie jak w przypadku wielokrotnego
podawania innych niesteroidowych leków przeciwzapalnych działania niepożądane najczęściej dotyczą przewodu pokarmowego i nerek.
Nie obserwowano znaczącego wpływu na płodność, niemniej jednak istnieją dowody na to, że leki hamujące cyklooksygenazę (enzym uczestniczący w syntezie prostaglandyn) mogą powodować
zaburzenia płodności u kobiet przez wpływ na owulację. Działanie to jest przemijające i ustępuje po zakończeniu terapii.
Nie obserwowano działania embriotoksycznego i teratogennego. Jednak naproksen sodowy podawany w późnym okresie ciąży, powoduje wydłużenie czasu trwania ciąży i opóźnienie porodu. Ustalono
także, że naproksen sodowy może mieć niepożądany wpływ na układ sercowo-naczyniowy u płodu (przedwczesne zamknięcie przewodu Botalla, zastoinowa niewydolność serca, nadciśnienie płucne). Nie stwierdzono mutagennego lub karcynogennego działania naproksenu sodowego.
Naproksen sodowy przenika przez łożysko oraz przedostaje się do mleka.
W badaniach pozaklinicznych skutki obserwowano jedynie w przypadkach narażenia, które uznano za przekraczające w stopniu wystarczającym maksymalne narażenie człowieka, co wskazuje na
niewielkie znaczenie tych obserwacji w aspekcie użycia klinicznego.
Rdzeń tabletki:
Powidon K 30
Celuloza mikrokrystaliczna Talk
Magnezu stearynian
Otoczka tabletki:
Opadry YS-1-4215, E 132
o składzie:
Hypromeloza
Tytanu dwutlenek (E 171) Makrogol 8000
Indygotyna (E 132) Hypromeloza 6cp Makrogol 8000 Candurin Silver Lustre o składzie:
Tytanu dwutlenek (E 171)
Krzemian glinowo-potasowy (E 555)
Nie dotyczy.
3 lata.
Nie przechowywać w temperaturze powyżej 25°C.
Przechowywać w oryginalnym opakowaniu w celu ochrony przed światłem.
Blister (folia PVC/Aluminium): 10, 20 lub 30 tabletek powlekanych w tekturowym pudełku. Nie wszystkie wielkości opakowań muszą znajdować się w obrocie.
Bez specjalnych wymagań dotyczących usuwania.
KRKA, d.d., Novo mesto Šmarješka cesta 6
8501 Novo mesto Słowenia
Pozwolenie nr 21304
Data wydania pierwszego pozwolenia na dopuszczenie do obrotu: 03.07.2013 Data ostatniego przedłużenia pozwolenia: 03.08.2020
30.09.2021
Szczegółowe informacje o tym leku znajdują się na stronie internetowej Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych http://urpl.gov.pl











