Spis treści:
- NAZWA PRODUKTU LECZNICZEGO
- SKŁAD JAKOŚCIOWY I ILOŚCIOWY
- POSTAĆ FARMACEUTYCZNA
- SZCZEGÓŁOWE DANE KLINICZNE
- WŁAŚCIWOŚCI FARMAKOLOGICZNE
- DANE FARMACEUTYCZNE
- PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU
- NUMERY POZWOLEŃ NA DOPUSZCZENIE DO OBROTU
- DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU I DATA PRZEDŁUŻENIA POZWOLENIA
- DATA ZATWIERDZENIA LUB CZĘŚCIOWEJ ZMIANY TEKSTU CHARAKTERYSTYKI PRODUKTU LECZNICZEGO
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
NAZWA PRODUKTU LECZNICZEGO
SKŁAD JAKOŚCIOWY I ILOŚCIOWY
POSTAĆ FARMACEUTYCZNA
SZCZEGÓŁOWE DANE KLINICZNE
Wskazania do stosowania
dorosłych pacjentów oraz dzieci i młodzieży z nowo rozpoznaną przewlekłą białaczką szpikową (ang. Chronic Myeloid Leukaemia - CML) z chromosomem Philadelphia (Bcr-Abl, Ph+), którzy nie kwalifikują się do zabiegu transplantacji szpiku jako leczenia pierwszego rzutu.
dorosłych pacjentów oraz dzieci i młodzieży z CML Ph+ w fazie przewlekłej, gdy leczenie interferonem alfa jest nieskuteczne, w fazie akceleracji choroby lub w przebiegu przełomu blastycznego;
dorosłych pacjentów oraz dzieci i młodzieży z nowo rozpoznaną ostrą białaczką limfoblastyczną z chromosomem Philadelphia (Ph+ ALL) w skojarzeniu z chemioterapią.
dorosłych pacjentów z nawracającą lub oporną na leczenie Ph+ ALL w monoterapii.
dorosłych pacjentów z zespołami mielodysplastycznymi/mieloproliferacyjnymi (ang. myelodysplastic/myeloproliferate - MDS/MPD) związanymi z rearanżacją genu receptora płytkopochodnego czynnika wzrostu (ang. platelet-derived growth factor receptor - PDGFR).
dorosłych pacjentów z zaawansowanym zespołem hipereozynofilowym (ang. Hypereosinophilic Syndrome - HES) i (lub) przewlekłą białaczką eozynofilową (ang. Chronic Eosinophilic Leukemia - CEL) z rearanżacją FIP1L1-PDGFR.
Nie określono wpływu produktu leczniczego Meaxin na wynik transplantacji szpiku.
Meaxin jest wskazany w:
leczeniu dorosłych pacjentów ze złośliwymi, nieoperacyjnymi i (lub) z przerzutami, Kit (CD 117) dodatnimi nowotworami podścieliskowymi przewodu pokarmowego (ang. Gastrointestinal Stromal Tumors - GIST).
leczeniu adjuwantowym dorosłych pacjentów z istotnym ryzykiem nawrotu po zabiegu usunięcia Kit (CD 117)-dodatnich nowotworów podścieliskowych przewodu pokarmowego (GIST). Pacjenci z małym lub bardzo małym ryzykiem nawrotu nie powinni otrzymywać leczenia adjuwantowego.
leczeniu dorosłych pacjentów z nieoperacyjnymi guzowatymi włókniakomięsakami skóry (ang. dermatofibrosarcoma protuberans - DFSP) oraz dorosłych pacjentów z nawracającymi i (lub) z przerzutami DFSP, którzy nie kwalifikują się do zabiegu chirurgicznego.
Dawkowanie i sposób podawania
Przeciwwskazania
Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania
Interakcje z innymi produktami leczniczymi i inne rodzaje interakcji
Wpływ na płodność, ciążę i laktację
Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn
Działania niepożądane
Zapalenie płuc zgłaszano najczęściej u pacjentów z CML po transformacji oraz u pacjentów z GIST.
Ból głowy występował najczęściej u pacjentów z GIST.
W analizie pacjento-lat, zdarzenia niepożądane ze strony serca, w tym zastoinowa niewydolność serca były częściej obserwowane u pacjentów z CML po transformacji niż u pacjentów z CML w fazie przewlekłej.
Zaczerwienienie twarzy występowało najczęściej u pacjentów z GIST, a krwawienie (krwiak, krwotok) było najczęściej obserwowane u pacjentów z GIST oraz u pacjentów z CML po transformacji (CML-AP i CML-BC).
Wysięk opłucnowy zgłaszano częściej u pacjentów z GIST oraz u pacjentów z CML po transformacji (CML-AP i CML-BC) niż u pacjentów z CML w fazie przewlekłej.
Zgłoszono kilka przypadków niewydolności wątroby i martwicy wątroby zakończonych zgonem.
Bóle mięśniowo-szkieletowe występujące podczas stosowania imatynibu lub po zaprzestaniu stosowania, które obserwowano po wprowadzeniu do obrotu.
Bóle mięśniowo-szkieletowe i związane z nimi działania niepożądane występowały częściej u pacjentów z CML w porównaniu z pacjentami z GIST.
Przypadki zgonów zgłaszano u pacjentów z chorobą zaawansowaną, ciężkimi zakażeniami, znaczną neutropenią i innymi poważnymi chorobami współistniejącymi.
W tym rumień guzowaty.
Przedawkowanie
WŁAŚCIWOŚCI FARMAKOLOGICZNE
Właściwości farmakodynamiczne
Właściwości farmakokinetyczne
Przedkliniczne dane o bezpieczeństwie
DANE FARMACEUTYCZNE
Wykaz substancji pomocniczych
Niezgodności farmaceutyczne
Okres ważności
Specjalne środki ostrożności podczas przechowywania
Rodzaj i zawartość opakowania
Specjalne środki ostrożności dotyczące usuwania
PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU
NUMERY POZWOLEŃ NA DOPUSZCZENIE DO OBROTU
DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU I DATA PRZEDŁUŻENIA POZWOLENIA
DATA ZATWIERDZENIA LUB CZĘŚCIOWEJ ZMIANY TEKSTU CHARAKTERYSTYKI PRODUKTU LECZNICZEGO
Meaxin, 100 mg, tabletki do sporządzania zawiesiny doustnej Meaxin, 400 mg, tabletki do sporządzania zawiesiny doustnej
Meaxin, 100 mg, tabletki do sporządzania zawiesiny doustnej
Każda tabletka do sporządzania zawiesiny doustnej zawiera 100 mg imatynibu (w postaci imatynibu mezylanu).
Meaxin, 400 mg, tabletki do sporządzania zawiesiny doustnej
Każda tabletka do sporządzania zawiesiny doustnej zawiera 400 mg imatynibu (w postaci imatynibu mezylanu).
Pełny wykaz substancji pomocniczych, patrz punkt 6.1.
Tabletka do sporządzania zawiesiny doustnej
100 mg: żółtawobiałe, okrągłe tabletki ze ściętymi brzegami, z linią podziału po jednej stronie i średnicy 12 mm. Tabletkę można podzielić na równe dawki.
400 mg: żółtawobiałe, okrągłe, obustronnie wypukłe tabletki o średnicy 21 mm.
Produkt leczniczy Meaxin jest wskazany w leczeniu:
U dorosłych pacjentów oraz dzieci i młodzieży skuteczność imatynibu oceniana jest na podstawie wskaźnika ogólnej odpowiedzi hematologicznej i cytogenetycznej oraz okresu przeżycia wolnego od progresji choroby w CML, współczynnika odpowiedzi hematologicznej i cytogenetycznej w Ph+ ALL, MDS/MPD, współczynnika odpowiedzi hematologicznej w HES/CEL oraz na podstawie obiektywnego współczynnika odpowiedzi u dorosłych pacjentów z nieoperacyjnymi i (lub) z przerzutami GIST i DFSP oraz na podstawie okresu przeżycia bez wznowy w leczeniu adjuwantowym GIST. Doświadczenie ze stosowaniem imatynibu u pacjentów z MDS/MPD związanymi z rearanżacją genu PDGFR jest bardzo ograniczone (patrz punkt 5.1). Z wyjątkiem nowo rozpoznanej przewlekłej białaczki szpikowej (CML), brak kontrolowanych badań klinicznych wykazujących korzyść kliniczną lub zwiększone przeżycie w tych wskazaniach.
Dawkowanie
Leczenie powinien rozpoczynać lekarz mający doświadczenie w leczeniu pacjentów z hematologicznymi nowotworami złośliwymi i mięsakami złośliwymi.
Dla dawek 400 mg i większych (zalecane dawkowanie - patrz poniżej) dostępna jest tabletka o mocy 400 mg (nie można jej podzielić na równe dawki).
Dla dawek innych niż 400 mg i 800 mg (zalecane dawkowanie - patrz poniżej) dostępna jest podzielna tabletka o mocy 100 mg.
Zalecaną dawkę należy przyjmować doustnie podczas posiłku, w celu zminimalizowania ryzyka podrażnienia przewodu pokarmowego. Dawki 400 mg lub 600 mg należy podawać raz na dobę, natomiast dobową dawkę 800 mg należy podawać w dwóch dawkach po 400 mg, rano i wieczorem.
Tabletkę do sporządzania zawiesiny doustnej należy zawiesić w niegazowanej wodzie lub soku jabłkowym. Potrzebną ilość tabletek należy umieścić w odpowiedniej ilości płynu (co najmniej 25 ml dla tabletki 100 mg i co najmniej 100 ml dla tabletki 400 mg) i mieszać łyżeczką, aż do uzyskania jednorodnej zawiesiny. Zawiesina powinna zostać podana natychmiast po całkowitym rozpadzie tabletki (tabletek).
Po wypiciu zawiesiny, pozostałość należy ponownie zawiesić w niewielkiej ilości wody lub soku i połknąć. Tabletek nie należy żuć ani połykać w całości.
Dawkowanie w CML u dorosłych pacjentów
Zalecane dawkowanie produktu leczniczego Meaxin wynosi 400 mg na dobę u dorosłych pacjentów w fazie przewlekłej CML. Faza przewlekła jest definiowana jako stan, który spełnia wszystkie podane kryteria: ilość blastów we krwi i szpiku jest <15%, ilość granulocytów zasadochłonnych we krwi obwodowej jest <20%, a liczba płytek jest >100 x 109/l.
Zalecane dawkowanie produktu leczniczego Meaxin wynosi 600 mg na dobę u dorosłych pacjentów w fazie akceleracji. Faza akceleracji jest definiowana jako stan, który spełnia którekolwiek z podanych kryteriów: ilość blastów we krwi lub szpiku jest ≥15% ale <30%, ilość blastów i promielocytów we
krwi lub szpiku jest ≥30% (pod warunkiem, że ilość blastów jest <30%), ilość granulocytów zasadochłonnych we krwi obwodowej jest ≥20%, liczba płytek jest <100 x 109/l i jest to niezwiązane z leczeniem.
Zalecane dawkowanie produktu leczniczego Meaxin wynosi 600 mg na dobę u dorosłych pacjentów w przebiegu przełomu blastycznego. Przełom blastyczny jest definiowany jako stan, w którym liczba blastów we krwi lub szpiku wynosi ≥30%, lub jako obecność ognisk pozaszpikowych choroby innych niż w wątrobie i śledzionie.
Czas trwania leczenia: W badaniach klinicznych leczenie imatynibem było kontynuowane do czasu progresji choroby. Nie badano wpływu zaprzestania leczenia po osiągnięciu pełnej odpowiedzi cytogenetycznej.
U pacjentów, u których nie występują ciężkie działania niepożądane oraz ciężka neutropenia lub trombocytopenia nie spowodowane białaczką, można rozważyć zwiększenie dawki z 400 mg do 600 mg lub 800 mg w leczeniu fazy przewlekłej choroby, lub z 600 mg do 800 mg (podawanych w dwóch dawkach po 400 mg) w leczeniu fazy akceleracji lub przełomu blastycznego w następujących przypadkach: postęp choroby (na każdym jej etapie), brak zadowalającej odpowiedzi hematologicznej po co najmniej 3 miesiącach leczenia, brak odpowiedzi cytogenetycznej po 12 miesiącach leczenia, lub utrata osiągniętej uprzednio odpowiedzi hematologicznej i (lub) cytogenetycznej. Po zwiększeniu dawki należy uważnie obserwować pacjentów, ponieważ jej zwiększenie może spowodować nasilenie występowania działań niepożądanych.
Dawkowanie w CML u dzieci
Dawkowanie u dzieci i młodzieży należy ustalać na podstawie powierzchni ciała (mg/m2 pc.). U dzieci i młodzieży w fazie przewlekłej CML i fazach zaawansowanych CML zaleca się dawkę 340 mg/m2 pc. na dobę (nie należy przekraczać całkowitej dawki 800 mg). Produkt można podawać w postaci jednej dawki na dobę lub można podzielić dawkę dobową na dwie części - jedną podawaną rano
i drugą wieczorem. Zalecenia dotyczące dawkowania są oparte na stosowaniu u małej liczby dzieci i młodzieży (patrz punkty 5.1 i 5.2).
Brak doświadczenia w leczeniu dzieci w wieku poniżej 2 lat.
U dzieci i młodzieży, u których nie występują ciężkie działania niepożądane oraz ciężka neutropenia lub trombocytopenia nie spowodowane białaczką, można rozważyć zwiększenie dawki z 340 mg/m2 pc. do 570 mg/m2 pc. na dobę (nie należy przekraczać całkowitej dawki 800 mg) w następujących przypadkach: postęp choroby (na każdym jej etapie), brak zadowalającej odpowiedzi hematologicznej po co najmniej 3 miesiącach leczenia, brak odpowiedzi cytogenetycznej po 12 miesiącach leczenia, lub utrata osiągniętej uprzednio odpowiedzi hematologicznej i (lub) cytogenetycznej. Po zwiększeniu dawki należy uważnie obserwować pacjentów, ponieważ jej zwiększenie może spowodować nasilenie występowania działań niepożądanych.
Dawkowanie w Ph+ ALL u dorosłych pacjentów
Zalecana dawka produktu leczniczego Meaxin to 600 mg/dobę u dorosłych pacjentów z Ph+ ALL. We wszystkich fazach leczenia konieczny jest nadzór hematologów doświadczonych w prowadzeniu pacjentów z tą chorobą.
Schemat dawkowania: Na podstawie istniejących danych, wykazano skuteczność i bezpieczeństwo stosowania imatynibu w dawce 600 mg na dobę w skojarzeniu z chemioterapią w fazie indukcji, konsolidacji i leczenia podtrzymującego (patrz punkt 5.1) u dorosłych pacjentów z nowo rozpoznaną Ph+ ALL. Czas trwania leczenia imatynibem może różnić się w zależności od wybranego programu leczenia, jednak na ogół dłuższa ekspozycja na imatynib dawała lepsze wyniki.
Dla dorosłych pacjentów z nawracającą lub oporną na leczenie Ph+ ALL monoterapia imatynibem w dawce 600 mg na dobę jest bezpieczna, skuteczna i może być stosowana do czasu wystąpienia progresji choroby.
Dawkowanie w Ph+ ALL u dzieci
Dawkowanie u dzieci należy ustalać na podstawie powierzchni ciała (mg/m2 pc.). U dzieci z Ph+ ALL zaleca się dawkę dobową w wysokości 340 mg/m2 pc. (nie należy stosować dawki całkowitej większej niż 600 mg).
Dawkowanie w MDS/MPD
Zalecana dawka produktu leczniczego Meaxin to 400 mg/dobę u dorosłych pacjentów z MDS/MPD.
Czas trwania leczenia: W jedynym badaniu klinicznym przeprowadzonym do tej pory, leczenie imatynibem kontynuowano do chwili wystąpienia progresji choroby (patrz punkt 5.1). W momencie przeprowadzania analizy, mediana czasu leczenia wynosiła 47 miesięcy (24 dni - 60 miesięcy).
Dawkowanie w HES/CEL
Zalecana dawka produktu leczniczego Meaxin wynosi 100 mg na dobę u dorosłych pacjentów z HES/CEL.
Można rozważyć zwiększenie dawki ze 100 mg do 400 mg przy braku reakcji niepożądanych na lek, jeśli badania wykażą niewystarczającą odpowiedź na leczenie.
Leczenie powinno być kontynuowane tak długo, jak długo pacjent odnosi z niego korzyść. Dawkowanie w GIST
Zalecana dawka produktu leczniczego Meaxin u dorosłych pacjentów z postaciami GIST
nieoperacyjnymi i (lub) z przerzutami, wynosi 400 mg/dobę.
Dane dotyczące zwiększenia dawki leku z 400 mg do 600 mg lub 800 mg u pacjentów, u których wystąpiła progresja choroby w czasie stosowania mniejszej dawki, są ograniczone (patrz punkt 5.1).
Czas leczenia: w badaniach klinicznych prowadzonych u pacjentów z GIST imatinib był podawany aż do wystąpienia progresji choroby. W momencie analizy danych mediana czasu leczenia wynosiła 7 miesięcy (od 7 dni do 13 miesięcy). Skutek zaprzestania leczenia po osiągnięciu odpowiedzi na leczenie nie został zbadany.
Zalecana dawka produktu leczniczego Meaxin w leczeniu adjuwantowym dorosłych pacjentów po resekcji GIST wynosi 400 mg na dobę. Optymalny czas trwania leczenia nie został jeszcze ustalony. Długość leczenia tego wskazania w badaniu klinicznym wynosiła 36 miesięcy (patrz punkt 5.1).
Dawkowanie w DFSP
U dorosłych pacjentów z DFSP zalecana dawka produktu leczniczego Meaxin to 800 mg na dobę.
Zmiana dawkowania ze względu na działania niepożądane
Pozahematologiczne działania niepożądane
W przypadku wystąpienia ciężkich, pozahematologicznych działań niepożądanych należy przerwać leczenie imatynibem do czasu ich ustąpienia. Następnie, w zależności od początkowego stopnia ciężkości działania niepożądanego, można wznowić właściwe leczenie.
Jeśli stężenie bilirubiny przekroczy 3-krotnie górną granicę normy (ang. IULN) lub aktywność aminotransferaz wątrobowych przekroczy 5-krotnie górną granicę normy, należy zaprzestać podawania imatynibu do czasu, gdy stężenie bilirubiny będzie mniejsze niż 1,5-krotna wartość górnej granicy normy, a aktywność aminotransferaz będzie mniejsza niż 2,5-krotna wartość górnej granicy normy. Leczenie imatynibem można kontynuować stosując zmniejszone dawki dobowe. U dorosłych dawkę należy zmniejszyć z 400 mg do 300 mg lub z 600 mg do 400 mg, lub z 800 mg do 600 mg,
a u dzieci i młodzieży z 340 mg/m2 pc. do 260 mg/m2 pc. na dobę.
Hematologiczne działania niepożądane
Zaleca się zmniejszenie dawki leku lub przerwanie leczenia w przypadku ciężkiej neutropenii lub trombocytopenii, zgodnie ze wskazówkami podanymi w poniższej tabeli.
Dostosowanie dawki u pacjentów z neutropenią i trombocytopenią:
HES/CEL (dawka początkowa 100 mg) | ANC <1,0 x 109/l i (lub) płytki krwi <50 x 109/l | |
CML w fazie przewlekłej, MDS/MPD i GIST (dawka początkowa 400 mg) HES/CEL (w dawce 400 mg) | ANC <1,0 x 109/l i (lub) płytki krwi <50 x 109/l | ≥75 x 109/l. zmniejszonej do 300 mg. |
CML w fazie przewlekłej u dzieci i młodzieży (w dawce 340 mg/m2 pc.) | ANC <1,0 x 109/l i (lub) płytki krwi <50 x 109/l | ≥75 x 109/l. <50 x 109/l, powtórzyć postępowanie podane w punkcie 1, a następnie wrócić do podawania imatynibu w dawce zmniejszonej do 260 mg/m2 pc. |
CML w fazie akceleracji i przełomu blastycznego oraz Ph+ ALL (dawka początkowa 600 mg) | aANC <0,5 x 109/l i (lub) płytki krwi <10 x 109/l | ≥1 x 109/l i płytki krwi ≥20 x 109/l. Następnie, należy ponownie podjąć leczenie podając dawkę 300 mg. |
Nadwrażliwość na substancję czynną lub na którąkolwiek substancję pomocniczą wymienioną w punkcie 6.1.
W przypadku stosowania imatynibu jednocześnie z innymi lekami istnieje prawdopodobieństwo wystąpienia interakcji. Należy zachować ostrożność podczas stosowania imatynibu z inhibitorami proteazy, azolowymi lekami przeciwgrzybiczymi, niektórymi antybiotykami makrolidowymi (patrz punkt 4.5), substratami CYP3A4 o wąskim indeksie terapeutycznym (np. cyklosporyna, pimozyd, takrolimus, syrolimus, ergotamina, diergotamina, fentanyl, alfentanyl, terfenadyna, bortezomib, docetaksel, chinidyna) lub warfaryną i innymi pochodnymi kumaryny (patrz punkt 4.5).
Jednoczesne podawanie imatynibu z innymi lekami, które indukują CYP3A4 (np. deksametazon, fenytoina, karbamazepina, ryfampicyna, fenobarbital lub ziele dziurawca zwyczajnego Hypericum perforatum) może istotnie zmniejszać ekspozycję na imatynib, potencjalnie zwiększając ryzyko niepowodzenia terapeutycznego. Dlatego nie należy stosować jednocześnie silnych induktorów CYP3A4 i imatynibu (patrz punkt 4.5).
Niedoczynność tarczycy
W czasie leczenia imatynibem, donoszono o klinicznych przypadkach niedoczynności tarczycy, występujących u pacjentów po usunięciu gruczołu tarczowego, którym zastępczo podawano lewotyroksynę (patrz punkt 4.5). U tych pacjentów należy ściśle kontrolować stężenie hormonu tyreotropowego (ang. thyroid-stimulating hormone - TSH).
Toksyczność dla wątroby
Metabolizm imatynibu zachodzi głównie w wątrobie, a tylko 13% jest wydalane przez nerki.
U pacjentów z zaburzeniami czynności wątroby (łagodnymi, umiarkowanymi lub ciężkimi) należy szczegółowo monitorować obraz krwi obwodowej oraz aktywność enzymów wątrobowych (patrz punkty 4.2, 4.8 i 5.2). Należy zauważyć, że pacjenci z GIST mogą mieć przerzuty do wątroby, które mogą prowadzić do zaburzenia jej czynności.
Podczas stosowania imatynibu obserwowano przypadki uszkodzenia wątroby, w tym niewydolność wątroby oraz martwicę wątroby. W przypadku leczenia skojarzonego imatynibem i chemioterapią
w dużych dawkach, odnotowano zwiększenie częstości występowania ciężkich działań niepożądanych dotyczących wątroby. Należy dokładnie monitorować czynność wątroby w przypadku jednoczesnego stosowania imatynibu i schematów chemioterapii, o których wiadomo, że mogą powodować zaburzenia czynności wątroby (patrz punkty 4.5 i 4.8).
Zatrzymanie płynów
U około 2,5% pacjentów z nowo rozpoznaną CML, przyjmujących imatynib występowało znacznego stopnia zatrzymanie płynów (wysięk opłucnowy, obrzęki, obrzęk płuc, wodobrzusze, powierzchowny obrzęk). Dlatego jest wysoce wskazane regularne kontrolowanie masy ciała pacjentów.
Nieoczekiwany, szybki przyrost masy ciała należy dokładnie przeanalizować. W razie konieczności należy zastosować odpowiednie leczenie wspomagające i inne działania terapeutyczne. W badaniach klinicznych stwierdzono zwiększenie liczby takich przypadków u pacjentów w podeszłym wieku oraz pacjentów z chorobą serca w wywiadzie. Dlatego należy zachować ostrożność u pacjentów z zaburzeniem czynności serca.
Pacjenci z chorobami serca
Należy uważnie monitorować pacjentów z chorobami serca lub czynnikami ryzyka niewydolności serca lub niewydolnością nerek w wywiadzie, a wszyscy pacjenci z przedmiotowymi lub podmiotowymi objawami odpowiadającymi niewydolności serca lub nerek wymagają oceny lekarskiej i leczenia.
U pacjentów z zespołem hipereozynofilowym (HES) z utajonym naciekaniem komórek zespołu hipereozynofilowego w obrębie mięśnia sercowego, występowanie pojedynczych przypadków wstrząsu kardiogennego/zaburzeń czynności lewej komory było związane z degranulacją komórek zespołu hipereozynofilowego przed rozpoczęciem leczenia imatynibem. Donoszono, że stan ten ustępuje po podaniu steroidów o działaniu ogólnoustrojowym, zastosowaniu środków podtrzymujących krążenie i czasowym odstawieniu imatynibu. Ponieważ po zastosowaniu imatynibu sporadycznie zgłaszano działania niepożądane ze strony serca, należy przed rozpoczęciem leczenia dokonać uważnej oceny stosunku korzyści do ryzyka związanego z leczeniem imatynibem w populacji z HES/CEL.
Zespoły mielodysplastyczne/mieloproliferacyjne (MDS/MPD) z rearanżacją genu PDGFR mogą być związane z dużą liczbą eozynofilów. Dlatego u pacjentów z HES/CEL oraz u pacjentów z zespołami mielodysplastycznymi/mieloproliferacyjnymi związanymi z dużą liczbą eozynofilów, przed rozpoczęciem leczenia należy rozważyć przeprowadzenie konsultacji z kardiologiem, wykonanie echokardiogramu oraz oznaczenie stężenia troponiny w surowicy. Jeśli którykolwiek z wyników tych badań okaże się nieprawidłowy, należy rozważyć dalszą obserwację kardiologiczną i profilaktyczne zastosowanie steroidów układowych (1-2 mg/kg) przez jeden lub dwa tygodnie na początku leczenia, jednocześnie z podawaniem imatynibu.
Krwawienie z przewodu pokarmowego
W badaniu z udziałem pacjentów z GIST nieoperacyjnymi i (lub) z przerzutami stwierdzono zarówno krwawienia z przewodu pokarmowego, jak i krwawienia wewnątrz guza (patrz punkt 4.8). Na podstawie dostępnych danych nie określono czynników predysponujących (np. wielkość guza, umiejscowienie guza, zaburzenia krzepnięcia), które mogłyby identyfikować pacjentów z GIST do grupy zwiększonego ryzyka wystąpienia jednego z tych dwóch rodzajów krwawienia. Ponieważ zwiększenie unaczynienia i skłonność do krwawień jest cechą charakterystyczną i naturalnym obrazem klinicznym GIST, należy zastosować standardowe postępowanie i procedury w celu monitorowania i leczenia krwawienia u wszystkich pacjentów.
Ponadto, po wprowadzeniu leku do obrotu, u pacjentów z CML, ALL i innymi chorobami zgłaszano występowanie poszerzenia naczyń okolicy przedodźwiernikowej żołądka, tzw. żołądka arbuzowatego (ang. gastric antral vascular ectasia - GAVE), rzadkiej przyczyny krwawienia z przewodu pokarmowego (patrz punkt 4.8). W razie potrzeby można rozważyć przerwanie leczenia imatinibem
Zespół rozpadu guza
Ze względu na możliwość wystąpienia zespołu rozpadu guza (ang. tumour lysis syndrome - TLS), przed rozpoczęciem leczenia imatynibem zaleca się wyrównanie klinicznie istotnego odwodnienia oraz leczenie zmniejszające zwiększone stężenie kwasu moczowego (patrz punkt 4.8).
Reaktywacja wirusowego zapalenia wątroby typu B
U pacjentów będących przewlekłymi nosicielami wirusa zapalenia wątroby typu B dochodziło do reaktywacji zapalenia wątroby po otrzymaniu przez nich inhibitorów kinazy tyrozynowej BCR-ABL. Niektóre przypadki prowadziły do ostrej niewydolności wątroby lub piorunującego zapalenia wątroby, a w konsekwencji do przeszczepienia wątroby lub zgonu pacjenta.
U pacjentów należy wykonać badania pod kątem zakażenia wirusem HBV przed rozpoczęciem leczenia produktem leczniczym Meaxin. Przed rozpoczęciem leczenia u pacjentów z dodatnim wynikiem badania serologicznego w kierunku wirusowego zapalenia wątroby typu B (w tym
u pacjentów z aktywną chorobą) i w przypadku pacjentów z dodatnim wynikiem badania w kierunku zakażenia wirusem HBV w trakcie leczenia należy skonsultować się z ekspertami ds. chorób wątroby i leczenia wirusowego zapalenia wątroby typu B. Nosiciele wirusa HBV, którzy wymagają leczenia produktem leczniczym Meaxin, powinni być poddawani ścisłej obserwacji pod kątem objawów podmiotowych i przedmiotowych aktywnego zakażenia wirusem HBV w trakcie całego okresu leczenia i przez kilka miesięcy po jego zakończeniu (patrz punkt 4.8).
Fototoksyczność
Należy unikać bezpośredniej ekspozycji lub zminimalizować bezpośrednią ekspozycję na światło słoneczne ze względu na ryzyko wystąpienia fototoksyczności związanej z leczeniem imatynibem. Pacjenci powinni zostać poinformowani o konieczności stosowania środków zapobiegawczych takich jak odzież ochronna oraz preparaty z filtrem o wysokim wskaźniku ochrony przeciwsłonecznej (SPF).
Mikroangiopatia zakrzepowa
Stosowanie inhibitorów kinazy tyrozynowej (TKI) BCR-ABL jest związane z występowaniem mikroangiopatii zakrzepowej (ang. thrombotic microangiopathy - TMA), co obejmuje zgłoszenia pojedynczych przypadków po zastosowaniu produktu leczniczego Meaxin (patrz punkt 4.8). Jeśli u pacjenta otrzymującego Meaxin wystąpią laboratoryjne lub kliniczne cechy TMA, leczenie należy przerwać i przeprowadzić gruntowną ocenę w celu wykrycia TMA, obejmującą aktywność ADAMTS13 i oznaczenie miana przeciwciał przeciwko ADAMTS13. Jeśli miano przeciwciał przeciwko ADAMTS13 jest podwyższone z jednocześnie występującą małą aktywnością ADAMTS13, leczenia produktem Meaxin nie należy wznawiać.
Badania laboratoryjne
U pacjentów przyjmujących imatynib należy regularnie wykonywać pełne badanie krwi. Leczenie imatynibem pacjentów z CML może być związane z wystąpieniem neutropenii lub trombocytopenii. Jednakże pojawienie się zmniejszonej liczby krwinek prawdopodobnie zależy od stopnia zaawansowania choroby i jest częstsze u pacjentów w fazie akceleracji choroby lub w przełomie blastycznym, niż u pacjentów w fazie przewlekłej CML. W takich przypadkach można przerwać leczenie imatynibem lub zmniejszyć dawkę leku, zgodnie z zaleceniami określonymi w punkcie 4.2.
U pacjentów otrzymujących imatynib należy regularnie oceniać czynność wątroby (aminotransferazy, bilirubina, fosfataza zasadowa).
U pacjentów z zaburzeniami czynności nerek, całkowity wpływ imatynibu zawartego w osoczu na organizm wydaje się być większy niż u pacjentów z prawidłową czynnością nerek. Jest to prawdopodobnie spowodowane zwiększonym stężeniem kwaśniej alfa-glikoproteiny (ang. alpha-acid glycoprotein - AGP), białka wiążącego imatynib, w osoczu u tych pacjentów. U pacjentów
z zaburzeniami czynności nerek należy stosować najmniejszą dawkę początkową. Pacjenci z ciężkim zaburzeniem czynności nerek powinni być leczeni z zachowaniem ostrożności. W przypadku nietolerancji dawkę można zmniejszyć (patrz punkty 4.2 i 5.2).
Długotrwałe leczenie imatynibem może być związane z klinicznie istotnym pogorszeniem czynności nerek. Z tego względu należy dokonać oceny czynności nerek przed rozpoczęciem leczenia imatynibem i ściśle ją monitorować w czasie trwania terapii, zwracając szczególną uwagę na pacjentów z czynnikami ryzyka dysfunkcji nerek. W przypadku wystąpienia zaburzeń czynności nerek należy zlecić odpowiednie postępowanie i leczenie, zgodnie ze standardowymi wytycznymi medycznymi.
Dzieci i młodzież
Donoszono o przypadkach opóźnienia wzrostu u dzieci i młodzieży otrzymujących imatynib przed okresem dojrzewania. W badaniach obserwacyjnych w populacji dzieci i młodzieży z CML,
raportowano statystycznie istotne (ale o niepewnym znaczeniu klinicznym) obniżenie mediany odchylenia standardowego wzrostu po 12 i 24 miesiącach leczenia, w dwóch małych podgrupach niezależnie od dojrzewania płciowego lub płci. Zalecane jest ścisłe monitorowanie wzrostu u dzieci w czasie leczenia imatynibem (patrz punkt 4.8).
Sód
Produkt leczniczy zawiera mniej niż 1 mmol (23 mg) sodu na tabletkę, to znaczy produkt uznaje się za
„wolny od sodu”.
Substancje czynne, które mogą zwiększać stężenie imatynibu w osoczu:
Substancje hamujące aktywność izoenzymu CYP3A4 cytochromu P450 (np. inhibitory proteazy, takie jak indynawir, lopinawir/rytonawir, rytonawir, sakwinawir, telaprewir, nelfinawir, boceprewir; azolowe leki przeciwgrzybicze, w tym ketokonazol, itrakonazol, pozakonazol, worykonazol; niektóre antybiotyki makrolidowe, takie jak erytromycyna, klarytromycyna i telitromycyna) mogą spowalniać metabolizm imatynibu i powodować zwiększenie jego stężenia. Obserwowano znacząco większe narażenie na imatynib (średnie wartości Cmax i AUC imatynibu wzrosły odpowiednio o 26% i 40%) zdrowych ochotników, którym jednocześnie podano jednorazowo ketokonazol (inhibitor
CYP3A4). Należy zachować ostrożność w czasie jednoczesnego stosowania imatynibu z inhibitorami enzymów rodziny CYP3A4.
Substancje czynne, które mogą zmniejszać stężenie imatynibu w osoczu:
Substancje będące induktorami CYP3A4 (np. deksametazon, fenytoina, karbamazepina, ryfampicyna, fenobarbital, fosfenytoina, prymidon lub ziele dziurawca zwyczajnego - Hypericum perforatum) mogą istotnie zmniejszać ekspozycję na imatynib, potencjalnie zwiększając ryzyko niepowodzenia terapeutycznego. Uprzednie wielokrotne podawanie ryfampicyny w dawce 600 mg, a następnie
podanie jednej dawki 400 mg imatynibu spowodowało zmniejszenie Cmax i AUC(0-∞) odpowiednio o co najmniej 54% i 74%, w stosunku do wartości uzyskanych bez uprzedniego podawania ryfampicyny.
Podobne wyniki obserwowano u pacjentów z glejakami złośliwymi leczonych imatynibem podczas przyjmowania leków przeciwpadaczkowych indukujących enzymy (EIAEDs), takich jak karbamazepina, okskarbazepina i fenytoina. Pole pod krzywą AUC (krzywa zależności stężenia imatynibu w osoczu od czasu) zmniejszyło się o 73% w porównaniu z pacjentami nie przyjmującymi leków przeciwpadaczkowych pobudzających enzymy. Należy unikać jednoczesnego stosowania ryfampicyny oraz innych silnych induktorów CYP3A4 i imatynibu.
Substancje czynne, których stężenie w osoczu może ulec zmianie pod wpływem imatynibu Imatynib powoduje zwiększenie średnich wartości Cmax i AUC symwastatyny (substratu CYP3A4) odpowiednio 2- oraz 3,5-krotnie, co wskazuje na hamowanie aktywności CYP3A4 przez imatynib. Dlatego zaleca się ostrożność w czasie podawania imatynibu z substratami CYP3A4 o wąskim indeksie terapeutycznym (np. cyklosporyna, pimozyd, takrolimus, syrolimus, ergotamina, diergotamina, fentanyl, alfentanyl, terfenadyna, bortezomib, docetaksel i chinidyna). Imatynib może zwiększać stężenie innych leków metabolizowanych przez CYP3A4 (triazolobenzodiazepin, antagonistów kanału wapniowego z grupy dihydropirydyny, niektórych inhibitorów reduktazy HMG- CoA, tj. statyn, itp.).
Ze względu na znane zwiększone ryzyko krwawienia, wynikające z zastosowania imatynibu (np. krwotok), pacjenci, u których wymagane jest stosowanie leków przeciwzakrzepowych powinni otrzymywać niskocząsteczkową lub standardową heparynę zamiast pochodnych kumaryny, takich jak warfaryna.
In vitro imatynib hamuje aktywność izoenzymu CYP2D6 cytochromu P450 w stężeniach podobnych do tych, które mają wpływ na aktywność CYP3A4. Imatynib w dawce 400 mg podawanej dwa razy na dobę wykazuje działanie hamujące metabolizm metoprololu zależny od CYP2D6, przy czym Cmax
i AUC metoprololu wzrastają o około 23% (90%CI [1,16-1,30]). Wydaje się, że jeśli imatynib jest stosowany jednocześnie z substratami CYP2D6, modyfikacja dawki nie jest konieczna. Jednakże,
zaleca się zachowanie ostrożności w przypadku substratów CYP2D6 o wąskim indeksie terapeutycznym, takich jak metoprolol. U pacjentów leczonych metoprololem należy rozważyć monitorowanie kliniczne.
In vitro imatynib hamuje O-glukuronidację paracetamolu przy wartości Ki = 58,5 mikromol/l. Tego hamowania nie obserwowano in vivo po podaniu imatynibu w dawce 400 mg oraz paracetamolu
w dawce 1000 mg. Większe dawki imatynibu i paracetamolu nie były badane.
Należy więc zachować ostrożność stosując jednocześnie duże dawki imatynibu i paracetamolu.
U pacjentów po usunięciu gruczołu tarczowego, otrzymujących lewotyroksynę, całkowity wpływ lewotyroksyny zawartej w osoczu na organizm może zmniejszyć się w przypadku jednoczesnego stosowania imatynibu (patrz punkt 4.4). Dlatego też zalecana jest ostrożność. Mechanizm obserwowanej interakcji nie jest obecnie znany.
Istnieje kliniczne doświadczenie w jednoczesnym stosowaniu imatynibu i chemioterapii u pacjentów z Ph+ ALL (patrz punkt 5.1), ale interakcje typu lek-lek między imatynibem, a chemioterapeutykami nie są dobrze scharakteryzowane. Działania niepożądane związane ze stosowaniem imatynibu, np. hepatotoksyczność, mielosupresja czy inne, mogą się nasilać. Donoszono, że jednoczesne stosowanie z L-asparaginazą mogło wiązać się ze zwiększeniem hepatotoksyczności (patrz punkt 4.8). Dlatego stosowanie imatynibu w skojarzeniu z innymi lekami wymaga szczególnej ostrożności.
Kobiety w wieku rozrodczym
Kobiety w wieku rozrodczym muszą być poinformowane o konieczności stosowania skutecznej metody antykoncepcji w trakcie leczenia i przez co najmniej 15 dni po zakończeniu leczenia imatynibem.
Ciąża
Istnieją ograniczone dane dotyczące stosowania imatynibu u kobiet w ciąży. Po wprowadzeniu do obrotu zgłaszano występowanie samoistnych poronień i wad wrodzonych u dzieci matek, które przyjmowały imatynib. Badania na zwierzętach wykazały szkodliwy wpływ na reprodukcję (patrz punkt 5.3). Potencjalne zagrożenie dla płodu nie jest znane. Imatynib nie powinien być stosowany w okresie ciąży, jeśli nie jest to bezwzględnie konieczne. Jeśli imatynib jest stosowany u kobiety w ciąży, pacjentka musi być poinformowana o potencjalnym ryzyku dla płodu.
Karmienie piersią
Informacje dotyczące przenikania imatynibu do mleka kobiecego są ograniczone. Badania z udziałem dwóch kobiet karmiących wykazały, że zarówno imatynib, jak i jego czynny metabolit mogą przenikać do mleka matki. Proporcja stężenia w mleku do stężenia w osoczu, badana u jednej z pacjentek wynosiła 0,5 dla imatynibu i 0,9 dla metabolitu, co sugeruje większe przenikanie metabolitu do mleka. Biorąc pod uwagę połączone stężenie imatynibu i metabolitu oraz maksymalne dobowe spożycie mleka przez niemowlęta, całkowite przewidywane narażenie jest małe (~10% dawki leczniczej). Jednakże, ponieważ skutki narażenia niemowlęcia na małe dawki imatynibu są nieznane, kobiety nie powinny karmić piersią w trakcie leczenia i przez co najmniej 15 dni po zakończeniu leczenia imatynibem.
Płodność
W badaniach nieklinicznych wykazano brak wpływu na płodność samców i samic szczura, aczkolwiek obserwowano wpływ na parametry reprodukcyjne (patrz punkt 5.3). Badań z udziałem pacjentów otrzymujących imatynib, dotyczących wpływu na płodność i gametogenezę nie przeprowadzono.
Pacjenci leczeni imatynibem, zwracający uwagę na swoją płodność, powinni skonsultować się z lekarzem.
Pacjentów należy uprzedzić, że w czasie leczenia imatynibem mogą wystąpić u nich takie działania niepożądane, jak zawroty głowy, zaburzenia widzenia lub senność. Dlatego zaleca się ostrożność w czasie prowadzenia pojazdów i obsługiwania maszyn.
Podsumowanie profilu bezpieczeństwa
Pacjenci w zaawansowanym stadium nowotworów złośliwych mogą mieć szereg objawów, których związek z działaniami niepożądanymi jest trudny do ustalenia ze względu na różnorodność objawów związanych z chorobą podstawową, jej postępem i jednoczesnym przyjmowaniem licznych leków.
W badaniach klinicznych z przewlekłą białaczką szpikową (CML) przerwanie leczenia ze względu na wystąpienie działań niepożądanych leku odnotowano u 2,4% pacjentów z nowo rozpoznaną chorobą, u 4% pacjentów w późnym okresie fazy przewlekłej, u których terapia interferonem okazała się nieskuteczna, u 4% pacjentów w fazie akceleracji choroby po niepowodzeniu terapii interferonem oraz u 5% pacjentów z przełomem blastycznym po niepowodzeniu terapii interferonem. W badaniach klinicznych dotyczących GIST leczenie przerwano u 4% pacjentów z powodu wystąpienia działań niepożądanych związanych z lekiem.
Poza dwoma wyjątkami, działania niepożądane były podobne we wszystkich wskazaniach.
U pacjentów z CML obserwowano więcej przypadków mielosupresji, niż u pacjentów z GIST, co jest prawdopodobnie związane z chorobą podstawową. W badaniu z udziałem pacjentów z nieoperacyjnymi i (lub) z przerzutami GIST u 7 pacjentów (5%) wystąpiły objawy niepożądane w stopniu 3. lub 4. według CTC (ang. Common Toxicity Criteria - CTC) w postaci krwawienia z przewodu pokarmowego (3 pacjentów), krwawienia wewnątrz guza (3 pacjentów) lub obydwu rodzajów krwawień (1 pacjent). Umiejscowienie guza w przewodzie pokarmowym może być przyczyną krwawienia z przewodu pokarmowego (patrz punkt 4.4). Krwawienia z przewodu pokarmowego i krwawienia wewnątrz guza mogą być ciężkie i czasami mogą zakończyć się zgonem. Do najczęściej zgłaszanych (≥10%) działań niepożądanych związanych ze stosowaniem leku w obu wskazaniach należały: nudności o niewielkim nasileniu, wymioty, biegunka, bóle brzucha, zmęczenie, bóle mięśni, skurcze mięśni i wysypka. We wszystkich badaniach często obserwowano powierzchowne obrzęki opisywane głównie jako obrzęki wokół oczu i obrzęki kończyn dolnych.
Obrzęki te rzadko były ciężkie i ustępowały po podaniu leków moczopędnych, innych środków wspomagających, lub po zmniejszeniu dawki imatynibu.
Po podaniu imatynibu w skojarzeniu z chemioterapią w dużych dawkach u pacjentów z Ph+ ALL obserwowano przemijające działanie uszkadzające wątrobę w postaci zwiększonej aktywności aminotransferaz i hiperbilirubinemii. Biorąc pod uwagę ograniczoną bazę danych o bezpieczeństwie, zdarzenia niepożądane zgłaszane do tej pory u dzieci są zgodne z profilem bezpieczeństwa znanym u dorosłych pacjentów z Ph+ ALL. Dane dotyczące bezpieczeństwa u dzieci z Ph+ ALL są bardzo ograniczone, jednak nie odnotowano żadnych nowych kwestii związanych z bezpieczeństwem.
Różnorodne działania niepożądane, takie jak: wysięk opłucnowy, wodobrzusze, obrzęk płuc
i gwałtowne zwiększenie masy ciała, w obecności lub braku obrzęków powierzchniowych, można ogólnie opisać jako „zatrzymanie płynów”. Działania te najczęściej ustępują po tymczasowym odstawieniu imatynibu oraz podaniu leków moczopędnych i innych środków pomocniczych.
Jednakże, niektóre z wyżej wymienionych działań niepożądanych mogą być ciężkie lub stanowić bezpośrednie zagrożenie dla życia. Opisano kilka przypadków zgonów pacjentów w przełomie blastycznym, spowodowanych wysiękiem opłucnowym, zastoinową niewydolnością serca
i niewydolnością nerek. W badaniach klinicznych u dzieci i młodzieży nie stwierdzono szczególnych zagrożeń dotyczących bezpieczeństwa stosowania.
Działania niepożądane
Poniżej podano wykaz działań niepożądanych, które występowały częściej niż w pojedynczych przypadkach. Działania te przedstawiono wg klasyfikacji układów narządów i częstości występowania. Częstość występowania zdefiniowano zgodnie z następującą konwencją: bardzo często
(≥1/10), często (≥1/100 do <1/10), niezbyt często (≥1/1000 do <1/100), rzadko (≥1/10 000 do <1000), bardzo rzadko (<1/10 000), częstość nieznana (częstość nie może być określona na podstawie dostępnych danych).
W obrębie każdej grupy o określonej częstości występowania, działania niepożądane przedstawiono według częstości ich występowania, zaczynając od najczęstszych.
Działania niepożądane i częstość ich występowania przedstawione są w Tabeli 1.
Tabela 1 Tabelaryczne zestawienie działań niepożądanych
Zakażenia i zarażenia pasożytnicze | |
Niezbyt często: | Zakażenia wirusem Herpes zoster, Herpes simplex, zapalenie nosogardła, zapalenie płuc1, zapalenie zatok, zapalenie tkanki łącznej, zakażenie górnych dróg oddechowych, grypa, zakażenie dróg moczowych, zapalenie żołądka i jelit, posocznica |
Rzadko: | Zakażenia grzybicze |
Częstość nieznana: | Reaktywacja wirusowego zapalenia wątroby typu B* |
Nowotwory łagodne, złośliwe i nieokreślone (w tym torbiele i polipy) | |
Rzadko: | Zespół rozpadu guza |
Częstość nieznana: | Krwawienie z guza/martwica guza* |
Zaburzenia układu immunologicznego | |
Częstość nieznana: | Wstrząs anafilaktyczny* |
Zaburzenia krwi i układu chłonnego | |
Bardzo często: | Neutropenia, trombocytopenia, niedokrwistość |
Często: | Pancytopenia, neutropenia z gorączką |
Niezbyt często: | Trombocytoza, limfopenia, zahamowanie czynności szpiku kostnego, eozynofilia, powiększenie węzłów chłonnych |
Rzadko: | Niedokrwistość hemolityczna, mikroangiopatia zakrzepowa |
Zaburzenia metabolizmu i odżywiania | |
Często: | Jadłowstręt |
Niezbyt często: | Hipokaliemia, zwiększony apetyt, hipofosfatemia, zmniejszony apetyt, odwodnienie, dna, hiperurykemia, hiperkalcemia, hiperglikemia, hiponatremia |
Rzadko: | Hiperkaliemia, hipomagnezemia |
Zaburzenia psychiczne | |
Często: | Bezsenność |
Niezbyt często: | Depresja, osłabienie popędu płciowego, lęk |
Rzadko: | Stan splątania |
Zaburzenia układu nerwowego | |
Bardzo często: | Ból głowy2 |
Często: | Zawroty głowy, parestezje, zaburzenia smaku, niedoczulica |
Niezbyt często: | Migrena, senność, omdlenia, neuropatia obwodowa, zaburzenia pamięci, rwa kulszowa, zespół niespokojnych nóg, drżenie, krwotok mózgowy |
Rzadko: | Zwiększenie ciśnienia śródczaszkowego, drgawki, zapalenie nerwu wzrokowego |
Częstość nieznana: | Obrzęk mózgu* |
Zaburzenia oka | |
Często: | Obrzęk powiek, nasilone łzawienie, krwotok spojówkowy, zapalenie spojówek, suchość oka, nieostre widzenie |
Niezbyt często: | Podrażnienie oka, ból oka, obrzęk oczodołu, krwotok twardówkowy, krwotok z siatkówki, zapalenie brzegów powiek, obrzęk plamki |
Rzadko: | Zaćma, jaskra, obrzęk tarczy nerwu wzrokowego |
Częstość nieznana: | Krwotok do ciała szklistego* |
Zaburzenia ucha i błędnika | |
Niezbyt często: | Zawroty głowy pochodzenia błędnikowego, szum uszny, utrata słuchu |
Zaburzenia serca | |
Niezbyt często: | Kołatania, częstoskurcz, zastoinowa niewydolność serca3, obrzęk płuc |
Rzadko: | Niemiarowość, migotanie przedsionków, zatrzymanie serca, zawał mięśnia sercowego, dławica piersiowa, wysięk osierdziowy |
Częstość nieznana: | Zapalenie osierdzia*, tamponada serca* |
Zaburzenia naczyniowe4 | |
Często: | Zaczerwienienie twarzy, krwotok |
Niezbyt często: | Nadciśnienie, krwiak, krwiak podtwardówkowy, zimne palce nóg i rąk, niedociśnienie, zespół Raynauda |
Częstość nieznana: | Zakrzepica/zator* |
Zaburzenia układu oddechowego, klatki piersiowej i śródpiersia | |
Często: | Duszności, krwawienie z nosa, kaszel |
Niezbyt często: | Wysięk opłucnowy5, ból gardła i krtani, zapalenie gardła |
Rzadko: | Ból związany z zapaleniem opłucnej, zwłóknienie płuc, nadciśnienie płucne, krwotok płucny |
Częstość nieznana: | Ostra niewydolność oddechowa11*, choroba śródmiąższowa płuc* |
Zaburzenia żołądka i jelit | |
Bardzo często: | Nudności, biegunka, wymioty, niestrawność, ból brzucha6 |
Często: | Wzdęcia, rozdęcie brzucha, refluks żołądkowo- przełykowy, zaparcia, suchość jamy ustnej, zapalenie błony śluzowej żołądka |
Niezbyt często: | Zapalenie jamy ustnej, owrzodzenie jamy ustnej, krwotok z przewodu pokarmowego7, odbijanie się, smoliste stolce, zapalenie przełyku, wodobrzusze, wrzód żołądka, krwawe wymioty, zapalenie warg, dysfagia, zapalenie trzustki |
Rzadko: | Zapalenie okrężnicy, niedrożność jelita, nieswoiste zapalenia jelit |
Częstość nieznana: | Niedrożność jelit*, perforacja przewodu pokarmowego*, zapalenie uchyłka*, poszerzenie naczyń okolicy przedodźwiernikowej żołądka - tzw. żołądek arbuzowaty (GAVE)* |
Zaburzenia wątroby i dróg żółciowych | |
Często: | Zwiększenie aktywności enzymów wątrobowych |
Niezbyt często: | Hiperbilirubinemia, zapalenie wątroby, żółtaczka |
Rzadko: | Niewydolność wątroby8, martwica wątroby |
Zaburzenia skóry i tkanki podskórnej | |
Bardzo często: | Obrzęk okołooczodołowy, zapalenie skóry/wyprysk/wysypka |
Często: | Świąd, obrzęk twarzy, sucha skóra, rumień, łysienie, poty nocne, reakcja nadwrażliwości na światło |
Niezbyt często: | Wysypka krostkowa, siniaki, nasilone pocenie, pokrzywka, wylew krwawy podskórny, wzmożona tendencja do występowania siniaków, skąpe owłosienie, odbarwienie skóry, złuszczające zapalenie skóry, łamliwość paznokci, zapalenie mieszków włosowych, wybroczyny, łuszczyca, plamica, nadmierna pigmentacja skóry, wysypki pęcherzowe, zapalenie tkanki tłuszczowej12 |
Rzadko: | Ostra dermatoza z gorączką i neutrofilią (zespół Sweeta), przebarwienia paznokci, obrzęk naczynioruchowy, wysypka pęcherzykowa, rumień wielopostaciowy, leukocytoklastyczne zapalenie naczyń, zespół Stevensa-Johnsona, ostra uogólniona osutka krostkowa (ang. acute generalised exanthematous pustulosis - AGEP), pęcherzyca* |
Częstość nieznana: | Zespół erytrodyzestezji dłoniowo-podeszwowej*, rogowacenie liszajowate*, liszaj płaski*, toksyczne martwicze oddzielanie się naskórka*, osutka polekowa z eozynofilią i objawami układowymi (DRESS)*, pseudoporfiria* |
Zaburzenia mięśniowo-szkieletowe i tkanki łącznej | |
Bardzo często: | Skurcze mięśni, bóle mięśniowo-szkieletowe w tym bóle mięśni9, bóle stawów i bóle kości10 |
Często: | Obrzęk stawów |
Niezbyt często: | Sztywność stawów i mięśni, martwica kości* |
Rzadko: | Osłabienie mięśni, zapalenie stawów, rabdomioliza/miopatia |
Częstość nieznana: | Opóźnienie wzrostu u dzieci* |
Zaburzenia nerek i dróg moczowych | |
Niezbyt często: | Ból w okolicy nerek, krwiomocz, ostra niewydolność nerek, częste oddawanie moczu |
Częstość nieznana: | Przewlekła niewydolność nerek |
Zaburzenia układu rozrodczego i piersi | |
Niezbyt często: | Ginekomastia, zaburzenia wzwodu, krwotok miesiączkowy, nieregularne miesiączkowanie, zaburzenia seksualne, ból brodawek sutkowych, powiększenie piersi, obrzęk moszny |
Rzadko: | Krwotoczne ciałko żółte/krwotoczna torbiel jajnika |
Zaburzenia ogólne i stany w miejscu podania | |
Bardzo często: | Zatrzymanie płynów i obrzęk, uczucie zmęczenia |
Często: | Osłabienie, gorączka, obrzęk tkanki podskórnej, dreszcze, zesztywnienie mięśni |
Niezbyt często: | Ból klatki piersiowej, złe samopoczucie |
Badania diagnostyczne | |
Bardzo często: | Zwiększenie masy ciała |
Często: | Zmniejszenie masy ciała |
Niezbyt często: | Zwiększenie stężenia kreatyniny we krwi, zwiększenie aktywności fosfokinazy kreatynowej we krwi, zwiększenie aktywności dehydrogenazy mleczanowej we krwi, zwiększenie aktywności fosfatazy zasadowej we krwi |
Rzadko: | Zwiększenie aktywności amylazy we krwi |
*Wymienione działania niepożądane były zgłaszane głównie w związku ze stosowaniem imatinibu
w okresie po wprowadzeniu do obrotu. Należą do nich doniesienia spontaniczne, jak również poważne działania niepożądane zgłaszane podczas nadal trwających badań, programów rozszerzonego dostępu, badań farmakologii klinicznej i badań eksploracyjnych w niezarejestrowanych wskazaniach. Ponieważ działania te zgłaszano w populacji o nieokreślonej liczebności, oszacowanie ich częstości lub ustalenie związku przyczynowo-skutkowego z narażeniem na imatynib nie zawsze jest możliwe.
6+7 Ból brzucha i krwotok z przewodu pokarmowego były najczęściej obserwowane u pacjentów z GIST.
Nieprawidłowości w badaniach diagnostycznych
Hematologia
We wszystkich badaniach u pacjentów z CML obserwowano niedobór krwinek, a zwłaszcza częste występowanie neutropenii i małopłytkowości. Sugerowano, że zmiany te występują z większą częstością u pacjentów leczonych dużymi dawkami ≥750 mg (badania I fazy). Jednak niedobór krwinek miał także ścisły związek ze stopniem zaawansowania choroby. Częstość występowania neutropenii 3. lub 4. stopnia (ANC <1,0 x 109/l) i trombocytopenii (liczba płytek krwi <50 x 109/l) była 4-6 razy większa u pacjentów w przełomie blastycznym i fazie akceleracji choroby (59-64% i 44- 63% odpowiednio dla neutropenii i małopłytkowości) w porównaniu z pacjentami z nowo rozpoznaną CML w fazie przewlekłej choroby (16,7% neutropenia i 8,9% trombocytopenia). U pacjentów z nowo rozpoznaną CML w przewlekłej fazie choroby, neutropenię 4. stopnia (ANC <0,5 x 109/l)
i trombocytopenię 4. stopnia (liczba płytek krwi <10 x 109/l) obserwowano odpowiednio u 3,6% i <1% pacjentów. Średni czas trwania neutropenii i trombocytopenii wynosił odpowiednio 2 do 3
tygodni oraz 3 do 4 tygodni. W takich przypadkach zwykle zmniejsza się dawkę leku lub okresowo przerywa się leczenie imatynibem. Sporadycznie objawy te mogą być przyczyną rezygnacji z dalszego stosowania leku. U dzieci i młodzieży z CML najczęściej obserwowanymi zaburzeniami były niedobory krwinek 3. lub 4. stopnia obejmujące neutropenię, trombocytopenię i niedokrwistość.
Zasadniczo występowały one podczas kilku pierwszych miesięcy leczenia.
W badaniu z udziałem pacjentów z nieoperacyjnymi i (lub) przerzutowymi GIST niedokrwistość 3. i
Doświadczenie z dawkami większymi niż zalecana dawka lecznicza jest ograniczone. Pojedyncze przypadki przedawkowania imatynibu były zgłaszane spontanicznie i opisywane w literaturze medycznej. W przypadku przedawkowania należy obserwować pacjenta i zastosować odpowiednie leczenie objawowe. Na ogół zgłaszanym rezultatem w tych przypadkach było „polepszenie” lub
„wyzdrowienie”. Przy różnych zakresach dawek, donoszono o następujących zdarzeniach:
Pacjenci dorośli
1200 mg do 1600 mg (różny czas trwania między 1 do 10 dni): nudności, wymioty, biegunka, wysypka, rumień, obrzęk, obrzmienie, zmęczenie, skurcze mięśni, trombocytopenia, pancytopenia, ból brzucha, ból głowy, zmniejszenie apetytu;
1800 mg do 3200 mg (aż do 3200 mg na dobę przez 6 dni): osłabienie, bóle mięśni, zwiększenie stężenia fosfokinazy kreatynowej, zwiększenie stężenia bilirubiny, bóle żołądka i jelit;
6400 mg (pojedyncza dawka): w literaturze zanotowano jeden przypadek pacjenta, u którego wystąpiły nudności, wymioty, ból brzucha, gorączka, obrzęk twarzy, zmniejszenie liczby granulocytów obojętnochłonnych, zwiększenie aktywności aminotransferaz;
8 g do 10 g (pojedyncza dawka): donoszono o wymiotach oraz bólu żołądka i jelit.
Dzieci i młodzież
U jednego 3-letniego chłopca narażonego na pojedynczą dawkę 400 mg wystąpiły: wymioty, biegunka i brak łaknienia, u innego 3-letniego chłopca narażonego na pojedynczą dawkę 980 mg wystąpiło zmniejszenie liczby białych krwinek i biegunka.
W przypadku przedawkowania, pacjenta należy obserwować oraz zastosować odpowiednie leczenie wspomagające.
Grupa farmakoterapeutyczna: leki przeciwnowotworowe, inhibitory kinaz tyrozynowych BCR-ABL, kod ATC: L01XE01.
Mechanizm działania
Imatynib jest małą cząsteczką inhibitora kinazy białkowo-tyrozynowej, która silnie hamuje aktywność kinazy tyrozynowej (KT) Bcr-Abl oraz wielu receptorów kinaz tyrozynowych: Kit, receptora czynnika wzrostu komórek macierzystych (SCF) kodowanego przez protoonkogen c-Kit, receptory domeny dyskoidynowej (DDR1 i DDR2), receptory czynnika stymulującego kolonie (CSF-1R) oraz receptory alfa i beta płytkopochodnego czynnika wzrostu (PDGFR-alfa i PDGFR-beta). Imatynib może również hamować procesy komórkowe, w aktywacji których pośredniczą wymienione receptory kinaz.
Działanie farmakodynamiczne
Imatynib jest inhibitorem kinazy białkowo-tyrozynowej, który silnie hamuje kinazę tyrozynową Bcr- Abl in vitro, w komórce i in vivo. Związek ten w takim samym stopniu wybiórczo hamuje proliferację i wywołuje apoptozę w komórkach linii Bcr-Abl dodatnich, jak w komórkach białaczkowych świeżo pobranych od pacjentów z CML z dodatnim chromosomem Philadelphia i od pacjentów z ostrą białaczką limfoblastyczną (ang. Acute Lymphoblastic Leukemia - ALL).
W badaniach in vivo na modelach zwierzęcych z użyciem Bcr-Abl dodatnich komórek nowotworowych, imatynib samodzielnie wykazuje działanie przeciwnowotworowe.
Imatynib jest również inhibitorem receptorów kinaz tyrozynowych płytkopochodnego czynnika aktywacji (ang. Platelet-Derived Growth Factor - PDGF), PDGF-R i czynnika komórek pnia (ang. Stem Cell Factor - SCF), c-Kit i hamuje procesy komórkowe aktywowane przez PDGF i SCF. In vitro imatynib hamuje proliferację i indukuje apoptozę komórek nowotworów podścieliskowych przewodu pokarmowego (GIST), w których stwierdzono ekspresję mutacji kit. Istotna aktywacja receptora PDGF lub kinaz białkowo-tyrozynowych Abl w wyniku połączenia się różnych odpowiadających sobie białek lub istotne wytwarzanie PDGF są wpisane w patogenezę MDS/MPD, HES/CEL i DFSP. Imatynib hamuje przekazywanie sygnałów i proliferację komórek zależną od zaburzonej regulacji aktywności PDGFR i kinazy Abl.
Badania kliniczne w przewlekłej białaczce szpikowej
Skuteczność imatynibu jest oceniana na podstawie stopnia całkowitej odpowiedzi hematologicznej
i cytogenetycznej oraz czasu przeżycia wolnego od progresji choroby. Z wyjątkiem nowo rozpoznanej przewlekłej białaczki szpikowej, brak kontrolowanych badań klinicznych wykazujących takie korzyści kliniczne, jak zmniejszenie objawów związanych z chorobą lub zwiększone przeżycie.
Przeprowadzono trzy duże, międzynarodowe, otwarte badania II fazy, bez grupy kontrolnej, z udziałem pacjentów: z CML z dodatnim chromosomem Philadelphia (Ph+), w przełomie blastycznym lub w fazie akceleracji; innym typem białaczki ale z obecnym chromosomem Philadelphia oraz pacjentów z CML w fazie przewlekłej po uprzednim niepowodzeniu leczenia interferonem alfa (IFN). Przeprowadzono jedno duże, otwarte, wieloośrodkowe, międzynarodowe, randomizowane badanie III fazy u pacjentów z nowo rozpoznaną CML Ph+. Dodatkowo, w dwóch badaniach I fazy i jednym badaniu II fazy leczono dzieci i młodzież.
We wszystkich badaniach klinicznych 38-40% pacjentów było w wieku ≥60 lat, a 10-12% pacjentów było w wieku ≥70 lat.
Faza przewlekła, nowo rozpoznana: W badaniu tym, będącym badaniem III fazy u dorosłych pacjentów porównywano monoterapię imatynibem z leczeniem interferonem alfa (IFN) z cytarabiną (Ara-C). Pacjenci nie wykazujący odpowiedzi [brak całkowitej odpowiedzi hematologicznej (ang. Complete Haematological Response - CHR) w 6 miesiącu, zwiększenie liczby białych krwinek, brak większej odpowiedzi cytogenetycznej (ang. Major Cytogenetic Response - MCyR) w 24 miesiącu], utratę odpowiedzi (utratę CHR lub MCyR) lub ciężką nietolerancję leczenia mogli być przeniesieni do alternatywnego ramienia badania. Grupa pacjentów leczonych imatynibem otrzymywała dawkę 400 mg/dobę. Grupie leczonych IFN podawano dawkę docelową 5 mln j.m./m2 pc./dobę podskórnie w kombinacji z podawanym podskórnie przez 10 dni w miesiącu Ara-C w dawce 20 mg/m2 pc./dobę.
Całkowita liczba 1 106 pacjentów została randomizowna do dwóch grup po 553 osoby każda. Charakterystyka pacjentów była podobna przed podaniem leku w obu grupach. Mediana wieku wynosiła 51 lat (zakres 18–70 lat). 21,9% stanowili pacjenci ≥60 lat. 59% pacjentów stanowili mężczyźni a 41% kobiety; 89,9% stanowiła rasa kaukaska a 4,7% rasa czarna. Siedem lat po włączeniu ostatniego pacjenta, mediana okresu leczenia pierwszego rzutu wynosiła odpowiednio 82 i 8 miesięcy w grupie pacjentów otrzymujących imatynib oraz w grupie leczonej IFN. Mediana okresu leczenia drugiego rzutu imatynibem wynosiła 64 miesiące. U pacjentów przyjmujących imatynib w leczeniu pierwszego rzutu, przeciętna dawka dobowa wynosiła 406 ± 76 mg. Głównym parametrem skuteczności leczenia był czas przeżycia bez objawów postępu choroby. Postęp choroby był definiowany jako jedno z następujących wydarzeń: przejście w fazę akceleracji lub przełom blastyczny, śmierć, utrata CHR lub MCyR, lub u pacjentów, którzy nie osiągnęli CHR zwiększenie liczby białych krwinek pomimo odpowiedniego leczenia. Większa odpowiedź cytogenetyczna, odpowiedź hematologiczna, odpowiedź molekularna (ocena choroby resztkowej), czas do wystąpienia fazy akceleracji lub przełomu blastycznego i czas przeżycia były głównymi parametrami drugorzędowymi. Dane dotyczące odpowiedzi przedstawiono w Tabeli 2.
Tabela 2 Odpowiedź na leczenie w badaniu (dane po 84 miesiącach) u pacjentów z nowo rozpoznaną CML
(Wskaźniki najlepszej odpowiedzi) | imatynib n=553 | IFN+Ara-C n=553 |
Odpowiedź hematologiczna | ||
Wskaźnik CHR n (%) | 534 (96,6%)* | 313 (56,6%)* |
[95% przedział ufności (CI)] | [94,7%, 97,9%] | [52,4%, 60,8%] |
Odpowiedź cytogenetyczna | ||
Większa odpowiedź n (%) | 490 (88,6%)* | 129 (23,3%)* |
[95% CI] | [85,7%, 91,1%] | [19,9%, 27,1%] |
Całkowita CyR n (%) | 456 (82,5%)* | 64 (11,6%)* |
Częściowa CyR n (%) | 34 (6,1%) | 65 (11,8%) |
Odpowiedź molekularna** | ||
Większa odpowiedź w 12 miesiącu (%) | 153/305=50,2% | 8/83=9,6% |
Większa odpowiedź w 24 miesiącu (%) | 73/104=70,2% | 3/12=25% |
Większa odpowiedź w 84 miesiącu (%) | 102/116=87,9% | 3/4=75% |
* p<0,001, test Fischera ** odsetki odpowiedzi molekularnej są oparte na ocenie dostępnych próbek Kryteria odpowiedzi hematologicznej (wszystkie odpowiedzi powinny być potwierdzone po ≥4 tygodniach): leukocyty <10 x 109/l, płytki <450 x 109/l, mielocyty+metamielocyty <5% we krwi, brak blastów i promielocytów we krwi, granulocyty zasadochłonne <20%, brak pozaszpikowych ognisk białaczki. Kryteria odpowiedzi cytogenetycznej: całkowita (0% Ph+ metafaz), częściowa (1–35%), mniejsza (36–65%) lub minimalna (66–95%). Większa odpowiedź (0–35%) stanowi połączenie całkowitej i częściowej. Kryteria większej odpowiedzi molekularnej: zmniejszenie ilości transkryptu Bcr-Abl we krwi obwodowej ≥3 logarytmy (mierzone ilościową metodą RT-PCR w czasie rzeczywistym) w stosunku do wystandaryzowanych wartości wyjściowych. | ||
Wskaźniki całkowitej odpowiedzi hematologicznej, większej odpowiedzi cytogenetycznej oraz całkowitej odpowiedzi cytogenetycznej w leczeniu pierwszego rzutu szacowano stosując metodę Kaplana-Meier’a, w której obserwacje przypadków bez uzyskanej odpowiedzi były cenzorowane datą ostatniego badania. Uzyskane z zastosowaniem tej metody szacowane skumulowane wskaźniki odpowiedzi u pacjentów leczonych w pierwszej linii imatynibem uległy poprawie: CHR z 96,4% do 98,4% i CCyR z 69,5% do 87,2% po odpowiednio 12 i 84 miesiącach leczenia.
W ciągu 7 lat obserwacji, odnotowano 93 (16,8%) przypadków progresji choroby w grupie pacjentów otrzymujących imatynib: 37 (6,7%) przypadków progresji do fazy akceleracji/przełomu blastycznego, 31 (5,6%) przypadków utraty MCyR, 15 (2,7%) utraty CHR lub wzrostu liczby WBC oraz 10 (1,8%) przypadków zgonów bez związku z CML. Natomiast w ramieniu IFN+Ara-C obserwowano 165 (29,8%) zdarzeń, z czego 130 wystąpiło podczas stosowania IFN+Ara-C jako leczenia pierwszego rzutu.
Szacowany współczynnik pacjentów bez progresji do fazy akceleracji lub przełomu blastycznego po 84 miesiącach był istotnie większy w grupie pacjentów otrzymujących imatynib w porównaniu do pacjentów leczonych IFN (92,5% w porównaniu do 85,1%, p<0,001). Roczny współczynnik progresji do fazy akceleracji lub przełomu blastycznego zmniejszał się w miarę czasu trwania leczenia i był mniejszy niż 1% rocznie w czwartym i piątym roku. Szacowany współczynnik przeżycia bez postępu choroby po 84 miesiącach wyniósł 81,2% w ramieniu z imatynibem oraz 60,6% w ramieniu kontrolnym (p<0,001). Roczne współczynniki progresji jakiegokolwiek typu dla imatynibu także zmniejszały się w czasie.
Łącznie zmarło 71 (12,8%) pacjentów z grupy leczonej imatynibem i 85 (15,4%) pacjentów z grupy otrzymującej IFN+Ara-C. Po 84 miesiącach szacowane przeżycie całkowite wynosi 86,4% (83, 90) w porównaniu do 83,3% (80, 87), odpowiednio dla pacjentów zrandomizowanych do grupy leczonej imatynibem oraz do grupy otrzymującej IFN+Ara-C (p=0,073, logarytmiczny test rang). Na ten punkt końcowy, czas do wystąpienia zdarzenia, duży wpływ miał wysoki odsetek pacjentów, u których zmieniono leczenie z IFN+Ara-C na imatynib. Wpływ leczenia imatynibem na przeżycie pacjentów z nowo rozpoznaną CML w fazie przewlekłej był dalej badany w retrospektywnej analizie powyższych danych dotyczących imatynibu z uwzględnieniem danych z innego badania III fazy z zastosowaniem IFN+Ara-C (n=325) o identycznym schemacie dawkowania. W tej analizie retrospektywnej, wykazano przewagę leczenia imatynibem nad leczeniem z zastosowaniem schematu IFN+Ara-C w zakresie wpływu na czas całkowitego przeżycia (p<0,001); w ciągu 42 miesięcy zmarło 47 (8,5%) pacjentów leczonych imatynibem i 63 (19,4%) pacjentów leczonych wg schematu IFN+Ara-C.
Stopień odpowiedzi cytogenetycznej i odpowiedzi molekularnej miał wyraźny wpływ na długoterminowe wyniki leczenia wśród pacjentów otrzymujących imatynib. Podczas, gdy szacunkowo 96% (93%) pacjentów z CCyR (PCyR) w 12. miesiącu było wolnych od progresji do fazy akceleracji/przełomu blastycznego po 84 miesiącach, jedynie u 81% pacjentów bez MCyR w 12. miesiącu nie doszło do progresji do zaawansowanej fazy CML po 84 miesiącach trwania badania
(całkowite p<0,001, p=0,25 pomiędzy CCyR a PCyR). U pacjentów ze zmniejszeniem ilości transkrypcji Bcr-Abl nie mniejszej niż 3 logarytmy po 12 miesiącach, prawdopodobieństwo pozostawania w grupie bez progresji do fazy akceleracji/przełomu blastycznego wynosiło 99% po 84 miesiącach. Podobne obserwacje zebrano w oparciu o analizę badania po 18 miesiącach.
W badaniu tym możliwe było zwiększenie dawki z 400 mg na dobę do 600 mg na dobę, a następnie z 600 mg na dobę do 800 mg na dobę. Po 42 miesiącach obserwacji, u 11 pacjentów nastąpiła potwierdzona utrata (w ciągu 4 tygodni) odpowiedzi cytogenetycznej. Wśród tych 11 pacjentów, u 4 dawkę leku zwiększono do 800 mg na dobę, przy czym u 2 z nich odpowiedź cytogenetyczną odzyskano (u 1 pacjenta - częściową i u 1 pacjenta - całkowitą, a w tym ostatnim przypadku uzyskano również odpowiedź molekularną), natomiast wśród pozostałych 7 pacjentów, u których nie zwiększano dawki leku, całkowitą odpowiedź cytogenetyczną odzyskano tylko u 1 pacjenta. U 40 pacjentów, którym dawkę leku zwiększono do 800 mg na dobę, w porównaniu z populacją pacjentów przed zwiększeniem dawki (n=551) odsetek pewnych działań niepożądanych był większy. Do częściej występujących działań niepożądanych należały krwotoki z przewodu pokarmowego, zapalenie spojówek, podwyższona aktywność aminotransferaz lub stężenia bilirubiny. Inne działania niepożądane występowały z mniejszą lub równą częstością.
Faza przewlekła, niepowodzenie leczenia interferonem: 532 dorosłych pacjentów było leczonych dawką początkową 400 mg. Pacjentów podzielono na trzy główne grupy: niepowodzenie w zakresie parametrów hematologicznych (29%), niepowodzenie w zakresie parametrów cytogenetycznych (35%) oraz nietolerancja interferonu (36%). Uprzednio pacjenci byli leczeni IFN przez średnio 14 miesięcy w dawkach ≥25 x 106 j.m./tydzień. Wszyscy pacjenci byli w późnej fazie przewlekłej, a średni czas od chwili rozpoznania choroby wynosił 32 miesiące. Głównym parametrem skuteczności ocenianym w trakcie tego badania był wskaźnik większej odpowiedzi cytogenetycznej (odpowiedź całkowita + odpowiedź częściowa, 0 do 35% metafaz Ph+ w szpiku kostnym).
W badaniu osiągnięto dużą odpowiedź cytogenetyczną u 65% pacjentów, w tym u 53% była to odpowiedź całkowita (potwierdzona u 43%) (Tabela 3). Całkowitą odpowiedź hematologiczną uzyskano u 95% pacjentów.
Faza akceleracji: Do badania włączono 235 dorosłych pacjentów w fazie akceleracji. U pierwszych 77 pacjentów rozpoczęto leczenie podając lek w dawce 400 mg, a następnie po wprowadzeniu poprawek do protokołu umożliwiających podawanie większych dawek leku, kolejnych 158 pacjentów rozpoczynało leczenie od dawki 600 mg.
Głównym parametrem skuteczności był wskaźnik odpowiedzi hematologicznej, określany jako całkowita odpowiedź hematologiczna, brak objawów białaczki (tzn. brak blastów w szpiku i krwi, ale bez pełnej normalizacji obrazu krwi obwodowej jak ma to miejsce w przypadku całkowitej odpowiedzi hematologicznej) lub powrót do fazy przewlekłej CML. Potwierdzoną odpowiedź hematologiczną uzyskano u 71,5% pacjentów (Tabela 3). Ważne jest, że 27,7% pacjentów osiągnęło także większą odpowiedź cytogenetyczną, w tym 20,4% pacjentów całkowitą odpowiedź cytogenetyczną (potwierdzoną u 16%). Dla pacjentów leczonych dawką 600 mg, obecna szacunkowa mediana przeżycia bez progresji choroby i przeżycie całkowite wynosiły odpowiednio 22,9 i 42,5 miesięcy.
Mieloidalny przełom blastyczny: Do badania włączono 260 pacjentów z mieloidalnym przełomem blastycznym. 95 pacjentów (37%) otrzymywało uprzednio chemioterapię z powodu fazy akceleracji lub przełomu blastycznego („pacjenci uprzednio leczeni”), natomiast 165 pacjentów (63%) nie było poddanych chemioterapii („pacjenci uprzednio nieleczeni”). U pierwszych 37 pacjentów rozpoczęto leczenie podając lek w dawce 400 mg, a następnie po wprowadzeniu poprawek do protokołu umożliwiających podawanie większych dawek leku, kolejnych 223 pacjentów rozpoczynało leczenie od dawki 600 mg.
Głównym parametrem skuteczności był wskaźnik odpowiedzi hematologicznej, określany jako całkowita odpowiedź hematologiczna, brak objawów białaczki lub powrót do fazy przewlekłej CML.
Przyjęto takie same kryteria oceny jak w badaniu z udziałem pacjentów w fazie akceleracji. W tym badaniu, odpowiedź hematologiczną uzyskano u 31% pacjentów (36% w grupie pacjentów uprzednio nieleczonych, a 22% w grupie pacjentów uprzednio leczonych) (Tabela 3). Wskaźnik odpowiedzi hematologicznej był większy wśród pacjentów leczonych dawką 600 mg (33%), w porównaniu z pacjentami leczonymi dawką 400 mg (16%, p=0,0220). Szacuje się, że średnie przeżycie w grupie pacjentów uprzednio nieleczonych oraz pacjentów uprzednio leczonych wynosiło odpowiednio 7,7 i 4,7 miesiąca.
Limfoidalny przełom blastyczny: do badań I fazy została włączona ograniczona liczba pacjentów (n=10). Wskaźnik odpowiedzi hematologicznej wynosił 70% i utrzymywał się 2-3 miesiące.
Tabela 3 Odpowiedź na leczenie u dorosłych pacjentów z CML
Badanie 0110 Dane po 37 miesiącach Faza przewlekła, niepowodzenie leczenia IFN (n=532) | Badanie 0109 Dane po 40,5 miesiącach Faza akceleracji (n=235) | Badanie 0102 Dane po 38 miesiącach Mieloidalny przełom blastyczny (n = 260) | |
% pacjentów (CI 95%) | |||
Odpowiedź hematologiczna1 | 95% (92,3–96,3) | 71% (65,3–77,2) | 31% (25,2–36,8) |
Całkowita odpowiedź | 95% | 42% | 8% |
hematologiczna (CHR) | |||
Brak objawów białaczki | Nie dotyczy | 12% | 5% |
(NEL) | |||
Powrót do fazy przewlekłej | Nie dotyczy | 17% | 18% |
(RTC) | |||
Większa odpowiedź | 65% (61,2–69,5) | 28% (22,0–33,9) | 15% (11,2–20,4) |
cytogenetyczna2 | |||
Całkowita | 53% | 20% | 7% |
(Potwierdzona3) [95% CI] | (43%) [38,6–47,2] | (16%) [11,3– | (2%) [0,6–4,4] |
21,0] | |||
Częściowa | 12% | 7% | 8% |
1Kryteria odpowiedzi hematologicznej (wszystkie odpowiedzi powinny być potwierdzone po ≥4 tygodniach): CHR (ang. Complete Haematological Response): badanie 0110 [leukocyty <10 x 109/l, płytki krwi <450 x 109/l, mielocyty+metamielocyty <5% we krwi, brak blastów i promielocytów we krwi, granulocyty zasadochłonne <20%, brak pozaszpikowych ognisk białaczki],w badaniach 0102 oraz 0109 [ANC ≥1,5 x 109/l, płytki krwi ≥100 x 109/l, brak blastów we krwi, blasty w szpiku kostnym <5% i brak pozaszpikowych ognisk białaczki]. NEL (ang. No Evidence of Leukaemia): Kryteria jak w przypadku całkowitej CHR, ale ANC ≥1 x 109/l, płytki krwi ≥20 x 109/l (tylko w badaniach 0102 i 0109). RTC (ang. Return to Chronic Phase): <15% blastów w BM i PB, <30% blastów + promielocytów w BM i PB, <20% granulocytów zasadochłonnych we PB, brak pozaszpikowych ognisk białaczki z wyjątkiem śledziony i wątroby (tylko w badaniach 0102 i 0109). BM = szpik kostny, PB = krew obwodowa 2Kryteria odpowiedzi cytogenetycznej: Duża odpowiedź cytogenetyczna zawiera połączone wskaźniki odpowiedzi całkowitej i częściowej: odpowiedź całkowita (0% metafaz Ph+), odpowiedź częściowa (1-35%). 3Całkowita odpowiedź cytogenetyczna potwierdzona drugim badaniem cytogenetycznym szpiku wykonanym co najmniej jeden miesiąc po badaniu wstępnym. | |||
Dzieci i młodzież: 26 pacjentów w wieku <18 lat z fazą przewlekłą CML (n=11) lub z CML w przełomie blastycznym lub z Ph+ ostrymi białaczkami (n=15) brało udział w badaniu I fazy dotyczącym ustalenia dawki. Pacjenci ci byli uprzednio bardzo intensywnie leczeni: 46%
transplantacją szpiku (BMT), a 73% programami chemioterapii wielolekowej. Pacjenci byli leczeni imatynibem w dawce 260 mg/m2 pc./dobę (n=5), 340 mg/m2 pc./dobę (n=9), 440 mg/m2 pc./dobę (n=7) i 570 mg/m2 pc./dobę (n=5). Z 9 pacjentów w fazie przewlekłej CML i wykonanymi badaniami cytogenetycznymi, 4 (44%) i 3 (33%) osiągnęło, odpowiednio, całkowitą i częściową odpowiedź cytogetyczną, a odsetek MCyR wynosił 77%.
51 pacjentów z populacji dzieci i młodzieży z nowo rozpoznaną i nieleczoną CML w fazie przewlekłej zostało włączonych do otwartego, wieloośrodkowego, jednoramiennego badania II fazy. Pacjenci byli leczeni imatynibem w dawce 340 mg/m2 pc./dobę bez przerw przy braku toksyczności zależnej od dawki. Leczenie produktem Meaxin powodowało szybką odpowiedź hematologiczną (ang. complete haematological response - CHR) u 78% dzieci i młodzieży z nowo zdiagnozowaną CML po
8 tygodniach leczenia. Wysoki współczynnik CHR u 65% pacjentów towarzyszył całkowitej odpowiedzi cytogenetycznej (ang. complete cytogenetic response - CCyR), która jest porównywalna do wyników obserwowanych u dorosłych. Ponadto, w grupie badanej obserwowano częściową odpowiedź cytogenetyczną (ang. partial cytogenetic response - PCyR) u 16% pacjentów, a dużą odpowiedź cytogenetyczną (ang. major cytogenetic response - MCyR) u 81% pacjentów. Większość pacjentów osiągnęło CCyR między 3., a 10. miesiącem, z medianą czasu do uzyskania odpowiedzi na podstawie analizy Kaplana-Meiera, wynoszącą 5,6 miesiąca.
Badania kliniczne w Ph+ ALL
Nowo rozpoznana Ph+ ALL: W badaniu kontrolowanym (ADE10) porównującym imatynib
z chemioterapią indukcyjną u 55 pacjentów w wieku co najmniej 55 lat z nowo rozpoznaną chorobą, imatynib stosowany w monoterapii spowodował istotnie wyższy wskaźnik całkowitej odpowiedzi hematologicznej niż chemioterapia (96,3% w porównaniu do 50%; p=0,0001). Kiedy u pacjentów bez odpowiedzi lub ze słabą odpowiedzią na chemioterapię wprowadzono imatynib, całkowitą odpowiedź hematologiczną uzyskano u 9 z 11 pacjentów (81,8%). Ten efekt kliniczny związany był z większym zmniejszeniem ilości transkryptów Bcr-Abl po 2 tygodniach leczenia wśród pacjentów leczonych imatynibem w porównaniu z pacjentami leczonymi chemioterapią (p=0,02). Po indukcji wszyscy pacjenci otrzymywali imatynib oraz chemioterapię konsolidacyjną (patrz Tabela 4) i po 8 tygodniach po indukcji, a ilość transkryptów Bcr-Abl była identyczna w obu ramieniach badania. Jak można było się spodziewać na podstawie projektu badania, nie stwierdzono różnic w czasie trwania remisji, okresie przeżycia bez choroby i całkowitym czasie przeżycia, jednak pacjenci, u których stwierdzono całkowitą odpowiedź molekularną i minimalną chorobę resztkową osiągnęli lepsze wyniki zarówno w odniesieniu do czasu trwania remisji (p=0,01) jak i czasu przeżycia bez choroby (p=0,02).
Wyniki uzyskane w populacji 211 pacjentów z nowo rozpoznaną Ph+ ALL, uczestniczących
w czterech niekontrolowanych badaniach klinicznych (AAU02, ADE04, AJP01 i AUS01) są zgodne z wynikami opisanymi powyżej. Imatynib w skojarzeniu z chemioterapią indukcyjną (patrz Tabela 4) wywołał całkowitą odpowiedź hematologiczną w 93% (u 147 z 158 pacjentów podlegających ocenie) oraz 90% wskaźnik większej odpowiedzi cytogenetycznej (19 z 21 pacjentów podlegających ocenie). Wskaźnik całkowitej odpowiedzi molekularnej wyniósł 48% (49 ze 102 pacjentów podlegających ocenie). Okres przeżycia bez choroby (ang. diseaese-free survival - DFS) oraz całkowity czas przeżycia (ang. overall survival - OS) stale przekraczały 1 rok i były zwiększone w porównaniu
z historyczną grupą kontrolną (DFS p<0,001; OS p<0,0001) w dwóch badaniach (AJP01 i AUS01).
Tabela 4 Chemioterapia stosowana w połączeniu z imatynibem
Badanie ADE10 | |
Faza wstępna | DEX 10 mg/m2 doustnie, dni 1-5; CP 200 mg/m2 iv., dni 3, 4, 5; MTX 12 mg dooponowo, dzień 1 |
Indukcja remisji | DEX 10 mg/m2 doustnie, dni 6-7, 13-16; VCR 1 mg iv., dni 7, 14; IDA 8 mg/m2 iv. (0,5 h), dni 7, |
8, 14, 15; CP 500 mg/m2 iv. (1 h), dzień 1; Ara-C 60 mg/m2 iv., dni 22-25, 29-32 | |
Konsolidacja leczenia I, III, V | MTX 500 mg/m2 iv. (24 h), dni 1, 15; 6-MP 25 mg/m2 doustnie, dzień 1-20 |
Konsolidacja leczenia II, IV | Ara-C 75 mg/m2 iv. (1 h), dni 1-5; VM26 60 mg/m2 iv. (1 h), dni 1-5 |
Badanie AAU02 | |
Leczenie indukcyjne (de novo Ph+ ALL) | Daunorubicyna 30 mg/m2 iv., dni 1-3, 15-16; VCR 2 mg całkowita dawka iv., dni 1, 8, 15, 22; CP 750 mg/m2 iv., dni 1, 8; prednizon 60 mg/m2 doustnie, dni 1-7, 15-21; IDA 9 mg/m2 doustnie, dni 1-28; MTX 15 mg dooponowo, dni 1, 8, 15, 22; Ara-C 40 mg dooponowo, dni 1, 8, 15, 22; Metyloprednizolon 40 mg dooponowo, dni 1, 8, 15, 22 |
Konsolidacja leczenia (de novo Ph+ ALL) | Ara-C 1000 mg/m2/12 h iv. (3 h), dni 1-4; Mitoksantron 10 mg/m2 iv., dni 3-5; MTX 15 mg dooponowo, dzień 1; Metyloprednizolon 40 mg dooponowo, dzień 1 |
Badanie ADE04 | |
Faza wstępna | DEX 10 mg/m2 doustnie dni 1-5; CP 200 mg/m2 iv., dni 3-5; MTX 15 mg dooponowo, dzień 1 |
Leczenie indukcyjne I | DEX 10 mg/m2 doustnie, dni 1-5; VCR 2 mg iv., dni 6, 13, 20; Daunorubicyna 45 mg/m2 iv., dni 6-7, 13-14 |
Leczenie indukcyjne II | CP 1 g/m2 iv. (1 h), dni 26, 46; Ara-C 75 mg/m2 iv. (1 h), dni 28-31, 35-38, 42-45; 6-MP 60 mg/m2 doustnie, dni 26-46 |
Konsolidacja leczenia | DEX 10 mg/m2 doustnie, dni 1-5; Windezyna 3 mg/m2 iv., dzień 1; MTX 1,5 g/m2 iv. (24 h), dzień 1; Etopozyd 250 mg/m2 iv. (1 h), dni 4-5; Ara-C 2x 2 g/m2 iv. (3 h, q 12 h), dzień 5 |
Badanie AJP01 | |
Leczenie indukcyjne | CP 1,2 g/m2 iv. (3 h), dzień 1; Daunorubicyna 60 mg/m2 iv. (1 h), dni 1-3; Winkrystyna 1,3 mg/m2 iv., dni 1, 8, 15, 21; Prednizolon 60 mg/m2/doba doustnie |
Konsolidacja leczenia | Naprzemienna chemioterapia: duże dawki chemioterapii z MTX 1 g/m2 iv. (24 h), dzień 1 i Ara-C 2 g/m2 iv. (q 12 h), dni 2-3, dla 4 cykli |
Podtrzymywanie remisji | VCR 1,3 g/m2 iv., dzień 1; Prednizolon 60 mg/m2 doustnie, dni 1-5 |
Badanie AUS01 | |
Leczenie indukcyjno-konsolidacyjne | Schemat Hyper-CVAD regimen: CP 300 mg/m2 iv. (3 h, q 12 h), dzień 1-3; Winkrystyna 2 mg iv., dni 4, 11; Doksorubicyna 50 mg/m2 i.v. (24 h), dzień 4; DEX 40 mg/doba w dniach 1-4 i 11-14, naprzemiennie z MTX 1 g/m2 iv. (24 h), dzień 1, |
Ara-C 1 g/m2 iv. (2 h, q 12 h), dni 2-3 (ogółem 8 kursów leczenia) | |
Podtrzymywanie remisji | VCR 2 mg iv. co miesiąc przez 13 miesięcy; Prednizolon 200 mg doustnie, 5 dni w ciągu miesiąca przez 13 miesięcy |
Wszystkie schematy leczenia zawierają stosowanie steroidów jako profilaktykę dla ośrodkowego układu nerwowego. | |
Ara-C: arabinozyd cytozyny; CP: cyklofosfamid; DEX: deksametazon; MTX: metotreksat; 6-MP: 6-merkaptopuryna; VM26: tenipozyd; VCR: winkrystyna; IDA: idarubicyna; iv.: dożylnie | |
Dzieci i młodzież: Do badania I2301, będącego otwartym, wieloośrodkowym, nierandomizowanym sekwencyjnym badaniem kohortowym III fazy włączono w sumie 93 dzieci, młodzieży i młodych dorosłych (w wieku od 1 do 22 lat) z Ph (+) ALL, którym podawano imatynib (340 mg/m2 pc./dobę) w skojarzeniu z intensywną chemioterapią po leczeniu indukcyjnym. Imatynib podawano z przerwami kohortom 1-5, zwiększając czas trwania i przyspieszając rozpoczęcie leczenia imatynibem
w poszczególnych kohortach; przy czym kohorta 1 otrzymywała leczenie imatynibem o najmniejszej intensywności, a kohorta 5 otrzymywała leczenie o największej intensywności (najdłuższy czas trwania liczony w dniach z ciągłym, codziennym podawaniem imatynibu w pierwszych cyklach chemioterapii). Nieprzerwana, codzienna ekspozycja na imatynib na wczesnym etapie leczenia
w skojarzeniu z chemioterapią w kohorcie 5 (n=50) spowodowała poprawę 4-letniego przeżycia bez zdarzeń (EFS) w porównaniu z historyczną grupą kontrolną (n=120), która otrzymywała standardową chemioterapię bez imatynibu (odpowiednio 69,6% w porównaniu z 31,6%). Szacowane 4-letnie przeżycie całkowite (OS) w kohorcie 5 wyniosło 83,6% w porównaniu z 44,8% w historycznej grupie kontrolnej. U 20 z 50 (40%) pacjentów z kohorty 5 dokonano przeszczepienia hematopoetycznych komórek macierzystych.
Tabela 5 Schemat chemioterapii stosowany w skojarzeniu z imatynibem w badaniu I2301
Konsolidacja blok 1 (3 tygodnie) | VP-16 (100 mg/m2 pc./dobę, iv.): dni 1-5 Ifosfamid (1,8 g/m2 pc./dobę, iv.): dni 1-5 MESNA (360 mg/m2 pc./dawka co 3 godz., x 8 dawek/dobę, iv.): dni 1-5 G-CSF (5 μg/kg mc., sc.): dni 6-15 lub do czasu, gdy ANC > 1500 po osiągnięciu nadiru IT Metotreksat (dostosowany do wieku): TYLKO dzień 1 Potrójna terapia IT (dostosowana do wieku): dzień 8, 15 |
Konsolidacja blok 2 (3 tygodnie) | Metotreksat (5 g/m2 pc. w ciągu 24 godzin, iv.): dzień 1 Leukoworyna (75 mg/m2 pc. w godzinie 36, iv.; 15 mg/m2 pc. iv. lub po. co 6 godz. x 6 dawek)iii: Dni 2 i 3 Potrójna terapia IT (dostosowana do wieku): dzień 1 ARA-C (3 g/m2 pc./dawkę co 12 godz. x 4, iv.): dni 2 i 3 G-CSF (5 μg/kg mc., sc.): dni 4-13 lub do czasu, gdy ANC > 1500 po osiągnięciu nadiru |
Reindukcja blok 1 (3 tygodnie) | VCR (1,5 mg/m2 pc./dobę, iv.): dni 1, 8 i 15 DAUN (45 mg/m2 pc./dobę w bolusie, iv.): dni 1 i 2 CPM (250 mg/m2 pc./dawkę co 12 godz. x 4 dawki, iv.): dni 3 i 4 PEG-ASP (2500 j.m./m2 pc., im.): dzień 4 G-CSF (5 μg/kg mc., sc.): dni 5-14 lub do czasu, gdy ANC > 1500 po osiągnięciu nadiru Potrójna terapia IT (dostosowana do wieku): dni 1 i 15 DEX (6 mg/m2 pc./dobę, po.): dni 1-7 i 15-21 |
Intensyfikacja blok 1 (9 tygodni) | Metotreksat (5 g/m2 pc. w ciągu 24 godzin, iv.): dni 1 i 15 Leukoworyna (75 mg/m2 pc. w godzinie 36, iv.; 15 mg/m2 pc. iv. lub po. co 6 godz. x 6 dawek)iii: Dni 2, 3, 16 i 17 Potrójna terapia IT (dostosowana do wieku): dni 1 i 22 VP-16 (100 mg/m2 pc./dobę, iv.): dni 22-26 CPM (300 mg/m2 pc./dobę, iv.): dni 22-26 |
MESNA (150 mg/m2 pc./dobę, iv.): dni 22-26 G-CSF (5 μg/kg mc., sc.): dni 27-36 lub do czasu, gdy ANC > 1500 po osiągnięciu nadiru ARA-C (3 g/m2 pc., co 12 godz., iv.): dni 43, 44 L-ASP (6000 j.m./m2 pc., im.): dzień 44 | |
Reindukcja blok 2 (3 tygodnie) | VCR (1,5 mg/m2 pc./dobę, iv.): dni 1, 8 i 15 DAUN (45 mg/m2 pc./dobę w bolusie, iv.): dni 1 i 2 CPM (250 mg/m2 pc./dawkę co 12 godz. x 4 dawki, iv.): Dni 3 i 4 PEG-ASP (2500 j.m./m2 pc., im.): dzień 4 G-CSF (5 μg/kg mc., sc.): dni 5-14 lub do czasu, gdy ANC > 1500 po osiągnięciu nadiru Potrójna terapia IT (dostosowana do wieku): dni 1 i 15 DEX (6 mg/m2 pc./dobę, po.): dni 1-7 i 15-21 |
Intensyfikacja blok 2 (9 tygodni) | Metotreksat (5 g/m2 pc. w ciągu 24 godzin, iv.): dni 1 i 15 Leukoworyna (75 mg/m2 pc. w godzinie 36, iv.; 15 mg/m2 pc. iv. lub po. co 6 godz. x 6 dawek)iii: dni 2, 3, 16 i 17 Potrójna terapia IT (dostosowana do wieku): dni 1 i 22 VP-16 (100 mg/m2 pc./dobę, iv.): dni 22-26 CPM (300 mg/m2 pc./dobę, iv.): dni 22-26 MESNA (150 mg/m2 pc./dobę, iv.): dni 22-26 G-CSF (5 μg/kg mc., sc.): dni 27-36 lub do czasu, gdy ANC > 1500 po osiągnięciu nadiru ARA-C (3 g/m2 pc., co 12 godz., iv.): dni 43, 44 L-ASP (6000 j.m./m2 pc., im.): dzień 44 |
Leczenie podtrzymujące (cykle 8-tygodniowe) Cykle 1-4 | Metotreksat (5 g/m2 pc. w ciągu 24 godzin, iv.): dzień 1 Leukoworyna (75 mg/m2 pc. w godzinie 36, iv.; 15 mg/m2 pc. iv. lub po. co 6 godz. x 6 dawek)iii: dni 2 i 3 Potrójna terapia IT (dostosowana do wieku): dni 1, 29 VCR (1,5 mg/m2 pc., iv.): dni 1, 29 DEX (6 mg/m2 pc./dobę po.): dni 1-5; 29-33 6-MP (75 mg/m2 pc./dobę, po.): dni 8-28 Metotreksat (20 mg/m2 pc./tydzień, po.): dni 8, 15, 22 VP-16 (100 mg/m2 pc., iv.): dni 29-33 CPM (300 mg/m2 pc., iv.): dni 29-33 MESNA IV dni 29-33 G-CSF (5 μg/kg mc., sc.): dni 34-43 |
Leczenie podtrzymujące (cykle 8-tygodniowe) Cykl 5 | Napromienianie czaszki (Tylko blok 5) 12 Gy w 8 frakcjach u wszystkich pacjentów zaklasyfikowanych jako pozostających w stanie CNS1 i CNS2 w chwili rozpoznania 18 Gy w 10 frakcjach u pacjentów zaklasyfikowanych, jako pozostających w stanie CNS3 w chwili rozpoznania VCR (1,5 mg/m2 pc./dobę, iv.): dni 1, 29 DEX (6 mg/m2 pc./dobę, po.): dni 1-5; 29-33 6-MP (75 mg/m2/dobę, po.): dni 11-56 (wstrzymanie 6-MP podczas 6-10 dni napromieniania czaszki poczynając od dnia 1 Cyklu 5. Rozpoczęcie podawania 6-MP 1-szego dnia po zakończeniu naświetlania głowy.) Metotreksat (20 mg/m2 pc./tydzień, po.): dni 8, 15, 22, 29, 36, 43, 50 |
Leczenie podtrzymujące (cykle 8-tygodniowe) Cykle 6-12 | VCR (1,5 mg/m2 pc./dobę, iv.): dni 1, 29 DEX (6 mg/m2 pc./dobę, po.): dni 1-5; 29-33 6-MP (75 mg/m2 pc./dobę, po.): dni 1-56 Metotreksat (20 mg/m2 pc./tydzień, po.): dni 1, 8, 15, 22, 29, 36, 43, 50 |
G-CSF = czynnik stymulujący kolonie granulocytarne, VP-16 = etopozyd, iv. = dożylnie, sc. = podskórnie, IT = dooponowo, po. = doustnie, im. = domięśniowo, ARA-C = cytarabina, CPM = cyklofosfamid, VCR = winkrystyna, DEX = deksametazon, DAUN = daunorubicyna, 6-MP = 6- merkaptopuryna, E.Coli L-ASP = L-Asparaginaza, PEG-ASP = PEG-Asparaginaza, MESNA= 2-
merkaptoetanosulfonian sodowy, iii= lub do czasu, gdy stężenie MTX wyniesie <0,1 μM, q6h = co 6 godz., Gy= Gray
Badanie AIT07 było wieloośrodkowym, otwartym, badaniem II/III fazy z randomizacją, z udziałem 128 pacjentów (w wieku 1 do < 18 lat) leczonych imatynibem w skojarzeniu z chemioterapią. Dane
z tego badania dotyczące bezpieczeństwa wydają się być zgodne z profilem bezpieczeństwa imatynibu u pacjentów z Ph+ ALL.
Nawracająca/oporna na leczenie Ph+ ALL: Po podaniu imatynibu w monoterapii pacjentom
z nawracającą/oporną na leczenie Ph+ ALL u 53 z 411 pacjentów, u których odpowiedź była możliwa do oceny, wskaźnik odpowiedzi hematologicznej wyniósł 30% (9% odpowiedzi całkowitej),
a wskaźnik większej odpowiedzi cytogenetycznej wyniósł 23%. (Co istotne, 353 z 411 pacjentów otrzymywało leczenie według rozszerzonego programu dostępu, bez zebrania danych dotyczących pierwszej odpowiedzi). Mediana czasu do progresji w całej populacji 411 pacjentów
z nawracającą/oporną na leczenie Ph+ ALL wahała się od 2,6 do 3,1 miesiąca, a mediana całkowitego przeżycia u 401 pacjentów podlegających ocenie wahała się od 4,9 do 9 miesięcy. Podobne dane uzyskano po powtórnej analizie z udziałem tylko pacjentów w wieku 55 lat i starszych.
Badania kliniczne w MDS/MPD
Doświadczenie z zastosowaniem imatynibu w tym wskazaniu jest bardzo ograniczone i opiera się na wskaźnikach odpowiedzi hematologicznej i cytogenetycznej. Brak badań klinicznych wykazujących korzyść kliniczną lub wydłużone przeżycie. Przeprowadzono jedno otwarte wieloośrodkowe badanie II fazy (badanie B2225) testujące imatynib w różnorodnych populacjach pacjentów cierpiących na zagrażające życiu choroby związane z kinazą białkowo-tyrozynową Abl, Kit lub PDGFR. W badaniu tym uczestniczyło 7 pacjentów z MDS/MPD leczonych imatynibem w dawce 400 mg na dobę. U 3 pacjentów wystąpiła całkowita odpowiedź hematologiczna (CHR), a u 1 pacjenta – odpowiedź częściowa (PHR). W momencie pierwszej analizy u trzech z czterech pacjentów, u których wykryto rearanżacje genu PDGFR wystąpiła odpowiedź hematologiczna (2 CHR i 1 PHR). Wiek tych pacjentów wahał się od 20 do 72 lat.
Prowadzono rejestr obserwacyjny (badanie L2401) w celu zgromadzenia danych o długotrwałym bezpieczeństwie stosowania i skuteczności produktu u pacjentów z nowotworami mieloproliferacyjnymi z rearanżacją PDGFR-β, leczonych imatynibem. 23 pacjentów włączonych do tego rejestru otrzymywało imatynib w dawce dobowej o medianie 264 mg (zakres: 100 do 400 mg) przez medianę 7,2 lat (zakres 0,1 do 12,7 lat). Z uwagi na obserwacyjny typ tego rejestru, dane dotyczące oceny hematologicznej, cytogenetycznej i molekularnej były dostępne odpowiednio dla 22, 9 i 17 z 23 włączonych pacjentów. Przyjmując zachowawcze założenie, że pacjenci z brakującymi danymi byli pacjentami bez odpowiedzi, CHR obserwowano u 20/23 (87%) pacjentów, CCyR u 9/23 (39,1%) pacjentów, a MR u 11/23 (47,8%) pacjentów. Obliczając wskaźnik odpowiedzi na podstawie danych pochodzących od pacjentów z przynajmniej jedną ważną oceną, wskaźnik odpowiedzi CHR, CCyR i MR wyniósł odpowiednio 20/22 (90,9%), 9/9 (100%) i 11/17 (64,7%).
Ponadto, donoszono o przypadkach kolejnych 24 pacjentów z MDS/MPD opisanych w 13 publikacjach. 21 pacjentów otrzymywało imatynib w dawce 400 mg na dobę, a kolejnych 3 pacjentów było leczonych mniejszymi dawkami. U 11 pacjentów wykryto rearanżacje genu PDGFR, 9 pacjentów uzyskało całkowitą odpowiedź hematologiczną (CHR), a 1 pacjent - odpowiedź częściową (PHR).
Wiek tych pacjentów wynosił od 2 do 79 lat. W ostatniej publikacji przedstawiono uaktualnione dane dotyczące 6 z 11 wspomnianych pacjentów, zgodnie z którymi wszyscy ci pacjenci pozostawali
w fazie remisji cytogenetycznej (zakres 32-38 miesięcy). W tej samej publikacji opisywano dane
z długoterminowej obserwacji 12 pacjentów z MDS/MPD i rearanżacjami genu PDGFR (5 pacjentów z badania B2225). Wspomniani pacjenci otrzymywali imatynib średnio przez 47 miesięcy (zakres 24 dni - 60 miesięcy). U 6 z tych pacjentów czas obserwacji w chwili obecnej przekracza 4 lata. U 11 pacjentów całkowita odpowiedź cytogenetyczna (CHR) wystąpiła szybko; u dziesięciu pacjentów anomalie cytogenetyczne ustąpiły całkowicie i obserwowano również zmniejszenie się lub zanik liczby transkryptów fuzyjnych mierzonych za pomocą RT-PCR. Odpowiedź hematologiczna
i cytogenetyczna utrzymywała się odpowiednio przez 49 miesięcy (zakres 19-60) i 47 miesięcy
(zakres 16-59). Całkowite przeżycie od chwili postawienia rozpoznania wynosi 65 miesięcy od chwili postawienia rozpoznania (zakres 25-234). Podawanie imatynibu pacjentom bez translokacji genów zazwyczaj nie daje poprawy.
Nie ma kontrolowanych badań z udziałem dzieci i młodzieży z MDS/MPD. W 4 publikacjach opisano 5 pacjentów z MDS/MPD związanych z rearanżacjami genu PDGFR. Wiek tych pacjentów mieścił się w zakresie od 3 miesięcy do 4 lat, a imatynib podawano w dawce wynoszącej 50 mg na dobę lub w dawkach wynoszących od 92,5 do 340 mg/m2 pc. na dobę. U wszystkich pacjentów uzyskano całkowitą odpowiedź hematologiczną, odpowiedź cytogenetyczną i (lub) odpowiedź kliniczną.
Badania kliniczne w HES/CEL
Przeprowadzono jedno otwarte, wieloośrodkowe badanie kliniczne II fazy (badanie B2225), testujące imatynib w różnych populacjach pacjentów z zagrażającymi życiu chorobami związanymi z kinazą białkowo-tyrozynową Abl, Kit lub PDGFR. W badaniu tym 14 pacjentów z HES/CEL otrzymywało imatynib w dawce od 100 mg do 1000 mg na dobę. Kolejnych 162 pacjentów z HES/CEL opisywanych w 35 opublikowanych opisach przypadków i seriach przypadków otrzymywało imatynib w dawce od 75 do 800 mg na dobę. Anomalie cytogenetyczne oceniano u 117 ze wszystkich 176 pacjentów. U 61 z tych 117 pacjentów zidentyfikowano kinazę fuzyjną FIP1L1-PDGFRα. W trzech innych publikacjach opisano dodatkowo czterech pacjentów z HES i dodatnim wynikiem na obecność kinazy fuzyjnej FIP1L1-PDGFRα. U wszystkich 65 pacjentów z obecnością kinazy fuzyjnej FIP1L1- PDGFRα uzyskano całkowitą odpowiedź hematologiczną utrzymującą się przez wiele miesięcy (zakres od 1+ do 44+ miesięcy do czasu publikacji). Jak donoszono w ostatnio opublikowanej pracy, 21 ze wspomnianych 65 pacjentów również uzyskało całkowitą remisję molekularną, przy medianie czasu trwania obserwacji wynoszącej 28 miesięcy (zakres 13-67 miesięcy). Wiek tych pacjentów wahał się od 25 do 72 lat. Ponadto, w kartach obserwacji klinicznej badacze donosili o poprawie
w zakresie objawów i innych zaburzeń funkcji narządów. Poprawa dotyczyła serca, układu nerwowego, skóry/tkanki podskórnej, układu oddechowego/klatki piersiowej/śródpiersia, układu mięśniowo-szkieletowego/tkanki łącznej/naczyń oraz przewodu pokarmowego.
Nie ma kontrolowanych badań z udziałem dzieci i młodzieży z HES/CEL. W 3 publikacjach opisano 3 pacjentów z HES/CEL i rearanżacjami genu PDGFR. Wiek tych pacjentów mieścił się w zakresie od 2 do 16 lat, a imatynib podawano w dawce wynoszącej 300 mg/m2 pc. na dobę lub w dawkach wynoszących od 200 do 400 mg na dobę. U wszystkich pacjentów uzyskano całkowitą odpowiedź hematologiczną, całkowitą odpowiedź cytogenetyczną i (lub) całkowitą odpowiedź molekularną.
Badania kliniczne z nieoperacyjnymi i (lub) z przerzutami GIST
Przeprowadzono jedno, międzynarodowe, randomizowane, niekontrolowane, otwarte badanie drugiej fazy z udziałem pacjentów ze złośliwymi, nieoperacyjnymi lub przerzutowymi nowotworami podścieliskowymi przewodu pokarmowego (GIST). Do badania włączono i randomizowano 147 pacjentów, którzy otrzymywali doustnie 400 lub 600 mg imatynibu jeden raz na dobę przez okres do 36 miesięcy. Pacjenci byli w wieku od 18 do 83 lat z rozpoznaną Kit pozytywną, złośliwą, nieoperacyjną i (lub) z przerzutami postacią GIST. Przeprowadzono rutynowe badanie immunohistochemiczne z przeciwciałem Kit (A-4502, królicza poliklonalna surowica odpornościowa, 1:100; DAKO Corporation, Carpinteria, CA) zgodnie z analizą prowadzoną złożoną metodą awidynabiotyna-peroksydaza po odzyskaniu antygenu.
Pierwszorzędowe kryterium skuteczności ustalono na podstawie obiektywnego odsetka odpowiedzi. Guzy musiały być mierzalne przynajmniej w jednym ognisku choroby, a charakterystyka odpowiedzi opierała się na kryteriach SWOG (ang. Southwestern Oncology Group). Wyniki przedstawiono w Tabeli 6.
Tabela 6 Najlepsza odpowiedź na leczenie w badaniu STIB2222 (GIST)
Wszystkie dawki (n=147) 400 mg (n=73)
600 mg (n=74)
Najlepsza odpowiedź | n (%) |
Odpowiedź całkowita | 1(0,7) |
Odpowiedź częściowa | 98 (66,7) |
Stabilizacja choroby | 23 (15,6) |
Progresja choroby | 18 (12,2) |
Nieocenialne | 5 (3,4) |
Nieznane | 2 (1,4) |
Nie było różnicy w stopniu odpowiedzi między obu grupami. Znaczna liczba pacjentów ze stabilizacją choroby w czasie analizy tymczasowej uzyskała częściową odpowiedź w wyniku dłuższego leczenia (mediana czasu obserwacji 31 miesięcy). Mediana czasu do uzyskania odpowiedzi wynosiła 13 tygodni (95% CI 12–23). Mediana czasu do niepowodzenia leczenia u osób z odpowiedzią wynosiła 122 tygodnie (95% CI, 106–147), natomiast w całej populacji badania, były to 84 tygodnie (95% CI 71–109). Nie uzyskano mediany całkowitego przeżycia. Wynik analizy przeżywalności przeprowadzonej metodą Kaplana-Meiera dla przeżycia po 36 miesiącach obserwacji wynosi 68%.
W dwóch badaniach klinicznych (badanie B2222 i badanie międzygrupowe S0033) dobową dawkę imatynibu zwiększono do 800 mg u pacjentów z progresją po najmniejszych dawkach dobowych w wysokości 400 mg lub 600 mg. Dawkę dobową zwiększono do 800 mg u 103 pacjentów; u 6 pacjentów uzyskano odpowiedź częściową, a u 21 pacjentów – stabilizację choroby po zwiększeniu dawki, w sumie uzyskano poprawę kliniczną u 26%. Jak wynika z dostępnych danych o bezpieczeństwie, zwiększenie dawki do 800 mg na dobę u pacjentów z progresją po najmniejszych dawkach leku w wysokości 400 mg i 600 mg na dobę wydaje się nie mieć wpływu na profil bezpieczeństwa imatynibu.
Badania kliniczne z leczeniem adjuwantowym w GIST
W leczeniu adjuwantowym stosowanie imatynibu badano w wieloośrodkowym, podwójnie zaślepionym, długoterminowym badaniu III fazy z grupą kontrolną otrzymującą placebo (Z9001) z udziałem 773 pacjentów. Wiek pacjentów wahał się od 18 do 91 lat. Do badania włączono pacjentów z histologicznym rozpoznaniem pierwotnego GIST z ekspresją białka Kit w badaniu immunochemicznym oraz guzem wielkości ≥ 3 cm w największym wymiarze, z całkowitą resekcją pierwotnego GIST w okresie 14-70 dni przed rejestracją. Po resekcji pierwotnego guza GIST pacjentów zrandomizowano do jednego z dwóch ramion badania: z imatynibem w dawce 400 mg/dobę lub odpowiadającym mu placebo. Leczenie było prowadzone przez rok.
Pierwszorzędowym punktem końcowym był czas przeżycia wolnego od nawrotu (ang. recurrence-free survival - RFS), określany jako czas od daty randomizacji do daty wystąpienia nawrotu choroby lub zgonu z jakiejkolwiek przyczyny.
Imatynib znamiennie wydłużał RFS. W grupie pacjentów otrzymujących imatynib 75% było wolnych od nawrotu po 38 miesiącach w porównaniu z 20 miesiącami w grupie otrzymującej placebo (95% CI odpowiednio [30 – nie do oceny]); [14 – nie do oceny]); (współczynnik ryzyka = 0,398 [0,259-0,610], p<0,0001). Po jednym roku całkowity wskaźnik RFS był znamiennie lepszy dla grupy otrzymującej imatynib (97,7%) w porównaniu z grupą otrzymującą placebo (82,3%), (p<0,0001). Ryzyko wznowy w porównaniu z grupą otrzymującą placebo było zatem zmniejszone o około 89% (współczynnik ryzyka = 0,113 [0,049-0,264]).
Ryzyko nawrotu u pacjentów po operacji pierwotnego nowotworu GIST było oceniane retrospektywnie na podstawie następujących czynników prognostycznych: wielkość guza, indeks mitotyczny, umiejscowienie guza pierwotnego. Dane dotyczące indeksu mitotycznego uzyskano od 556 z 713 pacjentów z populacji ITT. W Tabeli 7 przedstawiono wyniki analizy podgrup pacjentów zgodnie z klasyfikacją ryzyka wg Narodowego Instytutu Zdrowia Stanów Zjednoczonych (NIH) oraz
Instytutu Patologii Sił Zbrojnych (AFIP). Nie zaobserwowano korzyści w grupach małego i bardzo małego ryzyka. Nie obserwowano poprawy przeżycia całkowitego.
Tabela 7 Wyniki analizy RFS badania Z9001 w klasyfikacji ryzyka wg NIH i AFIP
Kryterium ryzyka | Poziom ryzyka | % pacjentów | Liczba zdarzeń / Liczba pacjentów | Całkowity wspólczynnik ryzyka (95%CI)* | Wskaźnik | RFS (%) |
12 miesiąc | 24 miesiąc | |||||
imatynib vs placebo | imatynib vs placebo | imatynib vs placebo | ||||
NIH | Małe | 29,5 | 0/86 vs. 2/90 | N.E. | 100 vs. | 100 vs. |
98,7 | 95,5 | |||||
Średnie | 25,7 | 4/75 vs. 6/78 | 0,59 (0,17; | 100 vs. | 97,8 vs. | |
2,10) | 94,8 | 89,5 | ||||
Duże | 44,8 | 21/140 vs. | 0,29 (0,18; | 94,8 vs. | 80,7 vs. | |
51/127 | 0,49) | 64,0 | 46,6 | |||
AFIP | Bardzo małe | 20,7 | 0/52 vs. 2/63 | N.E. | 100 vs. | 100 vs. 93. |
98,1 | ||||||
Małe | 25,0 | 2/70 vs. 0/69 | N.E. | 100 vs. | 97,8 vs. 10 | |
100 | ||||||
Umiarkowane | 24,6 | 2/70 vs. | 0,16 (0,03; | 97,9 vs. | 97,9 vs. | |
11/67 | 0,70) | 90,8 | 73,3 | |||
Duże | 29,7 | 16/84 vs. | 0,27 (0,15; | 98,7 vs. | 79,9 vs. | |
39/81 | 0,48) | 56,1 | 41,5 |
* Cały okres obserwacji (follow-up); NE – niemożliwe do oceny
Drugie, wieloośrodkowe otwarte badanie III fazy (SSG XVIII/AIO), w którym porównano 12- miesięczne leczenie imatynibem w dawce 400 mg na dobę z 36-miesięcznym leczeniem u pacjentów po chirurgicznej resekcji GIST (nowotwór podścieliskowy przewodu pokarmowego), spełniających jeden z wymienionych warunków: średnica guza > 5 cm i indeks mitotyczny > 5/50 pól widzenia w dużym powiększeniu; lub średnica guza > 10 cm i każda wartość wskaźnika mitotycznego lub każdy wymiar guza z odsetkiem mitoz > 10/50 pól widzenia w dużym powiększeniu lub guzy, które ulegają pęknięciu do jamy otrzewnej. Łącznie 397 pacjentów wyraziło zgodę na udział w badaniu i zostali oni randomizowani do grup badawczych (199 pacjentów do grupy leczonej przez 12 miesięcy i 198 pacjentów do grupy leczonej przez 36 miesięcy). Mediana wieku wyniosła 61 lat (zakres 22-84 lata). Mediana okresu obserwacji pacjentów wyniosła 54 miesiące (od daty randomizacji do momentu zakończenia zbierania danych). Od randomizacji pierwszego pacjenta do daty zakończenia upłynęły 83 miesiące.
Pierwszorzędowym punktem końcowym badania był czas przeżycia bez nawrotu (RFS) określany, jako okres od randomizacji do daty nawrotu lub śmierci z jakiegokolwiek powodu.
Leczenie imatynibem przez 36 miesięcy znacząco wydłużało czas przeżycia bez nawrotu w porównaniu z 12-miesięczną terapią imatynibem (całościowy współczynnik ryzyka (HR) = 0,46 [0,32; 0,65], p<0,0001) (Tabela 8, Rysunek 1).
Ponadto, 36-miesięczne leczenie imatynibem znacząco wydłużało całkowity czas przeżycia w porównaniu z 12-miesięcznym leczeniem imatynibem (HR = 0,45 [0,22; 0,89],
p=0,0187) (Tabela 8, Rysunek 2).
Dłuższe leczenie (> 36 miesięcy) może opóźnić wystąpienie kolejnych nawrotów; jednak wpływ tego wyniku na całkowite przeżycie pacjentów pozostaje nieznany.
Całkowita liczba zgonów wyniosła 25 w grupie leczonej przez 12 miesięcy i 12 w grupie leczonej przez 36 miesięcy.
Analiza populacji ITT, tzn. całej populacji badania wykazała, że leczenie imatynibem przez 36 miesięcy było lepsze od leczenia trwającego 12 miesięcy. W planowanej analizie podgrup wyodrębnionych na podstawie typu mutacji, HR dla RFS w przypadku leczenia trwającego 36 miesięcy u pacjentów z mutacją w eksonie 11 wyniósł 0,35 [95% CI: 0,22; 0,56]. Z uwagi na małą liczbę obserwowanych zdarzeń nie można wyciągnąć wniosków dla podgrup z innymi, rzadszymi mutacjami.
Tabela 8 12-miesięczne i 36-miesięczne leczenie imatynibem (Badanie SSGXVIII/AIO)
12-miesięczne leczenie | 36- miesięczne leczenie | |
RFS | %(przedział ufności) | %(przedział ufności) |
12 miesięcy | 93,7 (89,2-96,4) | 95,9 (91,9-97,9) |
24 miesięcy | 75,4 (68,6-81,0) | 90,7 (85,6-94,0) |
36 miesięcy | 60,1 (52,5-66,9) | 86,6 (80,8-90,8) |
48 miesięcy | 52,3 (44,0-59,8) | 78,3 (70,8-84.1) |
60 miesięcy | 47,9 (39,0-56,3) | 65,6 (56,1-73,4) |
Przeżycie | ||
36 miesięcy | 94,0 (89,5-96,7) | 96,3 (92,4-98,2) |
48 miesięcy | 87,9 (81,1-92,3) | 95,6 (91,2-97,8) |
60 miesięcy | 81,7 (73,0-87,8) | 92,0 (85,3-95,7) |
Rysunek 1 Estymator Kaplana-Meiera dla pierwszorzędowego punktu końcowego – czasu przeżycia bez nawrotu (populacja ITT)
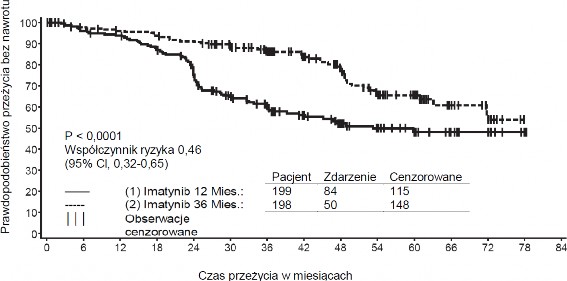
Z ryzykiem zdarzeń
(1) | 199:0 | 182:8 | 177:12 | 163:25 | 137:46 | 105:65 | 88:72 | 61:77 | 49:81 | 36:83 | 27:84 | 14:84 | 10:84 | 2:84 | 0:84 |
(2) | 198:0 | 189:5 | 184:8 | 181:11 | 173:18 | 152:22 | 133:25 | 102:29 | 82:35 | 54:46 | 39:47 | 21:49 | 8:50 | 0:50 |
Rysunek 2 Estymator Kaplana-Meiera dla całkowitego czasu przeżycia (populacja ITT)
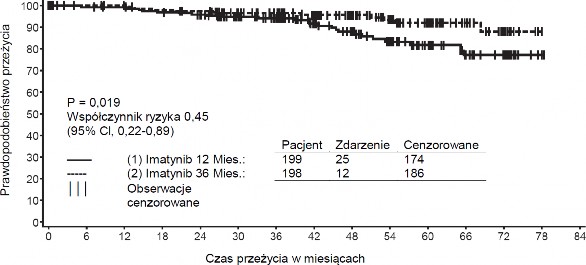
Z ryzykiem zdarzeń
(1) | 199:0 | 190:2 | 188:2 | 183:6 | 176:8 | 156:10 | 140:11 | 105:14 | 87:18 | 64:22 | 46:23 | 27:25 | 20:25 | 2:25 | 0:25 |
2) | 198:0 | 196:0 | 192:0 | 187:4 | 184:5 | 164:7 | 152:7 | 119:8 | 100:8 | 76:10 | 56:11 | 31:11 | 13:12 | 0:12 |
Nie ma kontrolowanych badań z udziałem dzieci i młodzieży z c-Kit dodatnim GIST. W 7 publikacjach opisano przypadki 17 pacjentów z GIST (z lub bez obecności Kit oraz mutacjami PDGFR). Wiek tych pacjentów wahał się od 8 do 18 lat, a imatynib podawano zarówno w leczeniu adjuwantowym, jak i w leczeniu przerzutów w dawkach wynoszących od 300 do 800 mg na dobę. U większości dzieci i młodzieży leczonych z powodu GIST brak jest danych potwierdzających występowanie c-kit lub mutacji PDGFR, co mogłoby prowadzić do mieszanych rezultatów klinicznych.
Badania kliniczne w DFSP
Przeprowadzono jedno otwarte, wieloośrodkowe badanie kliniczne II fazy (badanie B2225)
z udziałem 12 pacjentów z DFSP leczonych imatynibem w dawce 800 mg na dobę. Wiek pacjentów z DFSP wahał się od 23 do 75 lat. Byli to pacjenci z DFSP z przerzutami i miejscową wznową po wstępnej resekcji, którzy w chwili włączenia do badania zostali uznani jako nie kwalifikujący się do ponownej resekcji. Wstępne dowody skuteczności leku uzyskano na podstawie obiektywnych wskaźników odpowiedzi. Spośród 12 pacjentów włączonych do badania, u 9 uzyskano całkowitą
odpowiedź, a u 8 - odpowiedź częściową. Trzech spośród pacjentów z odpowiedzią częściową zostało następnie wyleczonych za pomocą zabiegu chirurgicznego. Mediana czasu trwania leczenia w badaniu B2225 wynosiła 6,2 miesięcy, maksymalnie 24,3 miesiące. Kolejnych 6 pacjentów z DFSP leczonych imatynibem, w wieku od 18 miesięcy do 49 lat opisano w 5 opublikowanych opisach przypadków.
Dorosłych pacjentów opisywanych w literaturze leczono dawką 400 mg (4 przypadki) lub 800 mg (1 przypadek) imatynibu na dobę. Dziecko otrzymywało dawkę 400 mg/m2 pc. na dobę, zwiększoną następnie do 520 mg/m2 pc. na dobę. U pięciu (5) pacjentów uzyskano odpowiedź: u 3 - całkowitą, a u 2 - częściową. Mediana czasu trwania leczenia opisywanego w literaturze wahała się od 4 tygodni do ponad 20 miesięcy. Translokacja (17:22)[(q22:q13)] lub jej produkt genowy były obecne u prawie wszystkich pacjentów odpowiadających na leczenie imatynibem.
Nie ma kontrolowanych badań z udziałem dzieci i młodzieży z DFSP. W 3 publikacjach opisano 5 pacjentów z DFSP i rearanżacjami genu PDGFR. Byli to pacjenci w wieku od noworodka do 14 lat,
a imatynib podawano w dawce 50 mg na dobę lub w dawkach wynoszących od 400 do 520 mg/m2 pc. na dobę. U wszystkich pacjentów uzyskano częściową i (lub) całkowitą odpowiedź.
Farmakokinetyka imatynibu
Właściwości farmakokinetyczne imatynibu oszacowano w zakresie dawek od 25 do 1000 mg. Profile farmakokinetyczne w osoczu analizowano po 1 dniu oraz po 7 lub 28 dniach, kiedy stężenie imatynibu w osoczu osiągnęło stan stacjonarny.
Wchłanianie
Średnia bezwzględna dostępność biologiczna imatynibu wynosi 98%. Po podaniu doustnym stwierdzono dużą międzyosobniczą zmienność wartości AUC imatynibu w osoczu pacjentów.
W przypadku podania leku z wysokotłuszczowym posiłkiem, stopień wchłaniania imatynibu był minimalnie zmniejszony (11% obniżenie Cmax i wydłużenie tmax o 1,5 h), z niewielkim zmniejszeniem AUC (7,4%) w porównaniu do pacjentów przyjmujących lek na czczo. Nie badano wpływu uprzedniej operacji w obrębie przewodu pokarmowego na wchłanianie imatynibu.
Dystrybucja
W badaniach in vitro, z zastosowaniem stężeń imatynibu o znaczeniu klinicznym, 95% imatynibu wiązało się z białkami osocza, przede wszystkim z albuminą i kwaśną alfa-glikoproteiną oraz
w niewielkim stopniu z lipoproteiną.
Metabolizm
Głównym metabolitem imatynibu we krwi człowieka jest pochodna N-demetylowa piperazyny, która in vitro charakteryzuje się podobną siłą działania jak związek macierzysty. AUC metabolitu w osoczu wynosiło zaledwie 16% wartości AUC imatynibu. Wiązanie N-demetylowanego metabolitu
z białkami osocza jest podobne jak w przypadku związku macierzystego.
Imatinib i jego N-demetylowy metabolit stanowią łącznie około 65% radioaktywności we krwi (AUC(0-48h)). Pozostała część radioaktywności we krwi była związana z obecnymi w mniejszej ilości metabolitami.
Badania in vitro wykazały, że CYP3A4 jest głównym enzymem z grupy ludzkiego cytochromu P450 biorącym udział w biotransformacji imatynibu. Z leków, które mogą być stosowane jednocześnie
z imatynibem (acetaminofen, acyklowir, allopurynol, amfoterycyna, cytarabina, erytromycyna, flukonazol, hydroksymocznik, norfloksacyna, penicylina V) tylko erytromycyna (IC50=50 μM)
i flukonazol (IC50=118 μM) hamowały metabolizm imatynibu w stopniu, który może mieć kliniczne znaczenie.
W badaniach in vitro z zastosowaniem standardowych substratów CYP2C9, CYP2D6 i CYP3A4/5 wykazano, że imatynib jest inhibitorem konkurencyjnym wobec tych izoenzymów. Wartości Ki
w mikrosomach izolowanych z ludzkiej wątroby wynosiły odpowiednio 27; 7,5 i 7,9 μmol/l. Maksymalne stężenie imatynibu w osoczu pacjentów wynosi 2-4 μmol/l. Dlatego możliwe jest zahamowanie metabolizmu leków podawanych jednocześnie z imatynibem i metabolizowanych przez CYP2D6 lub CYP3A4/5. Imatynib nie wpływa na biotransformację 5-fluorouracylu, ale w wyniku hamowania konkurencyjnego CYP2C8 (Ki = 34,7 μM) hamuje metabolizm paklitakselu. Ta wartość Ki jest dużo większa niż oczekiwane stężenie imatynibu w osoczu pacjentów i dlatego nie należy spodziewać się interakcji po równoczesnym podaniu 5-fluorouracylu lub paklitakselu z imatynibem.
Eliminacja
W oparciu o wykrywanie związku(ów) po doustnym podaniu znakowanego 14C-imatynibu stwierdzono, że około 81% dawki wykrywane jest w ciągu 7 dni w kale (68%) i moczu (13%). 25% dawki imatynibu jest wydalane w postaci niezmienionej (5% z moczem, 20% z kałem), pozostałą część stanowią metabolity.
Właściwości farmakokinetyczne w osoczu
Po doustnym podaniu leku zdrowym ochotnikom, okres półtrwania (t½) wynosił około 18 godzin, co wskazywałoby, że podawanie leku raz na dobę jest właściwe. Po podaniu doustnym imatynibu obserwowano liniowe proporcjonalne do dawki zwiększenie średnich wartości AUC zgodnie ze wzrastającymi dawkami leku w zakresie od 25 mg do 1000 mg. Nie odnotowano zmian farmakokinetyki imatynibu po wielokrotnym podawaniu, a kumulacja leku w organizmie była 1,5-2,5- krotnie większa w stanie równowagi, kiedy lek podawano raz na dobę.
Właściwości farmakokinetyczne u pacjentów z GIST
U pacjentów z GIST ekspozycja w stanie równowagi po podaniu tych samych dawek (400 mg na dobę) była 1,5-raza większa niż obserwowana u pacjentów z CML. Na podstawie wstępnej oceny właściwości farmakokinetycznych w populacji pacjentów z GIST znaleziono trzy wskaźniki (albuminy, krwinki białe i bilirubina), które miały statystycznie istotny wpływ na farmakokinetykę imatynibu. Zmniejszone stężenie albumin spowodowało zmniejszenie klirensu (CL/f); zwiększona liczba krwinek białych prowadzi do zmniejszenia CL/f. Jednakże zależności te nie są wystarczająco wyrażone, aby stanowiły podstawę do zmiany dawkowania. W tej populacji pacjentów, występowanie przerzutów nowotworowych w wątrobie może potencjalnie prowadzić do niewydolności wątroby i zmniejszyć metabolizm.
Farmakokinetyka populacyjna
W oparciu o analizę farmakokinetyki w populacji pacjentów z CML stwierdzono, że wiek pacjentów miał niewielki wpływ na objętość dystrybucji (12% zwiększenie u pacjentów >65 lat). Zmiana ta nie ma znaczenia klinicznego. Wpływ masy ciała na klirens imatynibu jest następujący: u pacjentów
o masie ciała 50 kg, średni klirens będzie wynosił 8,5 l/h, podczas gdy u pacjentów o masie ciała 100 kg - klirens zwiększy się do 11,8 l/h. Uważa się, że zmiany te nie wymagają dostosowania dawki
w zależności od masy ciała pacjenta. Płeć pacjentów nie ma wpływu na właściwości farmakokinetyczne imatynibu.
Farmakokinetyka u dzieci i młodzieży
Tak jak u dorosłych pacjentów, imatynib był szybko wchłaniany po podaniu doustnym dzieciom i młodzieży biorącym udział zarówno w badaniu I jak i II fazy. Dawki w zakresie od 260 do 340
mg/m2 pc. spowodowały taką samą ekspozycję jak odpowiednio dawki 400 mg i 600 mg u dorosłych pacjentów. Porównanie AUC(0-24) w 8. i 1. dniu podawania dawki 340 mg/m2 pc. wykazało 1,7-krotną kumulację po wielokrotnym podaniu raz na dobę.
W oparciu o zbiorczą analizę farmakokinetyki w populacji dzieci i młodzieży z zaburzeniami hematologicznymi (CML, Ph+ ALL lub innymi zaburzeniami hematologicznymi leczonymi imatynibem) stwierdzono, że klirens imatynibu zwiększa się wraz ze zwiększeniem powierzchni ciała (pc.). Po dokonaniu korekty względem pc. inne parametry demograficzne takie, jak wiek, masa ciała i wskaźnik masy ciała nie miały klinicznie istotnego wpływu na ekspozycję na imatynib. Analiza
potwierdziła, że ekspozycja na imatynib u dzieci i młodzieży otrzymujących dawkę 260 mg/m2 pc. raz na dobę (nie więcej niż 400 mg raz na dobę) lub 340 mg/m2 pc. raz na dobę (nie więcej niż 600 mg raz na dobę) była podobna do ekspozycji u pacjentów dorosłych, którzy otrzymywali imatynib w dawce 400 mg lub 600 mg raz na dobę.
Zaburzenia czynności narządów
Imatynib i jego metabolity nie są w znaczącym stopniu wydalane przez nerki. Pacjenci z łagodnymi i umiarkowanymi zaburzeniami czynności nerek wykazują większą całkowitą ekspozycję na lek
zawarty w osoczu niż pacjenci z prawidłową czynnością nerek. Jest to zwiększenie średnio 1,5- do 2- krotne, co związane jest z 1,5-krotnym zwiększeniem w osoczu stężenia AGP, białka, z którym silnie wiąże się imatynib. Ponieważ imatynib jest tylko w nieznacznym stopniu wydalany przez nerki, klirens wolnego leku u pacjentów z zaburzeniami czynności nerek jest prawdopodobnie zbliżony do takiego, jak u pacjentów z prawidłową czynnością nerek (patrz punkty 4.2 i 4.4).
Mimo, iż wyniki analizy farmakokinetycznej wykazały istnienie znacznych różnic międzyosobniczych, średnia ekspozycja na imatynib nie wzrosła u pacjentów z różnym stopniem zaburzeń czynności wątroby w porównaniu z pacjentami z prawidłową czynnością tego narządu (patrz punkty 4.2, 4.4 i 4.8).
W badaniach przedklinicznych profil bezpieczeństwa imatynibu oceniano u szczurów, psów, małp i królików.
W badaniach toksyczności u szczurów, psów i małp po podaniu wielokrotnym stwierdzono zmiany hematologiczne o nasileniu łagodnym do umiarkowanego. U szczurów i psów towarzyszyły im zmiany w szpiku.
U szczurów i psów narządem docelowym była wątroba. U obu gatunków stwierdzono łagodne do umiarkowanego zwiększenie aktywności aminotransferaz i nieznaczne zmniejszenie stężenia cholesterolu, triglicerydów, białka całkowitego i albumin. Nie stwierdzono zmian histopatologicznych w wątrobie szczurów. U psów, którym podawano imatynib przez 2 tygodnie obserwowano ciężkie uszkodzenie wątroby ze zwiększeniem aktywności enzymów wątrobowych, martwicą komórek wątrobowych, martwicą w obrębie przewodów żółciowych i hiperplazją przewodów żółciowych.
U małp, którym podawano imatynib przez 2 tygodnie obserwowano uszkodzenie nerek z ogniskową mineralizacją, rozszerzeniem kanalików nerkowych i zwyrodnieniem kanalików nerkowych. U kilku małp stwierdzono zwiększenie stężenia azotu mocznikowego we krwi (BUN) i kreatyniny.
U szczurów, po podaniu dawki ≥6 mg/kg przez 13 tygodni, obserwowano rozrost przejściowego nabłonka brodawek nerkowych i pęcherza moczowego, bez zmian wskaźników w surowicy i moczu. W czasie długotrwałego podawania imatynibu stwierdzono zwiększenie częstości zakażeń oportunistycznych.
W 39-tygodniowym badaniu na małpach, dawkę NOAEL (ang. No Observed Adverse Effect Level, czyli stężenie przy którym nie obserwowano działań niepożądanych) ustalono na poziomie najmniejszej dawki leku 15 mg/kg, co stanowi około 1/3 maksymalnej dawki u ludzi (800 mg)
w przeliczeniu na powierzchnię ciała. Podawanie imatynibu powodowało pogorszenie normalnie zahamowanego przewlekłego zakażenia malarią u tych zwierząt.
Imatynib nie miał działania genotoksycznego w badaniach in vitro z zastosowaniem komórek bakteryjnych (test Amesa), w badaniu in vitro z zastosowaniem komórek ssaków (chłoniaka mysiego) i in vivo w mikrojądrowym teście u szczurów. Dodatnie działanie genotoksyczne imatynibu uzyskano
w badaniu in vitro komórek ssaków (komórki jajnika chomika chińskiego) wykrywającym działanie klastogenne (aberracje chromosomowe) w czasie aktywności metabolicznej. Dwa z 27 produktów pośrednich procesu wytwarzania, obecnych w produkcie końcowym, miały działanie mutagenne w teście Amesa. Jeden z nich miał również działanie mutagenne w teście z zastosowaniem komórek chłoniaka mysiego.
W badaniach wpływu na płodność, u samców szczurów otrzymujących 60 mg/kg imatynibu przez 70 dni przed kojarzeniem, masa jąder i najądrzy oraz procent ruchliwych plemników były zmniejszone. Dawka ta jest zbliżona do maksymalnej zalecanej dawki klinicznej (800 mg/dobę) w przeliczeniu na powierzchnię ciała. Podobnego działania nie obserwowano w dawkach ≤20 mg/kg. Nieznaczne do umiarkowanego zmniejszenie spermatogenezy obserwowano u psów po podaniu dawek doustnych
≥30 mg/kg. Nie stwierdzono wpływu na przebieg kojarzenia i liczbę ciężarnych samic szczurów
w grupie otrzymującej imatynib między 14. dniem przed kojarzeniem do 6. dnia potencjalnej ciąży. Po podaniu dawki 60 mg/kg u samic szczurów stwierdzono istotne zwiększenie poimplantacyjnych utrat płodów i zmniejszenie liczby żywych płodów. Podobnego działania nie obserwowano po dawkach
≤20 mg/kg.
W badaniu przed- i pourodzeniowego rozwoju u szczurów stwierdzono czerwoną wydzielinę
z pochwy w 14. lub 15. dniu ciąży, w grupie otrzymującej doustnie dawkę 45 mg/kg mc./dobę.
Po podaniu tej samej dawki liczba urodzonych martwych młodych oraz tych, które padły między 0. i 4. dniem po porodzie była zwiększona. U młodych pokolenia F1, ta sama dawka spowodowała
zmniejszenie średniej masy ciała od porodu do końca badania, a liczba młodych osiągających stadium odwiedzenia napletka była nieznacznie zmniejszona. Płodność w pokoleniu F1 nie była zmieniona, ale zwiększyła się liczba resorpcji i zmniejszyła liczba żywych płodów po podaniu dawki 45 mg/kg/dobę. Dawka NOEL (brak działań) zarówno dla matek potomstwa, jak i pokolenia F1 wynosiła 15 mg/kg mc./dobę (jedna czwarta maksymalnej dawki stosowanej u ludzi, czyli 800 mg).
Imatynib miał działanie teratogenne u szczurów, gdy był podawany w okresie organogenezy
w dawkach ≥ 100 mg/kg. Dawka ta jest zbliżona do maksymalnej dawki klinicznej (800 mg/dobę)
w przeliczeniu na powierzchnię ciała. Działanie teratogenne dotyczyło: częściowego lub całkowitego braku kości czaszki, przepukliny mózgowej, nieobecności/redukcji kości czołowej i nieobecności kości ciemieniowej. Działania takiego nie obserwowano po dawkach ≤30 mg/kg.
W badaniu toksykologicznym, prowadzonym na młodych rozwijających się szczurach (dzień 10-70 po porodzie), nie wykazano żadnego nowego toksycznego wpływu na narządy docelowe w odniesieniu do znanych narządów docelowych u dorosłych szczurów. W badaniu toksykologicznym na młodych osobnikach obserwowano wpływ na wzrost, opóźnienie otwarcia pochwy i oddzielenia napletka, przy około 0,3 do 2-krotności przeciętnej ekspozycji u dzieci i młodzieży po podaniu największej zalecanej dawki 340 mg/m2 pc. Ponadto u młodych zwierząt (w fazie usamodzielniania się) obserwowano śmiertelność przy około 2-krotności przeciętnej ekspozycji u dzieci i młodzieży po podaniu największej zalecanej dawki 340 mg/m2pc.
W 2-letnim badaniu rakotwórczego działania leku na szczury podawanie imatynibu w dawce 15, 30 i 60 mg/kg/dobę spowodowało statystycznie istotne skrócenie czasu życia samców po dawkach 60 mg/kg/dobę i samic po dawkach ≥30 mg/kg/dobę. Badanie histopatologiczne martwych osobników jako główną przyczynę śmierci lub powód uśmiercenia zwierząt laboratoryjnych wykazało kardiomiopatię (u szczurów obu płci), przewlekłą postępującą chorobę nerek (u samic) oraz
brodawczaka gruczołu napletkowego. Narządami docelowymi dla zmian nowotworowych były nerki, pęcherz moczowy, cewka moczowa, gruczoł napletkowy i łechtaczkowy, jelito cienkie, przytarczyce, nadnercza oraz dno żołądka.
Przypadki brodawczaka/raka gruczołów napletkowych/łechtaczkowych odnotowano po podaniu dawek od 30 mg/kg/dobę, co stanowi odpowiednio około 0,5 lub 0,3-krotność dobowej ekspozycji na lek u ludzi (na podstawie AUC) po podaniu dawki 400 mg/dobę lub 800 mg/dobę, oraz 0,4-krotność dobowej ekspozycji na lek u dzieci (na podstawie AUC) po podaniu dawki 340 mg/m2/dobę. Dawka NOEL (dawka, po której nie ma objawów działań niepożądanych) wynosiła 15 mg/kg/dobę.
Występowanie gruczolaka/raka nerek, brodawczaka pęcherza moczowego i cewki moczowej, gruczolakoraka jelita cienkiego, gruczolaków przytarczyc, łagodnych i złośliwych guzów rdzenia nadnerczy oraz brodawczaków/raków dna żołądka odnotowano po dawce 60 mg/kg/dobę, co stanowiło odpowiednio około 1,7- lub 1- krotność dobowej ekspozycji na lek u ludzi (na podstawie AUC) po podaniu dawki 400 mg/dobę lub 800 mg/dobę oraz 1,2-krotność dobowej ekspozycji na lek u dzieci (na podstawie AUC) po podaniu dawki 340 mg/m2 pc./dobę. Dawka, po której nie ma objawów działań niepożądanych (NOEL) wynosiła 30 mg/kg/dobę.
Mechanizm oraz znaczenie danych z badań rakotwórczości prowadzonych na szczurach dla ludzi nie zostały jeszcze wyjaśnione.
Do zmian nienowotworowych, nie obserwowanych we wcześniejszych badaniach przedklinicznych należały zmiany w układzie sercowo-naczyniowym, w trzustce, w narządach układu wewnątrzwydzielniczego i w zębach. Najważniejsze zmiany to przerost mięśnia sercowego i rozstrzeń jam serca, prowadzące u niektórych zwierząt do objawów niewydolności serca.
Substancja czynna imatynib wykazuje zagrożenie dla środowiska dla organizmów żyjących w materiałach osadowych.
Mannitol (E 421)
Celuloza mikrokrystaliczna Krzemionka koloidalna bezwodna Wapnia krzemian
Celuloza mikrokrystaliczna krzemowana Kwas cytrynowy bezwodny Krospowidon typ A
Magnezu stearynian Sodu stearylofumaran
Nie dotyczy.
3 lata
Przechowywać w oryginalnym odpakowaniu w celu ochrony przed wilgocią i światłem.
100 mg, tabletki do sporządzania zawiesiny doustnej
Blister jednodawkowy z folii OPA/Aluminium/PVC/PET/Aluminium typu „unit dose”, w tekturowym pudełku
Wielkość opakowań: 20 x 1, 30 x 1, 60 x 1, 90 x 1, 120 x 1 i 180 x 1 tabletka do sporządzania zawiesiny doustnej
400 mg, tabletki do sporządzania zawiesiny doustnej
Blister jednodawkowy z folii OPA/Aluminium/PVC/PET/Aluminium typu „unit dose”, w tekturowym
pudełku
Wielkość opakowań: 10 x 1, 30 x 1, 60 x 1 i 90 x 1 tabletka do sporządzania zawiesiny doustnej Nie wszystkie wielkości opakowań muszą znajdować się w obrocie.
Wszelkie niewykorzystane resztki produktu leczniczego lub jego odpady należy usunąć zgodnie z lokalnymi przepisami.
KRKA, d.d. Novo mesto Šmarješka cesta 6
8501 Novo mesto Słowenia
100 mg: pozwolenie nr 24376
400 mg: pozwolenie nr 24377
Data wydania pierwszego pozwolenia na dopuszczenie do obrotu: 14.11.2017 r.
10.11.2022











