Spis treści:
- NAZWA PRODUKTU LECZNICZEGO
- SKŁAD JAKOŚCIOWY I ILOŚCIOWY
- POSTAĆ FARMACEUTYCZNA
- SZCZEGÓŁOWE DANE KLINICZNE
- WŁAŚCIWOŚCI FARMAKOLOGICZNE
- DANE FARMACEUTYCZNE
- PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE
- NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
- DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU I DATA PRZEDŁUŻENIA POZWOLENIA
- DATA ZATWIERDZENIA LUB CZĘŚCIOWEJ ZMIANY TEKSTU CHARAKTERYSTYKI PRODUKTU LECZNICZEGO
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
NAZWA PRODUKTU LECZNICZEGO
SKŁAD JAKOŚCIOWY I ILOŚCIOWY
POSTAĆ FARMACEUTYCZNA
SZCZEGÓŁOWE DANE KLINICZNE
Wskazania do stosowania
w celu zmniejszenia obrzęku błony śluzowej w zapaleniu błony śluzowej nosa oraz we wspomagającym leczeniu uszkodzeń błony śluzowej nosa,
w łagodzeniu objawów naczynioruchowego zapalenia błony śluzowej nosa (rhinitis vasomotorica),
w leczeniu niedrożności przewodów nosowych po przebytej operacji nosa.
Sudafed Xylospray DEX dla dzieci (0,5 mg + 50 mg)/ml jest wskazany do stosowania u dzieci w wieku od 2 do 6 lat.
4.2. Dawkowanie i sposób podawania
Dawkowanie
Dzieci
Zalecana dawka Sudafed Xylospray DEX dla dzieci to jedna dawka aerozolu do każdego otworu nosowego do trzech razy na dobę. Dawkowanie zależy od indywidualnej wrażliwości pacjenta
i odpowiedzi klinicznej.
W celu określenia czasu leczenia u dzieci należy skonsultować się z lekarzem. Nie należy stosować dłużej niż 7 dni. Ponowne stosowanie jest możliwe tylko po kilkudniowej przerwie.
Dzieci powinny stosować produkt leczniczy pod opieką dorosłych. Jeżeli po 3 dniach leczenia nie zauważono poprawy lub zaobserwowano nasilenie objawów, należy ponownie dokonać oceny klinicznej.
Nie przekraczać zalecanej dawki.
Ze względów higienicznych, w celu uniknięcia zakażeń, produkt leczniczy powinien być stosowany tylko przez jedną osobę.
Sudafed Xylospray DEX dla dzieci jest przeciwwskazany u dzieci w wieku poniżej 2 lat (patrz punkt 4.3).
Sposób podawania
Produkt leczniczy jest przeznaczony do stosowania donosowego.
Należy zdjąć nasadkę ochronną z końcówki dozownika.
Przed pierwszym użyciem należy 5-krotnie nacisnąć pompkę, aż do pojawienia się jednolitej mgiełki. Jeśli aerozol nie jest stosowany przez dłuższy okres, przed użyciem należy 2-krotnie nacisnąć pompkę.
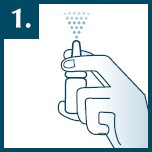
Końcówkę dozownika należy umieścić w otworze nosowym w pozycji zbliżonej do pionowej,
a następnie jednokrotnie nacisnąć pompkę. Podczas podawania należy delikatnie wciągnąć powietrze nosem. Jeśli to konieczne, czynność tę powtórzyć w drugim otworze nosowym.
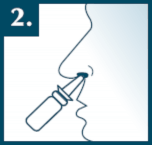
Po każdorazowym użyciu wytrzeć końcówkę dozownika papierową chusteczką i nałożyć nasadkę ochronną.
Przeciwwskazania
Nadwrażliwość na substancje czynne lub na którąkolwiek substancję pomocniczą wymienioną
w punkcie 6.1.
Suche zapalenie błony śluzowej nosa (rhinitis sicca).
Po przezklinowym usunięciu przysadki mózgowej lub innych zabiegach chirurgicznych,
przebiegających z odsłonięciem opony twardej.
Sudafed Xylospray DEX dla dzieci (0,5 mg + 50 mg)/ml jest przeciwwskazany u dzieci w wieku
poniżej 2 lat.
Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania
Sudafed Xylospray DEX dla dzieci, (0,5 mg + 50 mg)/ml, aerozol do nosa, roztwór
Każdy ml roztworu zawiera 0,5 mg ksylometazoliny chlorowodorku i 50 mg deksopantenolu. Jedna dawka aerozolu do nosa (0,1 ml roztworu) zawiera 0,05 mg ksylometazoliny chlorowodorku i 5,0 mg deksopantenolu.
Pełny wykaz substancji pomocniczych, patrz punkt 6.1.
Aerozol do nosa, roztwór.
Przezroczysty, bezbarwny do lekko żółtawego roztwór, wolny od cząstek. pH: 5,5 – 6,4
Osmolalność: 400 - 455 mOsmol/kg
Sudafed Xylospray DEX dla dzieci jest wskazany:
Produkt leczniczy powinien być stosowany tylko po uważnej ocenie korzyści i ryzyka w przypadku:
pacjentów przyjmujących inhibitory monoaminooksydazy (IMAO) i inne leki, które
potencjalnie zwiększają ciśnienie tętnicze krwi,
zwiększonego ciśnienia wewnątrzgałkowego, szczególnie w przypadku jaskry z wąskim kątem przesączania,
ciężkich chorób układu krążenia (np. choroby niedokrwiennej serca, nadciśnienia tętniczego),
guza chromochłonnego,
zaburzeń metabolicznych (np. nadczynności tarczycy, cukrzycy),
porfirii,
rozrostu gruczołu krokowego.
Pacjenci z zespołem długiego odstępu QT leczeni ksylometazoliną mogą być w większym stopniu narażeni na ciężkie arytmie komorowe.
Ze względu na niebezpieczeństwo zaniku błony śluzowej nosa, produkt leczniczy można stosować
w okresie przewlekłego zapalenia błony śluzowej nosa tylko pod nadzorem lekarza.
Długotrwałe stosowanie i stosowanie w dawkach większych niż zalecane leków sympatykomimetycznych może prowadzić do reaktywnego przekrwienia błony śluzowej nosa.
Ten efekt „z odbicia” prowadzi do zwężenia dróg oddechowych, co powoduje, że pacjent wielokrotnie stosuje produkt, aż jego stosowanie staje się ciągłe. Konsekwencją tego jest przewlekły obrzęk błony śluzowej nosa (rhinitis medicamentosa) lub nawet zanik błony śluzowej nosa.
W łagodniejszych przypadkach można rozważyć przerwanie stosowania leku sympatykomimetycznego najpierw w jednym z otworów nosowych, a po ustąpieniu objawów podanie w drugim otworze nosowym w celu utrzymania oddychania w części nosa.
Należy unikać bezpośredniego kontaktu produktu leczniczego z oczami.
Podczas niewłaściwego użycia lub użycia nadmiernej ilości aerozolu, absorpcja ksylometazoliny może powodować układowe działania niepożądane, szczególnie u dzieci (działania niepożądane ze strony układu krążenia i układu nerwowego) (patrz punkty 4.8 i 4.9).
Interakcje z innymi produktami leczniczymi i inne rodzaje interakcji
Ksylometazoliny chlorowodorek
Należy unikać jednoczesnego stosowania Sudafed Xylospray DEX dla dzieci z lekami przeciwnadciśnieniowymi (np. metylodopa) ze względu na możliwy wzrost ciśnienia krwi, będący wynikiem działania ksylometazoliny.
Należy unikać jednoczesnego stosowania Sudafed Xylospray DEX dla dzieci z lekami zwiększającymi ciśnienie krwi (np. doksapram, ergotamina, oksytocyna, inhibitory monoaminooksydazy typu tranylcyprominy lub trójpierścieniowe leki przeciwdepresyjne) ze względu na możliwe nasilenie działania wazopresyjnego.
Jednoczesne stosowanie Sudafed Xylospray DEX dla dzieci z sympatykomimetykami (np. pseudoefedryna, efedryna, fenylefryna, oksymetazolina, ksylometazolina, tramazolina, nafazolina, tuaminoheptan) może prowadzić do działań niepożądanych ze strony układu krążenia
i ośrodkowego układu nerwowego.
Deksopantenol
Nieznane.
Wpływ na płodność, ciążę i laktację
Ciąża
Nie należy stosować produktu leczniczego Sudafed Xylospray DEX dla dzieci w okresie ciąży ze względu na brak wystarczających danych dotyczących stosowania ksylometazoliny chlorowodorku przez kobiety w ciąży.
Karmienie piersią
Nie wiadomo, czy ksylometazoliny chlorowodorek przenika do mleka matki, dlatego nie należy
stosować produktu Sudafed Xylospray DEX dla dzieci u kobiet karmiących piersią.
Płodność
Brak danych dotyczących wpływu produktu leczniczego Sudafed Xylospray DEX dla dzieci na
płodność.
Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn
Sudafed Xylospray DEX dla dzieci stosowany w dawkach zalecanych nie powinien wpływać na
zdolność prowadzenia pojazdów i obsługiwania maszyn.
Działania niepożądane
Częstość występowania działań niepożądanych przedstawiono zgodnie z następującym schematem:
Bardzo często (≥1/10)
- Często (≥1/100 do <1/10)
Niezbyt często (≥1/1 000 do <1/100)
- Rzadko (≥1/10 000 do <1/1 000)
Bardzo rzadko (<1/10 000)
Częstość nieznana (częstość nie może być określona na podstawie dostępnych danych).
Tabelaryczne zestawienie działań niepożądanych
Niezbyt często | Rzadko | Bardzo rzadko | Częstość nieznana | |
Zaburzenia układu immunologicznego | reakcje nadwrażliwości (obrzęk naczynioruchowy, wysypka skórna, świąd) | |||
Zaburzenia psychiczne | niepokój, bezsenność, omamy (głównie u dzieci) | |||
Zaburzenia układu nerwowego | zmęczenie (senność, sedacja), ból głowy, drgawki (głównie u dzieci) | |||
Zaburzenia serca | kołatanie serca, tachykardia, nadciśnienie tętnicze | arytmie |
Zaburzenia układu oddechowego, klatki piersiowej i śródpiersia | obrzęk błony śluzowej „z odbicia”, krwawienia z nosa | kichanie, pieczenie lub suchość błony śluzowej nosa |
Zgłaszanie podejrzewanych działań niepożądanych
Po dopuszczeniu produktu leczniczego do obrotu istotne jest zgłaszanie podejrzewanych działań niepożądanych. Umożliwia to nieprzerwane monitorowanie stosunku korzyści do ryzyka stosowania produktu leczniczego. Osoby należące do fachowego personelu medycznego powinny zgłaszać wszelkie podejrzewane działania niepożądane za pośrednictwem Departamentu Monitorowania Niepożądanych Działań Produktów Leczniczych Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych, Al. Jerozolimskie 181C, 02-222 Warszawa,
tel.: + 48 22 49 21 301, faks: + 48 22 49 21 309, strona internetowa: https://smz.ezdrowie.gov.pl.
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Ksylometazoliny chlorowodorek
Obraz kliniczny zatrucia pochodnymi imidazolu może być zróżnicowany, a fazy pobudzenia mogą przeplatać się z okresami hamowania ośrodkowego układu nerwowego i układu krążenia.
Szczególnie u dzieci przedawkowanie wynika głównie z działania na ośrodkowy układ nerwowy: drgawki i śpiączka, bradykardia, bezdech, nadciśnienie tętnicze oraz niedociśnienie tętnicze.
Objawy pobudzenia ośrodkowego układu nerwowego to niepokój, pobudzenie, omamy i drgawki. Objawy zahamowania ośrodkowego układu nerwowego to obniżenie temperatury ciała, letarg, senność i śpiączka.
Ponadto mogą wystąpić: zwężenie źrenic, rozszerzenie źrenic, obfite pocenie się, gorączka, bladość, sinica, nudności, tachykardia, bradykardia, zaburzenia rytmu serca, zatrzymanie akcji serca, nadciśnienie, niedociśnienie podobne do wstrząsu, obrzęk płuc, zaburzenia oddychania i bezdech.
W przypadku ciężkiego przedawkowania wskazane jest intensywne leczenie szpitalne.
W związku z szybkim wchłanianiem ksylometazoliny należy natychmiast zastosować węgiel (absorbent), siarczan sodu (środek przeczyszczający) lub płukanie żołądka (w przypadku dużych ilości). W celu obniżenia ciśnienia krwi możliwe jest zastosowanie leków blokujących nieselektywne receptory α-adrenergiczne.
Środki wazopresyjne są przeciwwskazane. Jeśli to konieczne, należy podać leki przeciwgorączkowe,
przeciwdrgawkowe oraz tlen.
Deksopantenol
Kwas pantotenowy i jego pochodne, włącznie z deksopantenolem, wykazują bardzo małą toksyczność. W razie przedawkowania nie jest konieczne specjalne postępowanie.
WŁAŚCIWOŚCI FARMAKOLOGICZNE
Właściwości farmakodynamiczne
Właściwości farmakokinetyczne
Grupa farmakoterapeutyczna: leki udrażniające nos i inne produkty do stosowania miejscowego do nosa. Sympatykomimetyki w skojarzeniu z innymi lekami, z wyjątkiem kortykosteroidów,
kod ATC: R01AB06
Produkt leczniczy jest połączeniem α-sympatykomimetyku z analogiem witaminy, stosowanym miejscowo na błonę śluzową nosa. Ksylometazolina ma właściwości obkurczające naczynia krwionośne i tym samym powoduje zmniejszenie przekrwienia zatkanego nosa. Deksopantenol jest
pochodną witaminy kwasu pantotenowego, która przyspiesza gojenie się ran oraz chroni błonę śluzową.
Ksylometazoliny chlorowodorek
Ksylometazoliny chlorowodorek to pochodna imidazolu o działaniu sympatykomimetycznym na receptory α-adrenergiczne. Wykazuje działanie obkurczające naczynia krwionośne, w wyniku czego zmniejsza obrzęk i przekrwienie błony śluzowej. Początek działania zwykle obserwuje się w ciągu 5 do 10 minut, jako łatwiejsze oddychanie przez nos poprzez zmniejszenie obrzęku błony śluzowej i poprawę przepływu wydzieliny.
Deksopantenol
Deksopantenol (alkohol D-(+)-pantotenylowy) jest alkoholowym analogiem kwasu pantotenowego
i z powodu pośredniej transformacji posiada takie samo działanie biologiczne jak kwas pantotenowy. Związane jest to z prawostronną konfiguracją-D. Kwas pantotenowy i jego sole są rozpuszczalnymi w wodzie witaminami, które jako koenzym A zaangażowane są w liczne procesy metaboliczne, takie jak synteza białka i kortykoidów oraz wytwarzanie przeciwciał. Koenzym A uczestniczy również, między innymi, w tworzeniu lipidów, poprzez które tkanka tłuszczowa skóry pełni ważną funkcję ochronną, a także w acetylowaniu aminocukrów, które przyczyniają się do tworzenia różnych mukopolisacharydów.
Deksopantenol ma właściwości chroniące nabłonek i przyspieszające gojenie się ran.
U szczurów z niedoborem deksopantenolu jego zastosowanie na skórę miało wpływ troficzny. Stosowany zewnętrznie deksopantenol i (lub) pantenol może rekompensować zwiększone zapotrzebowanie na kwas pantotenowy przez uszkodzoną skórę lub błonę śluzową.
Ksylometazoliny chlorowodorek
Sporadycznie, podczas donosowego podania ksylometazoliny chlorowodorku, wchłonięta ilość może być wystarczająca do wywołania działania ogólnoustrojowego, np. w obrębie ośrodkowego układu nerwowego i układu krążenia.
Brak danych farmakokinetycznych z badań przeprowadzonych u ludzi.
Deksopantenol
Deksopantenol jest wchłaniany przez skórę i utleniany enzymatycznie w organizmie, także w skórze, do kwasu pantotenowego. W osoczu witamina jest transportowana w postaci związanej z białkami. Kwas pantotenowy jest kluczowym składnikiem koenzymu A, który bierze udział w wielu procesach biochemicznych.
Brak szczegółowych badań dotyczących metabolizmu deksopantenolu w obrębie skóry i błony śluzowej. Od 60% do 70% dawki podanej doustnie jest wydalane z moczem, a 30% do 40% z kałem.
5.3. Przedkliniczne dane o bezpieczeństwie
Dane niekliniczne wynikające z konwencjonalnych badań farmakologicznych dotyczących bezpieczeństwa, badań toksyczności po podaniu wielokrotnym, genotoksyczności, potencjalnego działania rakotwórczego oraz toksycznego wpływu na rozród i rozwój potomstwa nie ujawniają szczególnego zagrożenia dla człowieka.
DANE FARMACEUTYCZNE
Wykaz substancji pomocniczych
Niezgodności farmaceutyczne
Okres ważności
Specjalne środki ostrożności podczas przechowywania
Rodzaj i zawartość opakowania
Specjalne środki ostrożności dotyczące usuwania
Potasu diwodorofosforan
Disodu fosforan dwunastowodny Woda do wstrzykiwań
Nie dotyczy.
3 lata.
Okres ważności po pierwszym otwarciu butelki: 6 miesięcy.
Nie przechowywać w temperaturze powyżej 25ºC.
Warunki przechowywania produktu leczniczego po pierwszym otwarciu, patrz punkt 6.3.
Biała butelka z HDPE o pojemności 10 ml z pompką dozującą z PP/PE/stali, białym dozownikiem
z PP oraz nasadką ochronną z HDPE w tekturowym pudełku.
Wszelkie niewykorzystane resztki produktu leczniczego lub jego odpady należy usunąć zgodnie
z lokalnymi przepisami.
PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE
NA DOPUSZCZENIE DO OBROTU
McNeil Healthcare (Ireland) Limited Airton Road, Tallaght
Dublin 24 Irlandia
NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
Pozwolenie nr 24754
DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU I DATA PRZEDŁUŻENIA POZWOLENIA
Data wydania pierwszego pozwolenia na dopuszczenie do obrotu: 24.05.2018 Data ostatniego przedłużenia pozwolenia:










