Spis treści:
- NAZWA PRODUKTU LECZNICZEGO
- SKŁAD JAKOŚCIOWY I ILOŚCIOWY
- POSTAĆ FARMACEUTYCZNA
- SZCZEGÓŁOWE DANE KLINICZNE
- WŁAŚCIWOŚCI FARMAKOLOGICZNE
- DANE FARMACEUTYCZNE
- PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE
- NUMERY POZWOLEŃ NA DOPUSZCZENIE DO OBROTU
- DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU I
- DATA ZATWIERDZENIA LUB CZĘŚCIOWEJ ZMIANY TEKSTU
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
NAZWA PRODUKTU LECZNICZEGO
SKŁAD JAKOŚCIOWY I ILOŚCIOWY
POSTAĆ FARMACEUTYCZNA
SZCZEGÓŁOWE DANE KLINICZNE
Wskazania do stosowania
Dawkowanie i sposób podawania
Przeciwwskazania
Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania
Interakcje z innymi produktami leczniczymi i inne rodzaje interakcji Badania dotyczące interakcji przeprowadzono wyłącznie u dorosłych. Produkty lecznicze, które mogą zwiększać stężenie sunitynibu w osoczu
Wpływ na płodność, ciążę i laktację
Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn
Działania niepożądane
Zakażenie górnych dróg oddechowych i opryszczkowe zapalenie jamy ustnej
Zapalenie oskrzeli, zapalenie dolnych dróg oddechowych, zapalenie płuc i zapalenie dróg oddechowych
Ropień, ropień w obrębie kończyny, ropień odbytu, ropień dziąsłowy, ropień wątroby, ropień trzustki, ropień krocza, ropień okolic odbytu i odbytnicy, ropień odbytniczy, ropień podskórny i ropień zęba
Kandydoza przełyku i kandydoza jamy ustnej
Zapalenie tkanki łącznej i zakażenie skóry
Posocznica i wstrząs septyczny
Ropień w jamie brzusznej, posocznica z punktem wyjścia w jamie brzusznej, zapalenie uchyłka i zapalenie kości i szpiku
Mikroangiopatia zakrzepowa, zakrzepowa plamica małopłytkowa oraz zespół hemolityczno-mocznicowy i Zmniejszenie łaknienia i jadłowstręt
Dysgeuzja, ageuzja i zaburzenia smaku
Ostry zespół wieńcowy, dławica piersiowa, niestabilna dławica piersiowa, zamknięcie tętnicy wieńcowej oraz niedokrwienie mięśnia sercowego
Zmniejszenie i (lub) nieprawidłowość frakcji wyrzutowej
Zawał mięśnia sercowego w ostrej fazie, zawał mięśnia sercowego oraz bezobjawowy zawał mięśnia
sercowego
Ból jamy ustnej i gardła oraz ból gardła i krtani
o Zapalenie jamy ustnej i afty jamy ustnej
Ból brzucha, ból w podbrzuszu i ból w nadbrzuszu
Perforacja przewodu pokarmowego i perforacja jelita
Zapalenie jelita grubego i niedokrwienne zapalenie jelita grubego
Zapalenie pęcherzyka żółciowego i zapalenie pęcherzyka żółciowego niekamiczne
Zażółcenie skóry, przebarwienia skórne i zaburzenia pigmentacji
Łuszczycopodobne zapalenie skóry, wysypka złuszczająca, wysypka, wysypka rumieniowa, wysypka pęcherzykowa, wysypka uogólniona, wysypka plamista, wysypka plamisto-grudkowa, wysypka grudkowa i swędząca wysypka
Reakcje skórne i zaburzenia skórne
Zaburzenia i odbarwienie płytki paznokciowej
Zmęczenie i astenia
Obrzęk twarzy, obrzęk oraz obrzęk obwodowy
Zwiększona aktywność amylazy
Opis wybranych działań niepożądanych
Zakażenia i zarażenia pasożytnicze
Zgłaszano przypadki ciężkiego zakażenia (z neutropenią lub bez neutropenii), w tym przypadki prowadzące do zgonu. Zgłaszano przypadki nekrotycznego zapalenia powięzi, w tym krocza, czasami prowadzące do zgonu (patrz również punkt 4.4).
Zaburzenia krwi i układu chłonnego
Zmniejszenie bezwzględnej liczby neutrofili 3. i 4. stopnia ciężkości stwierdzono, odpowiednio u 10% i 1,7% pacjentów z GIST w badaniu III fazy, u 16% i 1,6% pacjentów z MRCC w badaniu III fazy i u 13% i 2,4% pacjentów z pNET w badaniu III fazy. Zmniejszenie liczby płytek krwi 3. i 4. stopnia ciężkości obserwowano odpowiednio u 3,7% i 0,4% pacjentów z GIST w badaniu III fazy, u 8,2% i 1,1% pacjentów z MRCC w badaniu III fazy i u 3,7% i 1,2% pacjentów z pNET w badaniu III fazy (patrz punkt 4.4).
W badaniu klinicznym III fazy dotyczącym GIST krwawienia zgłoszono u 18% pacjentów otrzymujących sunitynib i 17% pacjentów otrzymujących placebo. W grupie pacjentów wcześniej nieleczonych z powodu raka nerkowokomórkowego z przerzutami (MRCC) – krwawienia występowały u 39% pacjentów otrzymujących sunitynib i u 11% pacjentów otrzymujących interferon- alfa (IFN-α). Krwawienia stopnia 3. lub wyższego wystąpiły u 17 (4,5%) pacjentów otrzymujących sunitynib i 5 (1,7%) pacjentów otrzymujących IFN-α. W grupie pacjentów otrzymujących sunitynib w leczeniu MRCC opornego na leczenie cytokinami krwawienia wystąpiły u 26%. W badaniu klinicznym III fazy dotyczącym leczenia pNET krwawienia (z wyjątkiem krwawienia z nosa) obserwowano u 21,7% pacjentów otrzymujących sunitynib i u 9,85% pacjentów otrzymujących placebo (patrz punkt 4.4).
W badaniach klinicznych krwotoki z guza nowotworowego występowały u około 2% pacjentów z
GIST.
Zaburzenia układu immunologicznego
Zgłaszano przypadki reakcji nadwrażliwości, w tym przypadki obrzęku naczynioruchowego (patrz
punkt 4.4).
Zaburzenia hormonalne
W 2 badaniach z udziałem pacjentów z rakiem nerkowokomórkowym z przerzutami (MRCC) opornym na leczenie cytokinami, u 7 pacjentów (4%) otrzymujących sunitynib wystąpiła niedoczynność tarczycy jako działanie niepożądane leku. W badaniu z udziałem pacjentów z rakiem nerkowokomórkowym z przerzutami (MRCC) wcześniej nieleczonych, niedoczynność tarczycy wystąpiła u 61 pacjentów (16%) w grupie otrzymującej sunitynib i u 3 pacjentów (<1%) w grupie otrzymującej IFN-α.
Ponadto u 4 pacjentów (2%) z rakiem nerkowokomórkowym z przerzutami (MRCC) opornym na leczenie cytokinami stwierdzono podwyższenie stężenia tyreotropiny (TSH, ang. thyroid-stimulating hormone). Ogółem u 7% pacjentów z rakiem nerkowokomórkowym z przerzutami (ang. MRCC) stwierdzono kliniczne lub laboratoryjne objawy niedoczynności tarczycy rozwijającej się w trakcie leczenia. Nabytą niedoczynność tarczycy stwierdzono u 6,2% pacjentów z GIST otrzymujących sunitynib i u 1% pacjentów otrzymujących placebo. W badaniu III fazy dotyczącym leczenia pNET niedoczynność tarczycy stwierdzono u 6 pacjentów (7,2%) otrzymujących sunitynib i u 1 pacjenta (1,2%) otrzymującego placebo.
Czynność tarczycy monitorowano w 2 prospektywnych badaniach z udziałem pacjentek z nowotworem piersi. Sunitynib nie jest dopuszczony do stosowania w leczeniu nowotworów piersi. W pierwszym ze wspomnianych badań niedoczynność tarczycy zgłoszono u 15 (13,6%) pacjentek otrzymujących sunitynib oraz u 3 (2,9%) pacjentek poddanych standardowym schematom leczenia. Podwyższone stężenie TSH we krwi wystąpiło u 1 (0,9%) pacjentki otrzymującej sunitynib, a w grupie pacjentek poddanych standardowym schematom leczenia nie wystąpiło u żadnej z nich.
Nadczynność tarczycy nie wystąpiła u żadnej z pacjentek otrzymujących sunitynib, wystąpiła natomiast u 1 (1,0%) pacjentki poddanej standardowemu schematowi leczenia. W drugim ze wspomnianych badań niedoczynność tarczycy wystąpiła łącznie u 31 (13%) pacjentek otrzymujących sunitynib oraz u 2 (0,8%) pacjentek otrzymujących kapecytabinę. Podwyższone stężenie TSH we krwi wystąpiło u 12 (5,0%) pacjentek otrzymujących sunitynib, a w grupie pacjentek otrzymujących kapecytabinę nie wystąpiło u żadnej z nich. Nadczynność tarczycy wystąpiła u 4 (1,7%) pacjentek otrzymujących sunitynib, a w grupie pacjentek otrzymujących kapecytabinę nie wystąpiła u żadnej z nich. Obniżone stężenie TSH we krwi wystąpiło u 3 (1,3%) pacjentek otrzymujących sunitynib, a w grupie pacjentek otrzymujących kapecytabinę nie wystąpiło u żadnej z nich. Podwyższone stężenie T4 we krwi wystąpiło u 2 (0,8%) pacjentek otrzymujących sunitynib oraz u 1 (0,4%) pacjentki otrzymującej kapecytabinę. Podwyższone stężenie T3 we krwi wystąpiło u 1 (0,8%) pacjentki otrzymującej sunitynib, natomiast w grupie pacjentek otrzymujących kapecytabinę nie wystąpiło u żadnej z nich. Wszystkie zgłoszone zdarzenia związane z czynnością tarczycy były 1. lub 2. stopnia ciężkości (patrz punkt 4.4).
Zaburzenia metabolizmu i odżywiania
Częstsze przypadki zdarzeń hipoglikemicznych zgłoszono u pacjentów z pNET w porównaniu z pacjentami z MRCC i GIST. Jednak większość działań niepożądanych obserwowanych w badaniach klinicznych nie została uznana za powiązane z leczeniem zastosowanym w badaniu (patrz punkt 4.4).
Zaburzenia układu nerwowego
W badaniach klinicznych sunitynibu oraz w ramach nadzoru po wprowadzeniu go do obrotu zgłoszono kilka przypadków (< 1%) wystąpienia drgawek i objawów radiologicznych zespołu odwracalnej tylnej leukoencefalopatii (RPLS); niektóre z nich zakończyły się zgonem. Drgawki obserwowano zarówno u pacjentów z obecnymi, jak i nieobecnymi objawami radiologicznymi przerzutów do mózgu (patrz punkt 4.4).
Zaburzenia serca
W badaniach klinicznych zmniejszenie frakcji wyrzutowej lewej komory (LVEF, ang. left ventricular ejection fraction) o ≥ 20% i poniżej dolnej granicy normy wystąpiło u około 2% pacjentów z GIST leczonych sunitynibem, u 4% pacjentów z rakiem nerkowokomórkowym z przerzutami (MRCC) opornym na leczenie cytokinami i u 2% pacjentów z GIST otrzymujących placebo. Nie wydaje się, aby spadek LVEF był postępujący, gdyż wartości tego parametru często ulegały poprawie w miarę kontynuowania leczenia. W badaniu klinicznym z udziałem pacjentów z rakiem nerkowokomórkowym z przerzutami (MRCC) wcześniej nieleczonym, wartości LVEF poniżej dolnej granicy normy wystąpiły u 27% pacjentów otrzymujących sunitynib i u 15% pacjentów, którzy otrzymywali IFN-α. U dwóch pacjentów (<1%) otrzymujących sunitynib rozpoznano przewlekłą niewydolność serca.
U pacjentów z GIST zdarzenia zakwalifikowane jako „niewydolność serca”, „zastoinowa niewydolność serca” lub „lewokomorowa niewydolność serca” wystąpiły u 1,2% pacjentów leczonych sunitynibem i 1% pacjentów otrzymujących placebo. W badaniu rejestracyjnym III fazy u pacjentów z GIST (N = 312) działania niepożądane ze strony układu krążenia zakończone zgonem wystąpiły u 1% pacjentów w każdej z grup (tj. w grupach otrzymujących sunitynib i placebo). W badaniu II fazy z udziałem pacjentów z rakiem nerkowokomórkowym z przerzutami (MRCC) opornym na leczenie cytokinami u 0,9% pacjentów wystąpił związany z leczeniem zawał mięśnia sercowego zakończony zgonem, natomiast wśród pacjentów z rakiem nerkowokomórkowym z przerzutami (MRCC) dotychczas nieleczonych w badaniu III fazy, zdarzenia niepożądane ze strony układu krążenia zakończone zgonem wystąpiły u 0,6% pacjentów w grupie otrzymującej IFN-α i u 0% pacjentów w grupie otrzymującej sunitynib. W badaniu III fazy dotyczącym pNET u jednego pacjenta (1%) otrzymującego sunitynib wystąpiła niewydolność serca zakończona zgonem związana z zastosowanym leczeniem.
Zaburzenia naczyniowe
Nadciśnienie tętnicze
Nadciśnienie tętnicze było bardzo częstym działaniem niepożądanym raportowanym w badaniach klinicznych. U około 2,7% pacjentów, u których wystąpiło nadciśnienie tętnicze, zmniejszono dawkę sunitynibu lub tymczasowo wstrzymano jego podawanie. U żadnego z tych pacjentów sunitynibu nie odstawiono jednak całkowicie. Ciężkie nadciśnienie tętnicze (ciśnienie skurczowe > 200 mm Hg lub ciśnienie rozkurczowe > 110 mm Hg) wystąpiło u 4,7% pacjentów z guzami litymi. Nadciśnienie tętnicze obserwowano u około 33,9% pacjentów otrzymujących sunitynib z powodu dotychczas nieleczonego raka nerkowokomórkowego z przerzutami (MRCC) i u 3,6% pacjentów otrzymujących IFN-α. Ciężkie nadciśnienie tętnicze wystąpiło u 12% dotychczas nieleczonych pacjentów otrzymujących sunitynib i u < 1% pacjentów otrzymujących IFN-α. W badaniu III fazy dotyczącym pNET nadciśnienie tętnicze wystąpiło u 26,5% pacjentów otrzymujących sunitynib i u 4,9% pacjentów otrzymujących placebo. Ciężkie nadciśnienie tętnicze stwierdzono u 10% pacjentów z pNET leczonych sunitynibem i u 3% pacjentów otrzymujących placebo.
Incydenty żylnej choroby zakrzepowo-zatorowej (ŻChZZ)
Incydenty ŻChZZ związane z leczeniem wystąpiły u około 1,0% pacjentów z guzami litymi, którzy
otrzymywali sunitynib w badaniach klinicznych, w tym u pacjentów z GIST i RCC.
W badaniu klinicznym III fazy z udziałem pacjentów z GIST incydenty ŻChZZ wystąpiły u 7 (3%) pacjentów w grupie otrzymującej sunitynib, natomiast w grupie otrzymującej placebo nie wystąpiły u żadnego z pacjentów. U 5 z 7 pacjentów rozpoznano zakrzepicę żył głębokich 3. stopnia, a u 2 pacjentów – 1. lub 2. stopnia. U 4 z 7 pacjentów przerwano leczenie po wystąpieniu pierwszych objawów zakrzepicy żył głębokich.
Incydenty ŻChZZ wystąpiły u 13 (3%) pacjentów otrzymujących sunitynib w badaniu III fazy dotyczącym wcześniej nieleczonego raka nerkowokomórkowego z przerzutami (MRCC) i u 4 (2%) pacjentów w 2 badaniach dotyczących raka nerkowokomórkowego z przerzutami (MRCC) opornego na leczenie cytokinami. U 9 z tych pacjentów wystąpiła zatorowość płucna – u 1 pacjenta 2. stopnia, a u 8 pacjentów 4. stopnia. U 8 z tych pacjentów rozpoznano zakrzepicę żył głębokich: 1 przypadek 1. stopnia, 2 przypadki 2. stopnia, 4 przypadki 3. stopnia i 1 przypadek 4. stopnia. U 1 pacjenta z zatorowością płucną w badaniu dotyczącym raka nerkowokomórkowego z przerzutami (MRCC) opornego na leczenie cytokinami podawanie leku przerwano.
W grupie dotychczas nieleczonych pacjentów z rakiem nerkowokomórkowym z przerzutami (MRCC), którzy otrzymywali IFN-α, incydenty ŻChZZ wystąpiły u 6 (2%) pacjentów: u 1 (< 1%) pacjenta wystąpiła zakrzepica żył głębokich 3. stopnia, a u 5 (1%) pacjentów — zatorowość płucna 4. stopnia.
W badaniu III fazy dotyczącym pNET incydenty ŻChZZ zgłoszono u 1 (1,2%) pacjenta w grupie otrzymującej sunitynib i u 5 (6,1%) pacjentów w grupie otrzymującej placebo. U dwóch spośród pacjentów otrzymujących placebo wystąpiła zakrzepica żył głębokich, u jednego 2. stopnia, a u drugiego 3. stopnia.
W badaniach rejestracyjnych u pacjentów z GIST, MRCC i pNET nie zgłoszono żadnego przypadku zgonu. Przypadki zakończone zgonem wystąpiły natomiast w ramach nadzoru po wprowadzeniu produktu do obrotu.
Przypadki zatorowości płucnej wystąpiły u około 3,1% pacjentów z GIST i u około 1,2% pacjentów z rakiem nerkowokomórkowym z przerzutami (MRCC) , którzy otrzymywali sunitynib w badaniach III fazy. W badaniu III fazy z udziałem pacjentów z pNET otrzymujących sunitynib nie stwierdzono żadnego przypadku zatorowości płucnej. Rzadkie przypadki zakończone zgonem wystąpiły natomiast w ramach nadzoru po wprowadzeniu produktu do obrotu.
Pacjenci, u których stwierdzono zatorowość płucną, w okresie poprzedzających 12 miesięcy zostali wykluczeni z badań klinicznych sunitynibu.
W grupie pacjentów, którzy otrzymywali sunitynib w badaniach rejestracyjnych III fazy, zdarzenia płucne (tj. duszność, wysięk opłucnowy, zatorowość płucną lub obrzęk płuc) wystąpiły u około 17,8% pacjentów z GIST, u około 26,7% pacjentów z rakiem nerkowokomórkowym z przerzutami (MRCC) i u 12% pacjentów z pNET.
W grupie pacjentów z guzami litymi, w tym z GIST i MRCC, którzy otrzymywali sunitynib w
badaniach klinicznych, zdarzenia płucne wystąpiły u około 22,2% pacjentów.
Zaburzenia żołądka i jelit
U pacjentów z GITS lub z rakiem nerkowokomórkowym z przerzutami (MRCC) otrzymujących sunitynib zgłaszano niezbyt częste (< 1%) przypadki zapalenia trzustki. U pacjentów z pNET biorących udział w badaniu III fazy nie stwierdzono żadnego przypadku zapalenia trzustki związanego z zastosowanym leczeniem (patrz punkt 4.4).
Przypadki krwawienia z przewodu pokarmowego zakończone zgonem wystąpiły u 0,98% pacjentów otrzymujących placebo w badaniu III fazy dotyczącym leczenia GIST.
Zaburzenia wątroby i dróg żółciowych
Zgłaszano przypadki dysfunkcji wątroby, które mogą obejmować nieprawidłowe wartości parametrów czynnościowych wątroby, zapalenie wątroby lub niewydolność wątroby (patrz punkt 4.4).
Zaburzenia skóry i tkanki podskórnej
Zgłaszano przypadki piodermii zgorzelinowej, która zazwyczaj ustępowała po odstawieniu sunitynibu
(patrz również punkt 4.4).
Zaburzenia mięśniowo-szkieletowe i tkanki łącznej
Zgłaszano przypadki miopatii i (lub) rabdomiolizy, niekiedy z towarzyszącą ostrą niewydolnością nerek. Pacjentów z powikłaniami ze strony mięśni należy leczyć zgodnie ze standardowymi zasadami postępowania (patrz punkt 4.4).
Zgłaszano przypadki tworzenia się przetok, czasem związane z martwicą guza nowotworowego lub regresją, w niektórych przypadkach zakończone zgonem (patrz punkt 4.4).
Zgłaszano przypadki martwicy kości szczęki i (lub) żuchwy u pacjentów leczonych sunitynibem, przy czym większość z nich odnotowano u osób, u których stwierdzono znane czynniki ryzyka rozwoju ONJ, zwłaszcza takie jak przyjmowanie bisfosfonianów dożylnie i (lub) choroby stomatologiczne w wywiadzie wymagające przeprowadzenia inwazyjnych procedur dentystycznych (patrz również punkt 4.4).
Badania diagnostyczne
Dane z badań nieklinicznych (in vitro i in vivo), w których stosowano dawki większe niż zalecane u ludzi, wskazują, że sunitynib może hamować proces repolaryzacji błon komórkowych (skutkując np. wydłużeniem odstępu QT).
Wydłużenie odstępu QTc do ponad 500 ms wystąpiło u 0,5%, natomiast zmiany od wartości wyjściowej o więcej niż 60 ms wystąpiły u 1,1% spośród 450 pacjentów z guzami litymi; zmiany obu powyższych parametrów są uznawane za potencjalnie istotne. Wykazano, że sunitynib w stężeniach w przybliżeniu dwukrotnie większych niż terapeutyczne wydłuża odstęp QTcF (odstęp QT skorygowany wg wzoru Fridericia).
Wydłużenie odstępu QTc oceniano w badaniu z udziałem 24 pacjentów w wieku od 20 do 87 lat z zaawansowanymi nowotworami złośliwymi. Wyniki tego badania wykazały, że sunitynib miał wpływ na odstęp QTc [określany jako średnia zmiana skorygowana o placebo > 10 ms z górną granicą 90% przedziału ufności (CI) wynoszącą > 15 ms] przy stężeniu terapeutycznym (dzień 3.) z zastosowaniem metody korygowania codziennym stanem początkowym oraz przy stężeniu większym od terapeutycznego (dzień 9.) z zastosowaniem obu metod korygowania według stanu początkowego. U żadnego pacjenta wartość QTc nie była > 500 ms. Pomimo zaobserwowanego wpływu na odstęp QTcF w dniu 3. w okresie 24 godzin po podaniu dawki (tj. przy oczekiwanym terapeutycznym stężeniu w osoczu po podaniu zalecanej dawki początkowej 50 mg) z zastosowaniem metody korygowania codziennym stanem początkowym, znaczenie kliniczne tej obserwacji jest nieznane.
U żadnego z pacjentów populacji kwalifikującej się do oceny lub populacji zgodnej z zamiarem
leczenia (ang. ITT, intent-to-treat) nie odnotowano wydłużenia odstępu QTc, który zostałby uznany za
„ciężki” [tj. równy lub większy od stopnia 3. wg „Wspólnych kryteriów terminologicznych dla zdarzeń niepożądanych” (CTCAE, ang. Common Terminology Criteria for Adverse Events wersja 3.0)] na podstawie serii kompleksowych badań EKG przeprowadzonych w punktach czasowych odpowiadających ekspozycji terapeutycznej lub większej niż terapeutyczna.
Przy stężeniach terapeutycznych w osoczu maksymalna średnia zmiana odstępu QTcF (odstęp QT skorygowany wg wzoru Fridericia) od stanu wyjściowego wynosiła 9 ms (90% CI: 15,1 ms). Przy około dwukrotnie większych stężeniach terapeutycznych maksymalna zmiana odstępu QTcF w porównaniu ze stanem wyjściowym wyniosła 15,4 ms (90% CI: 22,4 ms). Po podaniu moksyfloksacyny (400 mg) jako kontroli dodatniej wykazano, że maksymalna średnia zmiana odstępu QTcF wynosi 5,6 ms w porównaniu ze stanem wyjściowym. U żadnego z pacjentów nie stwierdzono wydłużenia odstępu QTc w stopniu ciężkości większym niż 2. (CTCAE, wersja 3.0) (patrz punkt 4.4).
Ocena długookresowego bezpieczeństwa u pacjentów z rakiem nerkowokomórkowym z przerzutami
(MRCC)
Długookresowe bezpieczeństwo stosowania sunitynibu u pacjentów z rakiem nerkowokomórkowym z przerzutami (MRCC) analizowano w 9 zakończonych badaniach klinicznych w schematach leczenia pierwszego rzutu, oporności na bewacyzumab oraz oporności na cytokiny u 5739 pacjentów, z których 807 (14%) było leczonych przez okres od ≥ 2 lat do 6 lat. U 807 pacjentów, którzy otrzymywali sunitynib przez długi czas, większość działań niepożądanych związanych ze stosowanym leczeniem wystąpiła po raz pierwszy w okresie pierwszych 6–12 miesięcy, a następnie ich częstość występowania utrzymywała się na stałym poziomie lub zmniejszała się w miarę upływu czasu, z wyjątkiem niedoczynności tarczycy, której częstość występowania stopniowo zwiększała się, a nowe przypadki pojawiały się w ciągu kolejnych 6 lat. Długotrwałe leczenie sunitynibem nie było powiązane z nowymi rodzajami działań niepożądanych związanych z leczeniem.
Dzieci i młodzież
Profil bezpieczeństwa sunitynibu opracowano na podstawie badania I fazy ze zwiększeniem dawki, otwartego badania II fazy, jednoramiennego badania I/II fazy oraz publikacji, jak opisano to poniżej.
Badanie I fazy ze zwiększeniem dawki sunitynibu podawanego doustnie przeprowadzono z udziałem 35 pacjentów, w tym 30 pacjentów z populacji dzieci i młodzieży (w wieku od 3 do 17 lat) i 5 pacjentów z grupy młodych osób dorosłych (w wieku od 18 do 21 lat) z guzami litymi opornymi na leczenie. U większości pacjentów pierwotnie rozpoznano guza mózgu. U wszystkich uczestników badania wystąpiły działania niepożądane; większość działań niepożądanych miała przebieg ciężki (stopień toksyczności ≥3), w tym kardiotoksyczność. Najczęstszymi działaniami niepożądanymi były: toksyczność żołądkowo-jelitowa, neutropenia, zmęczenie i zwiększenie aktywności aminotransferazy alaninowej (AlAT). Ryzyko występowania kardiologicznych działań niepożądanych wydawało się być większe w grupie dzieci i młodzieży wcześniej leczonych antracyklinami lub radioterapią, której zasięg obejmował serce w porównaniu do grupy pacjentów, u których nie stosowano tego typu terapii. U tych pacjentów z populacji dzieci i młodzieży, którzy nie byli wcześniej leczeni antracyklinami ani radioterapią, której zasięg obejmował serce, ustalono maksymalną tolerowaną dawkę (ang. maximum tolerated dose, MTD) (patrz punkt 5.1).
Otwarte badanie II fazy przeprowadzono z udziałem 29 pacjentów, w tym 27 pacjentów z populacji dzieci i młodzieży (w wieku od 3 do 16 lat) i 2 pacjentów z grupy młodych osób dorosłych (w wieku 18 do 19 lat) z nawrotowym/progresywnym/opornym na leczenie glejakiem o wysokim stopniu złośliwości (ang. high-grade glioma, HGG) lub wyściółczakiem. W żadnej z grup nie wystąpiły działania niepożądane stopnia 5. Najczęstszymi (≥10%) zdarzeniami niepożądanymi związanymi z leczeniem były: zmniejszenie liczby neutrofili [u 6 (20,7%) pacjentów] i krwotok wewnątrzczaszkowy [u 3 (10,3%) pacjentów].
Jednoramienne badanie I/II fazy przeprowadzono z udziałem 6 pacjentów z populacji dzieci i młodzieży (w wieku od 13 do 16 lat) z zaawansowanym nieoperacyjnym GIST. Najczęstszymi działaniami niepożądanymi, głównie o nasileniu 1. lub 2. stopnia, były: biegunka, nudności, zmniejszenie liczby krwinek białych, neutropenia i ból głowy, przy czym każde z nich wystąpiło u 3 (50,0%) pacjentów. U 4 z 6 pacjentów (66,7%) wystąpiły zdarzenia niepożądane związane z leczeniem 3. lub 4. stopnia nasilenia (do zdarzeń o 3. stopniu nasilenia należały: hipofosfatemia, neutropenia i małopłytkowość, przy czym każde z nich wystąpiło u 1 pacjenta oraz neutropenia 4. stopnia u 1 pacjenta. W badaniu tym nie zgłoszono ciężkich zdarzeń niepożądanych ani działań niepożądanych związanych z leczeniem o stopniu nasilenia 5. Zarówno w badaniu klinicznym, jak i w publikacjach profil bezpieczeństwa był zgodny ze stwierdzonym już wcześniej profilem bezpieczeństwa u osób dorosłych.
Zgłaszanie podejrzewanych działań niepożądanych
Po dopuszczeniu produktu leczniczego do obrotu istotne jest zgłaszanie podejrzewanych działań niepożądanych. Umożliwia to nieprzerwane monitorowanie stosunku korzyści do ryzyka stosowania produktu leczniczego. Osoby należące do fachowego personelu medycznego powinny zgłaszać wszelkie podejrzewane działania niepożądane za pośrednictwem Departamentu Monitorowania
Niepożądanych Działań Produktów Leczniczych Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych:
Al. Jerozolimskie 181C 02-222 Warszawa
Tel.: + 48 22 49 21 301
Faks: + 48 22 49 21 309
Strona internetowa: https://smz.ezdrowie.gov.pl
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Przedawkowanie
WŁAŚCIWOŚCI FARMAKOLOGICZNE
Właściwości farmakodynamiczne
Właściwości farmakokinetyczne
Przedkliniczne dane o bezpieczeństwie
DANE FARMACEUTYCZNE
Wykaz substancji pomocniczych
Niezgodności farmaceutyczne
Okres ważności
Specjalne środki ostrożności podczas przechowywania
Rodzaj i zawartość opakowania
Specjalne środki ostrożności dotyczące usuwania
PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE
NUMERY POZWOLEŃ NA DOPUSZCZENIE DO OBROTU
DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU I
DATA ZATWIERDZENIA LUB CZĘŚCIOWEJ ZMIANY TEKSTU
Subinit, 12,5 mg, kapsułki, twarde Subinit, 25 mg, kapsułki, twarde Subinit, 50 mg, kapsułki, twarde
Subinit, 12,5 mg, kapsułki twarde
Każda kapsułka zawiera 16,70 mg sunitynibu jabłczanu w ilości odpowiadającej 12,5 mg sunitynibu.
Subinit, 25 mg, kapsułki twarde
Każda kapsułka zawiera 33,40 mg sunitynibu jabłczanu w ilości odpowiadającej 25 mg sunitynibu.
Subinit, 50 mg, kapsułki twarde
Każda kapsułka zawiera 66,80 mg sunitynibu jabłczanu w ilości odpowiadającej 50 mg sunitynibu. Pełny wykaz substancji pomocniczych, patrz punkt 6.1.
Kapsułka, twarda.
Subinit, 12,5 mg, kapsułki twarde
Kapsułki żelatynowe twarde z nieprzezroczystym czerwonym wieczkiem i korpusem, nr 4,
zawierające granulki o barwie od żółtej do pomarańczowej.
Subinit, 25 mg, kapsułki twarde
Kapsułki żelatynowe twarde z nieprzezroczystym żółtym wieczkiem i nieprzezroczystym czerwonym korpusem, nr 2, zawierające granulki o barwie od żółtej do pomarańczowej.
Subinit, 50 mg, kapsułki twarde
Kapsułki żelatynowe twarde z nieprzezroczystym żółtym wieczkiem i korpusem, nr 1, zawierające granulki o barwie od żółtej do pomarańczowej.
Nowotwory podścieliskowe przewodu pokarmowego (ang. Gastrointestinal stromal tumour, GIST) Subinit jest wskazany w leczeniu nowotworów podścieliskowych przewodu pokarmowego (GIST) nieoperacyjnych i (lub) z przerzutami u dorosłych po niepowodzeniu leczenia imatynibem ze względu na oporność lub nietolerancję.
Rak nerkowokomórkowy z przerzutami (ang. Metastatic renal cell carcinoma, MRCC) Subinit jest wskazany w leczeniu zaawansowanego raka nerkowokomórkowego i (lub) raka nerkowokomórkowego z przerzutami (MRCC) u dorosłych.
Nowotwory neuroendokrynne trzustki (ang. Pancreatic neuroendocrine tumours, pNET)
Subinit jest wskazany w leczeniu wysoko zróżnicowanych nowotworów neuroendokrynnych trzustki (pNET) nieoperacyjnych lub z przerzutami u dorosłych, u których doszło do progresji choroby.
Leczenie produktem Subinit powinien rozpoczynać lekarz doświadczony w podawaniu leków
przeciwnowotworowych.
Dawkowanie
W przypadku GIST i MRCC, zalecana dawka produktu Subinit wynosi 50 mg raz na dobę, przyjmowana doustnie przez 4 kolejne tygodnie, po czym następuje 2-tygodniowa przerwa (schemat 4/2), co stanowi pełny cykl 6 tygodni.
W przypadku pNET zalecana dawka produktu Subinit wynosi 37,5 mg raz na dobę, przyjmowana doustnie w sposób ciągły.
Dostosowanie dawki
Bezpieczeństwo i tolerancja
W przypadku GIST i MRCC można stopniowo dokonywać zmian dawkowania za każdym razem o 12,5 mg, zależnie od indywidualnie ocenianego bezpieczeństwa i tolerancji leczenia. Dawka dobowa nie powinna być większa niż 75 mg ani nie powinna być mniejsza niż 25 mg.
W przypadku pNET można stopniowo dokonywać zmian dawkowania za każdym razem o 12,5 mg, zależnie od indywidualnie ocenianego bezpieczeństwa i tolerancji leczenia. Dawka maksymalna podawana w badaniu III fazy dotyczącym pNET wynosiła 50 mg na dobę.
W zależności od indywidualnej oceny bezpieczeństwa i tolerancji leczenia może być konieczne
zastosowanie przerw w podawaniu produktu.
Inhibitory i (lub) induktory CYP3A4
Należy unikać jednoczesnego podawania sunitynibu z silnymi induktorami CYP3A4, takimi jak ryfampicyna (patrz punkty 4.4 i 4.5). Jeżeli nie jest to możliwe, może być konieczne zwiększanie dawki sunitynibu, za każdym razem o 12,5 mg (do 87,5 mg na dobę w przypadku GIST i MRCC lub 62,5 mg na dobę w przypadku pNET) z jednoczesnym starannym monitorowaniem tolerancji.
Należy unikać jednoczesnego podawania sunitynibu z silnymi inhibitorami CYP3A4, takimi jak ketokonazol (patrz punkty 4.4 i 4.5). Jeżeli nie jest to możliwe, może zaistnieć konieczność zmniejszenia dawek sunitynibu do minimum 37,5 mg na dobę w przypadku GIST i MRCC lub 25 mg na dobę w przypadku pNET, z jednoczesnym starannym monitorowaniem tolerancji.
Należy rozważyć wybranie do leczenia skojarzonego alternatywnego produktu o minimalnym
działaniu hamującym CYP3A4, lub bez takiego działania.
Szczególne populacje
Dzieci i młodzież
Nie określono bezpieczeństwa stosowania ani skuteczności sunitynibu u pacjentów w wieku poniżej
18 lat.
Aktualne dane przedstawiono w punktach 4.8, 5.1 i 5.2, ale brak zaleceń dotyczących dawkowania.
Pacjenci w podeszłym wieku
Około jedna trzecia uczestników badań klinicznych, u której zastosowano sunitynib była w wieku 65 lat lub powyżej. Nie obserwowano istotnych różnic pod względem bezpieczeństwa lub skuteczności leczenia pomiędzy młodszymi i starszymi pacjentami.
Zaburzenia czynności wątroby
U pacjentów z łagodnymi lub umiarkowanymi zaburzeniami czynności wątroby (stopnia A i B według
klasyfikacji Child-Pugh), którym podaje się sunitynib, nie jest zalecane modyfikowanie początkowego
dawkowania. Nie przeprowadzono badań z sunitynibem stosowanym u pacjentów z ciężkimi zaburzeniami czynności wątroby stopnia C według klasyfikacji Child-Pugh i dlatego jego stosowanie u pacjentów z ciężkimi zaburzeniami czynności wątroby nie jest zalecane (patrz punkt 5.2).
Zaburzenia czynności nerek
Nie ma konieczności modyfikowania dawki początkowej podczas podawania sunitynibu pacjentom z zaburzeniami czynności nerek (lekkimi do ciężkich) ani u pacjentów ze schyłkową niewydolnością nerek (ang. End-Stage Renal Disease, ESRD) poddawanym hemodializie. Późniejsze modyfikacje dawkowania powinny zależeć od bezpieczeństwa i tolerancji leczenia u poszczególnych pacjentów (patrz punkt 5.2).
Sposób podawania
Subinit jest podawany doustnie i może być przyjmowany z posiłkiem lub niezależnie od posiłków.
W przypadku pominięcia jednej z dawek nie należy stosować dodatkowej dawki. Pacjent powinien przyjąć zwykłą przepisaną dawkę następnego dnia.
Nadwrażliwość na substancję czynną lub na którąkolwiek substancję pomocniczą wymienioną
w punkcie 6.1.
Należy unikać jednoczesnego stosowania z silnymi induktorami CYP3A4, ponieważ może to powodować zmniejszenie stężenia sunitynibu w osoczu (patrz punkty 4.2 i 4.5).
Należy unikać jednoczesnego stosowania z silnymi inhibitorami CYP3A4, ponieważ może to powodować zwiększenie stężenia sunitynibu w osoczu (patrz punkty 4.2 i 4.5).
Zaburzenia skóry i tkanki podskórnej
Pacjentów należy poinformować, że w trakcie stosowania sunitynibu może dojść do odbarwienia włosów lub skóry. Do innych możliwych objawów dermatologicznych należą suchość, zgrubienie lub pękanie skóry, pęcherze lub wysypka na powierzchni dłoni i na podeszwach stóp.
Powyższe reakcje nie występowały łącznie, były na ogół odwracalne i zasadniczo nie wiązały się z koniecznością przerwania leczenia. Zgłaszano przypadki wystąpienia piodermii zgorzelinowej, której objawy zazwyczaj ustępowały po przerwaniu leczenia sunitynibem. Zgłaszano ciężkie reakcje skórne, w tym przypadki rumienia wielopostaciowego (ang. erythema multiforme, EM), przypadki przypominające zespół Stevensa-Johnsona (ang. SJS, Stevens-Johnson syndrome, SJS) oraz martwicę toksyczno-rozpływną naskórka (ang. toxic epidermal necrolysis, TEN), niektóre prowadzące do zgonu. Jeżeli wystąpią objawy przedmiotowe lub podmiotowe SJS, TEN lub EM (np. postępująca wysypka skórna często występująca z pęcherzami lub zmiany na błonie śluzowej jamy ustnej), należy przerwać leczenie sunitynibem. Jeżeli potwierdzi się diagnoza SJS lub TEN, nie wolno wznawiać leczenia. W niektórych przypadkach podejrzenia EM, pacjenci tolerowali ponowne wprowadzenie sunitynibu w mniejszej dawce po ustąpieniu reakcji skórnej; niektórzy z tych pacjentów byli również jednocześnie leczeni kortykosteroidami lub lekami przeciwhistaminowymi (patrz punkt 4.8).
Krwotoki i krwawienie z guza
Zdarzenia krwotoczne, w niektórych przypadkach prowadzące do zgonu, zgłaszane w badaniach klinicznych z sunitynibem oraz w ramach nadzoru po wprowadzeniu do obrotu obejmowały krwotoki z przewodu pokarmowego, układu oddechowego, dróg moczowych oraz mózgu (patrz punkt 4.8).
Rutynowa ocena zdarzeń krwotocznych powinna obejmować pełną morfologię krwi oraz badanie
fizykalne.
Krwotok z nosa był najczęściej występującym krwotocznym działaniem niepożądanym, obserwowanym u około połowy pacjentów z guzami litymi, u których wystąpiły powikłania krwotoczne. Niektóre z tych krwotoków z nosa były ciężkie, ale bardzo rzadko prowadziły do zgonu.
Zgłaszano przypadki krwotoku z guza, czasami związane z martwicą nowotworu; niektóre z nich prowadziły do zgonu.
Krwotoki z guza nowotworowego mogą występować nagle, a w przypadku guzów płuc mogą mieć postać ciężkiego, zagrażającego życiu krwioplucia lub krwotoku płucnego. W badaniach klinicznych oraz po wprowadzeniu do obrotu, u pacjentów z MRCC, GIST i rakiem płuc leczonych sunitynibem, zgłaszano przypadki krwotoku płucnego; niektóre z nich prowadziły do zgonu. Subinit nie jest zarejestrowany do stosowania u pacjentów z rakiem płuc.
Pacjenci otrzymujący jednocześnie leki przeciwzakrzepowe (np. warfarynę, acenokumarol) mogą być poddawani okresowym kontrolom obejmującym wykonanie morfologii krwi (z oznaczeniem liczby płytek krwi), badanie czynników krzepnięcia [czas protrombinowy (PT) i (lub) wskaźnik INR] oraz badaniu przedmiotowemu.
Zaburzenia żołądka i jelit
Najczęściej obserwowanymi działaniami niepożądanymi ze strony układu pokarmowego były biegunka, nudności i (lub) wymioty, ból brzucha, niestrawność oraz zapalenie jamy ustnej i (lub) ból w jamie ustnej; zgłaszano również przypadki zapalenia przełyku (patrz punkt 4.8).
W razie wystąpienia tego typu działań niepożądanych zastosowane leczenie wspomagające może obejmować stosowanie leków przeciwwymiotnych, przeciwbiegunkowych lub zobojętniających kwas żołądkowy.
U pacjentów z nowotworami w jamie brzusznej, u których zastosowano sunitynib zgłaszano ciężkie, czasem prowadzące do zgonu powikłania ze strony przewodu pokarmowego, w tym perforacje.
Nadciśnienie tętnicze
Zgłaszano przypadki nadciśnienia tętniczego powiązane ze stosowaniem sunitynibu, w tym ciężkie nadciśnienie tętniczego (ciśnienie skurczowe >200 mmHg lub ciśnienie rozkurczowe 110 mmHg). Należy badać pacjentów w celu wykrycia nadciśnienia tętniczego i odpowiednio ich kontrolować.
U pacjentów z ciężkim nadciśnieniem tętniczym, którego nie udaje się kontrolować farmakologicznie, zaleca się czasowe przerwanie stosowania produktu Subinit. Można je ponownie podjąć po uzyskaniu skutecznej kontroli nadciśnienia (patrz punkt 4.8).
Zaburzenia hematologiczne
Zgłaszano zmniejszenie bezwzględnej liczby neutrofili i płytek krwi powiązane ze stosowaniem sunitynibu (patrz punkt 4.8). Powyższe zdarzenia nie występowały łącznie, były na ogół odwracalne i zasadniczo nie wiązały się z koniecznością przerwania leczenia. Żaden z tych epizodów w badaniach III fazy nie był śmiertelny, ale w ramach nadzoru po wprowadzeniu sunitynibu do obrotu, zgłaszano rzadkie przypadki epizodów hematologicznych o skutkach śmiertelnych, w tym krwotoki związane z małopłytkowością i zakażenia w przebiegu neutropenii.
Obserwowano przypadki niedokrwistości, które występowały zarówno na początku jak i w trakcie
leczenia sunitynibem.
U pacjentów, u których stosuje się sunitynib, należy oznaczyć morfologię krwi na początku każdego
cyklu leczenia (patrz punkt 4.8).
Zaburzenia serca
U pacjentów leczonych sunitynibem zgłaszano zdarzenia sercowo-naczyniowe, w tym niewydolność serca, kardiomiopatię, zmniejszenie frakcji wyrzutowej lewej komory poniżej dolnej granicy normy, zapalenie mięśnia sercowego, niedokrwienie mięśnia sercowego oraz zawał mięśnia sercowego, z czego niektóre przypadki były zakończone zgonem. Dane te wskazują na to, że sunitynib zwiększa
ryzyko rozwoju kardiomiopatii. U leczonych pacjentów nie zidentyfikowano żadnych dodatkowych czynników ryzyka rozwoju kardiomiopatii wywołanej przez sunitynib poza wpływem samego leku. U pacjentów zagrożonych wystąpieniem zdarzeń sercowo-naczyniowych lub, u których takie zdarzenia wystąpiły w przeszłości, sunitynib należy stosować ostrożnie (patrz punkt 4.8).
Ze wszystkich badań klinicznych nad sunitynibem wykluczono pacjentów, u których w ciągu 12 miesięcy przed podaniem produktu miały miejsce incydenty związane z układem krążenia, takie jak zawał mięśnia sercowego (w tym ciężka i (lub) niestabilna dławica piersiowa), przeszczep pomostujący tętnicy wieńcowej i (lub) tętnicy obwodowej, objawowa zastoinowa niewydolność serca, udar mózgu lub przejściowy napad niedokrwienny, bądź też zator tętnicy płucnej. Nie wiadomo, czy pacjenci z wymienionymi schorzeniami współistniejącymi mogą być narażeni na większe ryzyko rozwoju dysfunkcji lewej komory związanej z sunitynibem.
Lekarz powinien rozważyć stosunek ryzyka do potencjalnych korzyści ze stosowania sunitynibu. Pacjentów, a w szczególności pacjentów z kardiologicznymi czynnikami ryzyka i (lub) chorobą wieńcową w wywiadzie, należy uważnie monitorować pod kątem występowania ewentualnych klinicznych objawów podmiotowych i przedmiotowych zastoinowej niewydolności serca podczas stosowania sunitynibu. Należy również rozważyć wykonywanie oznaczeń LVEF na początku terapii i okresowo w trakcie leczenia sunitynibem. U pacjentów, u których nie występują kardiologiczne czynniki ryzyka należy rozważyć wykonanie wyjściowej oceny frakcji wyrzutowej.
W przypadku wystąpienia objawów klinicznych zastoinowej niewydolności serca zaleca się przerwanie stosowania sunitynibu. U pacjentów bez klinicznych objawów zastoinowej niewydolności serca, ale z frakcją wyrzutową <50% i >20% poniżej wartości wyjściowej należy przerwać stosowanie sunitynibu i (lub) zmniejszyć dawkę.
Wydłużenie odstępu QT
Wydłużenie odstępu QT oraz torsade de pointes obserwowano u pacjentów otrzymujących sunitynib. Wydłużenie odstępu QT może prowadzić do zwiększenia ryzyka występowania komorowych zaburzeń rytmu, w tym typu torsade de pointes.
Należy zachować ostrożność podczas stosowania sunitynibu u pacjentów z wydłużonym odstępem QT w wywiadzie, pacjentów przyjmujących leki przeciwarytmiczne lub leki mogące powodować wydłużenie odstępu QT oraz u pacjentów z istotnymi chorobami serca w wywiadzie, bradykardią lub zaburzeniami elektrolitowymi. Należy ograniczyć jednoczesne podawanie sunitynibu z silnymi inhibitorami CYP3A4, które mogą powodować zwiększenie stężenia sunitynibu w osoczu (patrz punkty 4.2, 4.5 i 4.8).
Żylne zaburzenia zakrzepowo-zatorowe
U pacjentów, którzy przyjmowali sunitynib , zgłaszano związane z leczeniem epizody żylnej choroby zakrzepowo-zatorowej, w tym zakrzepicę żył głębokich oraz zator tętnicy płucnej (patrz punkt 4.8). W ramach nadzoru po wprowadzeniu sunitynibu do obrotu obserwowano przypadki zatoru tętnicy płucnej zakończone zgonem.
Tętnicze zdarzenia zakrzepowo-zatorowe
U pacjentów leczonych sunitynibem obserwowano przypadki tętniczych zdarzeń zakrzepowo- zatorowych, czasem prowadzących do zgonu. Najczęstszymi z takich zdarzeń były: udar naczyniowy mózgu, przemijający napad niedokrwienny i zawał mózgu. Do czynników ryzyka związanych z tętniczymi zdarzeniami zakrzepowo-zatorowymi, poza chorobą nowotworową i wiekiem ≥65 lat, należały: nadciśnienie tętnicze, cukrzyca i choroba zakrzepowo-zatorowa w wywiadzie.
Tętniak i rozwarstwienie tętnicy
Stosowanie inhibitorów szlaku czynników wzrostu śródbłonka naczyniowego (VEGF) u pacjentów z nadciśnieniem tętniczym lub bez nadciśnienia tętniczego może sprzyjać tworzeniu tętniaka i (lub) rozwarstwieniu tętnicy. Przed rozpoczęciem leczenia sunitynibem należy starannie rozważyć ryzyko wystąpienia tych działań niepożądanych u pacjentów z czynnikami ryzyka, takimi, jak nadciśnienie tętnicze lub tętniak w wywiadzie.
Mikroangiopatia zakrzepowa
W przypadku wystąpienia niedokrwistości hemolitycznej, małopłytkowości, zmęczenia, objawów neurologicznych o charakterze zmiennym, zaburzeń czynności nerek oraz gorączki należy rozważyć możliwość wystąpienia mikroangiopatii zakrzepowej, w tym zakrzepowej plamicy małopłytkowej i zespołu hemolityczno-mocznicowego, czasami prowadzących do niewydolności nerek lub zgonu. U pacjentów, u których rozwinęła się mikroangiopatia zakrzepowa, należy przerwać terapię sunitynibem i szybko rozpocząć odpowiednie leczenie. Po zaprzestaniu leczenia obserwowano ustąpienie objawów mikroangiopatii zakrzepowej (patrz punkt 4.8).
Zaburzenia czynności tarczycy
Zaleca się wstępne badania laboratoryjne czynności tarczycy u wszystkich pacjentów. Pacjenci z niedoczynnością tarczycy lub nadczynnością tarczycy w wywiadzie powinni być leczeni w sposób standardowy przed rozpoczęciem leczenia sunitynibem. W trakcie leczenia sunitynibem należy kontrolować regularnie co 3 miesiące czynność tarczycy. Ponadto, pacjenci w czasie leczenia powinni być starannie obserwowani, czy nie występują u nich przedmiotowe i podmiotowe objawy zaburzeń czynności tarczycy. U pacjentów z objawami wskazującymi na zaburzenia czynności tarczycy konieczne jest wykonywanie badań laboratoryjnych czynności tarczycy zgodnie z klinicznymi wskazaniami. Pacjenci, u których rozwiną się zaburzenia czynności tarczycy powinni być leczeni zgodnie z obowiązującymi standardami praktyki medycznej.
Zarówno we wczesnym, jak i późniejszym okresie leczenia sunitynibem opisywano przypadki niedoczynności tarczycy (patrz punkt 4.8).
Zapalenie trzustki
U pacjentów z różnymi guzami litymi otrzymujących sunitynib, obserwowano zwiększenie aktywności lipazy i amylazy w surowicy. Zwiększenie aktywności lipazy był przemijający i na ogół nie towarzyszyły mu objawy podmiotowe i przedmiotowe zapalenia trzustki (patrz punkt 4.8).
Zgłaszano przypadki ciężkich działań niepożądanych ze strony trzustki, w niektórych przypadkach prowadzące do zgonu. W przypadku wystąpienia u pacjenta objawów zapalenia trzustki, należy przerwać stosowanie sunitynibu i zapewnić właściwe leczenie wspomagające.
Hepatotoksyczność
U pacjentów leczonych sunitynibem obserwowano przypadki hepatotoksyczności. Przypadki niewydolności wątroby, z których część zakończyła się zgonem, opisywano u <1% pacjentów z nowotworami litymi leczonych sunitynibem. Należy kontrolować parametry czynnościowe wątroby [aktywność aminotransferazy alaninowej (AlAT) i asparaginianowej (AspAT) oraz stężenie bilirubiny] przed rozpoczęciem leczenia, podczas każdego cyklu leczenia oraz w przypadku wystąpienia wskazań klinicznych. W przypadku wystąpienia objawów niewydolności wątroby należy przerwać stosowanie sunitynibu i zapewnić odpowiednie leczenie podtrzymujące (patrz punkt 4.8).
Czynność nerek
Obserwowano przypadki zaburzenia czynności nerek, niewydolności nerek i (lub) ostrej niewydolności nerek, które w niektórych przypadkach kończyły się zgonem (patrz punkt 4.8).
Do czynników ryzyka związanych z zaburzeniami czynności nerek i (lub) niewydolnością nerek u pacjentów otrzymujących sunitynib, poza rakiem nerkowokomórkowym, należały: podeszły wiek, cukrzyca, współistniejące zaburzenia czynności nerek, niewydolność serca, nadciśnienie tętnicze, posocznica, odwodnienie i (lub) hipowolemia oraz rabdomioliza.
Bezpieczeństwo stosowania sunitynibu u pacjentów z umiarkowanym lub ciężkim białkomoczem nie zostało odpowiednio zbadane.
Opisywano przypadki białkomoczu oraz rzadkie przypadki zespołu nerczycowego. Zaleca się przeprowadzenie badania moczu na początku leczenia oraz monitorowanie pacjentów w kierunku
wystąpienia lub nasilenia białkomoczu. U pacjentów z zespołem nerczycowym należy przerwać
stosowanie sunitynibu.
Przetoka
W przypadku tworzenia się przetok, leczenie sunitynibem powinno zostać przerwane. Dostępna jest ograniczona ilość informacji dotyczących kontynuacji stosowania sunitynibu u pacjentów z przetokami (patrz punkt 4.8).
Nieprawidłowy proces gojenia się ran
Podczas leczenia sunitynibem opisywano przypadki nieprawidłowego procesu gojenia się ran.
Nie przeprowadzano żadnych formalnych badań klinicznych oceniających wpływ stosowania sunitynibu na gojenie się ran. U pacjentów poddawanych dużym zabiegom chirurgicznym zaleca się, jako środek ostrożności, czasowe przerwanie leczenia sunitynibem. Istnieje ograniczone doświadczenie kliniczne dotyczące właściwego momentu ponownego włączenia sunitynibu po dużych interwencjach chirurgicznych. W związku z tym, decyzja o ponownym rozpoczęciu stosowania sunitynibu po dużych interwencjach chirurgicznych powinna być podejmowana w oparciu o kliniczną ocenę rekonwalescencji po zabiegu.
Martwica kości szczęki i (lub) żuchwy
Zgłaszano przypadki martwicy kości szczęki i (lub) żuchwy (ang. Osteonecrosis of the Jaw, ONJ)
u pacjentów leczonych sunitynibem. Większość z nich odnotowano u osób przyjmujących wcześniej lub jednocześnie dożylnie bisfosfoniany, u których ONJ stanowi rozpoznane zagrożenie. Z tego względu należy zachować ostrożność w przypadku jednoczesnego lub sekwencyjnego stosowania produktu Subinit i dożylnie bisfosfonianów.
Inwazyjne procedury dentystyczne są także znanym czynnikiem ryzyka rozwoju ONJ. Przed rozpoczęciem stosowania produktu Subinit należy rozważyć przeprowadzenie badania stomatologicznego i wdrożyć odpowiednie działania zapobiegawcze. U pacjentów przyjmujących wcześniej lub stosujących obecnie bisfosfoniany dożylnie, w miarę możliwości należy unikać inwazyjnych zabiegów dentystycznych (patrz punkt 4.8).
Nadwrażliwość i (lub) obrzęk naczynioruchowy
W przypadku wystąpienia obrzęku naczynioruchowego spowodowanego nadwrażliwością, stosowanie sunitynibu powinno zostać przerwane, a pacjenci powinni zostać objęci standardową opieką medyczną (patrz punkt 4.8).
Napady drgawkowe
W badaniach klinicznych sunitynibu oraz w ramach nadzoru po wprowadzeniu go do obrotu zgłaszano występowanie drgawek. U pacjentów z drgawkami i objawami podmiotowymi i (lub) przedmiotowymi wskazującymi na obecność zespołu odwracalnej tylnej leukoencefalopatii (ang. reversible posterior leukoencephalopathy syndrome, RPLS), takimi jak nadciśnienie, ból głowy, zmniejszona czujność, zmiany psychiczne i utrata wzroku, w tym ślepota korowa, należy kontrolować występujące zaburzenia poprzez zastosowanie właściwego leczenia, w tym farmakologicznej kontroli nadciśnienia. Zaleca się tymczasowe przerwanie stosowania sunitynibu. Po ustąpieniu objawów lekarz prowadzący może podjąć decyzję o kontynuacji leczenia (patrz punkt 4.8).
Zespół ostrego rozpadu guza
W badaniach klinicznych oraz w ramach nadzoru po wprowadzeniu sunitynibu do obrotu u pacjentów leczonych sunitynibem rzadko obserwowano przypadki zespołu ostrego rozpadu guza; niektóre z nich prowadziły do zgonu. Czynniki ryzyka zespołu ostrego rozpadu guza obejmują dużą wielkość guza, przewlekłą niewydolność nerek w wywiadzie, skąpomocz, odwodnienie, niedociśnienie tętnicze i kwaśny odczyn moczu. Pacjentów należy ściśle obserwować i podjąć leczenie w razie wystąpienia wskazań klinicznych, oraz rozważyć zastosowanie nawodnienia pacjenta jako profilaktyki.
Zakażenia
Zgłaszano ciężkie zakażenia, z neutropenią lub bez neutropenii, w tym niektóre zakończone zgonem. Zgłaszano nieliczne przypadki martwiczego zapalenia powięzi, w tym krocza, czasami prowadzące do zgonu (patrz punkt 4.8).
U pacjentów, u których wystąpi martwicze zapalenie powięzi, należy przerwać stosowanie sunitynibu i niezwłocznie wdrożyć odpowiednie leczenie.
Hipoglikemia
Podczas leczenia sunitynibem zgłaszano zmniejszenie stężenia glukozy we krwi, w niektórych przypadkach klinicznie objawowe i wymagające hospitalizacji z powodu utraty przytomności. W przypadku objawowej hipoglikemii należy tymczasowo przerwać podawanie sunitynibu. U pacjentów z cukrzycą należy regularnie sprawdzać stężenie glukozy we krwi w celu oceny, czy konieczne jest dostosowanie dawki leku przeciwcukrzycowego, aby zminimalizować ryzyko wystąpienia hipoglikemii (patrz punkt 4.8).
Substancje pomocnicze
Sód
Ten produkt leczniczy zawiera mniej niż 1 mmol (23 mg) sodu na kapsułkę, to znaczy produkt uznaje się za „wolny od sodu”.
Wpływ inhibitorów CYP3A4
Jednoczesne podanie jednorazowej dawki sunitynibu z silnym inhibitorem CYP3A4, ketokonazolem, powodowało u zdrowych ochotników wzrost wartości maksymalnej sumy stężenia sunitynibu i jego głównego metabolitu (Cmax) o 49% i pola powierzchni pod krzywą zależności sumy stężenia sunitynibu i jego głównego metabolitu we krwi od czasu (AUC0-∞) o 51%.
Podawanie sunitynibu jednocześnie z silnymi inhibitorami CYP3A4 (np. rytonawirem, itrakonazolem, erytromycyną, klarytromycyną, sokiem grejpfrutowym) może wiązać się ze zwiększeniem stężenia sunitynibu.
Z tego względu należy unikać jednoczesnego podawania sunitynibu z inhibitorami CYP3A4 lub należy rozważyć wybranie do leczenia skojarzonego alternatywnego produktu o minimalnym działaniu hamującym CYP3A4, lub bez takiego działania.
Jeżeli nie jest to możliwe, może zaistnieć konieczność zmniejszenia dawki produktu Subinit do minimum 37,5 mg na dobę w przypadku GIST i MRCC lub 25 mg na dobę w przypadku pNET, na podstawie dokładnie monitorowanej tolerancji (patrz punkt 4.2).
Wpływ inhibitorów białka oporności raka piersi (BCRP, ang. breast cancer resistance protein)
Dane kliniczne dotyczące interakcji między sunitynibem a inhibitorami BCRP są ograniczone, więc nie można wykluczyć możliwości występowania interakcji między sunitynibem a innymi inhibitorami BCRP (patrz punkt 5.2).
Produkty lecznicze, które mogą zmniejszyć stężenie sunitynibu w osoczu
Wpływ induktorów CYP3A4
Jednoczesne podanie jednorazowej dawki sunitynibu z induktorem CYP3A4, ryfampicyną, powodowało u zdrowych ochotników redukcję wartości Cmax i AUC0-∞ kompleksu [sunitynib + podstawowy metabolit] odpowiednio o 23% i 46%.
Podawanie sunitynibu z silnymi induktorami CYP3A4 (np. deksametazonem, fenytoiną, karbamazepiną, ryfampicyną, fenobarbitalem lub ziołami zawierającymi ziele dziurawca Hypericum perforatum) może prowadzić do zmniejszenia stężenia sunitynibu. Z tego względu należy unikać jednoczesnego stosowania z induktorami CYP3A4, bądź też należy rozważyć wybranie do leczenia skojarzonego alternatywnego produktu leczniczego, o minimalnym działaniu indukującym CYP3A4 lub bez takiego działania. Jeżeli nie jest to możliwe, może zaistnieć konieczność stopniowego zwiększania dawek produktu Subinit, za każdym razem o 12,5 mg (do 87,5 mg na dobę w przypadku GIST i MRCC lub 62,5 mg na dobę w przypadku pNET) na podstawie dokładnie monitorowanej tolerancji (patrz punkt 4.2).
Antykoncepcja u mężczyzn i kobiet
Kobietom w wieku rozrodczym należy doradzić stosowanie skutecznej metody antykoncepcyjnej oraz odradzić zajście w ciążę podczas leczenia produktem Subinit.
Ciąża
Nie przeprowadzono badań dotyczących stosowania sunitynibu u kobiet w ciąży. W badaniach na zwierzętach stwierdzono toksyczny wpływ sunitynibu na zdolność do rozrodu, objawiający się m.in. wadami wrodzonymi płodów (patrz punkt 5.3). Produktu Subinit nie należy stosować w czasie ciąży lub u kobiet, które nie stosują skutecznej metody antykoncepcyjnej z wyjątkiem przypadku, gdy możliwe korzyści z leczenia przeważają nad możliwym ryzykiem dla płodu. Jeżeli Subinit zostanie zastosowany w czasie ciąży, lub jeżeli pacjentka zajdzie w ciążę w trakcie stosowania produktu Subinit, należy ją poinformować o potencjalnym zagrożeniu dla płodu.
Karmienie piersią
Sunitynib i (lub) jego metabolity przenikają do mleka szczurów. Nie wiadomo, czy sunitynib lub jego główny czynny metabolit przenikają do mleka ludzkiego. Ze względu na to, że substancje czynne często przenikają do mleka ludzkiego i ze względu na możliwe występowanie ciężkich działań niepożądanych u niemowląt karmionych piersią, kobiety nie powinny karmić piersią podczas stosowania produktu Subinit.
Płodność
Dane niekliniczne wskazują, że leczenie sunitynibem może zmniejszać płodność u kobiet i u
mężczyzn (patrz punkt 5.3).
Subinit wywiera niewielki wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn. Pacjenci powinni być poinformowani o możliwości wystąpienia zawrotów głowy w trakcie leczenia sunitynibem.
Podsumowanie profilu bezpieczeństwa
Najbardziej ciężkie działania niepożądane związane z leczeniem sunitynibem to: niewydolność nerek, niewydolność serca, zator tętnicy płucnej, perforacja przewodu pokarmowego oraz krwotoki (np. krwotok z układu oddechowego, przewodu pokarmowego, guza, układu moczowego oraz krwotok mózgowy); niektóre z nich prowadziły do zgonu. Do najczęściej zgłaszanych działań niepożądanych o dowolnym stopniu nasilenia (występujących u pacjentów w badaniach rejestracyjnych RCC, GIST i pNET) należały: zmniejszenie apetytu, zaburzenia smaku, nadciśnienie tętnicze, uczucie zmęczenia, zaburzenia ze strony przewodu pokarmowego (takie jak biegunka, nudności, zapalenie jamy ustnej, niestrawność i wymioty), przebarwienia skórne oraz erytrodyzestezja dłoniowo-podeszwowa.
Nasilenie tych objawów może się zmniejszać wraz z kontynuacją leczenia. Podczas leczenia może rozwinąć się niedoczynność tarczycy. Do najczęściej występujących działań niepożądanych należą zaburzenia hematologiczne (np. neutropenia, małopłytkowość i niedokrwistość).
Prowadzące do zgonu działania niepożądane inne niż wymienione w punkcie 4.4 powyżej lub w punkcie 4.8 poniżej, których związek ze stosowaniem sunitynibu uznano za możliwy, obejmowały niewydolność wielonarządową, rozsiane krzepnięcie wewnątrznaczyniowe, krwotok do jamy otrzewnowej, niewydolność nadnerczy, odmę opłucnową, wstrząs lub nagły zgon.
Tabelaryczne zestawienie działań niepożądanych
Poniżej wymieniono działania niepożądane zgłaszane przez pacjentów z GIST, MRCC i pNET w danych zbiorczych obejmujących 7115 pacjentów, częstości występowania i stopnia ciężkości (NCI- CTCAE). Włączono również działania niepożądane stwierdzone w badaniach klinicznych po dopuszczeniu sunitynibu do obrotu. W obrębie każdej grupy o określonej częstości występowania działania niepożądane są wymienione zgodnie ze zmniejszającym się nasileniem.
Częstość występowania zdefiniowano następująco: bardzo często (≥1/10), często (od ≥1/100 do
<1/10), niezbyt często (od ≥1/1000 do <1/100), rzadko (od ≥1/10 000 do <1/1000), bardzo rzadko (<1/10 000), częstość nieznana (częstość nie może być określona na podstawie dostępnych danych).
Tabela 1. Działania niepożądane zgłaszane w badaniach klinicznych
Klasyfikacja układów i narządów | Bardzo często | Często | Niezbyt często | Rzadko | Częstość nieznana |
Zakażenia i | Zakażenia | Martwicze | |||
zarażenia pasożytnicze | wirusowea Zakażenia układu oddechowegob,* | zapalenie powięzi* Zakażenia bakteryjneg | |||
Ropieńc,* | |||||
Zakażenia | |||||
grzybiczed | |||||
Zakażenia dróg | |||||
moczowych | |||||
Zakażenia skórye | |||||
Posocznicaf,* | |||||
Zaburzenia | Neutropenia | Limfopenia | Pancytopenia | Mikroangiopatia | |
krwi i układu chłonnego | Małopłytkowość Niedokrwistość Leukopenia | zakrzepowah,* | |||
Zaburzenia | Nadwrażliwość | Obrzęk | |||
układu | naczynioruchowy | ||||
immunologicz | |||||
nego | |||||
Zaburzenia endokrynologi czne | Niedoczynność tarczycy | Nadczynność tarczycy | Zapalenie tarczycy | ||
Zaburzenia metabolizmu i odżywiania | Zmniejszenie łaknieniai | Odwodnienie Hipoglikemia | Zespół ostrego rozpadu guza* | ||
Zaburzenia psychiczne | Bezsenność | Depresja | |||
Zaburzenia | Zawroty głowy | Neuropatia | Krwotok | Zespół odwracalnej | |
układu nerwowego | Bóle głowy Zaburzenia smakuj | obwodowa Parestezje Niedoczulica | mózgowy* Udar mózgu* Przemijający | tylnej encefalopatii* | |
Przeczulica | napad | ||||
niedokrwienny | |||||
Zaburzenia | Obrzęk tkanek | ||||
oka | oczodołu Obrzęk powiek | ||||
Zwiększone | |||||
łzawienie |
Klasyfikacja układów i narządów | Bardzo często | Często | Niezbyt często | Rzadko | Częstość nieznana |
Zaburzenia | Niedokrwienie | Zastoinowa | Niewydolność | ||
serca | mięśnia sercowegok,* Zmniejszenie frakcji | niewydolność serca | lewokomorowa* Zaburzenia rytmu | ||
wyrzutowejl | Zawał mięśnia | typu torsade de | |||
sercowegom,* | pointes | ||||
Niewydolność | |||||
serca* | |||||
Kardiomiopatia* | |||||
Wysięk | |||||
osierdziowy | |||||
Wydłużenie | |||||
odstępu QT w | |||||
EKG | |||||
Zaburzenia | Nadciśnienie | Zakrzepica żył | Krwotok z guza* | Tętniak i | |
naczyniowe | tętnicze | głębokich Uderzenia gorąca | rozwar- stwienie | ||
Nagłe | tętnicy* | ||||
zaczerwienienie | |||||
twarzy | |||||
Zaburzenia | Duszność | Zator tętnicy | Krwotok płucny* | ||
układu oddechowego, klatki piersiowej i śródpiersia | Krwotok z nosa Kaszel | płucnej* Wysięk opłucnowy* Krwioplucie Duszność wysiłkowa Ból jamy ustnej i gardłan | Niewydolność oddechowa* | ||
Niedrożność nosa | |||||
Suchość błon | |||||
śluzowych nosa | |||||
Zaburzenia | Zapalenie błony | Choroba | Perforacja | ||
żołądka i jelit | śluzowej jamy ustnejo | refluksowa przełyku Dysfagia | przewodu pokarmowegoq,* | ||
Ból brzuchap | Krwotok z przewodu | Zapalenie trzustki | |||
Wymioty | pokarmowego* | Przetoka odbytu | |||
Biegunka | Zapalenie przełyku* | Zapalenie jelita | |||
Niestrawność | Wzdęcie brzucha | grubegor | |||
Nudności | Dyskomfort w | ||||
Zaparcia | nadbrzuszu | ||||
Krwotok z odbytu | |||||
Krwawienie z | |||||
dziąseł | |||||
Owrzodzenie jamy | |||||
ustnej | |||||
Ból odbytu | |||||
Zapalenie warg | |||||
Guzy krwawnicze | |||||
Ból języka | |||||
Ból w jamie ustnej | |||||
Suchość w jamie | |||||
ustnej | |||||
Wzdęcia | |||||
Dyskomfort w jamie | |||||
ustnej | |||||
Odbijanie się ze | |||||
zwracaniem treści | |||||
żołądkowej lub gazu | |||||
Zaburzenia wątroby i dróg żółciowych | Niewydolność wątroby* | Zapalenie wątroby |
Klasyfikacja układów i narządów | Bardzo często | Często | Niezbyt często | Rzadko | Częstość nieznana |
Zapalenie pęcherzyka żółciowegos,* Zaburzenia czynności wątroby | |||||
Zaburzenia | Przebarwienia | Złuszczanie skóry | Rumień | ||
skóry i tkanki podskórnej | skóryt Zespół erytrodyzestezj i | Reakcje skórnev Egzema Pęcherze Rumień | wielopostaciowy* Zespół Stevensa- Johnsona* | ||
dłoniowo- | Łysienie | Piodermia | |||
podeszwowej | Trądzik | zgorzelinowa | |||
Wysypkau | Świąd | Martwica | |||
Zmiany koloru | Hiperpigmentacja | toksyczno- | |||
włosów | skóry | rozpływna | |||
Suchość skóry | Zmiany skórne | naskórka* | |||
Rogowacenie skóry | |||||
Zapalenie skóry | |||||
Zaburzenia | |||||
dotyczące płytki | |||||
paznokciowejw | |||||
Zaburzenia | Ból w | Bóle mięśniowo- | Martwica kości | Rabdomioliza* | |
mięśniowo- szkieletowe i tkanki łącznej | kończynach Bóle stawowe Ból pleców | szkieletowe Kurcze mięśni Bóle mięśniowe Osłabienie mięśni | szczęki i (lub) żuchwy Przetoka* | Miopatia | |
Zaburzenia | Niewydolność | Krwotok z dróg | Zespół nerczycowy | ||
nerek i dróg moczowych | nerek* Ostra niewydolność nerek* | moczowych | |||
Zmiana barwy | |||||
moczu | |||||
Białkomocz | |||||
Zaburzenia | Zapalenie błon | Ból w klatce | Nieprawidłowy | ||
ogólne i stany w miejscu podania | śluzowych Zmęczeniex Obrzęky Gorączka | piersiowej Ból Zespół rzekomogrypowy Dreszcze | proces gojenia się ran | ||
Badania | Zmniejszenie masy | Zwiększenie | |||
diagnostyczne | ciała Zmniejszenie liczby | aktywności fosfokinazy | |||
białych krwinek | kreatynowej we | ||||
Zwiększenie | krwi | ||||
aktywności lipazy | Zwiększone | ||||
Zmniejszenie liczby | stężenie TSH we | ||||
płytek krwi | krwi | ||||
Zmniejszenie | |||||
stężenia | |||||
hemoglobiny | |||||
Zwiększona | |||||
aktywność amylazyz | |||||
Zwiększona | |||||
aktywność | |||||
aminotransferazy | |||||
asparaginianowej | |||||
Zwiększona | |||||
aktywność | |||||
aminotransferazy | |||||
alaninowej |
Klasyfikacja układów i narządów | Bardzo często | Często | Niezbyt często | Rzadko | Częstość nieznana |
Zwiększone stężenie kreatyniny we krwi Zwiększone ciśnienie tętnicze Zwiększone stężenie kwasu moczowego we krwi |
* W tym przypadki zgonów
Następujące działania zostały połączone w jedną kategorię:
Nie istnieje swoista odtrutka, a leczenie przedawkowania produktem Subinit powinno polegać na zastosowaniu standardowych środków wspomagających. O ile istnieją wskazania, można uzyskać eliminację niewchłoniętej substancji czynnej poprzez wywołanie wymiotów lub płukanie żołądka. Zgłaszano przypadki przedawkowania; niektóre z nich wiązały się z występowaniem działań niepożądanych zgodnych ze znanym profilem bezpieczeństwa stosowania sunitynibu.
Grupa farmakoterapeutyczna: Leki przeciwnowotworowe, inhibitory kinazy białkowej; kod ATC:
L01EX01..
Mechanizm działania
Sunitynib hamuje liczne receptory kinazy tyrozynowej (ang. RTK, receptor tyrosine kinase), które biorą udział we wzroście nowotworów, w neoangiogenezie i w rozsiewie choroby nowotworowej z przerzutami. Sunitynib został zidentyfikowany jako inhibitor receptorów płytkowego czynnika wzrostu (PDGFRα i PDGFRβ), receptorów czynników wzrostu śródbłonka naczyniowego (VEGFR1, VEGFR2 i VEGFR3), receptorów czynnika komórek pnia (KIT), kinazy tyrozynowej podobnej do Fms-3 (FLT3), receptorów czynnika stymulującego powstawanie kolonii (CSF-1R) i receptorów glejopochodnego czynnika neurotroficznego (RET). W testach biochemicznych i komórkowych podstawowy metabolit sunitynibu wykazuje działanie podobne do sunitynibu.
Skuteczność kliniczna i bezpieczeństwo stosowania
Skuteczność kliniczną i bezpieczeństwo stosowania sunitynibu badano podczas leczenia pacjentów z GIST opornymi na imatynib (tj. pacjentów, u których doszło do progresji choroby w trakcie leczenia imatynibem lub po nim) lub nietolerujących imatynibu (tj. pacjentów, u których wystąpiły istotne objawy toksyczności w trakcie leczenia imatynibem, które uniemożliwiły dalsze leczenie), leczenia pacjentów z MRCCi leczenia pacjentów z nieoperacyjnymi pNET.
Skuteczność leczenia ustalano na podstawie czasu do wystąpienia progresji nowotworu (ang. time to tumour progression, TTP) oraz wydłużenia czasu przeżycia u pacjentów z nowotworami podścieliskowymi przewodu pokarmowego, na podstawie czasu przeżycia bez progresji choroby (ang. progression free survival, PFS) i wskaźników obiektywnych odpowiedzi (ang. objective response rates, ORR) u pacjentów z rakiem nerkowokomórkowym z przerzutami, którzy dotychczas nie byli leczeni i po niepowodzeniu leczenia cytokinami oraz na podstawie przeżycia bez progresji choroby
u pacjentów z pNET.
Nowotwory podścieliskowe przewodu pokarmowego
Wstępne otwarte, zakładające zwiększanie dawkowania badanie zostało przeprowadzone u pacjentów z nowotworami podścieliskowymi przewodu pokarmowego po niepowodzeniu stosowania imatynibu (mediana maksymalnej dawki dobowej: 800 mg) ze względu na oporność lub nietolerancję leczenia. Do badania zakwalifikowano dziewięćdziesięciu siedmiu pacjentów, otrzymujących dawki według
różnych schematów; 55 pacjentów otrzymywało dawkę 50 mg według zalecanego schematu leczenia:
4 tygodnie przyjmowania leku/2 tygodnie przerwy (schemat 4/2).
W niniejszym badaniu mediana TTP wynosiła 34,0 tygodnie (95% CI: 22,0, 46,0).
Przeprowadzono randomizowane, podwójnie ślepe, kontrolowane placebo badanie fazy III sunitynibu, u pacjentów z nowotworami podścieliskowymi przewodu pokarmowego, którzy nie tolerowali leczenia imatynibem, lub u których doszło do progresji choroby w trakcie leczenia imatynibem (mediana maksymalnej dawki dobowej 800 mg). W badaniu tym 312 pacjentów w sposób randomizowany (w stosunku 2:1) przydzielono do grup otrzymujących odpowiednio sunitynib
w dawce 50 mg lub placebo doustnie, raz na dobę, według schematu 4/2, do momentu wystąpienia progresji choroby lub wycofania z badania z innego powodu (207 pacjentów otrzymywało sunitynib, a 105 pacjentów otrzymywało placebo). Podstawowym punktem końcowym oceny skuteczności
w badaniu był TTP definiowany jako czas od randomizacji do pierwszego potwierdzenia obiektywnej progresji guza. W chwili przeprowadzenia ustalonej z góry analizy okresowej, mediana TTP podczas stosowania sunitynibu wynosiła 28,9 tygodnia (95% CI: 21,3 - 34,1) w ocenie badacza i 27,3 tygodnia (95% CI: 16,0 - 32,1) w ocenie niezależnej komisji weryfikującej i była istotnie statystycznie dłuższa niż TTP w przypadku stosowania placebo, w którym to wypadku wynosiła 5,1 tygodnia (95% CI:
4,4 - 10,1) w ocenie badacza i 6,4 tygodnia (95% CI: 4,4 - 10,0) w ocenie niezależnej komisji weryfikującej. Różnica przeżywalności całkowitej (ang. overall survival, OS) była statystycznie większa na korzyść sunitynibu [współczynnik ryzyka (HR): 0,491 (95% CI: 0,290 - 0,831)]; ryzyko zgonu było 2 razy większe u pacjentów w grupie otrzymującej placebo w porównaniu do grupy leczonej sunitynibem.
Zgodnie z zaleceniem Niezależnej Komisji Monitorującej Badanie (ang. Data and Safety Monitoring Board, DSMB), po uzyskaniu pozytywnych wyników w zakresie skuteczności i bezpieczeństwa stosowania w analizie okresowej badanie zostało odślepione, i pacjentom z grupy placebo zaproponowano leczenie sunitynibem w otwartej fazie badania.
Ogółem, w fazie otwartej badania sunitynib otrzymało 255 pacjentów, w tym 99 pacjentów, którzy
pierwotnie otrzymywali placebo.
Analizy pierwszo- i drugorzędowych punktów końcowych w fazie otwartej badania potwierdziły
wyniki uzyskane w trakcie ustalonej z góry analizy okresowej, jak przedstawiono w tabeli 2.
Tabela 2. Podsumowanie punktów końcowych dotyczących skuteczności w leczeniu pacjentów
z GIST [populacja zgodna z zamiarem leczenia (ang. intent-to-treat, ITT)]
Punkt końcowy | Leczenie w warunkach podwójnie ślepej próbya | Leczenie w grupach skrzyżowanych z placebob | |||
Mediana (95% CI) | Współczynnik ryzyka | ||||
Sunitynib | Placebo | (95% CI) | p | ||
Pierwszorzędowy: | |||||
TTP (tygodnie) | |||||
Analiza okresowa | 27,3 (16,0 do 32,1) | 6,4 (4,4 do 10,0) | 0,329 (0,233 do 0,466) | <0,001 | - |
Analiza ostateczna | 26,6 (16,0 do 32,1) | 6,4 (4,4 do 10,0) | 0,339 (0,244 do 0,472) | <0,001 | 10,4 (4,3 do 22,0) |
Drugorzędowy: | |||||
PFS (tygodnie)c | |||||
Analiza okresowa | 24,1 (11,1 do 28,3) | 6,0 (4,4 do 9,9) | 0,333 (0,238 do 0,467) | <0,001 | - |
Analiza ostateczna | 22,9 (10,9 do 28,0) | 6,0 (4,4 do 9,7) | 0,347 (0,253 do 0,475) | <0,001 | - |
ORR (%)d | |||||
Analiza okresowa | 6,8 (3,7 do 11,1) | 0 (-) | NA | 0,006 | - |
Analiza ostateczna | 6,6 (3,8 do 10,5) | 0 (-) | NA | 0,004 | 10,1 (5,0 do 17,8) |
OS (tygodnie)e | |||||
Analiza okresowa | - | - | 0,491 (0,290 do 0,831) | 0,007 | - |
Analiza ostateczna | 72,7 (61,3 do 83,0) | 64,9 (45,7 do 96,0) | 0,876 (0,679 do 1,129) | 0,306 | - |
Skróty: CI = przedział ufności (ang. confidence interval); ITT = populacja ITT (ang. intent-to-treat); NA = nie dotyczy; ORR = odsetek obiektywnych odpowiedzi (ang. objective response rate); OS = czas przeżycia całkowitego (ang. overall survival); PFS = czas przeżycia bez progresji choroby (ang. progression-free survival); TTP = czas do pierwszego potwierdzenia obiektywnej progresji guza (ang. time-to-tumour progression)
a Wyniki dotyczące leczenia w warunkach podwójnie ślepej próby dotyczą populacji ITT i oparte są na
wynikach centralnej oceny radiologicznej.
b Wyniki dotyczące skuteczności dla 99 pacjentów z grupy placebo, u których rozpoczęto leczenie sunitynibem po odślepieniu badania. W momencie zmiany z placebo na Subinit ponownie wyznaczano wartości wyjściowe, a analizy skuteczności oparto na ocenie badaczy.
c Wartości PFS dla analizy okresowej uaktualniono po ponownym przeliczeniu danych oryginalnych.
d Wyniki dotyczące ORR podano jako odsetek pacjentów z potwierdzoną odpowiedzią na leczenie z 95% CI.
e Mediana nieustalona z powodu braku wystarczającej ilości danych.
Mediana OS w populacji ITT wyniosła 72,7 tygodni u pacjentów otrzymujących sunitynib i 64,9 tygodni u pacjentów otrzymujących placebo (HR: 0,876; 95% CI: 0,679 - 1,129, p = 0,306). W tej analizie grupa placebo obejmowała pacjentów zrandomizowanych do grupy placebo, którzy w późniejszym czasie otrzymywali sunitynib w ramach otwartej fazy badania.
Rak nerkowokomórkowy z przerzutami u pacjentów, którzy dotychczas nie byli leczeni Przeprowadzono randomizowane, wieloośrodkowe, międzynarodowe badanie III fazy oceniające skuteczność i bezpieczeństwo stosowania sunitynibu w porównaniu z IFN-α u pacjentów z rakiem nerkowokomórkowym z przerzutami, którzy dotychczas nie byli leczeni. 750 pacjentów w sposób randomizowany w stosunku 1:1 przydzielono do dwóch grup terapeutycznych otrzymujących odpowiednio sunitynib w cyklach sześciotygodniowych obejmujących codzienne podawanie leku doustnie przez 4 tygodnie w dawce 50 mg, po czym następowały 2 tygodnie przerwy (schemat 4/2), albo IFN-α podawany w postaci wstrzyknięć podskórnych w dawce 3 miliony jednostek (MU) w pierwszym tygodniu, 6 MU w drugim tygodniu i 9 MU w trzecim tygodniu oraz w następnych tygodniach, w 3 dawkach podawanych co drugi dzień.
Mediana okresu leczenia wynosiła 11,1 miesiąca (zakres: 0,4 – 46,1) w przypadku leczenia sunitynibem i 4,1 miesiąca (zakres: 0,1 – 45,6) w przypadku leczenia IFN-α. Ciężkie zdarzenia niepożądane związane z leczeniem odnotowano u 23,7% pacjentów otrzymujących sunitynib i 6,9% pacjentów otrzymujących IFN-α. Odsetek pacjentów, którzy zakończyli leczenie z powodu zdarzeń niepożądanych wyniósł 20% w przypadku sunitynibu i 23% w przypadku IFN-α. Przerwy w leczeniu nastąpiły u 202 pacjentów (54%) przyjmujących sunitynib i 141 pacjentów (39%) przyjmujących IFN- α. Dawkowanie zmniejszono u 194 pacjentów (52%) leczonych sunitynibem i u 98 pacjentów (27%) leczonych IFN-α. Pacjenci byli leczeni do momentu stwierdzenia progresji choroby lub wycofania z badania. Podstawowym punktem końcowym oceny skuteczności był PFS. W planowanej analizie okresowej z przebiegu badania stwierdzono istotną statystycznie przewagę sunitynibu nad IFN-α, w omawianym badaniu mediana PFS w grupie leczonej sunitynibem wyniosła 47,3 tygodnia w porównaniu do 22,0 tygodnia w grupie leczonej IFN-α. HR wyniósł natomiast 0,415 (95% CI: 0,320 - 0,539, p < 0,001). Inne punkty końcowe obejmowały ORR, OS i bezpieczeństwo. Podstawową ocenę
radiologiczną przerwano po osiągnięciu podstawowego punktu końcowego. W ostatecznej analizie ORR w ocenie badaczy wynosił 46% (95% CI: 41% – 51%) w grupie pacjentów stosujących sunitynib i 12,0% (95% CI: 9% – 16%) w grupie pacjentów stosujących IFN-α (p < 0,001).
Leczenie sunitynibem wiązało się z dłuższym przeżyciem całkowitym w porównaniu do leczenia IFN- α. Mediana OS wynosiła 114,6 tygodnia w grupie pacjentów stosujących sunitynib (95% CI: 100,1 – 142,9) i 94,9 tygodnia w grupie pacjentów stosujących IFN-α (95% CI: 77,7 – 117,0) z HR
wynoszącym 0,821 (95% CI: 0,673 – 1,001; p = 0,0510) według niestratyfikowanego testu
logarytmicznego rang.
Ogólne wartości PFS i OS, stwierdzone w populacji ITT na podstawie oceny dokonanej przez centralną pracownię radiologiczną, podano w tabeli 3.
Tabela 3. Podsumowanie punktów końcowych dotyczących skuteczności leczenia dotychczas nieleczonych pacjentów z rakiem nerkowokomórkowym z przerzutami (MRCC)
(populacja ITT)
Podsumowanie danych dotyczących przeżycia wolnego od progresji choroby | Sunitynib (N = 375) | IFN-α (N = 375) |
Liczba pacjentów, u których nie doszło do progresji choroby ani zgonu [n (%)] | 161 (42,9) | 176 (46,9) |
Liczba pacjentów, u których stwierdzono progresję choroby lub zgon [n (%)] | 214 (57,1) | 199 (53,1) |
PFS (tygodnie) | ||
Kwartyl (95% CI) | ||
25% | 22,7 (18,0 do 34,0) | 10,0 (7,3 do 10,3) |
50% | 48,3 (46,4 do 58,3) | 22,1 (17,1 do 24,0) |
75% | 84,3 (72,9 do 95,1) | 58,1 (45,6 do 82,1) |
Analiza bez stratyfikacji | ||
Współczynnik ryzyka (sunitynib w porównaniu z IFN-α) | 0,5268 | |
95% CI dla współczynnika ryzyka | (0,4316 do 0,6430) | |
Wartość pa | < 0,0001 | |
Podsumowanie danych dotyczących przeżycia całkowitego | ||
Liczba pacjentów, o których brak informacji o wystąpieniu zgonu [n (%)] | 185 (49,3) | 175 (46,7) |
Liczba pacjentów, u których nastąpił zgon [n (%)] | 190 (50,7) | 200 (53,3) |
OS (tygodnie) | ||
Kwartyl (95% CI) | ||
25% | 56,6 (48,7 do 68,4) | 41,7 (32,6 do 51,6) |
50% | 114,6 (100,1 do 142,9) | 94,9 (77,7 do 117,0) |
75% | NA (NA do NA) | NA (NA do NA) |
Analiza bez stratyfikacji | ||
Współczynnik ryzyka (sunitynib w porównaniu z IFN-α) | 0,8209 | |
95% CI dla współczynnika ryzyka | (0,6730 do 1,0013) | |
Wartość pa | 0,0510 | |
Skróty: CI = przedział ufności (ang. confidence interval); INF-α = interferon alfa; ITT = populacja ITT (ang. intent-to-treat); N = liczba pacjentów; NA = nie dotyczy; OS = czas przeżycia całkowitego (ang. overall survival); PFS = czas przeżycia bez progresji choroby (ang. progression-free survival);
a Dla dwustronnego testu log- rank
Rak nerkowokomórkowy z przerzutami po niepowodzeniu leczenia cytokinami
Badanie II fazy sunitynibu przeprowadzono u pacjentów opornych na wcześniejsze leczenie cytokinami, tzn. interleukiną-2 lub IFN-α. Sześćdziesięciu trzech pacjentów otrzymało dawkę początkową 50 mg sunitynibu doustnie, raz na dobę przez 4 kolejne tygodnie, po czym następował dwutygodniowy okres przerwy, który kończył pełny cykl 6 tygodni (schemat 4/2). Podstawowym punktem końcowym oceny skuteczności był ORR ustalany na podstawie kryteriów oceny odpowiedzi u pacjentów z guzami litymi (ang. RECIST, Response Evaluation Criteria in Solid Tumours).
W omawianym badaniu wskaźnik obiektywnych odpowiedzi wynosił 36,5% (95% CI: 24,7–49,6%), a
mediana TTP wynosiła 37,7 tygodnia (95% CI: 24,0 – 46,4).
Przeprowadzono potwierdzające, otwarte, obejmujące jedną grupę pacjentów, wieloośrodkowe badanie oceniające skuteczność i bezpieczeństwo stosowania sunitynibu u pacjentów z rakiem nerkowokomórkowym z przerzutami, którzy byli oporni na uprzednio stosowane leczenie cytokinami.
Stu sześciu (106) pacjentów otrzymało co najmniej jedną dawkę 50 mg sunitynibu według schematu
4/2.
Pierwszorzędowym punktem końcowym oceny skuteczności tego badania był ORR. Drugorzędowe punkty końcowe obejmowały TTP, okres utrzymywania się odpowiedzi (DR) i OS.
W niniejszym badaniu wskaźnik ORR wynosił 35,8% (95% CI: 26,8 – 47,5%). Mediany DR i OS nie
zostały jeszcze osiągnięte.
Nowotwory neuroendokrynne trzustki
W dodatkowym wieloośrodkowym badaniu otwartym II fazy oceniano skuteczność i bezpieczeństwo stosowania sunitynibu w dawce 50 mg na dobę w monoterapii w schemacie 4/2 u pacjentów z nieoperacyjnymi pNET. W kohorcie 66 pacjentów z wyspiakiem trzustki, odsetek odpowiedzi na leczenie (główny punkt końcowy badania) wyniósł 17%.
U pacjentów z nieoperacyjnymi pNET przeprowadzono główne, wieloośrodkowe, międzynarodowe, randomizowane, kontrolowane placebo badanie III fazy z zastosowaniem podwójnie ślepej próby, w którym oceniano stosowanie sunitynibu w monoterapii.
Pacjentów z udokumentowaną w ostatnich 12 miesiącach progresją choroby ocenianą wg kryteriów RECIST zrandomizowano (w stosunku 1:1) do grupy otrzymującej sunitynib w dawce 37,5 mg raz na dobę w schemacie ciągłym (N = 86) lub do grupy placebo (N = 85).
Głównym celem badania było porównanie PFS u pacjentów otrzymujących sunitynib i pacjentów otrzymujących placebo. Inne punkty końcowe obejmowały OS, ORR, PRO oraz parametry bezpieczeństwa.
Grupa otrzymująca sunitynib i grupa placebo były porównywalne pod względem charakterystyki demograficznej. Ponadto u 49% pacjentów otrzymujących sunitynib (wobec 52% pacjentów z grupy placebo) występowały nowotwory nieczynne hormonalnie, a u 92% pacjentów w obu badanych grupach stwierdzano przerzuty do wątroby.
W badaniu dozwolone było stosowanie analogów somatostatyny.
Uprzedniemu leczeniu układowemu poddawanych było łącznie 66% pacjentów otrzymujących sunitynib i 72% pacjentów otrzymujących placebo. Ponadto 24% pacjentów otrzymujących sunitynib i 22% pacjentów z grupy placebo otrzymywało w przeszłości analogi somatostatyny.
Stwierdzono klinicznie istotne wydłużenie ocenianego przez badacza PFS w przypadku sunitynibu
w porównaniu z placebo. Mediana PFS wyniosła 11,4 miesiąca w grupie otrzymującej sunitynib i 5,5 miesiąca w grupie placebo [HR: 0,418 (95% CI: 0,263, 0,662), p = 0,0001]; podobne wyniki uzyskano, kiedy w celu ustalenia progresji choroby zastosowano pochodne oceny odpowiedzi na
leczenie oparte na zastosowaniu kryteriów RECIST w pomiarach wielkości nowotworów wykonywanych przez badaczy, co ilustruje Tabela 5. We wszystkich podgrupach wyróżnionych ze względu na oceniane parametry wyjściowe, w tym liczbę rzutów uprzedniego leczenia układowego, stwierdzono HR na korzyść sunitynibu. Łącznie 29 pacjentów z grupy otrzymującej sunitynib i 24 z grupy placebo niepoddawanych było uprzednio żadnemu leczeniu układowemu; wśród tych pacjentów HR dla PFS wyniósł 0,365 (95% CI: 0,156, 0,857), p = 0,0156. Podobnie wśród 57
pacjentów z grupy otrzymującej sunitynib (w tym 28 pacjentów z jednym rzutem leczenia układowego w przeszłości i 29 z dwoma lub większą liczbą rzutów leczenia układowego w przeszłości) oraz wśród 61 pacjentów z grupy placebo (w tym 25 pacjentów z jednym rzutem leczenia układowego
w przeszłości i 36 z dwoma lub większą liczbą rzutów leczenia układowego w przeszłości) HR dla
PFS wyniósł 0,456 (95% CI: 0,264, 0,787), p = 0,0036.
Przeprowadzono analizę wrażliwości PFS w przypadkach, w których progresja choroby stwierdzana była na podstawie zgłaszanych przez badacza wyników pomiaru wielkości nowotworu, i w których dane wszystkich pacjentów ucinane z powodów innych niż przerwanie udziału w badaniu były traktowane jako zdarzenia PFS. Analiza umożliwiła konserwatywną ocenę działania leczniczego sunitynibu i dodatkowo wzmocniła analizę pierwotną, wykazując HR wynoszący 0,507 (95% CI: 0,350, 0,733), p = 0,000193. Główne badanie dotyczące pNET przerwano zgodnie z zaleceniem niezależnej komisji ds. monitorowania leków, a ocenę głównego punktu końcowego oparto na ocenie badaczy - oba czynniki mogły wpłynąć na ocenę działania leczniczego.
W celu wykluczenia błędu systematycznego w dokonywanej przez badaczy ocenie PFS, przeprowadzono ocenę BICR wyników badań obrazowych, która potwierdziła oceny przeprowadzone przez badaczy, co ilustruje Tabela 4.
Tabela 4. Wyniki dotyczące skuteczności leczenia pNET w badaniu III fazy
Parametr skuteczności | Sunitynib (N = 86) | Placebo (N = 85) | Współczynnik ryzyka (95% CI) | Wartość p |
Przeżycie wolne od progresji choroby [mediana, miesiące (95% CI)] na podstawie oceny badacza | 11,4 (7,4, 19,8) | 5,5 (3,6, 7,4) | 0,418 (0,263, 0,662) | 0,0001a |
Przeżycie wolne od progresji choroby [mediana, miesiące (95% CI)] na podstawie pochodnej oceny odpowiedzi na leczenie opartej na zastosowaniu kryteriów RECIST w pomiarach wielkości nowotworów wykonywanych przez badaczy | 12,6 (7,4, 16,9) | 5,4 (3,5, 6,0) | 0,401 (0,252, 0,640) | 0,000066a |
Przeżycie wolne od progresji choroby [mediana, miesiące (95% CI)] na podstawie zaślepionej niezależnej centralnej oceny nowotworu | 12,6 (11,1, 20,6) | 5,8 (3,8, 7,2) | 0,315 (0,181, 0,546) | 0,000015a |
Przeżycie całkowite [5 lat kontroli] [mediana, miesiące (95% CI)] | 38,6 (25,6, 56,4) | 29,1 (16,4, 36,8) | 0,730 (0,504, 1,057) | 0,0940a |
Odsetek obiektywnych odpowiedzi [%, (95% CI)] | 9,3 (3,2, 15,4) | 0 | NA | 0,0066b |
Skróty: CI = przedział ufności (ang. confidence interval); N = liczba pacjentów; NA = nie dotyczy ; pNET = nowotwory neuroendokrynne trzustki (ang. pancreatic neuroendocrine tumours); RECIST = kryteria oceny odpowiedzi u pacjentów z guzami litymi (ang. response evaluation criteria in solid tumours)
a Dwustronny test log- rank bez stratyfikacji
b Dokładny test Fishera
Rycina 1. Wykres Kaplana-Meiera dla PFS w badaniu III fazy dotyczącym pNET
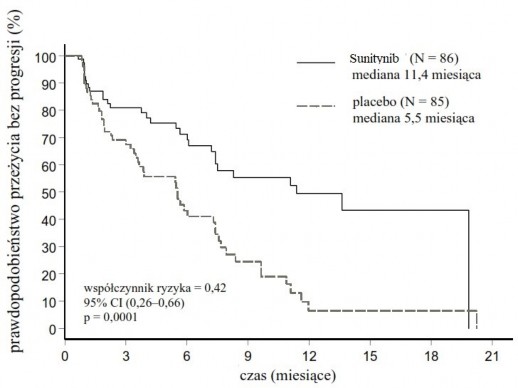
Liczba pacjentów zagrożonych | |||||||
Sunitynib | 86 | 52 | 34 | 20 | 15 | 4 | 2 |
placebo | 85 | 42 | 20 | 9 | 2 | 2 | 2 |
Skróty: CI = przedział ufności; N = liczba pacjentów; PFS = czas przeżycia bez progresji choroby;
pNET = nowotwory neuroendokrynne trzustki
Dane na temat OS nie były wystarczająco dojrzałe w momencie zamknięcia badania {20,6 miesiąca (95% CI: 20,6, NR [nie osiągnięto wartości]) w przypadku grupy sunitynibu, w porównaniu do NR (95% CI: 15,5, NR) dla grupy placebo, HR: 0,409 (95% CI: 0,187, 0,894), wartość p = 0,0204}.
Odnotowano 9 zgonów w grupie leczonej sunitynibem i 21 w grupie placebo.
W momencie stwierdzenia progresji choroby dane pacjentów odkodowano i pacjentom, którzy otrzymywali placebo zaproponowano dostęp do sunitynibu w odrębnym, otwartym badaniu będącym przedłużeniem poprzedniego badania. W wyniku przedwczesnego przerwania badania dane pozostałych pacjentów odkodowano, a pacjentom tym zaproponowano dostęp do sunitynibu w odrębnym, otwartym badaniu będącym przedłużeniem poprzedniego badania. Łącznie 59 spośród 85 pacjentów (69,4%) z grupy placebo przeszło do otwartego badania sunitynibu po wystąpieniu progresji choroby lub odkodowaniu podczas zamknięcia badania. OS obserwowane po 5 latach w przedłużonym badaniu wykazało HR wynoszący 0,730 (95% CI: 0,504, 1,057).
Ocena za pomocą kwestionariusza EORTC QLQ-C30 (European Organization for Research and Treatment of Cancer Quality of Life Questionnaire) wykazała, że ogólna globalna jakość życia związana ze stanem zdrowia oraz 5 domen funkcjonowania (fizyczna, ról społecznych, poznawcza, emocjonalna i społeczna) były utrzymane u pacjentów leczonych sunitynibem w porównaniu z grupą pacjentów otrzymujących placebo przy ograniczonych, objawowych działaniach niepożądanych.
Przeprowadzono międzynarodowe, wieloośrodkowe, jednoramienne badanie otwarte IV fazy, w którym oceniano skuteczność i bezpieczeństwo stosowania sunitynibu u pacjentów z postępującą, zaawansowaną/przerzutową, wysoko zróżnicowaną i nieoperacyjną postacią pNET.
Sunitynib podawano doustnie w dawce 37,5 mg raz na dobę w sposób ciągły 106 pacjentom (61 pacjentom w kohorcie wcześniej nieleczonej i 45 pacjentom w kohorcie otrzymującej sunitynib jako leczenie kolejnego rzutu).
Mediana PFS oceniana przez badacza wynosiła 13,2 miesiąca zarówno w populacji ogólnej (95% CI: 10,9; 16,7) jak i w kohorcie wcześniej nieleczonej (95% CI: 7,4; 16,8).
Dzieci i młodzież
Dane dotyczące stosowania sunitynibu u pacjentów pediatrycznych są ograniczone (patrz punkt 4.2).
Przeprowadzono badanie I fazy ze zwiększeniem dawki sunitynibu podawanego doustnie z udziałem 35 pacjentów, w tym 30 pacjentów z populacji dzieci i młodzieży (w wieku od 3 do 17 lat) i 5 pacjentów z grupy młodych osób dorosłych (w wieku od 18 do 21 lat) z guzami litymi opornymi na leczenie. U większości pacjentów pierwotnie rozpoznano guza mózgu. Kardiotoksyczność ograniczającą wielkość dawki zaobserwowano na pierwszym etapie badania, co wpłynęło na zmianę schematu badania w celu wykluczenia pacjentów z wcześniejszą ekspozycją na terapie potencjalnie kardiotoksyczne (w tym stosowanie antracyklin) lub radioterapię, której zasięg obejmował serce.
Na drugim etapie badania, w którym uwzględniono pacjentów wcześniej poddawanych leczeniu przeciwnowotworowemu, jednakże bez czynników ryzyka wystąpienia kardiotoksyczności, sunitynib był ogólnie tolerowany przez pacjentów i możliwy do kontrolowania klinicznie w dawce 15 mg/m2 pc. dobowo (MTD) według schematu 4/2. U żadnego z pacjentów nie osiągnięto całkowitej ani częściowej odpowiedzi. Stabilizację choroby zaobserwowano u 6 pacjentów (17%). W przypadku jednego pacjenta z nowotworem podścieliskowym przewodu pokarmowego przyjmującego dawkę 15 mg/m2 pc. nie odnotowano korzyści z leczenia. Zaobserwowane działania niepożądane były na ogół podobne do działań niepożądanych występujących u dorosłych pacjentów (patrz punkt 4.8).
Przeprowadzono też otwarte badanie II fazy z udziałem 29 pacjentów, w tym 27 pacjentów z populacji dzieci i młodzieży (w wieku od 3 do 16 lat) i 2 pacjentów z grupy młodych osób dorosłych (w wieku 18 do 19 lat) z HGG lub wyściółczakiem. Badanie to zostało zakończone w momencie planowanej analizy okresowej z powodu niemożności kontrolowania choroby. Mediana PFS w grupie pacjentów
z HGG wyniosła 2,3 miesiąca, a w grupie pacjentów z wyściółczakiem 2,7 miesiąca. Mediana OS w grupie pacjentów z HGG wyniosła 5,1 miesiąca, natomiast w grupie pacjentów z wyściółczakiem 12,3 miesiąca. Najczęstszymi (≥10%) zgłoszonymi zdarzeniami niepożądanymi związanymi z leczeniem u pacjentów w obu grupach łącznie były: obniżona liczba neutrofili [u 6 pacjentów (20,7%)] oraz krwotok śródczaszkowy [u 3 pacjentów (10,3%)] (patrz punkt 4.8).
Dane pochodzące z badania I/II fazy dotyczącego doustnego stosowania sunitynibu u 6 pacjentów z populacji dzieci i młodzieży z GIST w wieku od 13 do 16 lat, którzy otrzymywali sunitynib w schemacie 4/2 w dawkach od 15 mg/m2 pc. na dobę do 30 mg/m2 pc. na dobę, oraz dostępne opublikowane dane (pochodzące od 20 pacjentów z populacji dzieci i młodzieży lub młodych osób dorosłych z GIST) wykazały, że leczenie sunitynibem spowodowało stabilizację choroby u 18 z 26
(69,2%) pacjentów, u których stwierdzono niepowodzenie leczenia imatynibem lub jego nietolerancję (16 pacjentów z chorobą stabilną z 21) albo pacjentów de novo lub po zabiegu operacyjnym (2 pacjentów z chorobą stabilną z 5). W badaniu fazy 1/2 obserwowano stabilizację choroby u 3 z 6 pacjentów oraz progresję choroby również u 3 z 6 pacjentów (1 pacjent otrzymał leczenie neoadiuwantowe oraz 1 pacjent otrzymał leczenie uzupełniające [adiuwantowe] imatinibem).
W omawianym badaniu I/II fazy u 4 z 6 pacjentów (66,7%) wystąpiły zdarzenia niepożądane 3. lub 4. stopnia nasilenia (zdarzenia o 3. stopniu nasilenia: hipofosfatemia, neutropenia i małopłytkowość, przy czym każde z nich wystąpiło u 1 pacjenta oraz neutropenia o 4. stopniu nasilenia – u 1 pacjenta. Ponadto w publikacjach raportowano następujące działania niepożądane 3. stopnia nasilenia związane z lekiem, które wystąpiły u 5 pacjentów: zmęczenie (2), zaburzenia żołądkowo-jelitowe łącznie z
biegunką (2), zaburzenia hematologiczne łącznie z anemią (2), zapalenie pęcherzyka żółciowego (1), nadczynność tarczycy (1), zapalenie błony śluzowej (1).
Przeprowadzono analizę farmakokinetyczną populacji (PK) oraz analizę farmakokinetyczno- farmakodynamiczną (PK/PD) w zakresie ekstrapolacji farmakokinetyki oraz głównych punktów końcowych wymaganych do oceny bezpieczeństwa i skuteczności stosowania sunitynibu u dzieci i młodzieży z GIST (w wieku od 6 do 17 lat). Analiza została oparta na danych zebranych od dorosłych pacjentów z GIST lub guzami litymi oraz od dzieci i młodzieży z guzami litymi. Na
podstawie analiz modelowania nie wydaje się, aby młody wiek pacjentów oraz drobniejsza budowa ciała wpływały negatywnie na reakcje organizmu w zakresie skuteczności i bezpieczeństwa ekspozycji na sunitynib w osoczu. Nie stwierdzono, aby na stosunek korzyści do ryzyka sunitynibu negatywnie wpływały młody wiek lub drobniejsza budowa ciała pacjentów. Na ten stosunek głównie wpływa ekspozycja na ten lek w osoczu.
EMA uchyliła obowiązek dołączania wyników badań sunitynibu we wszystkich podgrupach populacji
dzieci i młodzieży w leczeniu raka nerkowokomórkowego lub raka miedniczki nerkowej
(z wyłączeniem nerczaka płodowego, nefroblastomatozy, mięsaka jasnokomórkowego, nerczaka
mezoblastycznego, raka rdzeniastego nerki i nowotworu rabdoidalnego nerki) (patrz punkt 4.2).
EMA uchyliła obowiązek dołączania wyników badań sunitynibu we wszystkich podgrupach populacji
dzieci i młodzieży w leczeniu nowotworów neuroendokrynnych żołądka, jelit i trzustki
(z wyłączeniem nerwiaka płodowego, neuroganglioblastoma i guza chromochłonnego nadnerczy)
(patrz punkt 4.2).
Właściwości farmakokinetyczne sunitynibu oceniono w badaniach obejmujących 135 zdrowych ochotników i 266 pacjentów z guzami litymi. Właściwości farmakokinetyczne były podobne we wszystkich badanych populacjach pacjentów z guzami litymi i u zdrowych ochotników.
W zakresie dawkowania od 25 do 100 mg pole pod krzywą zależności stężenia leku w osoczu od czasu (AUC) i Cmax zwiększa się proporcjonalnie do dawki. Podczas kilkakrotnego podania w ciągu doby sunitynib ulega kumulacji, przy czym jego stężenie zwiększa się 3–4-krotnie, a stężenie jego podstawowego czynnego metabolitu zwiększa się 7–10-krotnie. Stężenie sunitynibu i jego podstawowego czynnego metabolitu w stanie równowagi zostaje osiągnięte w ciągu od 10 do 14 dni. Do 14. dnia łączne stężenie osoczowe sunitynibu i jego podstawowego czynnego metabolitu wynosi 62,9–101 ng/ml, co jest docelowym stężeniem przewidywanym na podstawie danych z badań przedklinicznych jako stężenie hamujące fosforylację receptorów in vitro, prowadzącym do zatrzymania i (lub) zmniejszenia wzrostu guzów in vivo. Podstawowy czynny metabolit odpowiada za 23% do 37% całkowitej ekspozycji na lek. Nie obserwuje się istotnych zmian farmakokinetyki sunitynibu lub jego podstawowego czynnego metabolitu podczas kilkakrotnego podawania leku w ciągu doby, lub w trakcie powtarzanych cyklów badanych schematów dawkowania.
Wchłanianie
Po podaniu doustnym sunitynibu Cmax stwierdza się na ogół po upływie 6–12 godzin (tmax - czas od
podania do osiągnięcia stężenia maksymalnego).
Pokarm nie wpływa na dostępność biologiczną sunitynibu.
Dystrybucja
W badaniach in vitro stopień wiązania się sunitynibu i jego podstawowego czynnego metabolitu z ludzkimi białkami osocza wynosił odpowiednio 95% i 90% niezależnie od stężenia. Pozorna objętość dystrybucji (Vd) w przypadku sunitynibu była znaczna – 2230 l, co wskazuje na penetrację leku do tkanek.
Interakcje metaboliczne
Obliczone in vitro wartości stałej Ki dla wszystkich badanych izoenzymów cytochromu P450 (CYP)
(CYP1A2, CYP2A6, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6, CYP2E1, CYP3A4/5 i
CYP4A9/11) wskazują na to, że sunitynib i jego podstawowy czynny metabolit prawdopodobnie nie przyspieszają w stopniu istotnym klinicznie metabolizmu substancji czynnych metabolizowanych przez te enzymy.
Metabolizm
Sunitynib jest metabolizowany głównie przez izoenzym CYP3A4, izoformę CYP, która katalizuje reakcję powstawania głównego czynnego metabolitu dezetylosunitynibu podlegającego dalszemu metabolizmowi katalizowanemu przez ten sam izoenzym.
Należy unikać jednoczesnego podawania sunitynibu z silnymi induktorami lub inhibitorami CYP3A4,
ponieważ stężenie sunitynibu w osoczu może ulec zmianie (patrz punkty 4.4 i 4.5).
Eliminacja
Substancja czynna jest wydalana głównie z kałem (61%), natomiast przez nerki ulega wydaleniu 16% podanej dawki w postaci niezmienionej i metabolitów. Sunitynib i jego podstawowy czynny metabolit były głównymi związkami wykrywanymi w osoczu, moczu i kale, odpowiadając odpowiednio za 91,5%, 86,4% i 73,8% radioaktywności w zebranych próbkach. Pozostałe metabolity zostały zidentyfikowane w moczu i w kale, jednak na ogół nie były wykrywane w osoczu. Całkowity klirens leku po podaniu doustnym (CL/F) wynosił 34–62 l/h. Po podaniu doustnym zdrowym ochotnikom okres półtrwania sunitynibu i jego podstawowego czynnego metabolitu dietylowego wynosił odpowiednio około 40–60 godzin i 80–110 godzin.
Jednoczesne podawanie z produktami leczniczymi będącymi inhibitorami BCRP
W warunkach in vitro sunitynib jest substratem BCRP (białka oporności raka piersi), zaliczanego do transporterów czynnie usuwających substraty poza komórkę. W badaniu A6181038 jednoczesne podawanie z gefitynibem, który jest inhibitorem BCRP, nie wpływało w sposób klinicznie istotny na wartości Cmax i AUC sunitynibu ani łącznie sunitynibu i jego metabolitu (patrz punkt 4.5). Było to badanie wieloośrodkowe, otwarte, I/II fazy, mające na celu ocenę bezpieczeństwa i tolerancji, ustalenie maksymalnej tolerowanej dawki oraz aktywności przeciwnowotworowej sunitynibu w skojarzeniu z gefitynibem u pacjentów z MRCC. Jako drugorzędowy punkt końcowy badania oceniano parametry farmakokinetyczne gefitynibu (podawanego w dawce dobowej 250 mg) i sunitynibu [podawanego w dawce dobowej 37,5 mg w kohorcie nr 1 (n = 4) i 50 mg w kohorcie nr 2 (n = 7) w schemacie 4 tygodnie leczenia i 2 tygodnie przerwy] w okresach jednoczesnego podawania. Zmiany wartości parametrów farmakokinetycznych sunitynibu nie były klinicznie istotne ani nie wskazywały na występowanie jakichkolwiek interakcji międzylekowych, jednak ze względu na stosunkowo małą liczbę uczestników badania (N = 7 + 4) i umiarkowaną do dużej zmienność osobniczą w zakresie parametrów farmakokinetycznych uzyskane w tym badaniu wyniki dotyczące farmakokinetycznych interakcji międzylekowych należy interpretować z ostrożnością.
Wybrane grupy populacji
Zaburzenia czynności wątroby
Sunitynib i jego główny metabolit są metabolizowane przede wszystkim przez wątrobę. Całkowity wpływ na organizm sunitynibu podanego w pojedynczej dawce był podobny u pacjentów z łagodnymi lub umiarkowanymi zaburzeniami czynności wątroby (stopnia A i B według klasyfikacji Childa-Pugh) w porównaniu z pacjentami z prawidłową czynnością wątroby. Nie przeprowadzono badań z sunitynibem stosowanym u pacjentów z ciężkimi zaburzeniami czynności wątroby (stopnia C według klasyfikacji Childa-Pugh).
Z badań u pacjentów z nowotworami wykluczono pacjentów z aktywnością AlAT lub AspAT przekraczającą o ponad 2,5 x górną granicę normy, lub o ponad 5,0 x górną granicę normy, gdy zwiększenie to wiązało się z przerzutami do wątroby.
Zaburzenia czynności nerek
Populacyjne analizy farmakokinetyki wykazały, że klirens pozorny sunitynibu (CL/F) nie jest
uzależniony od klirensu kreatyniny (CLcr) w ocenianym zakresie stężeń (42–347 ml/min). Ekspozycja
ogólnoustrojowa po pojedynczej dawce sunitynibu była podobna u pacjentów z ciężkimi zaburzeniami czynności nerek (CLcr < 30 ml/min) i u pacjentów z prawidłową czynnością nerek (CLcr > 80 ml/min). Mimo, iż sunitynib i jego główny metabolit nie były eliminowane przez hemodializę u pacjentów z ESRD, całkowita ekspozycja ogólnoustrojowa była mniejsza o 47% dla sunitynibu i 31% dla głównego metabolitu w porównaniu z pacjentami z prawidłową czynnością nerek.
Masa ciała, sprawność fizyczna
Analiza danych demograficznych pod kątem farmakokinetyki populacyjnej wskazuje, że nie ma konieczności dostosowania dawki początkowej w zależności od masy ciała i sprawności fizycznej ocenianej za pomocą kwestionariusza Eastern Cooperative Oncology Group (ECOG).
Płeć
Dostępne dane wskazują, że kobiety mogą mieć o około 30% mniejszy pozorny klirens (CL/F) sunitynibu w porównaniu do mężczyzn: różnica ta nie wymaga jednak dostosowywania dawki początkowej.
Dzieci i młodzież
Dane dotyczące stosowania sunitynibu u dzieci i młodzieży są ograniczone (patrz punkt 4.2). Analizy farmakokinetyki populacji zbiorczych danych zebranych od dorosłych pacjentów z GIST i guzami litymi oraz od dzieci i młodzieży z guzami litymi zostały zakończone. Przeprowadzono analizy krokowego modelowania zmiennych kowariancji (ang. stepwise covariate modelling analyses) w celu oceny wpływu wieku oraz rozmiaru ciała (całkowitej masy ciała lub powierzchni ciała), jak również innych zmiennych kowariancji na istotne parametry farmakokinetyczne dla sunitynibu oraz jego czynnego metabolitu. Spośród analizowanych zmiennych związanych z wiekiem i rozmiarem ciała, wiek znacząco wpływał na pozorny klirens sunitynibu (zależność: im młodszy wiek pacjenta pediatrycznego, tym mniejszy pozorny klirens). W podobny sposób powierzchnia ciała znacząco wpływała na pozorny klirens czynnego metabolitu (zależność: im mniejsza powierzchnia ciała, tym mniejszy pozorny klirens).
Ponadto na podstawie zintegrowanej populacyjnej analizy farmakokinetycznej danych zbiorczych uzyskanych z 3 badań klinicznych przeprowadzonych z udziałem dzieci i młodzieży w wieku od 6 do 11 lat i od 12 do 17 lat (2 badania kliniczne przeprowadzone z udziałem dzieci i młodzieży z guzami litymi i 1 badanie kliniczne z udziałem dzieci i młodzieży z GIST) wyjściowe pole powierzchni ciała (BSA, od ang. body surface area) stanowiło istotną współzmienną, która wpływała na pozorny klirens sunitynibu i jego czynnego metabolitu. Opierając się na niniejszej analizie, przewiduje się, że po podaniu dawki około 20 mg/m2 pc. na dobę (zakres BSA: 1,10–1,87 m2) u dzieci i młodzieży uzyska się porównywalną ekspozycję na sunitynib i jego czynny metabolit w osoczu (pomiędzy 75 % a 125 % AUC), jak u dorosłych pacjentów z GIST leczonych dawką 50 mg na dobę według schematu 4/2 (AUC 1233 ng*h/ml) W badaniach pediatrycznych, dawka początkowa sunitynibu wynosiła 15 mg/m2 pc. (bazując na MTD ustalonej w badaniu fazy I z eskalacją dawki, patrz punkt 5.1), która u pacjentów z populacji dzieci i młodzieży z GIST została zwiększona do 22,5 mg/m2 pc., a następnie do 30 mg/m2 pc. (tak aby nie przekroczyć dawki całkowitej wynoszącej 50 mg na dobę) bazując na indywidualnym bezpieczeństwie/tolerancji pacjenta. Co więcej, zgodnie z opublikowanymi danymi literaturowymi u pacjentów z populacji dzieci i młodzieży z GIST, obliczona dawka początkowa, która mieściła się w zakresie od 16,6 mg/m2 pc. do 36 mg/m2 pc., uległa zwiększeniu do 40,4 mg/m2 pc. (nie przekraczając dawki całkowitej wynoszącej 50 mg na dobę).
W trwających do 9 miesięcy badaniach toksyczności po podaniu wielokrotnym u szczurów i małp stwierdzono, że podstawowymi narządami, na które wpływa lek, są: przewód pokarmowy (nudności i biegunki u małp), nadnercza (przekrwienie kory i (lub) krwotoki u szczurów i małp, z martwicą i następującym po niej włóknieniem u szczurów), układ limfatyczny i krwiotwórczy (zmniejszenie liczby komórek szpiku kostnego i zanik tkanki limfoidalnej grasicy, śledziony i węzłów chłonnych), zewnątrzwydzielnicza część trzustki (degranulacja komórek pęcherzykowych z martwicą pojedynczych komórek), ślinianki (przerost gronek), stawy (zgrubienie płytki wzrostu), macica (zanik) i jajniki (zmniejszony wzrost pęcherzyków). Wszystkie wyniki uzyskano przy istotnych klinicznie
poziomach stężenia osoczowego sunitynibu. Dodatkowe działania produktu obserwowane w innych badaniach obejmowały: wydłużenie odstępu QTc, zmniejszenie LVEF, zanik kanalików jądrowych, rozrost komórek mezangium w nerkach, krwotok z przewodu pokarmowego i do jamy ustnej, i przerost komórek płata przedniego przysadki. Uważa się, że zmiany w obrębie macicy (zanik błony śluzowej) i płytki wzrostowej kości (zgrubienie nasad kostnych lub dysplazja chrząstki) są związane z działaniem farmakologicznym sunitynibu. Większość z tych zmian była odwracalna po upływie od 2 do 6 tygodni od zakończenia leczenia.
Genotoksyczność
Potencjalne działanie genotoksyczne sunitynibu oceniano zarówno in vitro, jak i in vivo. Sunitynib nie wykazywał właściwości mutagennych w badaniach na bakteriach z zastosowaniem aktywacji metabolicznej przez wątrobę szczura. Sunitynib nie indukował strukturalnych aberracji chromosomalnych w ludzkich limfocytach krwi obwodowej in vitro. Obserwowano poliploidię (liczbowe aberracje chromosomalne) w ludzkich limfocytach krwi obwodowej in vitro, zarówno w przypadku zastosowania aktywacji metabolicznej, jak i bez niej. Sunitynib nie wykazywał działania klastogennego w szczurzym szpiku kostnym in vivo. Nie oceniano jego podstawowego czynnego metabolitu pod kątem potencjalnej genotoksyczności.
Działanie rakotwórcze
W trwającym 1 miesiąc badaniu określającym zakres wielkości dawek podawanych doustnie (0, 10, 25, 75 lub 200 mg/kg mc. na dobę) w sposób ciągły u myszy transgenicznych rasH2, rak i rozrost gruczołów Brunner’a w dwunastnicy obserwowano przy największej badanej dawce (200 mg/kg mc. na dobę).
Trwające 6 miesięcy badanie rakotwórczości, po codziennym podaniu doustnym (0, 8, 25, 75 [zmniejszone do 50] mg/kg mc. na dobę), przeprowadzono na myszach transgenicznych rasH2. Podczas stosowania dawek ≥ 25 mg/kg mc. na dobę po 1 miesiącu lub 6 miesiącach leczenia (ekspozycja ≥ 7,3 razy większa niż AUC u pacjentów otrzymujących zalecaną dawkę dobową) obserwowano przypadki raka żołądka i dwunastnicy, zwiększoną częstość występowania złośliwego śródbłoniaka krwionośnego w tle i (lub) hiperplazji błony śluzowej żołądka.
W trwającym 2 lata badaniu rakotwórczości u szczurów (0, 0,33, 1 lub 3 mg/kg mc. na dobę), podawanie sunitynibu w 28-dniowych cyklach, po których następowała 7-dniowa przerwa, powodowało zwiększenie odsetka guzów chromochłonnych i rozrostu rdzenia nadnerczy u samców szczurów po podaniu 3 mg/kg mc. na dobę przez > 1 rok (ekspozycja ≥ 7,8 razy większa niż AUC u pacjentów otrzymujących zalecaną dawkę dobową). Rak gruczołów Brunner’a w dwunastnicy wystąpił po dawce ≥ 1 mg/kg mc. na dobę u samic szczurów i po dawce 3 mg/kg mc. na dobę
u samców szczurów, a rozrost komórek błony śluzowej był jednoznaczny w gruczołach żołądka po dawce 3 mg/kg mc. na dobę u samców szczurów, co stanowiło odpowiednio ≥ 0,9, 7, 8 i 7,8 razy większą ekspozycję niż AUC u pacjentów otrzymujących zalecaną dawkę dobową. Nie ustalono znaczenia dla ludzi obserwowanych u mysz transgenicznych rasH2 i szczurów nowotworów w badaniach nad rakotwórczością sunitynibu.
Toksyczny wpływ na rozród i rozwój potomstwa
W badaniach toksycznego wpływu na rozród szczurów nie stwierdzono wpływu produktu na płodność samców lub samic. Jednak w badaniach toksyczności po podaniu wielokrotnym przeprowadzonych na szczurach i małpach obserwowano oddziaływanie leku na płodność samic w postaci atrezji pęcherzyków, zwyrodnienia ciałek żółtych, zmian błony śluzowej macicy oraz zmniejszenia masy macicy i jajników przy klinicznie istotnych poziomach ekspozycji układowej. U szczurów obserwowano wpływ leku na płodność samców w postaci zaniku kanalików jąder, zmniejszenia liczby plemników w najądrzach i zmniejszenia ilości koloidu w obrębie gruczołu krokowego i pęcherzyków nasiennych przy poziomach ekspozycji osoczowej 25 razy większych niż narażenie ogólnoustrojowe u ludzi.
U szczurów śmiertelność zarodków i płodów przejawiała się istotnym zmniejszeniem liczby żywych płodów, zwiększoną liczbą resorpcji, wzrostem utrat ciąży po zagnieżdżeniu zarodka i całkowitą utratą miotów u 8 z 28 samic ciężarnych przy poziomach stężenia leku w osoczu 5,5 razy większych niż
narażenie ogólnoustrojowe u ludzi. U królików redukcja masy macicy samic ciężarnych i liczby żywych płodów była związana ze zwiększeniem liczby resorpcji, wzrostem liczby utrat ciąży po zagnieżdżeniu zarodka i całkowitą utratą miotów u 4 z 6 samic ciężarnych przy poziomach stężenia leku w osoczu 3 razy większych niż narażenie ogólnoustrojowe u ludzi. Stosowanie sunitynibu u szczurów w okresie organogenezy w dawce ≥ 5 mg/kg mc./dobę prowadziło do zmian rozwojowych, polegających na zwiększonej częstości występowania wad rozwojowych szkieletu płodu, charakteryzujących się przede wszystkim opóźnieniem kostnienia kręgów piersiowych i (lub) lędźwiowych i obserwowanych przy poziomach stężenia leku w osoczu 5,5 razy większych niż narażenie ogólnoustrojowe u ludzi. U królików wpływ leku na rozwój polegał na zwiększeniu częstości występowania rozszczepu wargi przy poziomach stężenia leku w osoczu w przybliżeniu odpowiadających poziomom obserwowanym w warunkach klinicznych u ludzi oraz rozszczepu wargi i rozszczepu podniebienia przy poziomach stężenia leku w osoczu 2,7 razy większych niż narażenie ogólnoustrojowe u ludzi.
Sunitynib (0,3, 1,0 lub 3,0 mg/kg mc. na dobę) był oceniany w prenatalnym i postnatalnym badaniu rozwoju potomstwa u ciężarnych szczurów. Przyrost masy ciała matki był zmniejszony podczas ciąży i laktacji po dawce > 1 mg/kg mc. na dobę, ale nie obserwowano toksycznego wpływu na rozród do dawki 3 mg/kg mc. na dobę (szacowana ekspozycja ≥ 2,3 razy większa niż AUC u pacjentów otrzymujących zalecaną dawkę dobową). Zmniejszenie masy ciała potomstwa obserwowano w okresie przed odstawieniem od piersi i po odstawieniu od piersi po dawce 3 mg/kg mc. na dobę. Nie obserwowano toksycznego wpływu na rozród po dawce 1 mg/kg mc. na dobę (przybliżona ekspozycja
≥ 0,9 razy większa niż AUC u pacjentów otrzymujących zalecaną dawkę dobową).
12,5 mg kapsułki twarde Zawartość kapsułki Mannitol (E 421) Kroskarmeloza sodowa Powidon K-25 Hypromeloza 4 mPas Magnezu stearynian
Osłonka kapsułki (wieczko):
Erytrozyna (E 127) Tytanu dwutlenek (E 171) Indygotyna (E 132) Żelatyna
Osłonka kapsułki (korpus):
Indygotyna (E 132)
Erytrozyna (E 127) Tytanu dwutlenek (E 171) Żelatyna
25 mg kapsułki twarde Zawartość kapsułki Mannitol (E 421) Kroskarmeloza sodowa Powidon K-25 Hypromeloza 4 mPas Magnezu stearynian
Osłonka kapsułki (wieczko):
Żelaza tlenek żółty (E 172) Tytanu dwutlenek (E 171) Żelatyna
Osłonka kapsułki (korpus):
Indygotyna (E 132)
Erytrozyna (E 127) Tytanu dwutlenek (E 171) Żelatyna
50 mg kapsułki twarde Zawartość kapsułki Mannitol (E 421) Kroskarmeloza sodowa Powidon K-25 Hypromeloza 4 mPas Magnezu stearynian
Osłonka kapsułki (wieczko):
Tytanu dwutlenek (E 171) Żelaza tlenek żółty (E 172) Żelatyna
Osłonka kapsułki (korpus):
Tytanu dwutlenek (E 171) Żelaza tlenek żółty (E 172) Żelatyna
Nie dotyczy.
3 lata
Przechowywać w temperaturze poniżej 30°C. Przechowywać w oryginalnym opakowaniu w celu ochrony przed światłem.
Blister PVC/Aclar(PCTFE)/PVC/Aluminium w tekturowym pudełku, zawierający 28 kapsułek.
Bez specjalnych wymagań.
DO OBROTU
Przedsiębiorstwo Farmaceutyczne LEK-AM Sp. z o.o. ul. Ostrzykowizna 14A
05-170 Zakroczym
Subinit 12,5 mg kapsułki twarde: 26006
Subinit 25 mg kapsułki twarde: 26007
Subinit 50 mg kapsułki twarde: 26008
DATA PRZEDŁUŻENIA POZWOLENIA
Data wydania pierwszego pozwolenia na dopuszczenie do obrotu: 09.09.2020 r.
CHARAKTERYSTYKI PRODUKTU LECZNICZEGO
14.01.2022










