Spis treści:
- NAZWA PRODUKTU LECZNICZEGO
- SKŁAD JAKOŚCIOWY I ILOŚCIOWY
- POSTAĆ FARMACEUTYCZNA
- SZCZEGÓŁOWE DANE KLINICZNE
- WŁAŚCIWOŚCI FARMAKOLOGICZNE
- DANE FARMACEUTYCZNE
- PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU
- NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
- DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU I DATA PRZEDŁUŻENIA POZWOLENIA
- DATA ZATWIERDZENIA LUB CZĘŚCIOWEJ ZMIANY TEKSTU CHARAKTERYSTYKI PRODUKTU LECZNICZEGO
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
NAZWA PRODUKTU LECZNICZEGO
SKŁAD JAKOŚCIOWY I ILOŚCIOWY
POSTAĆ FARMACEUTYCZNA
SZCZEGÓŁOWE DANE KLINICZNE
Wskazania do stosowania
Dawkowanie i sposób podawania
Antykoncepcja hormonalna nie była uprzednio stosowana (w poprzednim miesiącu): Przyjmowanie tabletek należy rozpocząć 1. dnia naturalnego cyklu miesiączkowego (tj. pierwszego dnia krwawienia miesiączkowego).
Przyjmowanie tabletek można rozpocząć w dniach od 2. do 5., ale w takim przypadku przez pierwsze 7 dni cyklu zaleca się stosowanie dodatkowej metody antykoncepcji mechanicznej.
Zmiana z innego złożonego hormonalnego środka antykoncepcyjnego (złożone doustne środki antykoncepcyjne, system terapeutyczny dopochwowy lub system transdermalny)
Przyjmowanie produktu Liberelle należy najlepiej rozpocząć kolejnego dnia po przyjęciu aktywnej tabletki poprzedniego złożonego doustnego środka antykoncepcyjnego (ostatniej tabletki zawierającej substancję czynną), ale nie później niż następnego dnia po zakończeniu typowej przerwy
w przyjmowaniu tabletek lub po przyjęciu tabletek placebo poprzedniego złożonego doustnego środka antykoncepcyjnego. Jeśli stosowany był dopochwowy system terapeutyczny lub system transdermalny, kobieta powinna rozpocząć przyjmowanie produktu leczniczego Liberelle najlepiej
w dniu ich usunięcia, ale najpóźniej w dniu, kiedy powinna nastąpić kolejna aplikacja dotychczasowego systemu.
Zmiana z produktu zawierającego wyłącznie progestagen (tabletki zawierające tylko progestagen, wstrzyknięcia, implanty), lub z domacicznego systemu terapeutycznego uwalniającego progestagen (IUS, ang. Intrauterine System)
Zmiana z produktu zawierającego wyłącznie progestagen może być przeprowadzona w dowolnym dniu cyklu (w przypadku implantu lub IUS w dniu ich usunięcia, w przypadku produktu stosowanego we wstrzyknięciu – w dniu, gdy powinno zostać wykonane następne wstrzyknięcie). Jednak we wszystkich tych przypadkach, przez pierwsze 7 dni przyjmowania tabletek zaleca się zastosowanie dodatkowej metody antykoncepcji mechanicznej.
Po poronieniu w pierwszym trymestrze ciąży
Pacjentka może natychmiast rozpocząć przyjmowanie produktu. Wówczas nie jest konieczne stosowanie dodatkowych metod antykoncepcyjnych.
Po porodzie lub poronieniu w drugim trymestrze ciąży
Należy poinformować kobietę, że przyjmowanie tabletek należy rozpocząć pomiędzy 21. a 28. dniem po porodzie lub po poronieniu w drugim trymestrze ciąży. W przypadku późniejszego rozpoczęcia przyjmowania tabletek, należy poinformować pacjentkę o konieczności stosowania dodatkowo, przez pierwsze 7 dni, metody antykoncepcji mechanicznej. Jeśli doszło do stosunku, przed rozpoczęciem stosowania produktu leczniczego należy upewnić się, że pacjentka nie jest w ciąży lub poczekać do wystąpienia pierwszego krwawienia miesiączkowego.
Stosowanie produktu w okresie karmienia piersią, patrz punkt 4.6.
Postępowanie w przypadku pominięcia przyjmowania tabletek
Jeżeli od czasu planowego przyjęcia tabletki upłynęło mniej niż 12 godzin, skuteczność antykoncepcji nie jest zmniejszona. Należy przyjąć tabletkę najszybciej jak to możliwe, a kolejne tabletki przyjmować o zwykłej porze.
Jeżeli od czasu planowego przyjęcia tabletki upłynęło więcej niż 12 godzin, skuteczność antykoncepcji może być zmniejszona. W takim przypadku należy postępować zgodnie
z następującymi dwiema podstawowymi zasadami:
Przeciwwskazania
Występowanie lub ryzyko żylnej choroby zakrzepowo-zatorowej:
żylna choroba zakrzepowo-zatorowa - czynna (leczona przeciwzakrzepowymi produktami leczniczymi) lub przebyta żylna choroba zakrzepowo-zatorowa (np. zakrzepica żył głębokich lub zatorowość płucna);
znana dziedziczna lub nabyta predyspozycja do występowania żylnej choroby zakrzepowo- zatorowej, np. oporność na aktywowane białko C (w tym czynnik V Leiden), niedobór antytrombiny III, niedobór białka C, niedobór białka S;
rozległy zabieg operacyjny związany z długotrwałym unieruchomieniem (patrz punkt 4.4);
wysokie ryzyko żylnej choroby zakrzepowo-zatorowej wskutek występowania wielu czynników ryzyka (patrz punkt 4.4).
Występowanie lub ryzyko tętniczych zaburzeń zakrzepowo-zatorowych:
tętnicze zaburzenia zakrzepowo-zatorowe - czynne lub przebyte (np. zawał mięśnia sercowego) lub objawy prodromalne (np. dławica piersiowa);
choroby naczyń mózgowych - czynny udar, przebyty udar lub objawy prodromalne w wywiadzie (np. przemijający napad niedokrwienny);
stwierdzona dziedziczna lub nabyta skłonność do występowania tętniczych zaburzeń zakrzepowo-zatorowych np. hiperhomocysteinemia i obecność przeciwciał antyfosfolipidowych (przeciwciała antykardiolipinowe, antykoagulant toczniowy);
migrena z ogniskowymi objawami neurologicznymi w wywiadzie;
wysokie ryzyko zaburzeń zakrzepowo-zatorowych tętnic z powodu występowania wielu czynników ryzyka (patrz punkt 4.4) lub występowania jednego z poważnych czynników ryzyka, takich jak:
cukrzyca z powikłaniami naczyniowymi,
ciężkie nadciśnienie tętnicze,
ciężka dyslipoproteinemia.
Występująca obecnie lub w przeszłości ciężka choroba wątroby do momentu powrotu wyników prób czynnościowych wątroby do prawidłowych wartości
Występujący obecnie lub w przeszłości guz wątroby (łagodny lub złośliwy)
Potwierdzenie lub podejrzenie wystąpienia nowotworów złośliwych narządów płciowych lub piersi, zależnych od hormonów płciowych
Przerost endometrium
Krwawienie z dróg rodnych o nieustalonej etiologii
Żółtaczka cholestatyczna podczas ciąży lub żółtaczka podczas poprzedniego stosowania środka antykoncepcyjnego
Powikłana choroba zastawek serca
Występujące obecnie lub w przeszłości zapalenie trzustki z towarzyszącą ciężką hipertriglicerydemią
Nadwrażliwość na substancje czynne lub na którąkolwiek substancję pomocniczą wymienioną w punkcie 6.1.
Przeciwskazane jest jednoczesne stosowanie produktu leczniczego Liberelle z produktami leczniczymi zawierającymi ombitaswir, parytaprewir, rytonawir lub dazabuwir lub produktami leczniczymi zawierającymi glekaprewir z pibrentaswirem lub sofosbuwir z welpataswirem i woksylaprewirem (patrz punkty 4.5).
Jeśli którykolwiek z powyższych stanów wystąpi po raz pierwszy podczas stosowania produktu leczniczego Liberelle, należy natychmiast przerwać przyjmowanie tabletek.
Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania
Objawy zakrzepicy żył głębokich (DVT) mogą obejmować:
obrzęk nogi i (lub) stopy lub obrzęk wzdłuż żyły w nodze;
ból lub tkliwość w nodze, które mogą być odczuwane wyłącznie w czasie stania lub chodzenia;
zwiększona temperatura w zmienionej chorobowo nodze; czerwona lub przebarwiona skóra nogi.
Objawy zatorowości płucnej (ang. Pulmonary Embolism, PE) mogą obejmować:
nagły napad niewyjaśnionego spłycenia oddechu lub przyspieszenia oddechu;
nagły napad kaszlu, który może być połączony z krwiopluciem;
ostry ból w klatce piersiowej;
ciężkie zamroczenie lub zawroty głowy;
przyspieszone lub nieregularne bicie serca.
Niektóre z tych objawów (np. spłycenie oddechu, kaszel) są niespecyficzne i mogą być niepoprawnie zinterpretowane jako występujące częściej lub mniej poważne stany (np. zakażenia układu oddechowego).
Inne objawy zamknięcia naczyń mogą obejmować: nagły ból, obrzęk oraz lekko niebieskie przebarwienie kończyn.
Jeżeli zamknięcie naczynia wystąpi w oku, objawy mogą obejmować bezbolesne zaburzenia widzenia, które mogą przekształcić się w utratę widzenia. W niektórych przypadkach utrata widzenia może nastąpić niemal natychmiast.
Ryzyko tętniczych zaburzeń zakrzepowo-zatorowych (ATE)
Badania epidemiologiczne wykazały związek pomiędzy stosowaniem hormonalnych środków antykoncepcyjnych a zwiększonym ryzykiem tętniczych zaburzeń zakrzepowo-zatorowych (np. zawału mięśnia sercowego) lub incydentów naczyniowo-mózgowych (np. przemijającego napadu niedokrwiennego, udaru). Przypadki tętniczych zaburzeń zakrzepowo-zatorowych mogą być śmiertelne.
Czynniki ryzyka tętniczych zaburzeń zakrzepowo-zatorowych (ATE)
Ryzyko wystąpienia tętniczych powikłań zakrzepowo-zatorowych lub napadów naczyniowo- mózgowych u kobiet stosujących złożone hormonalne środki antykoncepcyjne jest zwiększone w przypadku występowania czynników ryzyka (patrz tabela). Stosowanie produktu leczniczego
Liberelle jest przeciwwskazane, jeżeli u pacjentki występuje jeden poważny lub jednocześnie kilka czynników ryzyka tętniczych zaburzeń zakrzepowo-zatorowych, które stawiają pacjentkę w grupie wysokiego ryzyka zakrzepicy tętniczej (patrz punkt 4.3). Jeśli u kobiety występuje więcej niż jeden czynnik ryzyka, możliwe jest, że wzrost ryzyka będzie większy niż suma pojedynczych czynników – w tym przypadku należy ocenić całkowite ryzyko. Jeśli ocena stosunku korzyści do ryzyka jest negatywna, nie należy przepisywać złożonych hormonalnych środków antykoncepcyjnych (patrz punkt 4.3).
Tabela: Czynniki ryzyka tętniczych zaburzeń zakrzepowo-zatorowych
Czynnik ryzyka
Uwagi
Wiek
Szczególnie wiek powyżej 35 lat
Palenie
Należy dokładnie pouczyć kobiety, aby nie paliły, jeśli zamierzają stosować złożone hormonalne środki antykoncepcyjne.
Kobietom w wieku powyżej 35 lat, które nie zaprzestały palenia, należy stanowczo doradzić stosowanie innej metody
antykoncepcji.
Nadciśnienie tętnicze
Otyłość (wskaźnik masy ciała - BMI - powyżej 30 kg/m2 ).
Ryzyko istotnie wzrasta wraz ze wzrostem BMI.
Jest to szczególnie ważne dla kobiet, u
których występują również inne czynniki ryzyka.
Dodatni wywiad rodzinny (występowanie tętniczych zaburzeń zakrzepowo-zatorowych u rodzeństwa bądź rodziców, szczególnie
w stosunkowo młodym wieku, np. przed 50 rokiem życia).
Jeśli podejrzewa się predyspozycję genetyczną, przed podjęciem decyzji
o stosowaniu złożonego hormonalnego środka antykoncepcyjnego kobieta powinna zostać
skierowana na konsultację u specjalisty.
Migrena
Zwiększenie częstości występowania lub nasilenia migreny w trakcie stosowania
złożonych hormonalnych środków antykoncepcyjnych (która może zapowiadać wystąpienie incydentu naczyniowo- mózgowego) może być powodem do
natychmiastowego przerwania stosowania
Inne schorzenia związane ze zdarzeniami niepożądanymi w obrębie naczyń.
Cukrzyca, hiperhomocysteinemia, wady zastawkowe serca, migotanie przedsionków, dyslipoproteinemia oraz toczeń rumieniowaty
układowy.
Objawy tętniczych zaburzeń zakrzepowo-zatorowych
Należy poinformować pacjentkę, że w razie wystąpienia następujących objawów należy natychmiast zgłosić się do lekarza i powiedzieć personelowi medycznemu, że stosuje się złożone hormonalne środki antykoncepcyjne.
Objawy napadu naczyniowo-mózgowego mogą obejmować:
nagłe zdrętwienie lub osłabienie twarzy, rąk lub nóg, szczególnie po jednej stronie ciała;
nagłe trudności z chodzeniem, zawroty głowy, utratę równowagi lub koordynacji;
nagłe splątanie, trudności z mówieniem lub rozumieniem;
nagłe zaburzenia widzenia w jednym oku lub obojgu oczach;
nagłe, ciężkie lub długotrwałe bóle głowy bez przyczyny;
utratę przytomności lub omdlenie z drgawkami lub bez drgawek.
Przejściowe objawy wskazujące, że zdarzenie jest przemijającym napadem niedokrwiennym.
Objawy zawału serca mogą być następujące:
ból, uczucie dyskomfortu, ciężaru, uczucie ściskania lub pełności w klatce piersiowej, ramieniu lub poniżej mostka;
uczucie dyskomfortu promieniujące do pleców, szczęki, gardła, ramienia, żołądka;
uczucie pełności, niestrawności lub zadławienia;
pocenie się, nudności, wymioty lub zawroty głowy;
skrajne osłabienie, niepokój lub spłycenie oddechu;
przyspieszone lub nieregularne bicie serca.
Gruczolaki wątroby
U pacjentek stosujących złożone doustne środki antykoncepcyjne rzadko opisywano występowanie łagodnych guzów wątroby, a jeszcze rzadziej – guzów złośliwych. W pojedynczych przypadkach tego typu nowotwory prowadziły do wystąpienia zagrażających życiu krwotoków do jamy brzusznej.
Dlatego, w razie wystąpienia silnego bólu w nadbrzuszu, powiększenia wątroby lub objawów krwotoku do jamy brzusznej u kobiet przyjmujących złożone doustne środki antykoncepcyjne należy wziąć pod uwagę guz wątroby w rozpoznaniu różnicowym.
Rak piersi
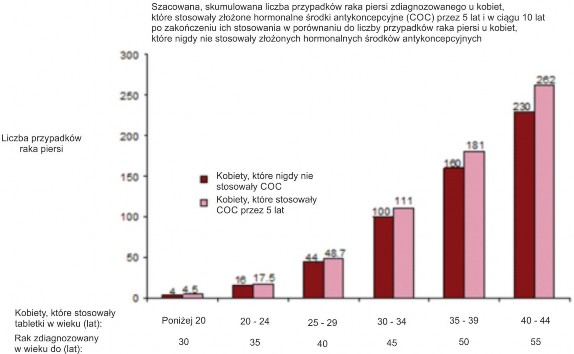
W metaanalizie 54 badań epidemiologicznych wykazano nieznaczne zwiększenie ryzyka względnego (Relative Risk, RR=1,24) rozpoznania raka piersi u kobiet stosujących złożone doustne środki antykoncepcyjne. Obserwowane zwiększone ryzyko może być spowodowane wcześniejszym rozpoznaniem raka piersi u kobiet stosujących złożone doustne środki antykoncepcyjne, działaniem biologicznym złożonych doustnych środków antykoncepcyjnych lub połączeniem obu tych czynników. Dodatkowo zdiagnozowane przypadki raka piersi u kobiet aktualnie stosujących złożone doustne środki antykoncepcyjne, lub u kobiet które je stosowały w czasie ostatnich 10 lat, wykazują większe prawdopodobieństwo zmian zlokalizowanych w porównaniu do przypadków u kobiet, które nigdy nie stosowały złożonych doustnych środków antykoncepcyjnych.
Rak piersi rzadko występuje u kobiet, które nie ukończyły 40 lat, niezależnie od tego czy przyjmują czy nie, złożone doustne środki antykoncepcyjne. Częstość występowania raka piersi zwiększa się wraz z wiekiem, a zwiększona liczba rozpoznań tego nowotworu u kobiet obecnie lub niedawno stosujących złożony doustny środek antykoncepcyjny jest niewielka w stosunku do całkowitego ryzyka wystąpienia raka piersi (patrz wykres poniżej).
Najbardziej istotnym czynnikiem ryzyka raka piersi u kobiet stosujących złożony doustny środek antykoncepcyjny jest wiek, w którym kobieta przerwała jego stosowanie; im wiek przerwania stosowania jest późniejszy, tym ilość zdiagnozowanych przypadków raka piersi jest większa. Długość stosowania jest mniej istotna i zwiększone ryzyko stopniowo zanika w ciągu 10 lat od zakończenia przyjmowania złożonego doustnego środka antykoncepcyjnego tak, że po 10 latach wydaje się nie być ono zwiększone.
Należy omówić z pacjentką możliwość wystąpienia zwiększonego ryzyka raka piersi i ocenić je w stosunku do korzyści wynikających ze stosowania złożonych doustnych środków
antykoncepcyjnych, biorąc pod uwagę dowody wskazujące na znaczącą ochronę przed wystąpieniem ryzyka innych nowotworów (np. raka jajnika i raka endometrium).
Rak szyjki macicy
Wyniki niektórych badań epidemiologicznych wskazują, że długotrwałe stosowanie złożonych doustnych środków antykoncepcyjnych (˃5 lat) może zwiększać ryzyko wystąpienia raka szyjki macicy. Tym niemniej, trwają spory dotyczące znaczenia czynników dodatkowych, takich jak zachowania seksualne i inne czynniki, jak zakażenie wirusem brodawczaka ludzkiego (ang. Human Papilloma Virus, HPV)
Inne nowotwory
Przyjmowanie złożonych doustnych środków antykoncepcyjnych o dużej zawartości substancji czynnej (50 μg etynyloestradiolu) powoduje zmniejszenie ryzyka wystąpienia raka endometrium i raka jajnika. Wymaga potwierdzenia, czy przyjmowanie złożonych doustnych środków antykoncepcyjnych o małej zawartości substancji czynnej ma takie samo działanie.
Nieregularne krwawienia
Podczas stosowania wszystkich doustnych środków antykoncepcyjnych może wystąpić krwawienie śródcykliczne, plamienie i (lub) brak krwawienia z odstawienia, zwłaszcza w pierwszych miesiącach przyjmowania tabletek.
Jeżeli nieregularne krwawienia utrzymują się przez ponad trzy cykle, lub występują u kobiety, u której uprzednio występowały regularne cykle, należy rozważyć przyczyny niehormonalne i przeprowadzić odpowiednie badania diagnostyczne w celu wykluczenia nowotworów złośliwych lub ciąży.
U niektórych kobiet mogą nie występować krwawienia z odstawienia podczas przerwy
w przyjmowaniu tabletek. Jeżeli złożony doustny środek antykoncepcyjny był przyjmowany zgodnie z zaleceniami opisanymi w punkcie 4.2, jest mało prawdopodobne, że kobieta jest w ciąży. Niemniej jednak, jeżeli złożony doustny środek antykoncepcyjny nie był przyjmowany zgodnie z zaleceniami a nie wystąpiło krwawienie z odstawienia lub jeżeli nie wystąpiły dwa kolejne krwawienia
z odstawienia, przed kontynuacją stosowania złożonego doustnego środka antykoncepcyjnego należy wykluczyć ciążę.
Inne stany
U kobiet z hipertriglicerydemią lub wywiadem rodzinnym w tym kierunku, podczas przyjmowania złożonych doustnych środków antykoncepcyjnych może być zwiększone ryzyko wystąpienia zapalenia trzustki.
U wielu kobiet przyjmujących złożone doustne środki antykoncepcyjne zgłaszano niewielkie zwiększenie ciśnienia tętniczego krwi, chociaż znaczące zwiększenie wartości ciśnienia występuje rzadko. Tylko w takich przypadkach uzasadnione jest natychmiastowe odstawienie złożonych doustnych środków antykoncepcyjnych. Jeśli podczas stosowania złożonych doustnych środków antykoncepcyjnych u kobiet z istniejącym wcześniej nadciśnieniem tętniczym, stale podwyższone ciśnienie tętnicze lub znaczący wzrost ciśnienia tętniczego krwi nie reaguje na odpowiednie leczenie przeciwnadciśnieniowe, należy odstawić złożone doustne środki antykoncepcyjne. Jeśli to właściwe, po powrocie wartości ciśnienia tętniczego krwi do normy po zastosowaniu leków przeciwnadciśnieniowych można ponownie zastosować złożone doustne środki antykoncepcyjne.
Zarówno podczas ciąży, jak i podczas przyjmowania złożonych doustnych środków antykoncepcyjnych zgłaszano występowanie następujących stanów chorobowych lub ich pogorszenie, chociaż nie ma dowodów na powiązanie ze stosowaniem złożonych doustnych środków antykoncepcyjnych: żółtaczka i (lub) świąd spowodowane cholestazą, kamica żółciowa; porfiria, toczeń rumieniowaty układowy, zespół hemolityczno-mocznicowy, pląsawica Sydenhama, opryszczka ciążowa, utrata słuchu w wyniku otosklerozy.
Egzogenne estrogeny mogą wywoływać lub nasilać objawy wrodzonego lub nabytego obrzęku naczynioruchowego.
Ostre lub przewlekłe zaburzenia czynności wątroby mogą powodować konieczność przerwania stosowania złożonych doustnych środków antykoncepcyjnych do momentu powrotu parametrów czynności wątroby do prawidłowych wartości. W przypadku nawrotu żółtaczki cholestatycznej i (lub) świądu spowodowanego cholestazą, u kobiet, u których takie objawy występowały podczas ciąży lub poprzedniego stosowania steroidów płciowych, konieczne jest przerwanie stosowania złożonych doustnych środków antykoncepcyjnych.
Mimo, że złożone doustne środki antykoncepcyjne mogą powodować obwodową insulinooporność i wpływać na tolerancję glukozy, nie ma dowodów na to, aby istniała konieczność zmiany schematu leczenia u pacjentek z cukrzycą, stosujących złożone doustne środki antykoncepcyjne o małej zawartości substancji czynnej (zawierających <0,05 mg etynyloestradiolu). Niemniej jednak, należy uważnie obserwować kobiety chorujące na
cukrzycę, zwłaszcza w początkowym okresie stosowania złożonych doustnych środków antykoncepcyjnych.
Podczas stosowania złożonych doustnych środków antykoncepcyjnych zgłaszano przypadki zaostrzenia padaczki, choroby Crohna i wrzodziejącego zapalenia jelita grubego.
Sporadycznie podczas stosowania złożonych doustnych środków antykoncepcyjnych może wystąpić ostuda, zwłaszcza u kobiet, u których wcześniej występowała ostuda ciążowa. Kobiety ze skłonnością do występowania ostudy, powinny unikać ekspozycji na słońce oraz światło ultrafioletowe podczas stosowania złożonych doustnych środków antykoncepcyjnych.
Nastrój depresyjny oraz depresja są znanymi działaniami niepożądanymi, występującymi podczas stosowania złożonych doustnych środków antykoncepcyjnych (patrz punkt 4.8). Depresja może być ciężka i jest znanym czynnikiem ryzyka zachowań i myśli samobójczych. Należy zalecić pacjentkom, aby skontaktowały się z lekarzem, jeśli zauważą zmiany nastroju i objawy depresji, w początkowym okresie leczenia.
Substancje pomocnicze
Tabletki zawierają laktozę. Lek nie powinien być stosowany u pacjentek z rzadko występującą dziedziczną nietolerancją galaktozy, brakiem laktazy lub zespołem złego wchłaniania glukozy- galaktozy.
Interakcje z innymi produktami leczniczymi i inne rodzaje interakcji
Wpływ innych produktów leczniczych na działanie produktu leczniczego Liberelle
Mogą wystąpić interakcje z produktami leczniczymi indukującymi enzymy mikrosomalne, które mogą spowodować zwiększenie klirensu hormonów płciowych, co może prowadzić do krwawienia śródcyklicznego i (lub) nieskuteczności działania antykoncepcyjnego.
Postępowanie
Indukcja enzymów może wystąpić po kilku dniach leczenia. Maksymalna indukcja enzymów występuje w ciągu kilku tygodni. Po zaprzestaniu leczenia indukcja enzymów może się utrzymywać przez około 4 tygodnie.
Leczenie krótkotrwałe
Kobiety leczone produktami leczniczymi indukującymi enzymy powinny stosować mechaniczną lub inną metodę antykoncepcji, oprócz złożonego doustnego środka antykoncepcyjnego. Mechaniczne metody antykoncepcji muszą być stosowane podczas całego okresu leczenia skojarzonego oraz przez 28 dni po jego zakończeniu. Jeśli leczenie to trwa dłużej, niż do zakończenia opakowania doustnego złożonego środka antykoncepcyjnego, należy od razu rozpocząć przyjmowanie tabletek z następnego opakowania, bez zwyczajowej przerwy w przyjmowaniu tabletek.
Leczenie długotrwałe
U kobiet długotrwale przyjmujących produkty lecznicze indukujące enzymy wątrobowe zaleca się stosowanie innej, niehormonalnej metody zapobiegania ciąży.
Następujące interakcje opisano w literaturze.
Substancje zwiększające klirens złożonych doustnych środków antykoncepcyjnych (zmniejszające skuteczność poprzez indukcję enzymów), np.:
Barbiturany, bosentan, karbamazepina, fenytoina, prymidon, ryfampicyna, produkt leczniczy stosowany w leczeniu zakażeń wirusem HIV - rytonawir, newirapina, efawirenz, prawdopodobnie również felbamat, gryzeofulwina, okskarbamazepina, topiramat oraz produkty ziołowe zawierające ziele dziurawca zwyczajnego (Hypericum perforatum).
Substancje wywierające różny wpływ na klirens złożonych doustnych środków antykoncepcyjnych: Równoczesne stosowanie złożonych doustnych środków antykoncepcyjnych z produktami złożonymi zawierającymi inhibitory proteazy HIV i nienukleozydowe inhibitory odwrotnej transkryptazy, w tym z produktami złożonymi zawierającymi inhibitory HCV, może zwiększać lub zmniejszać stężenie estrogenów albo progestagenów w osoczu. W efekcie końcowym, w niektórych przypadkach zmiany te mogą mieć znaczenie kliniczne.
Dlatego też, przepisując równoczesne stosowanie produktów leczniczych przeciwko HIV/HCV należy wziąć pod uwagę możliwe interakcje oraz odpowiednie zalecenia. W przypadku jakichkolwiek wątpliwości, kobiety podczas terapii inhibitorami proteazy lub nienukleozydowymi inhibitorami odwrotnej transkryptazy powinny stosować dodatkową, mechaniczną metodę antykoncepcji.
Substancje zmniejszające klirens złożonych doustnych środków antykoncepcyjnych (inhibitory enzymatyczne):
Znaczenie kliniczne potencjalnych interakcji z inhibitorami enzymatycznymi nie jest znane.
Jednoczesne przyjmowanie silnych inhibitorów CYP3A4 może zwiększać stężenia w osoczu estrogenu, progestagenu lub obu tych substancji jednocześnie.
Podczas jednoczesnego przyjmowania ze złożonym doustnym środkiem antykoncepcyjnym zawierającym 0,035 mg etynyloestradiolu wykazano, że etorykoksyb w dawkach od 60 do 120 mg/dobę zwiększa stężenie etynyloestradiolu w osoczu odpowiednio 1,4- i 1,6-krotnie.
Wpływ produktu leczniczego Liberelle na działanie innych produktów leczniczych
Wpływ na płodność, ciążę i laktację
Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn
Działania niepożądane
żylna choroba zakrzepowo-zatorowa;
tętnicza choroba zakrzepowo-zatorowa;
nadciśnienie tętnicze krwi;
guzy wątroby;
wystąpienie lub pogorszenie stanów chorobowych, których powiązanie z przyjmowaniem złożonych doustnych środków antykoncepcyjnych nie jest rozstrzygnięte: choroba Crohna, wrzodziejące zapalenie jelita, padaczka, mięśniaki macicy, porfiria, układowy toczeń rumieniowaty, opryszczka ciążowa, pląsawica Sydenhama, zespół hemolityczno-mocznicowy, żółtaczka cholestatyczna;
ostuda;
ostre lub przewlekłe zaburzenia czynności wątroby, które mogą wymagać przerwania stosowania złożonych doustnych środków antykoncepcyjnych aż do momentu powrotu parametrów czynności wątroby do prawidłowych wartości;
Przedawkowanie
Liberelle, 0,25 mg + 0,035 mg, tabletki
Każda tabletka zawiera 250 mikrogramów norgestimatu (Norgestimatum) i 35 mikrogramów etynyloestradiolu (Ethinylestradiolum).
Substancja pomocnicza o znanym działaniu Laktoza jednowodna 75,74 mg, patrz punkt 4.4.
Pełny wykaz substancji pomocniczych, patrz punkt 6.1.
Tabletka
Niebieskie, cylindryczne, obustronnie wypukłe tabletki o średnicy 6 mm (od 5,9 mm do 6,1 mm) i grubości 2,5 mm (od 1,5 mm do 3,5 mm).
Doustna antykoncepcja.
Decyzję o przepisaniu produktu leczniczego Liberelle należy podjąć na podstawie indywidualnej oceny czynników ryzyka u danej pacjentki, zwłaszcza dotyczących żylnej choroby zakrzepowo- zatorowej (VTE, ang. Venous Thromboembolism) oraz porównania ryzyka VTE dla produktu leczniczego Liberelle, z innymi złożonymi hormonalnymi środkami antykoncepcyjnymi (patrz punkty
4.3 oraz 4.4).
Podanie doustne.
Jak przyjmować produkt leczniczy Liberelle
Tabletki należy przyjmować codziennie, mniej więcej o tej samej porze, w kolejności wskazanej na blistrze, popijając w razie potrzeby niewielką ilością płynu. Należy przyjmować jedną tabletkę na dobę przez 21 kolejnych dni. Każde kolejne opakowanie należy rozpocząć po upływie 7-dniowej przerwy, podczas której występuje zazwyczaj krwawienie z odstawienia. Krwawienie występuje zwykle 2 lub 3 dni po przyjęciu ostatniej tabletki i może nie zakończyć się przed rozpoczęciem kolejnego opakowania tabletek.
Jak rozpoczynać przyjmowanie produktu leczniczego Liberelle
Ostrzeżenia
Jeśli występuje którykolwiek z poniższych stanów lub czynników ryzyka, należy omówić z pacjentką zasadność stosowania produktu leczniczego Liberelle.
W razie pogorszenia lub wystąpienia po raz pierwszy któregokolwiek z wymienionych stanów lub czynników ryzyka kobieta powinna zgłosić się do lekarza prowadzącego, który zadecyduje, czy konieczne jest przerwanie stosowania produktu leczniczego Liberelle.
Badanie lekarskie / konsultacja
Przed przyjęciem produktu leczniczego Liberelle po raz pierwszy lub po przerwie w jego stosowaniu, należy przeprowadzić dokładny wywiad (lekarski i rodzinny) i wykluczyć obecność ciąży. Należy dokonać pomiaru ciśnienia tętniczego krwi i przeprowadzić badanie lekarskie mając na uwadze przeciwwskazania (patrz punkt 4.3) i ostrzeżenia (patrz punkt 4.4).
Ważne jest zwrócenie uwagi kobiety na informacje dotyczące zakrzepicy żył i tętnic, w tym na ryzyko stosowania produktu leczniczego Liberelle w porównaniu z innymi złożonymi hormonalnymi środkami antykoncepcyjnymi, a także na objawy żylnej choroby zakrzepowo-zatorowej oraz zaburzeń zakrzepowo-zatorowych tętnic, znane czynniki ryzyka oraz co należy robić w przypadku podejrzenia zakrzepicy.
Lekarz powinien poinformować kobietę, aby zapoznała się z treścią ulotki i zastosowała do podanych w niej zaleceń.
Częstość wykonywania badań i ich rodzaj należy dobierać indywidualnie dla każdej pacjentki, na podstawie ustalonych schematów postępowania.
Należy poinformować kobietę, że doustne środki antykoncepcyjne NIE chronią przed zakażeniem wirusem HIV (AIDS) i innymi chorobami przenoszonymi drogą płciową.
Choroby układu krążenia
Ryzyko żylnej choroby zakrzepowo-zatorowej (VTE)
Stosowanie jakichkolwiek złożonych hormonalnych środków antykoncepcyjnych wiąże się ze zwiększonym ryzykiem żylnej choroby zakrzepowo-zatorowej w porównaniu do sytuacji, gdy terapia nie jest stosowana. Stosowanie produktów zawierających lewonorgestrel, norgestymat (w tym produktu Liberelle) lub noretysteron jest związane z najmniejszym ryzykiem żylnej choroby zakrzepowo-zatorowej. Decyzja o zastosowaniu produktu leczniczego Liberelle powinna zostać podjęta po rozmowie z pacjentką w celu zapewnienia, że rozumie ona ryzyko żylnej choroby zakrzepowo-zatorowej związane z produktem Liberelle i wpływ swoich innych czynników ryzyka na to ryzyko, jak również, że ryzyko żylnej choroby zakrzepowo-zatorowej jest największe w pierwszym roku stosowania. Istnieją pewne dowody świadczące o tym, że ryzyko zwiększa się, gdy złożone hormonalne środki antykoncepcyjne są przyjmowane ponownie po przerwie w stosowaniu trwającej 4 tygodnie lub więcej.
U około 2 na 10 000 kobiet, które nie stosują złożonych środków antykoncepcyjnych i nie są w ciąży, w okresie roku rozwinie się żylna choroba zakrzepowo-zatorowa. Jednakże, ryzyko to może być znacznie większe, w zależności od czynników ryzyka występujących u danej kobiety (patrz poniżej).
Szacuje się, że spośród 10 000 kobiet, które stosują złożone hormonalne środki antykoncepcyjne zawierające lewonorgestrel, u około 6 kobiet w okresie roku rozwinie się żylna choroba zakrzepowo- zatorowa.
Obecnie dostępne dane wskazują, że ryzyko wystąpienia żylnej choroby zakrzepowo-zatorowej podczas stosowania złożonych środków antykoncepcyjnych zawierających norgestymat jest podobne do ryzyka występującego podczas stosowania złożonych środków antykoncepcyjnych zawierających lewonorgestrel.
Taka liczba przypadków żylnej choroby zakrzepowo-zatorowej na rok jest mniejsza niż oczekiwana liczba przypadków u kobiet w ciąży lub w okresie poporodowym.
Żylna choroba zakrzepowo-zatorowa może być śmiertelna w 1-2% przypadków.
Liczba przypadków wystąpienia żylnej choroby zakrzepowo-zatorowej u 10 000 kobiet na rok
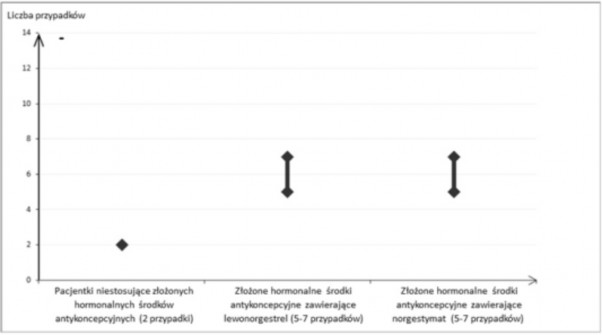
U pacjentek stosujących złożone hormonalne środki antykoncepcyjne niezwykle rzadko zgłaszano przypadki zakrzepicy w innych naczyniach krwionośnych, np. wątrobowych, krezkowych, nerkowych lub w żyłach i tętnicach siatkówki.
Czynniki ryzyka żylnej choroby zakrzepowo-zatorowej
Ryzyko żylnych powikłań zakrzepowo-zatorowych u pacjentek stosujących złożone hormonalne środki antykoncepcyjne może znacząco wzrosnąć w przypadku występowania dodatkowych czynników ryzyka, szczególnie, jeśli występuje kilka czynników ryzyka jednocześnie (patrz tabela).
Stosowanie produktu leczniczego Liberelle jest przeciwwskazane, jeśli u pacjentki występuje jednocześnie kilka czynników ryzyka, zwiększających ryzyko zakrzepicy żylnej (patrz punkt 4.3). Jeśli u kobiety występuje więcej niż jeden czynnik ryzyka, możliwe jest, że wzrost ryzyka jest większy niż suma pojedynczych czynników – w takim przypadku należy ocenić całkowite ryzyko żylnej choroby zakrzepowo-zatorowej. Jeśli ocena stosunku korzyści do ryzyka jest negatywna, nie należy przepisywać złożonych hormonalnych środków antykoncepcyjnych (patrz punkt 4.3).
Tabela: Czynniki ryzyka żylnej choroby zakrzepowo-zatorowej
Czynnik ryzyka | Uwagi |
Otyłość (wskaźnik masy ciała - BMI - powyżej 30 kg/m2) | Ryzyko istotnie zwiększa się ze wzrostem BMI. Czynnik należy szczególnie uwzględnić, jeśli występują również inne czynniki ryzyka. |
Długotrwałe unieruchomienie, rozległy zabieg operacyjny, jakikolwiek zabieg operacyjny w obrębie kończyn dolnych lub miednicy, zabieg neurochirurgiczny lub poważny uraz Uwaga: tymczasowe unieruchomienie, w tym podróż samolotem >4 godzin może również stanowić czynnik ryzyka żylnej choroby zakrzepowo-zatorowej, szczególnie u kobiet ze współistniejącymi innymi czynnikami ryzyka. | W takich sytuacjach zaleca się przerwanie stosowania tabletek (na co najmniej 4 tygodnie przed planowanym zabiegiem chirurgicznym) i nie wznawianie przed upływem dwóch tygodni od czasu powrotu do sprawności ruchowej. Należy stosować inną metodę antykoncepcji, aby uniknąć niezamierzonego zajścia w ciążę. Należy rozważyć leczenie przeciwzakrzepowe, jeśli stosowania produktu leczniczego Liberelle nie przerwano odpowiednio wcześnie. |
Dodatni wywiad rodzinny (występowanie żylnych zaburzeń zakrzepowo-zatorowych u rodzeństwa bądź rodziców, szczególnie w stosunkowo młodym wieku, np. przed 50. rokiem życia). | Jeśli podejrzewa się predyspozycję genetyczną, przed podjęciem decyzji o stosowaniu złożonego hormonalnego środka antykoncepcyjnego kobieta powinna zostać skierowana na konsultację u specjalisty. |
Inne schorzenia związane z żylną chorobą zakrzepowo-zatorową | Nowotwór, toczeń rumieniowaty układowy, zespół hemolityczno-mocznicowy, przewlekłe zapalne choroby jelit (np. choroba Leśniowskiego-Crohna lub wrzodziejące zapalenie jelita grubego) oraz niedokrwistość sierpowatokrwinkowa. |
Wiek | Szczególnie wiek powyżej 35 lat |
Nie osiągnięto konsensusu, co do możliwej roli żylaków oraz zakrzepowego zapalenia żył powierzchniowych na wystąpienie lub progresję żylnej choroby zakrzepowo-zatorowej.
Należy uwzględnić zwiększone ryzyko wystąpienia choroby zakrzepowo-zatorowej w ciąży a zwłaszcza w 6-tygodniowym okresie poporodowym (dalsze informacje w punkcie „Wpływ na płodność, ciążę i laktację” patrz punkt 4.6).
Objawy żylnej choroby zakrzepowo-zatorowej (zakrzepicy żył głębokich oraz zatorowości płucnej)
Należy poinformować pacjentkę, że w razie wystąpienia niżej wymienionych objawów należy natychmiast zgłosić się do lekarza i powiedzieć personelowi medycznemu, że stosuje się złożone hormonalne środki antykoncepcyjne.
Potencjalne zmniejszenie skuteczności antykoncepcyjnej związane z jednoczesnym stosowaniem innych produktów leczniczych:
Uwaga: należy zapoznać się z informacjami dotyczącymi innych stosowanych jednocześnie produktów leczniczych, aby rozpoznać możliwe interakcje.
Złożone doustne środki antykoncepcyjne mogą wpływać na metabolizm niektórych innych substancji czynnych. Odpowiednio, stężenie w osoczu i tkankach może ulec zwiększeniu (np. cyklosporyna) lub zmniejszeniu (np. lamotrygina).
Dane kliniczne wskazują, że etynyloestradiol hamuje klirens substratów CYP1A1, powodując słabe (np. teofilina) lub umiarkowane (np. tyzanidyna) zwiększenie stężenia tych substancji w osoczu.
Interakcje farmakodynamiczne
Podczas badań klinicznych u pacjentów leczonych z powodu zakażenia wirusem zapalenia wątroby typu C (HCV) produktami leczniczymi zawierającymi ombitaswir z parytaprewirem i rytonawirem oraz dazabuwir z rybawiryna lub bez, zwiększenie aktywności aminotransferaz (AlAT) do wartości ponad pięciokrotnie większych niż górna granica normy występowało znacząco częściej u kobiet stosujących produkty lecznicze zawierające etynyloestradiol, takie jak złożone hormonalne produkty antykoncepcyjne. Dodatkowo, również u pacjentów leczonych glekaprewirem z pibrentaswirem lub sofosbuwirem z welpataswirem i woksylaprewirem, obserwowano zwiększenie aktywności AlAT u kobiet stosujących leki zawierające etynyloestradiol, takie jak złożone hormonalne środki antykoncepcyjne (patrz punkt 4.3).
Dlatego kobiety stosujące produkt leczniczy Liberelle muszą, przed rozpoczęciem leczenia za pomocą tych połączeń przeciwwirusowych, zmienić metodę stosowanej antykoncepcji na alternatywną (np. antykoncepcja zawierająca wyłącznie progestagen lub metody niehormonalne).
Ponowne stosowanie produktu leczniczego Liberelle można rozpocząć po 2 tygodniach od zakończenia leczenia za pomocą wcześniej opisanych połączeń przeciwwirusowych.
Badania laboratoryjne
Przyjmowanie steroidów antykoncepcyjnych może wpływać na wyniki niektórych badań laboratoryjnych, w tym: biochemicznych parametrów czynności wątroby, tarczycy, nadnerczy i nerek, stężenia białek osocza (nośnikowych), np. globuliny wiążącej kortykosteroidy oraz stężenia frakcji lipidów lub lipoprotein, parametry metabolizmu węglowodanów i parametry krzepnięcia oraz fibrynolizy. Zmienione wyniki badań laboratoryjnych zazwyczaj pozostają w granicach wartości prawidłowych.
Ciąża
Jeśli podczas przyjmowania produktu leczniczego Liberelle kobieta zajdzie w ciążę, należy przerwać przyjmowanie produktu. W większości badań epidemiologicznych nie wykazano zwiększenia ryzyka wystąpienia wad wrodzonych u dzieci, których matki przyjmowały złożone doustne środki antykoncepcyjne zawierające etynyloestradiol przed zajściem w ciążę, ani działania teratogennego, gdy środki te były w sposób niezamierzony stosowane we wczesnym okresie ciąży.
Po wznowieniu przyjmowania produktu leczniczego Liberelle należy wziąć pod uwagę zwiększone ryzyko wystąpienia żylnej choroby zakrzepowo-zatorowej w okresie poporodowym (patrz punkty 4.2 i 4.4).
Karmienie piersią
Przyjmowanie złożonych doustnych środków antykoncepcyjnych może wpływać na laktację, poprzez zmniejszenie ilości oraz zmianę składu mleka kobiecego. W związku z tym, nie zaleca się stosowania złożonych doustnych środków antykoncepcyjnych aż do momentu przerwania karmienia dziecka piersią. Przyjmowanie złożonych doustnych środków antykoncepcyjnych może powodować, że niewielkie ilości steroidów zawartych w środku antykoncepcyjnym i (lub) ich metabolitów mogą przenikać do mleka. Te ilości mogą wywierać wpływ na dziecko.
Płodność
Produkt leczniczy Liberelle jest wskazany do zapobiegania ciąży. Informacje dotyczące wpływu na płodność, patrz punkt 5.1.
Nie przeprowadzono badań dotyczących wpływu na zdolność prowadzenia pojazdów i obsługiwania maszyn. U kobiet stosujących złożone doustne środki antykoncepcyjne nie obserwowano wpływu tych produktów leczniczych na zdolność prowadzenia pojazdów i obsługiwania maszyn.
Podsumowanie profilu bezpieczeństwa
U kobiet stosujących złożone hormonalne środki antykoncepcyjne odnotowano zwiększone ryzyko zakrzepicy żył i tętnic oraz zdarzeń zakrzepowo-zatorowych, w tym zawału serca, udaru, przemijającego napadu niedokrwiennego, zakrzepicy żylnej oraz zatorowości płucnej. Zagadnienie zostało szerzej omówione w punkcie 4.4.
W tabeli poniżej podano wszystkie działania niepożądane zgłoszone podczas stosowania Liberelle w badaniach klinicznych lub po wprowadzeniu do obrotu produktu leczniczego w postaci tabletek zawierającego norgestymat i etynyloestradiol.
Częstość występowania wymienionych działań niepożądanych określono w następujący sposób:
bardzo często (≥1/10), często (≥1/100 do <1/10), niezbyt często (≥1/1000 do <1/100), rzadko (≥1/10 000 do <1/1000), bardzo rzadko (<1/10 000) i częstość nieznana (częstość nie może być określona na podstawie dostępnych danych).
Tabelaryczne zestawienie działań niepożądanych | ||||||
Bardzo często | Często | Niezbyt często | Rzadko | Bardzo rzadko | Częstość nieznana | |
Zakażenia i zarażenia pasożytnicze | Zakażenia układu moczowego, zakażenia pochwy | |||||
Nowotwory | Dysplazja | Torbiele | Gruczolaki | |||
łagodne, złośliwe | szyjki macicy | piersi | wątroby, rak | |||
i nieokreślone (w | piersi, łagodne | |||||
tym torbiele i | nowotwory | |||||
polipy) | piersi, | |||||
ogniskowy | ||||||
rozrost | ||||||
guzkowy, | ||||||
gruczolako– | ||||||
włókniaki | ||||||
piersi | ||||||
Zaburzenia układu | Nadwrażliwość | Nasilenie | ||||
immunologicznego | objawów | |||||
wrodzonego | ||||||
lub nabytego | ||||||
obrzęku | ||||||
naczyniorucho | ||||||
wego | ||||||
Zaburzenia | Zatrzymanie | Zwiększenie | Dyslipidemia | |||
metabolizmu | płynu | i zmniejszenie | ||||
i odżywiania | apetytu, | |||||
wahania masy | ||||||
ciała | ||||||
Zaburzenia | Zmiana | Lęk, | ||||
psychiczne | nastroju, | zaburzenia | ||||
depresja, | libido | |||||
nerwowość, | ||||||
bezsenność | ||||||
Zaburzenia układu | Ból głowy | Migrena, | Omdlenia, | Incydent | ||
nerwowego | zawroty głowy | parestezja | naczyniowo- | |||
mózgowy, | ||||||
drgawki | ||||||
Zaburzenia oka | Zaburzenia | Nietolerancja | ||||
widzenia, | soczewek | |||||
suche oko | kontaktowych, | |||||
zator | ||||||
naczyniowy | ||||||
siatkówki* | ||||||
Zaburzenia ucha | Zawroty | |||||
i błędnika | głowy | |||||
pochodzenia | ||||||
ośrodkowego | ||||||
Zaburzenia serca | Kołatanie serca | Tachykardia | Zawał serca | |||
Zaburzenia | Zakrzepica, | Żylna | Zakrzepica żył | |||
naczyniowe | nadciśnienie | choroba | głębokich*, | |||
tętnicze, | zakrzepowo- | zakrzepica | ||||
uderzenia | zatorowa, | żylna** | ||||
gorąca | tętnicza | |||||
choroba | ||||||
zakrzepowo- | ||||||
zatorowa | ||||||
Zaburzenia układu | Duszność | Zatorowość | ||||
oddechowego, | płucna* | |||||
klatki piersiowej | ||||||
i śródpiersia | ||||||
Zaburzenia żołądka | Zaburzenia | Ból żołądka | Zapalenie | |||
i jelit | żołądkowo | i jelit, ból | trzustki | |||
-jelitowe, | brzucha, | |||||
wymioty, | rozdęcie | |||||
biegunka, | brzucha, | |||||
nudności | zaparcie, | |||||
wzdęcie | ||||||
z oddawaniem | ||||||
gazów | ||||||
Zaburzenia wątroby i dróg żółciowych | Zapalenie wątroby | |||||
Zaburzenia skóry | Trądzik, | Łysienie, | Nadmierne | Obrzęk | ||
i tkanki podskórnej | wysypka | hirsutyzm, | pocenie się, | naczyniorucho- | ||
pokrzywka, | reakcje | wy, rumień | ||||
rumień, | nadwrażliwo- | guzowaty, | ||||
przebarwienie | ści na światło | nocne pocenie | ||||
skóry | się | |||||
Zaburzenia | Skurcz mięśni, | Ból mięśni | ||||
mięśniowo- | ból kończyny, | |||||
szkieletowe i tkanki | ból pleców | |||||
łącznej | ||||||
Zaburzenia układu | Bolesne | Brak | Mlekotok, | Upławy z | Zahamowanie | |
rozrodczego i piersi | miesią- | miesiączki, | powiększenie | pochwy | laktacji | |
czkowanie, | upławy z | piersi, torbiel | ||||
krwotok | narządów | jajnika, | ||||
maciczny, | rodnych, ból | suchość | ||||
nieprawi- | piersi | pochwy | ||||
dłowe | i sromu | |||||
krwawie- | ||||||
nie z | ||||||
odstawie- | ||||||
nia | ||||||
Zaburzenia ogólne | Ból w klatce | |||||
i stany w miejscu | piersiowej, | |||||
podania | obrzęk, stany | |||||
osłabienia | ||||||
Badania diagnostyczne | Zwiększenie masy ciała | Zmniejszenie masy ciała |
* Nie zaobserwowano podczas badań klinicznych, więc nie można określić częstości. Patrz punkt 4.4, w celu określenia częstości w oparciu o standardową częstość zgłaszania dla innych złożonych hormonalnych środków antykoncepcyjnych.
** Ogólny termin dla zakrzepicy żylnej, obejmujący zespół Budda Chari’ego oraz zakrzepicę żył wątrobowych.
Opis wybranych działań niepożądanych
U kobiet przyjmujących złożone doustne środki antykoncepcyjne zaobserwowano zwiększone ryzyko wystąpienia tętniczych i żylnych zdarzeń zakrzepowo-zatorowych, w tym zawału serca, udaru mózgu, przejściowych ataków niedokrwiennych, zakrzepicy żylnej i zatorowości płucnej, co szczegółowo opisano w punkcie 4.4.
U kobiet przyjmujących złożone doustne środki antykoncepcyjne zgłaszano następujące ciężkie działania niepożądane, które omówiono w punkcie 4.4 „Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania”:
-
Częstość rozpoznania raka piersi jest bardzo nieznacznie zwiększona u kobiet przyjmujących złożone doustne środki antykoncepcyjne. Ponieważ rak piersi występuje rzadko u kobiet w wieku poniżej
40 lat, zwiększenie liczby przypadków jest niewielkie w stosunku do ogólnego ryzyka raka piersi. Nie jest znany związek przyczynowo-skutkowy ze stosowaniem złożonych doustnych środków antykoncepcyjnych. Dalsze informacje, patrz punkty 4.3 i 4.4.
Interakcje
Krwawienie śródcykliczne i (lub) nieskuteczność działania antykoncepcyjnego może być wynikiem interakcji innych produktów leczniczych (induktorów enzymatycznych) z doustnymi złożonymi środkami antykoncepcyjnymi (patrz punkt 4.5).
Zgłaszanie podejrzewanych działań niepożądanych
Po dopuszczeniu produktu leczniczego do obrotu istotne jest zgłaszanie podejrzewanych działań niepożądanych. Umożliwia to nieprzerwane monitorowanie stosunku korzyści do ryzyka stosowania produktu leczniczego. Osoby należące do fachowego personelu medycznego powinny zgłaszać wszelkie podejrzewane działania niepożądane za pośrednictwem Departamentu Monitorowania Niepożądanych Działań Produktów Leczniczych Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych: Al. Jerozolimskie 181C; 02-222 Warszawa; tel.:
+48 22 49 21 301; faks: +48 22 49 21 309; strona internetowa: https://smz.ezdrowie.gov.pl. Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Nie zgłaszano ciężkich objawów związanych z przedawkowaniem. Objawami przedawkowania mogą być nudności, wymioty i krwawienie z dróg rodnych. Nie istnieje antidotum a leczenie powinno być objawowe.
WŁAŚCIWOŚCI FARMAKOLOGICZNE
Właściwości farmakodynamiczne
Właściwości farmakokinetyczne Norgestymat
Przedkliniczne dane o bezpieczeństwie
DANE FARMACEUTYCZNE
Wykaz substancji pomocniczych
Niezgodności farmaceutyczne
Okres ważności
Specjalne środki ostrożności podczas przechowywania
Rodzaj i zawartość opakowania
Specjalne środki ostrożności dotyczące usuwania
PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU
NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU I DATA PRZEDŁUŻENIA POZWOLENIA
DATA ZATWIERDZENIA LUB CZĘŚCIOWEJ ZMIANY TEKSTU CHARAKTERYSTYKI PRODUKTU LECZNICZEGO
Grupa farmakoterapeutyczna: hormonalne środki antykoncepcyjne do stosowania wewnętrznego; progestagen i estrogen, produkty złożone o stałej dawce.
Kod ATC: G03AA11
Działanie antykoncepcyjne produktu leczniczego Liberelle oparte jest na współdziałaniu wielu czynników, z których najważniejsze to zahamowanie owulacji i zmiany w endometrium.
Wchłanianie: po podaniu doustnym norgestymat wchłania się szybko.
Po podaniu jednorazowym lub wielokrotnym (trzy cykle) produktu Liberelle, stężenie norgestymatu w surowicy wynosi poniżej limitu oznaczalności testu (0,1 ng/ml), podczas gdy metabolity norgestymatu, norelgestromin i norgestrel znajdują się w krążeniu w ilościach mierzalnych, osiągając maksymlne stężenia w surowicy po około 1,5 godziny od podania dawki leku. Zwiększenie wartości Cmax i AUC norelgestrominu są proporcjonalne w stosunku do podanej dawki w zakresie od 0,180 do 0,250 mg norgestymatu.
Dystrybucja: norelgestromin i norgestrel są w znacznym stopniu związane z białkami surowicy (˃97%). Norelgestromin jest związany z albuminami, ale nie z globuliną wiążącą hormony płciowe (SHBG, ang. Sex Hormone-binding Globulin), podczas gdy norgestrel jest przede wszystkim związany z globuliną wiążącą hormony płciowe, a w znacznie mniejszym stopniu z albuminami.
Badania wykazały, że brak wiązania norelgestrominu z globuliną wiążącą hormony płciowe jest unikalny w porównaniu do innych progestagenów zawartych w doustnych środkach antykoncepcyjnych i odgrywa kluczową rolę w nasileniu jego aktywności biologicznej. Odwrotnie, norgestrel powstający z norgestymatu jest głównie związany z globuliną wiążącą hormony płciowe, co ogranicza jego aktywność biologiczną.
Metabolizm: norgestymat jest szybko metabolizowany w mechanizmie pierwszego przejścia (przez jelita i (lub) wątrobę) do norelgestrominu (maksymalne stężenie jest obserwowane w ciągu 2 godzin) i norgestrelu, a oba metabolity są czynnymi farmakologiczne progestagenami.
Eliminacja: zarówno norelgestymat jak i norgestrel są dalej metabolizowane, a ich metabolity są wydalane przez nerki oraz z kałem. Czas półtrwania eliminacji w stanie stacjonarmym wynosi 24,9 godzin w przypadku norelgestrominu i 45 godzin w przypadku norgestrelu. Po podaniu 14C- norgestymatu, 47% podanej radioaktywności było wydalane z moczem a 37% z kałem.
Właściwości farmakokinetyczne w stanie stacjonarnym: po podaniu 0,250 mg norgestymatu +
0,035 mg etynyloestradiolu, średnie wartości AUC 0-24 w stanie stacjonarnym w oparciu o frakcję nie związaną w osoczu z globuliną wiążącą hormony płciowe wynosiła 18,1 godziny*ng/ml w przypadku norelgestrominu i 3,64 godziny*ng/ml w przypadku norgestrelu. Wartość AUC dla norgestrelu po podaniu 0,250 mg norgestymatu+0,035 mg etynyloestradiolu, odpowiada ekspozycji po dawce lewonorgestrelu wynoszącej około 30 mikrogramów w skojarzeniu z etynyloestradiolem.
Etynyloestradiol
Wchłanianie: etynyloestradiol podany doustnie wchłania się szybko i całkowicie. Stężenie etynyloestradiolu w surowicy jest mierzalne w ciągu 0,5 godziny do podaniu dawki leku i osiąga maksymalną wartość po około 1,2 godziny.
Dystrybucja: etynyloestradiol jest silnie wiązany z albuminami surowicy.
Metabolizm: etynyloestradiol jest metabolizowany do różnych metabolitów hydroksylowych i ich koniugatów glukuronowych i siarczanowych.
Eliminacja: etynyloestradiol jest dalej metabolizowany, a jego metabolity są wydalane przez nerki oraz z kałem. Czas półtrwania eliminacji etynyloestradiolu w stanie stacjonarmym wynosi od 10 do 15 godzin.
Dane niekliniczne nie wskazują na żadne swoiste ryzyko u ludzi, jeśli produkt jest stosowany zgodnie z zaleconym dawkowaniem. Takie wnioski wynikają z konwencjonalnych badań toksyczności po podaniu wielokrotnym, genotoksyczności, potencjalnego działania rakotwórczego oraz toksycznego wpływu na rozród i rozwój potomstwa. Należy jednak pamiętać, że hormony steroidowe mogą pobudzać wzrost niektórych tkanek i guzów hormonozależnych.
Skrobia kukurydziana Laktoza jednowodna Magnezu stearynian Indygotyna (E 132)
Nie dotyczy.
2 lata
Przechowywać w temperaturze poniżej 30°C.
Przechowywać w oryginalnym opakowaniu w celu ochrony przed światłem.
1 lub 3 blistry z folii PVC/PVDC/Aluminium w tekturowym pudełku. 21 tabletek w blistrze.
Nie wszystkie wielkości opakowań muszą znajdować się w obrocie.
Bez specjalnych wymagań.
Exeltis Poland Sp. z o.o. ul. Szamocka 8
01-748 Warszawa
25199
Data wydania pierwszego pozwolenia na dopuszczenie do obrotu: 2019-03-19
18.10.2022 r.











