Spis treści:
- NAZWA PRODUKTU LECZNICZEGO
- SKŁAD JAKOŚCIOWY I ILOŚCIOWY
- POSTAĆ FARMACEUTYCZNA
- SZCZEGÓŁOWE DANE KLINICZNE
- WŁAŚCIWOŚCI FARMAKOLOGICZNE
- DANE FARMACEUTYCZNE
- PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU
- NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
- DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU I DATA PRZEDŁUŻENIA POZWOLENIA
- DATA ZATWIERDZENIA LUB CZĘŚCIOWEJ ZMIANY TEKSTU CHARAKTERYSTYKI PRODUKTU LECZNICZEGO
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
NAZWA PRODUKTU LECZNICZEGO
SKŁAD JAKOŚCIOWY I ILOŚCIOWY
POSTAĆ FARMACEUTYCZNA
SZCZEGÓŁOWE DANE KLINICZNE
Wskazania do stosowania
poważnymi, objawowymi tachyarytmiami komorowymi;
objawowymi tachyarytmiami nadkomorowymi wymagającymi leczenia, takimi jak:
częstoskurcz węzłowy przedsionkowo-komorowy,
tachykardia nadkomorowa w zespole Wolffa-Parkinsona-White'a, lub
napadowe migotanie przedsionków.
Wskazanie to dotyczy pacjentów, którzy nie reagują na leczenie innymi lekami przeciwarytmicznymi lub u których inne leki przeciwarytmiczne nie są wskazane.
Leczenie należy rozpocząć i odpowiednio monitorować wyłącznie w warunkach szpitalnych lub pod nadzorem specjalisty.
Roztwór do wstrzykiwań stosowany jest wyłącznie w szpitalu, gdy konieczne jest uzyskanie szybkiego działania leku lub jeśli podanie doustne jest niemożliwe. Roztwór do wstrzykiwań należy stosować wyłącznie do ropoczęcia leczenia.
Dawkowanie i sposób podawania
Przeciwwskazania
Nadwrażliwość na substancję czynną, jod lub na którąkolwiek substancję pomocniczą wymienioną w punkcie 6.1 (jedna strzykawka zawiera około 112 mg jodu).
Bradykardia zatokowa i blok zatokowo-przedsionkowy.
U pacjentów z ciężkimi zaburzeniami przewodzenia (blok przedsionkowo-komorowy dużego stopnia, blok dwu- lub trójwiązkowy) lub chorobą węzła zatokowego amiodaron można stosować wyłącznie w wyspecjalizowanych ośrodkach i wyłącznie u pacjentów z wszczepionym rozrusznikiem serca.
Pacjenci z zespołem Brugadów.
Zaburzenia czynności tarczycy lub zaburzenia czynności tarczycy w wywiadzie. W razie konieczności, przed rozpoczęciem lecznia, należy wykonać testy czynności tarczycy u wszystkich pacjentów.
Ciężka niewydolność oddechowa, zapaść krążeniowa lub ciężkie niedociśnienie tętnicze; niedociśnienie, niewydolność serca i kardiomiopatia również stanowią przeciwwskazania do stosowania produktu Amiodaron Accord we wstrzyknięciu dożylnym typu bolus.
Jednoczesne stosowanie z innymi lekami, które mogą powodować zaburzenia rytmu serca typu torsade de pointes (patrz punkt 4.5).
Wcześniej istniejące wydłużenie odstępu QT.
Hipokaliemia.
Obrzęk naczynioruchowy w wywiadzie (dziedziczny lub idiopatyczny, np. w wyniku wcześniejszej terapii amiodaronem).
Jednoczesne leczenie inhibitorami MAO.
Ze względu na zawartość alkoholu benzylowego, dożylne podanie amiodaronu jest przeciwwskazane u wcześniaków, noworodków, niemowląt i dzieci w wieku poniżej 3 lat.
Ciąża: tylko w wyjątkowych okolicznościach i jeśli jest to bezwzględnie konieczne (patrz punkt 4.6).
Karmienie piersią (patrz punkt 4.6).
Wszystkie powyższe przeciwwskazania nie dotyczą stosowania amiodaronu w resuscytacji krążeniowo- oddechowej z powodu migotania komór odpornego na defibrylację.
Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania
Może wystąpić bradykardia zatokowa, która może być cięższa u pacjentów w podeszłym wieku lub u pacjentów z zaburzeniami czynności węzła zatokowego.
Leczenie należy przerwać w przypadku ciężkiej bradykardii lub bloku serca.
W wyniku proarytmogennego działania amiodaronu zgłaszano nowe arytmie lub nasilające się epizody leczonych arytmii, które w niektórych przypadkach kończyły się zgonem. W takich przypadkach należy ocenić koniczność przerwania leczenia amiodaronem. Ważne jest również, choć trudne do rozróżnienia, czy wynika to z braku skuteczności leku, który wykazuje działanie proarytmiczne, czy jest to związane z nasileniem zaburzeń rytmu serca. Rzadziej donoszono o działaniu proarytmicznym amiodaronu niż innych leków przeciwarytmicznych a występuje ono zwykle w obecności czynników wydłużających
odstęp QT, takich jak interakcje z lekami i (lub) zaburzenia elektrolitowe (patrz punkty 4.5 i 4.8). Pomimo wydłużenia odstępu QT, amiodaron wykazuje małą aktywność wywoływania zaburzeń rytmu typu torsade de pointes.
W trakcie długotrwałego leczenia (np. po przejściu na leczenie doustne) powinno się przeprowadzać kontrole kardiologiczne w regularnych odstępach (np. standardowe EKG co 1 miesiąc lub długoterminowe EKG co 3 miesiące oraz jeśli to konieczne, wysiłkowe EKG). Jeśli poszczególne parametry ulegną pogorszeniu, np. jeśli zespół QRS lub odstęp QT zostanie wydłużony o więcej niż 25%, lub odstęp PQ
o więcej niż 50%, lub jeśli QT zostanie wydłużony do ponad 500 ms, lub jeśli zwiększy się liczba lub nasilenie jeśli wystąpią zaburzenia rytmu serca, leczenie należy ocenić ponownie.
Pierwotna dysfunkcja przeszczepu (PGD, ang. Primary Graft Dysfunction) po przeszczepie serca:
W badaniach retrospektywnych stosowanie amiodaronu przed przeszczepem serca u biorcy przeszczepu, wykazało zwiększone ryzyko wystąpienia pierwotnej dysfunkcji przeszczepu.
Pierwotna dysfunkcja przeszczepu jest zagrażającym życiu powikłaniem przeszczepu serca, które charakteryzuje się zaburzeniami lewej komory, prawej komory lub zaburzeniami dwukomorowymi
i występuje w ciągu pierwszych 24 godzin po przeszczepie, dla której nie ma możliwej do zidentyfikowania wtórnej przyczyny (patrz punkt 4.8). Ciężka postać PGD może być nieodwracalna.
U pacjentów znajdujących się na liście oczekujących na przeszczep serca należy jak najwcześniej przed przeszczepem rozważyć zastosowanie alternatywnego leku przeciwarytmicznego.
Ciężka bradykardia i blok serca (patrz punkt 4.5)
Podczas stosowania schematów zawierających sofosbuwir jednocześnie z amiodaronem zaobserwowano zagrażające życiu przypadki ciężkiej bradykardii i bloku serca. Bradykardia występowała zwykle w ciągu kilku godzin do dni, ale obserwowano także przypadki, w których ten czas był dłuższy, najczęściej do 2 tygodni od rozpoczęcia leczenia HCV.
Amiodaron należy podawać pacjentom stosującym schemat zawierający sofosbuwir wyłącznie wtedy, gdy stosowanie innych alternatywnych leków przeciwarytmicznych jest przeciwwskazane lub nie są one tolerowane.
Jeśli równoczesne stosowanie amiodaronu jest konieczne, zaleca się monitorowanie czynności serca pacjentów w warunkach szpitalnych przez pierwsze 48 godzin od rozpoczęcia jednoczesnego podawania;
a następnie częstość pracy serca powinna być monitorowana w warunkach ambulatoryjnych lub samodzielnie przez pacjenta, codziennie przez co najmniej pierwsze 2 tygodnie leczenia.
Ze względu na długi okres półtrwania amiodaronu należy również monitorować czynność serca w sposób opisany powyżej u pacjentów, którzy przerwali stosowanie amiodaronu w ciągu ostatnich kilku miesięcy i mają rozpocząć leczenie schematem zawierającym sofosbuwir.
Należy powiadomić wszystkich pacjentów przyjmujących amiodaron w skojarzeniu ze schematem zawierającym sofosbuwir o ryzyku wystąpienia objawów bradykardii i bloku serca oraz o konieczności niezwłocznego zwrócenia się o pomoc lekarską w przypadku ich wystąpienia.
Nadczynność i niedoczynność tarczycy
Podczas leczenia lub do kilku miesięcy po zakończeniu leczenia amiodaronem może wystąpić nadczynność tarczycy. Lekarz powinien zwrócić uwagę na następujące, zwykle łagodne, objawy:
utratę masy ciała, tachykardię, drżenie, nerwowość, zwiększone pocenie się i nietolerancję ciepła, nawrót arytmii lub dusznicy bolesnej, niewydolność serca.
Kliniczne rozpoznanie nadczynności tarczycy jest oparte na wyraźnym zmniejszeniu aktywności hormonu TSH mierzonej metodą wysokoczułą oraz wzrostu stężeń T3 i T4.
W przypadku stwierdzenia nadczynności tarczycy, leczenie produktem Amiodaron Accord należy przerwać. Poprawa wraz z normalizacją wyników badań czynności tarczycy następuje w ciągu kilku miesięcy po zaprzestaniu leczenia.
Ciężkie przypadki (czasami prowadzące do zgonu) wymagają natychmiastowego zastosowania indywidualnego leczenia lekami przeciwtarczycowymi, beta-adrenolitykami i (lub) kortykosteroidami.
Tarczyca
Ze względu na ryzyko wystąpienia dysfunkcji tarczycy (nadczynności lub niedoczynności) podczas leczenia produktem Amiodaron Accord, przed rozpoczęciem leczenia należy wykonać badania czynności tarczycy.
Badania te należy regularnie powtarzać w trakcie leczenia i do około roku po zakończeniu leczenia, a pacjentów badać pod kątem klincznych objawów nadczynności i niedoczynności tarczycy.
Amiodaron zawiera jod i dlatego może wpływać na wychwyt radiojodu. Niemniej jednak wyniki badań czynnościowych tarczycy (fT3, fT4, TSH mierzony metodą ultraczułą usTSH) są możliwe do interpretacji. Amiodaron hamuje konwersję tyroksyny (T4) do trójjodotyroniny (T3) i może prowadzić do wzrostu stężenia T4 i zmniejszenia stężenia T3 u pacjentów w stadium klinicznej eutyreozy. Taka konfiguracja wyników nie powinna prowadzić do przerwania leczenia.
Następujące objawy mogą wskazywać na niedoczynność tarczycy:
Przyrost masy ciała, wrażliwość na zimno, zmęczenie, skrajna bradykardia wykraczająca poza objawy, których można się spodziewać w przypadku leczenia lekiem Amiodaron Accord.
Kliniczne rozpoznanie niedoczynności tarczycy opiera się na stwierdzeniu wyraźnego wzrostu stężenia TSH mierzonego metodą wysokoultraczułą i zmniejszonego stężenia T4. Stadium eutyreozy uzyskuje się zazwyczaj w okresie 1–3 miesięcy od zaprzestania leczenia.
W przypadku stwierdzenia niedoczynności tarczycy dawkę amiodaronu należy w miarę możliwości zmniejszyć i (lub) rozpocząć substytucję lewotyroksyną. W niektórych przypadkach może być konieczne przerwanie leczenia produktem Amiodaron Accord.
Zaburzenia układu oddechowego
Pojawienie się duszności i nieproduktywnego kaszlu może być związane z toksycznym działaniem na płuca, takim jak wystąpienie śródmiąższowego zapalenia płuc lub zapalenie płuc z nadwrażliwości.
Dlatego jeśli to możliwe, przed rozpoczęciem leczenia należy wykonać zdjęcie rentgenowskie klatki piersiowej i badania czynności płuc. W trakcie długotrwałego leczenia (np. po zmianie na amiodaron przyjmowany doustnie) badania te należy powtarzać co 3-6 miesięcy. U pacjentów z ciężkimi chorobami płuc należy częściej badać czynność płuc, ponieważ tacy pacjenci mają gorsze rokowania w przypadku toksycznego działania amiodaronu na płuca.
Bardzo rzadko zgłaszano przypadki śródmiąższowego zapalenia płuc po podaniu amiodaronu w postaci
dożylnej.
U pacjentów, u których wystąpią objawy toksyczności płucnej, takie jak duszność wysiłkowa lub związane z ogólnym pogorszeniem stanu zdrowia (zmęczenie, utrata masy ciała, gorączka), należy wykonać zdjęcie rentgenowskie klatki piersiowej.
W przypadku śródmiąższowego zapalenia płuc należy ponownie ocenić zasadność leczenia amiodaronem, ponieważ śródmiąższowe zapalenie płuc jest zwykle przemijające, jeżeli terapia lekiem zostanie szybko zakończona (kliniczne objawy zwykle ustępują w ciągu 3 do 4 tygodni, zmiany radiologiczne i poprawa czynności płuc następuje w ciągu kilku miesięcy). Należy rozważyć zastosowanie kortykosteroidów (patrz punkt 4.8).
W przypadku zapalenia płuc z nadwrażliwości należy przerwać leczenie amiodaronem i rozpocząć leczenie kortykosteroidami.
Obserwowano bardzo rzadkie przypadki ciężkich powikłań oddechowych, czasem prowadzących do zgonu, występujących zwykle bezpośrednio po zabiegu chirurgicznym (zespół ostrej niewydolności oddechowej dorosłych). Może być to związane z interakcją z tlenem podawanym w dużym stężeniu (patrz punkty 4.5 i 4.8).
Zaburzenia wątroby (patrz punkt 4.8)
Zaleca się bardzo dokładne kontrolowanie czynności wątroby (oznaczenie aktywności aminotransferaz) zaraz po rozpoczęciu leczenia amiodaronem i regularnie w trakcie leczenia.
Zarówno podczas podawania doustnego, jak i dożylnego mogą wystąpić ostre zaburzenia czynności wątroby (w tym ciężka niewydolność komórek wątroby lub czasami niewydolność wątroby prowadząca do zgonu) i przewlekłe zaburzenia czynności wątroby (w przypadku podania dożylnego już w ciągu pierwszych 24 godzin). Dlatego dawkowanie amiodaronu należy zmniejszyć lub zakończyć leczenie, jeśli wzrost aktywności aminotransferaz przekroczy trzykrotność wartości referencyjnych.
Kliniczne i biologiczne objawy przewlekłych zaburzeń czynności wątroby wywołanych doustnym podawaniem amiodaronu mogą być minimalne (żółtaczka cholestatyczna, powiększenie wątroby, aktywność aminotransferaz nawet pięciokrotnie przekraczająca wartości referencyjne) i odwracalne po przerwaniu leczenia; zgłaszano jednak przypadki zakończone zgonem.
Zaburzenia oka (patrz punkt 4.8)
Podczas leczenia amiodaronem wskazane są regularne badania okulistyczne, w tym badanie dna oka i lampą szczelinową. W przypadku niewyraźnego lub osłabionego widzenia należy niezwłocznie wykonać pełne badanie okulistyczne, w tym badanie dna oka. W przypadku wystąpienia neuropatii nerwu wzrokowego
i (lub) zapalenia nerwu wzrokowego należy przerwać leczenie amiodaronem ze względu na możliwość progresji do utraty wzroku.
Ciężkie reakcje skórne
Zagrażające życiu lub nawet prowadzące do zgonu reakcje skórne, takie jak zespół Stevensa-Johnsona (ang. SJS - Stevens-Johnson syndrome), toksyczne martwicze oddzielanie się naskórka (ang. TEN - Toxic Epidermal Necrolysis) (patrz punkt 4.8). Jeśli są obecne przedmiotowe lub podmiotowe objawy SJS, TEN (np. postępująca wysypka skórna często z pęcherzami lub zmianami na błonach śluzowych), należy natychmiast przerwać leczenie amiodaronem.
Zaburzenia nerwowo-mięśniowe (patrz punkt 4.8)
Amiodaron może powodować neuropatie obwodowe i (lub) miopatie. Zwykle objawy ustępują w ciągu kilku miesięcy po odstawieniu, ale w niektórych przypadkach mogą nie być całkowicie odwracalne.
Skóra
Podczas leczenia amiodaronem należy unikać ekspozycji na słońce; dotyczy to również promieniowania UV i solariów. Jeśli nie jest to możliwe, odsłonięte obszary skóry, a zwłaszcza twarz, należy zabezpieczyć maścią o wysokim współczynniku ochrony przeciwsłonecznej. Nawet po zakończeniu leczenia produktem Amiodaron Accord wymagana jest ochrona przeciwsłoneczna przez pewien czas.
Interakcje farmakologiczne (patrz punkt 4.5)
Nie zaleca się jednoczesnego stosowania amiodaronu z następującymi lekami: beta-adrenolityki, antagoniści
kanału wapniowego zwalniające rytm serca (werapamil, diltiazem), drażniące leki przeczyszczające, które mogą powodować hipokaliemię.
Amiodaron podawany dożylnie może być stosowany wyłącznie na oddziałach intensywnej terapii i pod stałym nadzorem (monitorowanie zapisu EKG i ciśnienia tętniczego).
W przypadku, gdy tylko jest to możliwe, amiodaron podawany dożylnie należy stosować przez centralny dostęp żylny, aby uniknąć reakcji niepożądanych w miejscu podania (patrz punkt 4.8).
Należy zachować ostrożność w przypadku niedociśnienia, ciężkiej niewydolności oddechowej, ciężkiej lub niewyrównanej niewydolności serca.
Niedawno odnotowano przypadki hepatotoksycznego działania amiodaronu po podaniu dożylnym, które mogły być spowodowane polisorbatem 80 (substancją pomocniczą o właściwościach emulgujących), a nie samym lekiem.
Dzieci i młodzież: Nie ustalono bezpieczeństwa stosowania i skuteczności amiodaronu u dzieci. Z tego powodu nie zaleca się stosowania amiodaronu u tych pacjentów.
Amiodaron do wstrzykiwań zawiera alkohol benzylowy (20 mg/ml) (patrz punkt 2). Alkohol benzylowy może powodować reakcje toksyczne i anafilaktyczne u dzieci poniżej 3. roku życia.
Po podaniu dożylnym roztworów zawierających ten konserwant zgłaszano występowanie niewydolności oddechowej prowadzącej do zgonu noworodków (ang. „gasping syndrome”). Objawy obejmują nagłe wystąpienie niewydolności oddechowej prowadzącej do zgonu, niedociśnienia tętniczego, bradykardii
i zapaści sercowo-krążeniowej.
Minimalna ilość alkoholu benzylowego, przy której mogą wystąpić objawy toksyczności jest nieznana.
Znieczulenie: Przed zabiegiem chirurgicznym należy poinformować anestezjologa, że pacjent jest leczony amiodaronem (patrz punkt 4.5).
Monitorowanie: Podczas leczenia konieczne jest monitorowanie stężenia potasu i amionotransferaz w surowicy (patrz punkt 4.4).
Zaburzenia elektrolitowe: Hipokaliemia może modyfikować działanie amiodaronu i zwiększać wydłużenie odstępu QT oraz ryzyko wystąpienia zaburzeń rytmu typu torsade de pointes. Przed rozpoczęciem leczenia amiodaronem należy wyrównać niedobór potasu w surowicy.
Ostrzeżenie dotyczące substancji pomocniczych
Ten produkt leczniczy zawiera 200 mg alkoholu benzylowego w każdej 10 ml strzykawce, co odpowiada 20 mg/ml.
Alkohol benzylowy może powodować reakcje toksyczne.
Duże objętości alkoholu benzylowego należy podawać z ostrożnością i tylko w razie koniecznośc u pacjentów z zaburzeniami czynności nerek lub wątroby oraz u kobiet w ciąży lub karmiących piersią, ze względu na ryzyko kumulacji i toksyczności (kwasica metaboliczna).
Interakcje z innymi produktami leczniczymi i inne rodzaje interakcji
leki przeciwarytmiczne klasy Ia, np. chinidyna, prokainamid, dyzopiramid;
leki przeciwarytmiczne klasy III, np. sotalol, bretylium;
leki inne niż przeciwarytmiczne, takie jak winkamina;
podawana dożylnie erytromycyna, kotrimoksazol lub pentamidyna;
niektóre leki przeciwpsychotyczne, np. chloropromazyna, lewomepromazyna, tiorydazyna, flufenazyna, sulpiryd, tiapryd, pimozyd, haloperydol, amisulpryd i sertindol, ponieważ leki te mają działanie arytmogenne i (lub) hamują aktywność CYP3A4 oraz mogą zwiększać stężenie amiodaronu w osoczu;
lit i trójpierścieniowe leki przeciwdepresyjne, np. doksepina, maprotylina, amitryptylina;
niektóre leki przeciwhistaminowe, np. terfenadyna, astemizol, mizolastyna;
leki przeciwmalaryczne, np. chinina, meflochina, chlorochina, halofantryna;
moksyfloksacyna;
inhibiory MAO.
Digoksyna
Podawanie amiodaronu pacjentom przyjmującym digoksynę powoduje zwiększenie stężenia digoksyny w osoczu, a tym samym pojawienie się objawów podmiotowych i przedmiotowych związanych z dużym
stężeniem digoksyny; mogą wystąpić zaburzenia automatyzmu (nasilona bradykardia) i przewodzenia. Zaleca się monitorowanie parametrów klinicznych, biologicznych i EKG, aby nie przeoczyć objawów toksyczności glikozydów nasercowych oraz zmniejeszenie dawki digoksyny o połowę. Możliwe jest również synergistyczne działanie na czynność serca i przewodzenie przedsionkowo-komorowe.
Dabigatran
Należy zachować ostrożność podczas jednoczesnego stosowania amiodaronu z dabigatranem, ze względu na ryzyko krwawienia. Konieczne może być dostosowanie dawki dabigatranu, zgodnie z zaleceniami.
Substraty CYP2C9
Amiodaron zwiększa stężenie w osoczu substratów CYP 2C9, takich jak doustne leki przeciwzakrzepowe (warfaryna, fenprokumon) i fenytoina, poprzez hamowanie enzymu 2C9 cytochromu P450.
Warfaryna i fenprokumon
Połączenie warfaryny i fenprokumonu z amiodaronem może nasilać działanie doustnych leków przeciwzakrzepowych, a tym samym zwiększać ryzyko krwawienia. Zaleca się częstsze kontrolowanie czasu protrombinowego, zarówno podczas leczenia, jak i po zakończeniu leczenia amiodaronem.
Należy odpowiednio zmniejszyć dawkę doustnych leków przeciwzakrzepowych (warfaryny i fenprokumonu).
Fentynoina
Połączenie fenytoiny i amiodaronu może prowadzić do przedawkowania fenytoiny, powodując objawy neurologiczne. Jeśli wystąpią objawy przedawkowania (np. zaburzenia widzenia, drżenie, zawroty głowy) należy zmniejszyć dawkę fenytoiny oraz oznaczyć stężenie fenytoiny w osoczu.
Substraty CYP2D6
Flekainid
Ponieważ flekainid jest metabolizowany głównie przez CYP 2D6, poprzez hamowanie tego enzymu, amiodaron może zwiększać stężenie flekainidu w osoczu. Zaleca się zmniejszenie dawki flekainidu o 50%
i ścisłe monitorowanie stanu pacjenta pod kątem działań niepożądanych. W takich przypadkach jest wysoce zalecane kontrolowanie stężenia flekainidu w osoczu.
Substraty CYP 3A4
Amiodaron jest inhibitorem wątrobowego mikrosomalnego enzymu cytochromu 3A4 (CYP 3A4). To zahamowanie może skutkować nieoczekiwanie wysokim stężeniem innych leków w osoczu, które są metabolizowane przez enzymy CYP 3A4.
Cyklosporyna: w przypadku stosowania skojarzonego, stężenie cyklosporyny w osoczu może zwiększyć się nawet dwukrotnie. Aby utrzymać stężenie cyklosporyny w osoczu w zakresie terapeutycznym konieczne może być zmniejszenie jej dawki.
Statyny: ryzyko toksycznego działania na mięśnie (miopatia, rabdomioliza) jest większe podczas podawania amiodaronu jednocześnie ze statynami metabolizowanymi przez CYP 3A4, takimi jak symwastatyna, atorwastatyna i lowastatyna. Podczas leczenia z amiodaronem należy stosować statyny niemetabolizowane przez CYP450 3A4.
Inne leki metabolizowane przez cytochrom P450 3A4: lidokaina, syrolimus, takrolimus, syldenafil,
fentanyl, midazolam, triazolam, antybiotyki makrolidowe (klarytromycyna), dihydroergotamina, ergotamina i kolchicyna.
Interakcja z substratami innych enzymów CYP P450
Badania in vitro wykazały, że amiodaron może także hamować CYP 1A2, CYP 2C19 i CYP 2D6 poprzez swój główny metabolit. Przewiduje się, iż amiodaron podawany jednocześnie z lekami, których metabolizm zależy od CYP 1A2, CYP 2C19 i CYP 2D6, może zwiększać stężenie tych leków w surowicy.
Wpływ innych produktów leczniczych na amiodaronu chlorowodorek
Inhibitory CYP3A4 i CYP2C8 mogą potencjalnie hamować metabolizm amiodaronu i zwiększać narażenie na amiodaron. Podczas leczenia amiodaronem zalecane jest unikanie inhibitorów CYP 3A4 (np. soku grejpfrutowego i niektórych produktów leczniczych). Podczas doustnego leczenia amiodaronem należy unikać spożywania soku grejpfrutowego.
Inne interakcje z amiodaronem (patrz punkt 4.4)
Jednoczesne podawanie amiodaronu ze schematami zawierającymi sofosbuwir może prowadzić do ciężkiej objawowej bradykardii.
Jeśli nie można uniknąć jednoczesnego podawania, zaleca się monitorowanie pracy serca (patrz punkt 4.4).
Wpływ na płodność, ciążę i laktację
Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn
Działania niepożądane
Bardzo rzadko
trombocytopenia,
niedokrwistość hemolityczna lub aplastyczna.
Częstość nieznana
neutropenia,
agranulocytoza.
Zaburzenia układu immunologicznego
Bardzo rzadko
wstrząs anafilaktyczny.
Częstość nieznana
obrzęk naczynioruchowy (obrzęk Quinckego).
Zaburzenia endokrynologiczne
Często
nadczynność i niedoczynność tarczycy. Zgłaszano przypadki ciężkiej nadczynności tarczycy (w pojedynczych przypadkach zakończonych zgonem) (patrz punkt 4.4).
Bardzo rzadko
zespół nieprawidłowego wydzielania hormonu antydiuretycznego (SIADH).
Zaburzenia psychiczne
Często
zmniejszone libido.
Częstość nieznana
majaczenie (w tym splątanie), omamy.
Zaburzenia układu nerwowego
Często
drżenia pochodzenia pozapiramidowego,
koszmary senne,
zaburzenia snu.
Niezbyt często
czuciowe obwodowe neuropatie i (lub) miopatie, zwykle przemijające po zakończeniu leczenia amiodaronem (patrz punkt 4.4),
zawroty głowy,
problemy z koordynacją,
parestezja.
Bardzo rzadko
nieznaczne zwiększenie ciśnienia wewnątrzczaszkowego (rzekomy guz mózgu),
ataksja móżdżkowa,
ból głowy.
Zaburzenia oka
Bardzo często
mikrozłogi na przedniej powierzchni rogówki (nazywana również rogówką wirowatą), które zwykle są ograniczone do obszaru poniżej źrenicy i mogą powodować zaburzenia widzenia (niewyraźne widzenie, widzenie kolorowych otoczek wokół źródła światła). Mikrozłogi składają się ze złożonych złogów lipidowych i zanikają zwykle 6-12 miesięcy po odstawieniu leku.
Bardzo rzadko
neuropatia / zapalenie nerwu wzrokowego, które może powodować ślepotę (patrz punkt 4.4).
Zaburzenia serca
Często
bradykardia, zazwyczaj umiarkowana.
Niezbyt często
zaburzenia przewodzenia (blok zatokowo-przedsionkowy, blok przedsionkowo-komorowy),
wystąpienie lub nasilenie zaburzeń rytmu serca, czasami z zatrzymaniem czynności serca (patrz punkty 4.4 i 4.5).
Bardzo rzadko
ciężka bradykardia, zatrzymanie czynności węzła zatokowego wymagające przerwania leczenia amiodaronem, szczególnie u pacjentów z zaburzeniem czynności węzła zatokowego i (lub)
u pacjentów w podeszłym wieku.
Częstość nieznana
zaburzenia rytmu typu torsades de pointes (patrz punkty 4.4. i 5.1). Zgłaszano pojedyncze przypadki migotania/trzepotania komór.
Zaburzenia naczyniowe
Często
obniżenie ciśnienia krwi, zwykle umiarkowane i przemijające. Zgłaszano przypadki niedociśnienia lub zapaści po przedawkowaniu lub zbyt szybkim wstrzyknięciu.
Rzadko
zapalenie naczyń.
Bardzo rzadko
uderzenia gorąca.
Zaburzenia układu oddechowego, klatki piersiowej i śródpiersia
Często
zapalenie płuc z nadwrażliwości, zapalenie pęcherzyków płucnych lub śródmiąższowe zapalenie płuc lub zwłóknienie, czasami prowadzące do zgonu (patrz punkt 4.4),
zapalenie opłucnej, zarostowe zapalenie oskrzelików z organizującym się zapaleniem płuc.
Bardzo rzadko
ciężkie powikłania oddechowe (zespół ostrej niewydolności oddechowej dorosłych), czasami zakończone zgonem, zwłaszcza bezpośrednio po zabiegu chirurgicznym (możliwa interakcja z tlenem w dużym stężeniu) (patrz punkty 4.4 i 4.5),
skurcz oskrzeli i (lub) bezdech w przypadku ciężkiej niewydolności oddechowej, zwłaszcza u pacjentów z astmą.
Zaburzenia żołądka i jelit
Bardzo często
nudności, wymioty,
zaburzenia smaku na początku leczenia (zwykle występujące podczas stosowania dawki nasycającej i ustępujące po zmniejszeniu dawki).
Niezbyt zęsto
ból brzucha, wzdęcia,
zaparcia,
jadłowstręt.
Częstość nieznana
zapalenie trzustki / ostre zapalenie trzustki.
Zaburzenia wątroby i dróg żółciowych
Bardzo często
izolowane i często umiarkowane zwiększenie aktywności aminotransferaz w surowicy (1,5 do 3 razy powyżej zakresu wartości prawidłowych) występujące na początku leczenia. Te nieprawidłowości mogą powrócić do wartości prawidłowych po zmniejszeniu dawki leku lub samoistnie.
Często
ostre zaburzenia czynności wątroby z wysoką aktywnością aminotransferaz w surowicy i (lub) żółtaczką, w tym niewydolność wątroby, czasami prowadzące do zgonu (patrz punkt 4.4).
Bardzo rzadko
przewlekła choroba wątroby (w pojedynczych przypadkach zakończona zgonem), marskość wątroby.
Zaburzenia skóry i tkanki podskórnej
Bardzo często
nadwrażliwość na światło ze zwiększoną skłonnością do oparzeń słonecznych, co może prowadzić do rumienia i wysypki skórnej (patrz punkt 4.4).
Często
wyprysk,
długotrwałe leczenie amiodaronem (po przejściu na terapię doustną) może powodować przebarwienia skóry o barwie czarnofioletowej do stalowoszarej (sinica rzekoma), szczególnie w miejscach narażonych na działanie promieni słonecznych. Przebarwienia będą powoli znikały w ciągu 1-4 lat od odstawienia leku.
Bardzo rzadko
pocenie się,
rumień podczas zabiegu radioterapii,
rumień guzowaty,
złuszczające zapalenie skóry,
łysienie.
Częstość nieznana
pokrzywka, ciężkie reakcje skórne, jak toksyczne martwicze oddzielanie się naskórka (TEN) / zespół Stevensa-Johnsona (SJS), pęcherzowe zapalenie skóry, wysypka polekowa z eozynofilią i objawami uogólnionymi (DRESS).
Zaburzenia mięśniowo-szkieletowe i tkanki łącznej
Często
osłabienie mięśni.
Częstość nieznana
ból pleców.
Zaburzenia nerek i dróg moczowych
Rzadko
przejściowe zaburzenia czynności nerek.
Zaburzenia układu rozrodczego i piersi
Bardzo rzadko
zapalenie najądrza,
zaburzenie erekcji.
Zaburzenia ogólne i stany w miejscu podania
Często
reakcje w miejscu wstrzyknięcia, takie jak ból, rumień, obrzęk, martwica, wynaczynienie, naciek, stan zapalny, stwardnienie, zakrzepowe zapalenie żył, zapalenie żył, zapalenie tkanki łącznej, zakażenie, zmiany pigmentacji.
Niezbyt często
zmęczenie.
Badania diagnostyczne
Bardzo rzadko
zwiększenie stężenia kreatyniny we krwi.
Urazy, zatrucia i powikłania po operacji:
Częstość nieznana
pierwotna dysfunkcja przeszczepu po przeszczepie serca (patrz punkt 4.4).
Przedawkowanie
WŁAŚCIWOŚCI FARMAKOLOGICZNE
Właściwości farmakodynamiczne
Dawka nasycająca: 10 do 20 mg/kg mc./dobę przez 7 do 10 dni (lub 500 mg/m2 pc./dobę, jeśli przeliczano na m2).
Dawka podtrzymująca: należy zastosować najmniejszą dawkę skuteczną; w zależności od indywidualnej reakcji pacjenta można zastosować dawki w zakresie od 5 do 10 mg/kg mc./dobę (lub 250 mg/m2 pc./dobę, jeśli przeliczano na m2).
Podanie dożylne:
Dawka nasycająca: 5 mg/kg masy ciała przez 20 minut do 2 godzin.
Dawka podtrzymująca: 10 do 15 mg/kg mc./dobę przez kilka godzin do kilku dni.
Właściwości farmakokinetyczne
Przedkliniczne dane o bezpieczeństwie
DANE FARMACEUTYCZNE
Wykaz substancji pomocniczych
Niezgodności farmaceutyczne
Okres ważności
Specjalne środki ostrożności podczas przechowywania
Rodzaj i zawartość opakowania
Specjalne środki ostrożności dotyczące usuwania i przygotowania produktu leczniczego do stosowania
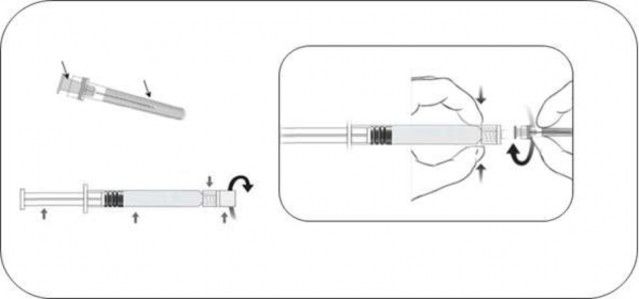
Należy odkręcić szklaną nasadkę ampułko-strzykawki poprzez przekręcenie jej w kierunku przeciwnym do ruchu wskazówek zegara (jak pokazano na rysunku 1).
Należy przymocować igłę do ampułko-strzykawki poprzez delikatne przyłączenie nasadki igły do adaptera Luer Lock i obrócenie jej ćwierć obrotu w prawo, do chwili aż poczuje się zablokowanie igły (jak pokazano na rysunku 2).
Należy ostrożnie zdjąć osłonkę igły, wyciągając ją prosto.
Rozcieńczyć (patrz punkt 4.2) roztworem 5% dekstrozy zgodnie z instrukcją dotyczącą podawania dożylnego.
PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU
NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU I DATA PRZEDŁUŻENIA POZWOLENIA
DATA ZATWIERDZENIA LUB CZĘŚCIOWEJ ZMIANY TEKSTU CHARAKTERYSTYKI PRODUKTU LECZNICZEGO
Amiodaron Accord, 30 mg/ml, koncentrat do sporządzania roztworu do wstrzykiwań/ do infuzji
1 ml roztworu zawiera 30 mg amiodaronu chlorowodorku.
Każda ampułko-strzykawka o pojemności 10 ml zawiera 300 mg amiodaronu chlorowodorku. Substancja pomocnicza o znanym działaniu:
Każda ampułko-strzykawka zawiera 20 mg/ml alkoholu benzylowego. Pełny wykaz substancji pomocniczych, patrz punkt 6.1.
Koncentrat do sporządzania roztworu do wstrzykiwań/ do infuzji. Przejrzysty, bezbarwny do jasnożółtego roztwór, praktycznie bez cząstek. pH 3,0-5,0
Amiodaron Accord wskazany w leczeniu pacjentów dorosłych z:
Dawkowanie
W przypadku napadu lub leczenia początkowego możliwe jest podanie leku we wstrzyknięciu dożylnym lub
infuzji dożylnej. Na ogół nie zaleca się wstrzyknięcia dożylnego. Jeśli to możliwe, zalecana jest infuzja dożylna (patrz także punkt 4.4).
Infuzja dożylna
Dawka początkowa lub w przypadku napadu
Zazwyczaj zalecana dawka to 5 mg/kg masy ciała, podawana w infuzji dożylnej, trwającej od 20 minut do 2 godzin. Lek należy podawać w postaci roztworu rozcieńczonego w 250 ml 5% roztworu dekstrozy 5%.
Działanie terapeutyczne pojawia się w ciągu kilku pierwszych minut i następnie stopniowo słabnie, dlatego w celu jego przedłużenia należy kontynuować podawanie leku w infuzji podtrzymującej.
Dawka podtrzymująca
Do 1200 mg (10-20 mg/kg masy ciała) w infuzji w 250-500 ml dekstrozy 5% na dobę; szybkość infuzji należy dostosować na podstawie reakcji klinicznej (patrz punkt 4.4).
Zmiana podawania dożylnego na doustne
Niezwłocznie po uzyskaniu właściwej reakcji należy równolegle rozpocząć leczenie doustne, podając zazwyczaj stosowaną dawkę nasycającą. Amiodaron Accord należy odstawiać stopniowo.
Wstrzyknięcie dożylne (patrz punkt 4.4)
W sytuacjach nagłych lek można podać – według uznania lekarza – w powolnym dożylnym wstrzyknięciu w dawce 150-300 mg (5 mg/kg masy ciała) w 10-20 ml dekstrozy 5%, trwającym co najmniej 3 minuty. Nie należy tego powtarzać przez co najmniej 15 minut, nawet jeśli przy pierwszym wstrzyknięciu nie została podana dawka maksymalna. Pacjentów otrzymujących amiodaron w ten sposób należy bardzo dokłanie monitorować, np. w oddziale intensywnej terapii (patrz punkt 4.4).
Resuscytacja krążeniowo-oddechowa w leczeniu migotania komór opornego na defibrylację
Dożylna dawka początkowa wynosi 300 mg (lub 5 mg/kg masy ciała) rozcieńczona w 20 ml dekstrozy 5%, podana w szybkim wstrzyknięciu. Jeżeli migotanie komór nie ustąpi, można rozważać podanie dodatkowej dawki 150 mg dożylnie (lub 2,5 mg/kg masy ciała).
Dzieci i młodzież
Nie ustalono bezpieczeństwa stosowania i skuteczności amiodaronu u dzieci i młodzieży. Obecnie dostępne dane zostały opisane są w punktach 5.1 i 5.2 ale brak jest zaleceń dotyczących dawkowania.
Ze względu na obecność alkoholu benzylowego, przeciwwskazane jest podawanie dożylne produktu Amiodaron Accord wcześniakom, noworodkom, niemowlętom i dzieciom w wieku do 3 lat (patrz punkt 4.3).
Pacjenci w podeszłym wieku
Podobnie jak w przypadku wszystkich pacjentów, ważne jest, aby stosować najmniejszą skuteczną dawkę. Chociaż brak danych dotyczących innych zaleceń odnośnie dawkowania w tej grupie pacjentów, pacjenci w podeszłym wieku mogą być bardziej podatni na bradykardię i zaburzenia przewodzenia, w przypadku zastosowania zbyt dużej dawki. Szczególną uwagę należy zwrócić na monitorowanie czynności tarczycy (patrz punkty 4.3, 4.4 i 4.8).
Zaburzenia czynności wątroby i nerek
Chociaż podczas długotrwałego stosowania doustnego amiodaronu u pacjentów z zaburzeniami czynności nerek lub wątroby nie stwierdzono konieczności dostosowania dawkowania, należy bardzo dokładnie monitorować stan kliniczny pacjentów w podeszłym wieku, np. w oddziale intensywnej terapii.
Sposób podawania
Przed podaniem dożylnym, amiodaron musi być rozcieńczony zgodnie z instrukcją powyżej.
W przypadku powolnych wstrzyknięć dożylnych (tylko w stanach nagłych) amiodaron musi być dodatkowo rozcieńczony 10 lub 20 ml 5% dekstrozy w zależności od podanej dawki i wskazania. Na przykład:
w przypadku resuscytacji krążeniowo-oddechowej, rozcieńczyć zawartość jednej strzykawki (300 mg/10 ml) dodatkowo z 20 ml 5% dekstrozy.
Wyłącznie do jednorazowego użytku.
W infuzji należy używać jedynie 5% roztworu dekstrozy (patrz punkt 6.2).
Instrukcje dotyczące rozcieńczania produktu leczniczego przed podaniem znajdują się w punkcie 6.6. Aby uniknąć zapalenia żył, podczas infuzji ciągłej należy założyć centralny cewnik żylny.
Amiodaron Accord jest podawany tylko w celu rozpoczęcia leczenia, nie dłużej niż przez tydzień.
Patrz także punkt 4.3.
Wstrzyknięcie dożylne jest generalnie odradzane ze względu na ryzyko hemodynamiczne (ciężkie niedociśnienie, zapaść krążeniowa); dlatego, gdy tylko jest to możliwe, preferowana jest infuzja dożylna.
Wstrzyknięcie dożylne powinno być ograniczone do sytuacji nagłych, gdy inne alternatywne terapie nie są skuteczne. Amioradon można podawać wyłącznie na oddziale intensywnej opieki i pod stałym nadzorem (monitorowanie zapisu EKG i ciśnienia tętniczego).
Dawka wynosi około 5 mg/kg masy ciała. Z wyjątkiem przypadków resuscytacji krążeniowo-oddechowej związanej z migotaniem komór, gdy defibrylacja nie jest skuteczna amiodaron powinien być podawany we wstrzyknięciu dożylnym trwającym co najmniej 3 minuty. Następne wstrzyknięcie można powtórzyć nie
wcześniej niż po 15 minutach, nawet jeśli przy pierwszym wstrzyknięciu nie została podana dawka maksymalna (ryzyko wystąpienia nieodwracalnej zapaści krążeniowej).
Nie należy mieszać innych leków z amiodaronem w tej samej strzykawce. Nie należy wstrzykiwać innych leków w ten sam dostęp żylny. Jeżeli konieczne jest przedłużenie leczenia, należy to zrobić w formie infuzji dożylnej.
Zaburzenia czynności serca:
Leki wywołujące zaburzenia rytmu serca typu torsade do pointes:
Leczenie skojarzone z lekami wywołującymi zaburzenia rytmu serca typu torsade do pointes jest przeciwwskazane (patrz punkt 4.3), na przykład:
Leki wydłużające odstęp QT
Podczas jednoczesnego podawania amiodaronu i leków o działaniu wydłużającym odstęp QT należy dokładnie ocenić stosunek korzyści do ryzyka u każdego pacjenta, ponieważ może zwiększyć się ryzyko zaburzeń rytmu serca typu torsade de pointes. Należy monitorować wydłużenie odstępu QT.
Fluorochinolony
U pacjentów przyjmujących amiodaron jednocześnie z fluorochinolonami zgłaszano rzadkie przypadki wydłużenia odstępu QTc z wystąpieniem zburzeń rytmu serca typu torsade de pointes lub bez tych zaburzeń.
Należy unikać jednoczesnego podawania amiodaronu i fluorochinolonów (jednoczesne stosowanie z moksyfloksacyną jest przeciwwskazane, patrz powyżej).
Leki zwalniające czynność serca, powodujące zaburzenia automatyzmu lub przewodzenia serca Nie zaleca się leczenia skojarzonego z następującymi lekami:
Beta-adrenolityki i niektórzy antagoniści kanału wapniowego (diltiazem, werapamil); może wystąpić nasilenie działania chronotropowego ujemnego i spowolnienie przewodzenia.
Leki powodujące hipokaliemię
Drażniące leki przeczyszczające mogą powodować hipokaliemię, zwiększając w ten sposób ryzyko wystąpienia zaburzeń rytmu serca typu torsade de pointes; należy stosować inne rodzaje środków przeczyszczających.
Należy zachować ostrożność w przypadku jednoczesnego stosowania następujących leków, które również mogą prowadzić do hipokaliemii i (lub) hipomagnezemii: leków moczopędnych stosowanych pojedynczo lub w skojarzeniu (np. z hydrochlorotiazydem, furosemidem), kortykosteroidów stosowanych ogólnoustrojowo (glikokortkoidy, mineralokortykoidy), tetrakozaktydu, amfoterycyny B podawanej dożylnie.
W przypadku hipokaliemii należy podjąć działania naprawcze i monitorować odstęp QT. W przypadku wystąpienia zaburzeń rytmu typu torsade de pointes nie należy stosować leków przeciwarytmicznych; można wdrożyć stymulację oraz podać dożylnie magneze.
Znieczulenie ogólne (patrz punkty 4.4 i 4.8)
Zaleca się zachowanie ostrożności u pacjentów poddawanych znieczuleniu ogólnemu lub otrzymujących tlenoterapię w dużych dawkach.
U pacjentów przyjmujących amiodaron poddawanych znieczuleniu ogólnemu zgłaszano potencjalnie ciężkie powikłania: bradykardia nie odpowiadająca na atropinę, niedociśnienie tętnicze, zaburzenia przewodzenia, zmniejszona pojemność minutowa serca.
Obserwowano kilka przypadków zespółu ostrej niewydolności oddechowej dorosłych, zwykle występujących w okresie bezpośrednio po zabiegu chirurgicznym. Może to być związane z interakcją z tlenem podawanym w dużym stężeniu. Należy poinformować anestezjologa, że pacjent przyjmuje amiodaron.
Wpływ amiodaronu chlorowodorku na inne produkty lecznicze
Amiodaron i (lub) jego metabolit, deetyloamiodaron, hamują CYP1A1, CYP1A2, CYP3A4, CYP2C9, CYP2D6 i glikoproteinę P i mogą zwiększać narażenie na ich substraty. Ze względu na długi okres półtrwania amiodaronu, interakcje można obserwować przez kilka miesięcy po odstawieniu tego leku.
Substraty glikoproteiny P
Amiodaron jest inhibitorem glikoproteiny P. Przypuszcza się, że jednoczesne stosowanie amiodaronu z substratami glikoproteiny P wiąże się ze zwiększeniem narażenia na te substraty.
Ciąża
Dane dotyczące narażenia na lek podczas ciąży są nieliczne. Amiodaron i N-desetyloaminodaron przenikają przez barierę łożyskową i osiągają u niemowląt stężenie odpowiadające 10–25% stężenia w osoczu matki.
Najczęstsze powikłania to zaburzenia wzrostu, poród przedwczesny i zaburzenia czynności tarczycy
u noworodków. U około 10% noworodków obserwowano niedoczynność tarczycy, bradykardię i wydłużenie odstępu QT. W pojedynczych przypadkach stwierdzono powiększenie tarczycy lub szmery sercowe. Wydaje się, że częstość występowania wad wrodzonych nie jest zwiększona. Należy jednak pamiętać o możliwości wystąpienia wad serca. W związku z tym nie należy stosować amiodaronu w czasie ciąży, chyba że jest to bezwzględnie konieczne. Należy wówczas ocenić, czy ryzyko nawrotu arytmii zagrażających życiu przeważa nad możliwym zagrożeniem dla płodu. Biorąc pod uwagę długi okres półtrwania amiodaronu, kobiety
w wieku rozrodczym powinny planować zajście w ciążę co najmniej pół roku po zakończeniu leczenia, aby uniknąć narażenia zarodka/płodu podczas wczesnego okresu ciąży.
Amiodaron jest przeciwwskazany w okresie ciąży, z wyjątkiem szczególnych okoliczności (patrz punkt 4.3). Karmienie piersią
Zarówno amiodaron, jak i jego czynny metabolit przenikają do mleka matki w znacznych ilościach. Karmienie
piersią jest przeciwwskazane podczas leczenia amiodaronem. Jeśli konieczne jest leczenie w okresie laktacji lub jeśli amiodaron był przyjmowany w czasie ciąży, należy przerwać karmienie piersią. Jeśli w okresie laktacji wymagane jest leczenie amiodaronem lub jeżeli lek był przyjmowany w czasie ciąży, należy przerwać karmienie piersią.
Płodność
U mężczyzn po długotrwałym leczeniu stwierdzono podwyższone stężenia hormonu luteinizującego (LH) i hormonu folikulotropowego (FSH) w surowicy, co wskazuje na zaburzenie czynności jąder.
Amiodaronu chlorowodorek może wpływać na zdolność prowadzenia pojazdów i obsługiwania maszyn. Leczenie tym lekiem wymaga regularnej kontroli lekarskiej. Ten produkt leczniczy, nawet stosowany zgodnie z przeznaczeniem, może zmieniać czas reakcji do takiego stopnia, że może zaburzać zdolność aktywnego uczestnictwa w ruchu drogowym, obsługi maszyn lub bezpiecznej pracy. Może to wystąpić w szczególności przy rozpoczynaniu leczenia, zwiększaniu dawki, zmianie leku, a także w połączeniu z alkoholem.
Działania niepożądane wynikające ze stosowania amiodaronu występują często, szczególnie toksyczne uszkodzenie serca, płuc i wątroby. Czasami objawy te są zależne od dawki i odwracalne po jej zmniejszeniu.
Działania niepożądane przedstawione są według malejącej ciężkości w obrębie każdej grupy częstości występowania.
Częstość występowania działań niepożądanych wymienionych poniżej została określona zgodnie z następującą konwencją:
bardzo często (≥1/10); często (≥1/100 do <1/10);
niezbyt często (≥1/1 000 do <1/100); rzadko (≥1/10 000 do <1/1 000); bardzo rzadko (<1/10 000);
częstość nieznana (nie może być określona na podstawie dostępnych danych).
Zaburzenia krwi i układu chłonnego
Inne możliwe działania niepożądane
Rzadko mogą wystąpić reakcje nadwrażliwości na alkohol benzylowy.
Zgłaszanie podejrzewanych działań niepożądanych
Po dopuszczeniu produktu leczniczego do obrotu istotne jest zgłaszanie podejrzewanych działań niepożądanych. Umożliwia to nieprzerwane monitorowanie stosunku korzyści do ryzyka stosowania produktu leczniczego. Osoby należące do fachowego personelu medycznego powinny zgłaszać wszelkie podejrzewane działania niepożądane za pośrednictwem Departamentu Monitorowania Niepożądanych Działań Produktów Leczniczych Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych
Al. Jerozolimskie 181C 02-222 Warszawa
tel.: + 48 22 49 21 301
faks: + 48 22 49 21 309
strona internetowa: https://smz.ezdrowie.gov.pl
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Brak danych na temat przedawkowania amiodaronu podawanego dożylnie.
W przypadku ostrego przedawkowania lub zbyt szybkiego podania dożylnego mogą wystąpić: nudności, wymioty, zaparcia, pocenie się, bradykardia, zaburzenia przewodzenia i wydłużenie odstępu QT. Po znacznym przedawkowaniu może również wystąpić niedociśnienie, blok serca i zaburzenia rytmu serca typu torsades de pointes. W wyjątkowych przypadkach może wystąpić nadczynność tarczycy.
Po znacznym przedawkowaniu należy prowadzić przedłużone monitorowanie zapisu EKG. Należy rozważyć przyjęcie pacjenta na oddział intensywnej terapii. Niedociśnienie można wyrównać podając w infuzji płyny lub leki wazopresyjne. Wskazane może być zastosowanie alfa- lub beta-adrenomimetyków lub czasowa stymulacja. Należy unikać podawania leków przeciwarytmicznych klasy Ia i III, ponieważ powodują one wydłużenie odstępu QT i sprzyjają wystąpieniu zaburzeń rytmu serca typu torsades de pointes. Należy stosować leczenie podtrzymujące i objawowe. Pacjenta należy monitorować, a w przypadku wystąpienia bradykardii, można podać leki beta-adrenostymulujące lub glukagon. Mogą również wystąpić samoistnie ustępujące napady częstoskurczu komorowego. Zgłaszano przypadki niewydolności krążenia i wątroby.
Bradykardia wywołana wstrzyknięciem amiodaronu jest oporna na atropinę.
Ze względu na farmakokinetykę amiodaronu należy odpowiednio i przez długi czas kontrolować stan pacjenta, szczególnie czynność serca. Ani amiodaronu, ani jego metabolitów nie można usunąć za pomocą dializy.
Grupa farmakoterapeutyczna: leki nasercowe, leki przeciwarytmiczne, klasa III Kod ATC: C01BD01
Mechanizm działania
Amiodaron jest dwujodową pochodną benzofuranu i jest zaliczany do leków przeciwarytmicznych klasy III, ze względu na zdolność do wydłużania czasu trwania potencjału czynnościowego serca w miocytach przedsionkowych i komorowych poprzez hamowanie czynności kanałów potasowych K+ w sercu (zablokowanie głównie szybkiego komponentu opóźnionego potasowego prądu prostującego, IKr). Wydłuża tym samym okres refrakcji potencjału czynnościowego, powodując hamowanie arytmii ektopowych
i nawrotnych oraz wydłużenie odstępu QTc w EKG. Ponadto, amiodaron hamuje również kanały sodowe Na+ (efekt klasy I) oraz kanały wapniowe Ca2+ (efekt klasy IV) w sercu. To ostatnie działanie może prowadzić do spowolnienia przewodzenia w węźle zatokowo-przedsionkowym i przedsionkowo-komorowym.
Wydaje się, że podczas długotrwałego podawania, amiodaron hamuje również migrację kanałów jonowych z retikulum endoplazmatycznego do błony komórkowej w kardiomiocytach, w związku z czym może wykazywać działanie elektrofizjologiczne podczas długotrwałego podawania.
Właściwości farmakodynamiczne
Amiodaron jest niekompetycyjnym antagonistą zarówno receptorów beta-, jak i alfa- adrenergicznych,
a zatem wywiera działanie hemodynamiczne: rozszerza tętnice wieńcowe i naczynia obwodowe, co prowadzi do obniżenia ciśnienia tętniczego. Wydaje się, że właściwości beta- adrenolityczne amiodaronu powodują ujemne działanie inotropowe, chronotropowe i dromotropowe.
Niektóre działania amiodaronu przypominają skutki niedoczynności tarczycy, co może wynikać z zahamowania syntezy hormonu tarczycy. Amiodaron jest silnym inhibitorem aktywności
5’-monodejodynazy jodotyroniny (głównego enzymu konwertującego T4-T3). U szczurów obserwowano zwiększenie stężenia hormonu stymulującego tarczycę (TSH), tyroksyny (T4) i trijodotyroniny odwrotnej (rT3) w surowicy oraz zmniejszenie stężenia trijodotyroniny (T3) w surowicy w wyniku zahamowania dejodynacji T4 do T3. To działanie przeciwtarczycowe amiodaronu może przyczynić się do jego działania elektrofizjologicznego na serce.
Główny metabolit, N-deetyloamiodaron, wykazuje wpływ elektrofizjologiczny na serce podobny do substancji macierzystej.
Skuteczność kliniczna i bezpieczeństwo stosowania
Bezpieczeństwo i skuteczność amiodaronu podawanego dożylnie u pacjentów z zatrzymaniem krążenia w warunkach pozaszpitalnych, w wyniku migotania komór odpornego na defibrylację, oceniano w dwóch
badaniach z podwójnie ślepą próbą: badaniu ARREST, w którym porównywano amiodaron z placebo oraz badaniu ALIVE, w którym porównywano amiodaron z lidokainą. Pierwszorzędowym punktem końcowym obu badań była liczba pacjentów, którzy przeżyli do momentu przyjęcia do szpitala.
W badaniu ARREST 504 pacjentom z pozaszpitalnym zatrzymaniem krążenia w wyniku migotania komór lub częstoskurczu komorowego bez tętna, opornego na 3 lub więcej defibrylacji i epinefrynę podano albo 300 mg amiodaronu rozcieńczonego w 20 ml glukozy 5% w szybkim wstrzyknięciu do żyły obwodowej (246 pacjentów) albo placebo (258 pacjentów). U 197 pacjentów (39%), którzy przeżyli transport do szpitala,
amiodaron znacznie zwiększył szanse resuscytacji i hospitalizacji: 44% w grupie leczonej amiodaronem, w porównaniu do 34% w grupie otrzymującej placebo (p = 0,03).
Po skorygowaniu o inne niezależne czynniki prognostyczne, skorygowany współczynnik przeżycia do momentu przyjęcia do szpitala wynosił 1,6 (95% przedział ufności, 1,1 - 2,4; p = 0,02) w grupie otrzymującej amiodaron w porównaniu z grupą placebo. Częstość występowania niedociśnienia (59% w stosunku do 25%, p = 0,04) i bradykardii (41% w porównaniu do 25%, p = 0,004) była większa u pacjentów otrzymujących amiodaron niż u pacjentów otrzymujących placebo.
W badaniu ALIVE 347 pacjentów z migotaniem komór opornym na trzy defibrylacje, epinefrynę podaną dożylnie i kolejną defibrylację lub z migotaniem komór nawracającym po początkowej udanej defibrylacji zostało poddanych randomizacji do grup, w których stosowano amiodaron (5 mg/kg szacowanej masy ciała, rozpuszczone w 30 ml 5% glukozy) z placebo odpowiadającym lidokainie, lub lidokainę (1,5 mg/kg
w stężeniu 10 mg/ml) z placebo odpowiadającym amiodaronowi, zwierającym ten sam rozpuszczalnik (polisorbat 80).
Spośród 347 pacjentów włączonych do badania, w przypadku podania amiodaronu uzyskano istotny wzrost szans na skuteczną resuscytację i przyjęcie do szpitala: 22,8% w grupie otrzymującej amiodaron (41 spośród 180 pacjentów) w porównaniu do 12% w grupie otrzymującej lidokainę (20 spośród 167 pacjentów), p=0,009. Po skorygowaniu o inne czynniki wpływające na prawdopodobieństwo przeżycia, skorygowany współczynnik przeżycia do momentu przyjęcia do szpitala wynosił 2,49 (95% przedział ufności, 1,28-4,85; p=0,007). Nie stwierdzono różnic pomiędzy grupami otrzymującymi amiodaron i lidokainę w zakresie odsetka pacjentów, którzy wymagali leczenia bradykardii z zastosowaniem atropiny lub leczenia presyjnego z zastosowaniem dopaminy, lub w zakresie odsetka chorych, którzy otrzymali lidokainę w badaniu otwartym.
Odsetek pacjentów, u których po defibrylacji utrzymało się zatrzymanie krążenia po podaniu pierwszego badanego leku, był istotnie większy w grupie otrzymującej lidokainę (28,9%) niż w grupie otrzymującej amiodaron (18,4%), p=0,04.
Dzieci i młodzież:
Nie przeprowadzono kontrolowanych badań z udziałem dzieci i młodzieży.
W opublikowanych badaniach, bezpieczeństwo amiodaronu oceniano u 1118 pacjentów pediatrycznych, z różnego typu zaburzeniami rytmu serca. W badaniach klinicznych z udziałem pacjentów pediatrycznych zastosowano następujące dawki.
Podanie doustne:
W razie konieczności można jednocześnie rozpocząć leczenie doustne, stosując zwykłą dawkę nasycającą.
Farmakokinetyka amiodaronu jest nietypowa oraz złożona i nie została w pełni wyjaśniona. Podanie dożylne
Wchłanianie
Po wstrzyknięciu maksymalne działanie osiąga się po 15 minutach.
Dystrybucja
Po tym czasie następuje dystrybucja do tkanek i szybkie zmniejszanie stężenia leku w osoczu, w ciągu 4 godzin.
Aby uzyskać wysycenie tkanki, należy kontynuować leczenie dożylnie lub doustnie. Podczas fazy wysycania amiodaron gromadzi się zwłaszcza w tkance tłuszczowej. Stan równowagi dynamicznej osiąga się w okresie od jednego do kilku miesięcy.
Ze względu na te właściwości, należy podać zalecaną dawkę nasycającą, aby osiągnąć szybkie wysycenie tkanki, co jest warunkiem skuteczności terapeutycznej. Amiodaron silnie wiąże się z białkami osocza
(> 95%).
Badanie przeprowadzone zarówno na zdrowych ochotnikach, jak i osobach chorych, którym dożylnie podano amiodaron wykazało, że wyliczone objętości dystrybucji oraz całkowity klirens krwi przy wykorzystaniu modelu dwukompartmentowego były podobne w obu grupach. Eliminacja amiodaronu po dożylnym podaniu okazała się zgodna z rozkładem dwuwykładniczym z fazą dystrybucji trwającą około 4 godzin. Bardzo duża objętość dystrybucji w połączeniu ze stosunkowo niewielką pozorną objętością w kompartmencie centralnym wskazuje na znaczne rozmieszczenie tkankowe.
Średnie wartości dystrybucji amiodaronu po podaniu dożylnym dawki pojedynczej (5 mg/kg mc. w ciągu
15 minut) są następujące: objętość dystrybucji centralnej 0,2 l/kg, a w fazie stacjonarnej: 40-84 l/kg. Objętość dystrybucji w fazie stacjonarnej dla jego aktywego metabolitu: 68-168 l/kg).
Metabolizm
Amiodaron jest głównie metabolizowany przez CYP 3A4, a także przez CYP 2C8.
Amiodaron i jego metabolit, deetyloamiodaron, wykazuje in vitro potencjał hamowania CYP 1A1,
CYP 1A2, CYP 2C9, CYP 2C19, CYP 2D6, CYP 3A4, CYP 2A6, CYP 2B6 oraz 2C8. Amiodaron
i deetyloamiodaron mają również potencjał hamowania niektórych transporterów takich jak glikoproteina P i organiczne transportery kationowe (OCT2) [jedno badanie wykazało 1,1% wzrostu stężenia kreatyniny (substratu OCT2) w surowicy].
Dane in vitro opisują interakcje amiodaronu z substratami CYP 3A4, CYP 2C9, CYP 2D6 oraz glikoproteiny P.
Głównym aktywnym metabolitem amiodaronu u ludzi jest deetyloamiodaron (DEA). Uważa się, że enzymem odpowiedzialnym za desetylację jest cytochrom P450 3A4.
Eliminacja
Amiodaronu chlorowodorek ma długi okres półtrwania, który wykazuje zmienność międzyosobniczą i wynosi od 20 do 100 dni.
Eliminowany jest głównie przez wątrobę z żółcią. 10% substancji jest wydalane z moczem.
Ze względu na niewielką eliminację przez nerki, pacjentom z niewydolnością nerek można podawać zazwyczaj stosowaną dawkę.
Po odstawieniu amiodaron jest wydalany przez kilka miesięcy.
Średnie wartości eliminacji amiodaronu po podaniu dożylnym dawki pojedynczej (5 mg/kg mc. w ciągu 15 minut) są następujące: klirens: 90-158 ml/h/kg i t½: 20-47 dni. Klirens dla jego aktywnego metabolitu: 197-290 ml/h/kg i t½ = t½ amiodaronu.
Badanie przeprowadzone zarówno na zdrowych ochotnikach, jak i osobach chorych, którym dożylnie podano amiodaron wykazało, że wyliczone objętości dystrybucji oraz całkowity klirens krwi przy wykorzystaniu modelu dwukompartmentowego były podobne w obu grupach. Eliminacja amiodaronu po dożylnym podaniu okazała się zgodna z rozkładem dwuwykładniczym. Okres półtrwania po podaniu 400 mg amiodaronu
w szybkim wstrzyknięciu dożylnym (bolusie) wyniósł w przybliżeniu 11 godzin.
Wiek, płeć, zaburzenia czynności nerek lub wątroby nie mają znaczącego wpływu na dystrybucję amiodaronu lub jego aktywnego metabolitu.
Dzieci i młodzież
Nie przeprowadzono kontrolowanych badań z udziałem dzieci i młodzieży. Ograniczone dostępne dane dotyczące dzieci i młodzieży nie wykazują różnic w porównaniu do danych dla pacjentów dorosłych.
W badaniach toksyczności po podaniu dawek wielokrotnych, amiodaron powodował uszkodzenie płuc (zwłóknienie, fosfolipidozę; u chomików, szczurów i psów). Toksyczny wpływ na płuca wynika
z powstawania rodników i zaburzeń wytwarzania energii w komórkach. Ponadto amiodaron powodował uszkodzenie wątroby u szczurów, psów, świń i pawianów. Amiodaron miał pośredni wpływ na lipidy
w surowicy poprzez zmiany stężeń hormonów tarczycy w osoczu.
W ramach badania genotoksyczności przeprowadzono badanie in vitro Ames oraz in vivo badanie mikrojąder komórek szpiku kostnego myszy. Wyniki obu badań były negatywne.
Amiodaronu chlorowodorek jest substancją silnie fototoksyczną. Istnieją dowody, że cytotoksyczne wolne rodniki powstają w obecności amiodaronu chlorowodorku pod wpływem promieniowania UV. To nie tylko prowadzi do ostrych reakcji fototoksycznych, ale także do uszkodzenia DNA (fotomutagenność), a następnie do skutków fotokarcynogennych. Do tej pory nie badano eksperymentalnie tych potencjalnie ciężkich działań niepożądanych amiodaronu chlorowodorku. Dlatego nie jest znany potencjał fotomutagenny
i fotokarcynogenny amiodaronu.
W trwającym dwa lata badaniu rakotwórczości na szczurach, amiodaron powodował istotne klinicznie zwiększenie liczby guzów pęcherzykowych tarczycy (gruczolaki i (lub) raki) u obu płci. Ponieważ nie stwierdzono działania mutagennego, przypuszcza się, że do indukcji tego typu nowotworu dochodzi raczej w wyniku mechanizmu epigenetycznego niż działania genotoksycznego. Nie odnotowano powstawania
nowotworów u myszy, zaobserwowano jednak zależny od dawki rozrost pęcherzykowy tarczycy. To działanie na tarczycę u szczurów i myszy wynika najprawdopodobniej z wpływu amiodaronu na syntezę i (lub) uwalnianie hormonów tarczycy. Znaczenie tych obserwacji w odniesieniu do ludzi jest małe.
W badaniach toksyczności reprodukcyjnej u szczurów amiodaron wykazał potencjalny niekorzystny wpływ na płodność i rozwój pourodzeniowy. Amiodaron był embriotoksyczny, ale nie teratogenny u szczurów
i królików w klinicznie istotnych dawkach.
Alkohol benzylowy Polisorbat 80
Woda do wstrzykiwań
Amiodaron jest niekompatybilny z roztworem soli.
Amiodaron może prowadzić do uwalniania substancji zmiękczającej DEHP (ftalan dwu-2- etyloheksylu) do roztworu w przypadku stosowania sprzętu medycznego zawierającego DEHP. W celu zminimalizowania narażenia na DEHP należy podawać amiodaron w roztworze do infuzji stosując zestawy niezawierające
DEHP.
Nie mieszać produktu leczniczego z innymi produktami leczniczymi, oprócz wymienionych w punkcie 6.6.
2 lata
Po rozcieńczeniu wykazano chemiczną i fizyczną stabilność roztworu przez 3 godziny, 48 godzin i 15 minut w stężeniu odpowiednio 1,2 mg/ml, 2,4 mg/ml i 15 mg/ml w temperaturze 20-25°C. Z mikrobiologicznego punktu widzenia produkt należy zużyć natychmiast. Jeśli nie zostanie zużyty natychmiast, za czas i warunki przechowywania przed użyciem odpowiada użytkownik.
Nie przechowywać w temperaturze powyżej 25°C. Przechowywać ampułko-strzykawkę w opakowaniu zewnętrznym w celu ochrony przed światłem.
Warunki przechowywania produktu leczniczego po rozcieńczeniu, patrz punkt 6.3.
Ampułko-strzykawka o pojemności 10 ml z bezbarwnego szkła typu I, z korkiem z gumy bromobutylowej i tłokiem z polipropylenu, w tekturowym pudełku.
Ampułko-strzykawka ma podziałkę na ml do 10 ml. Wielkości opakowania: 1 ampułko-strzykawka
Przed użyciem należy ocenić wzrokowo jałowy koncentrat, uwzględniając przejrzystość, obecność cząstek stałych i integralność pojemnika. Roztwór można zastosować tylko wtedy, gdy jest przezroczysty, bezbarwny do bladożółtego, a pojemnik nieuszkodzony i nienaruszony.
Instrukcje dotyczące przygotowania i podania leku
Nasadka igły
Igła
Osłonka na igłę
Ampułko-strzykawka
Tłok ampułko- strzykawki
Korpus ampułko- strzykawki
Rysunek 1
Nasadka na ampułko- strzykawkę
Rysunek 2
Adapter Luer Lock
Przed podaniem w infuzji dożylnej produkt leczniczy Amiodaron Accord musi być rozcieńczyczony zgodnie z instrukcją w 5% roztworze dekstrozy. Jedną ampułko-strzykawkę Amiodaron Accord należy rozcieńczyć zgodnie z zaleceniami w 500 ml 5% roztworu dekstrozy, aby uzyskać stężenie 0,6 mg/ml amiodaronu chlorowodorku.
Ze względu na stabilność roztworu, nie należy stosować stężeń poniżej 0,6 mg/ml i nie należy dodawać innych produktów leczniczych do płynu infuzyjnego.
Wszelkie niewykorzystane resztki produktu leczniczego lub jego odpady należy usunąć zgodnie z lokalnymi przepisami.
Tylko do jednorazowego użytku.
Accord Healthcare Polska Sp. z o.o. ul. Taśmowa 7
02-677 Warszawa
Data wydania pierwszego pozwolenia na dopuszczenie do obrotu:











