Spis treści:
- NAZWA I ADRES PODMIOTU ODPOWIEDZIALNEGO ORAZ WYTWÓRCY ODPOWIEDZIALNEGO ZA ZWOLNIENIE SERII, JEŚLI JEST INNY
- NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
- ZAWARTOŚĆ SUBSTANCJI CZYNNEJ (-CH) I INNYCH SUBSTANCJI
- WSKAZANIA LECZNICZE
- PRZECIWWSKAZANIA
- DZIAŁANIA NIEPOŻĄDANE
- DOCELOWE GATUNKI ZWIERZĄT
- DAWKOWANIE DLA KAŻDEGO GATUNKU, DROGA (-I) I SPOSÓB PODANIA
- ZALECENIA DLA PRAWIDŁOWEGO PODANIA
- OKRES(-Y) KARENCJI
- SPECJALNE ŚRODKI OSTROŻNOŚCI PODCZAS PRZECHOWYWANIA
- SPECJALNE OSTRZEŻENIA
- SPECJALNE ŚRODKI OSTROŻNOŚCI DOTYCZĄCE USUWANIA NIEZUŻYTEGO PRODUKTU LECZNICZEGO WETERYNARYJNEGO LUB POCHODZĄCYCH Z NIEGO ODPADÓW, JEŚLI MA TO ZASTOSOWANIE
- DATA ZATWIERDZENIA LUB OSTATNIEJ ZMIANY TEKSTU ULOTKI
- INNE INFORMACJE
B. ULOTKA INFORMACYJNA
ULOTKA INFORMACYJNA
Aurizon, krople do uszu, zawiesina dla psów
NAZWA I ADRES PODMIOTU ODPOWIEDZIALNEGO ORAZ WYTWÓRCY ODPOWIEDZIALNEGO ZA ZWOLNIENIE SERII, JEŚLI JEST INNY
NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
ZAWARTOŚĆ SUBSTANCJI CZYNNEJ (-CH) I INNYCH SUBSTANCJI
WSKAZANIA LECZNICZE
PRZECIWWSKAZANIA
DZIAŁANIA NIEPOŻĄDANE
DOCELOWE GATUNKI ZWIERZĄT
DAWKOWANIE DLA KAŻDEGO GATUNKU, DROGA (-I) I SPOSÓB PODANIA
ZALECENIA DLA PRAWIDŁOWEGO PODANIA
OKRES(-Y) KARENCJI
SPECJALNE ŚRODKI OSTROŻNOŚCI PODCZAS PRZECHOWYWANIA
SPECJALNE OSTRZEŻENIA
SPECJALNE ŚRODKI OSTROŻNOŚCI DOTYCZĄCE USUWANIA NIEZUŻYTEGO PRODUKTU LECZNICZEGO WETERYNARYJNEGO LUB POCHODZĄCYCH Z NIEGO ODPADÓW, JEŚLI MA TO ZASTOSOWANIE
DATA ZATWIERDZENIA LUB OSTATNIEJ ZMIANY TEKSTU ULOTKI
INNE INFORMACJE
Podmiot odpowiedzialny:
Vetoquinol Biowet Sp. z o.o.
ul. Kosynierów Gdyńskich 13-14, 66-400 Gorzów Wlkp.
Wytwórca odpowiedzialny za zwolnienie serii: Vetoquinol Biowet Sp. z o.o.
ul. Kosynierów Gdyńskich 13-14, 66-400 Gorzów Wlkp. lub
Vetoquinol S.A. Magny-Vernois BP 189
70204 Lure Cedex Francja
Aurizon, krople do uszu, zawiesina dla psów
1 ml zawiesiny zawiera:
Substancja czynna:
Marbofloksacyna 3 mg
Klotrimazol 10 mg
Deksametazonu octan 1 mg Substancje pomocnicze:
Propylu galusan (E310) 1 mg
Leczenie zapalenia ucha zewnętrznego wywołanego zarówno przez bakterie wrażliwe na marbofloksacynę, jak też przez grzyby, zwłaszcza Malassezia pachydermatis.
Nie podawać psom z uszkodzoną błoną bębenkową.
Nie podawać psom, u których stwierdzono nadwrażliwość na którąkolwiek substancję czynną lub pomocniczą.
Działania niepożądane zwykle są związane ze stosowaniem glikokortykosteroidów. Mogą wystąpić zmiany parametrów biochemicznych i hematologicznych krwi, takich jak wzrost aktywności fosfatazy zasadowej i aminotransferazy, ograniczona neutrofilia.
O wystąpieniu działań niepożądanych po podaniu tego produktu lub zaobserwowaniu jakichkolwiek niepokojących objawów nie wymienionych w ulotce (w tym również objawów u człowieka na skutek kontaktu z lekiem), należy powiadomić właściwego lekarza weterynarii, podmiot odpowiedzialny lub Urząd Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych.
Formularz zgłoszeniowy należy pobrać ze strony internetowej http://www.urpl.gov.pl (Pion Produktów Leczniczych Weterynaryjnych).
Pies.
Jedna kropla produktu zawiera 71 µg marbofloksacyny, 237 µg klotrimazolu i 2,7 µg octanu deksametazonu.
Podawać 10 kropli głęboko do przewodu słuchowego zewnętrznego raz dziennie przez 7 do 14 dni. Po 7 dniach leczenia lekarz weterynarii powinien ocenić, czy leczenie należy przedłużyć o kolejny tydzień.
Po podaniu podstawę ucha należy delikatnie i dokładnie wymasować, aby dobrze rozprowadzić produkt i ułatwić jego penetrację w niższych partiach przewodu słuchowego.
Jeśli lek ma być stosowany u kilku psów, należy używać osobnych kaniul dla każdego psa.
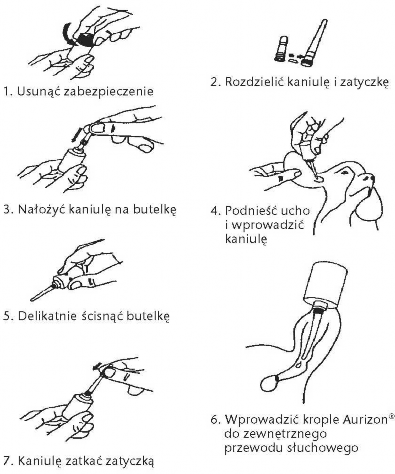
Przed użyciem należy energicznie wstrząsnąć opakowaniem.
Po podaniu podstawę ucha należy delikatnie i dokładnie wymasować, aby dobrze rozprowadzić produkt i ułatwić jego penetrację w niższych partiach przewodu słuchowego.
Jeśli lek ma być stosowany u kilku psów, należy używać osobnych kaniul dla każdego psa.
Nie dotyczy.
Przechowywać w miejscu niewidocznym i niedostępnym dla dzieci. Przechowywać w temperaturze poniżej 25°C
Nie używać tego produktu leczniczego weterynaryjnego po upływie terminu ważności podanego na etykiecie.
Okres ważności po pierwszym otwarciu opakowania: 2 miesiące.
Specjalne ostrzeżenia dla każdego z docelowych gatunków zwierząt:
Zewnętrzny przewód słuchowy powinien być bardzo dokładnie oczyszczony i wysuszony przed podaniem leku.
Specjalne środki ostrożności dotyczące stosowania u zwierząt:
Leczenie powinno być oparte na wynikach badania lekowrażliwości drobnoustrojów izolowanych od pacjenta.
Przed podaniem należy dokładnie zbadać ucho w celu upewnienia się, że błona bębenkowa nie jest uszkodzona.
Specjalne środki ostrożności dla osób podających produkt leczniczy weterynaryjny zwierzętom: Umyć dokładnie ręce po podaniu leku.
Unikać kontaktu z oczami. Po dostaniu się do oka, oko należy przemyć obfitą ilością wody. Osoby, które wykazują nadwrażliwość na składniki produktu powinny unikać bezpośredniego kontaktu z produktem.
Ciąża:
Nie stosować w okresie ciąży.
Laktacja:
Nie stosować w okresie laktacji.
Przedawkowanie (objawy, sposób postępowania przy udzielaniu natychmiastowej pomocy, odtrutki): Po trzykrotnym przekroczeniu zalecanej dawki obserwuje się zmiany parametrów biochemicznych i hematologicznych krwi (takich jak wzrost aktywności fosfatazy zasadowej i aminotransferazy, ograniczona neutrofilia, eozynofilia i limfopenia); zmiany te nie stanowią bezpośredniego zagrożenia dla życia i ustępują po odstawieniu leku.
Przedłużone (dłuższe niż zalecane) używanie zewnętrzne produktów glikokortykosteroidowych ma działanie miejscowe i ogólne, obejmujące supresję funkcji nadnerczy, ścieńczenie naskórka oraz
przedłużone gojenie się ran. W rzadkich przypadkach stosowanie produktu może wiązać się z przemijającą utratą słuchu, szczególnie u starszych psów.
Leków nie należy usuwać do kanalizacji ani wyrzucać do śmieci.
O sposoby usunięcia niepotrzebnych leków zapytaj lekarza weterynarii. Pomogą one chronić środowisko.
Dostępne opakowania:
Butelki z LDPE wraz z kroplomierzem z LDPE i z zakrętką z PP. Pudełko tekturowe zawiera:
butelkę o pojemności 10 ml wraz z 1 kaniulą z PVC
butelkę o pojemności 20 ml wraz z 2 kaniulami z PVC. Niektóre wielkości opakowań mogą nie być dostępne w obrocie.
W celu uzyskania informacji na temat niniejszego produktu leczniczego weterynaryjnego, należy kontaktować się z podmiotem odpowiedzialnym.











