Spis treści:
- NAZWA I ADRES PODMIOTU ODPOWIEDZIALNEGO ORAZ WYTWÓRCY ODPOWIEDZIALNEGO ZA ZWOLNIENIE SERII, JEŚLI JEST INNY
- NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
- ZAWARTOŚĆ SUBSTANCJI CZYNNEJ(-YCH) I INNYCH SUBSTANCJI
- WSKAZANIA LECZNICZE
- PRZECIWWSKAZANIA
- DZIAŁANIA NIEPOŻĄDANE
- DOCELOWE GATUNKI ZWIERZĄT
- DAWKOWANIE DLA KAŻDEGO GATUNKU, DROGA(-I) I SPOSÓB PODANIA
- ZALECENIA DLA PRAWIDŁOWEGO PODANIA
- OKRES(-Y) KARENCJI
- SPECJALNE ŚRODKI OSTROŻNOŚCI PODCZAS PRZECHOWYWANIA
- SPECJALNE OSTRZEŻENIA
- SPECJALNE ŚRODKI OSTROŻNOŚCI DOTYCZĄCE USUWANIA NIEZUŻYTEGO PRODUKTU LECZNICZEGO WETERYNARYJNEGO LUB POCHODZĄCYCH
- DATA ZATWIERDZENIA LUB OSTATNIEJ ZMIANY TEKSTU ULOTKI
- INNE INFORMACJE
B. ULOTKA INFORMACYJNA
ULOTKA INFORMACYJNA
Metrovis 100 mg tabletki dla psów i kotów
NAZWA I ADRES PODMIOTU ODPOWIEDZIALNEGO ORAZ WYTWÓRCY ODPOWIEDZIALNEGO ZA ZWOLNIENIE SERII, JEŚLI JEST INNY
NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
ZAWARTOŚĆ SUBSTANCJI CZYNNEJ(-YCH) I INNYCH SUBSTANCJI
WSKAZANIA LECZNICZE
PRZECIWWSKAZANIA
DZIAŁANIA NIEPOŻĄDANE
bardzo często (więcej niż 1 na 10 leczonych zwierząt wykazujących działanie(-a) niepożądane)
często (więcej niż 1, ale mniej niż 10 na 100 leczonych zwierząt)
niezbyt często (więcej niż 1, ale mniej niż 10 na 1000 leczonych zwierząt)
rzadko (więcej niż 1, ale mniej niż 10 na 10000 leczonych zwierząt)
bardzo rzadko (mniej niż 1 na 10000 leczonych zwierząt włączając pojedyncze raporty).
DOCELOWE GATUNKI ZWIERZĄT
DAWKOWANIE DLA KAŻDEGO GATUNKU, DROGA(-I) I SPOSÓB PODANIA
ZALECENIA DLA PRAWIDŁOWEGO PODANIA
OKRES(-Y) KARENCJI
SPECJALNE ŚRODKI OSTROŻNOŚCI PODCZAS PRZECHOWYWANIA
SPECJALNE OSTRZEŻENIA
SPECJALNE ŚRODKI OSTROŻNOŚCI DOTYCZĄCE USUWANIA NIEZUŻYTEGO PRODUKTU LECZNICZEGO WETERYNARYJNEGO LUB POCHODZĄCYCH
DATA ZATWIERDZENIA LUB OSTATNIEJ ZMIANY TEKSTU ULOTKI
INNE INFORMACJE
Podmiot odpowiedzialny:
LIVISTO Int'l S.L.
Av. Universitat Autònoma 29 08290 Cerdanyola del Vallès Barcelona, Hiszpania
Wytwórca odpowiedzialny za zwolnienie serii: aniMedica GmbH
Im Südfeld 9
48308 Senden-Bösensell Niemcy
LUB
aniMedica Herstellungs GmbH Im Südfeld 9
48308 Senden-Bösensell Niemcy
LUB
Industrial Veterinaria S.A.
Esmeralda 19, Esplugues de Llobregat 08950 Barcelona
Hiszpania
Metrovis 100 mg tabletki dla psów i kotów Metronidazol
1 tabletka zawiera:
Substancja czynna:
Metronidazol 100 mg
Beżowe, okrągłe tabletki z linią podziału w kształcie krzyża po jednej stronie. Tabletki mogą być dzielone na 2 lub 4 równe części.
Leczenie zakażeń układu pokarmowego wywołanych przez Giardia spp. i Clostridium spp. (tj.
C. perfringens lub C. difficile).
Leczenie zakażeń układu moczowo-płciowego, jamy ustnej, gardła oraz skóry wywołanych przez
bakterie bezwzględnie beztlenowe (np. Clostridium spp.) wrażliwe na metronidazol.
Nie stosować w przypadku zaburzeń czynności wątroby.
Nie stosować w przypadku nadwrażliwości na substancję czynną lub na dowolną substancję pomocniczą.
Po podaniu metronidazolu mogą wystąpić następujące działania niepożądane: wymioty, hepatotoksyczność, neutropenia oraz objawy neurologiczne.
Częstotliwość występowania działań niepożądanych przedstawia się zgodnie z poniższą regułą:
W razie zaobserwowania działań niepożądanych, również niewymienionych w ulotce informacyjnej, lub w przypadku podejrzenia braku działania produktu, poinformuj o tym lekarza weterynarii. Można również zgłosić działania niepożądane poprzez krajowy system raportowania www.urpl.gov.pl.
Psy i koty.
Do podania doustnego.
Zalecana dawka wynosi 50 mg metronidazolu na kg masy ciała dziennie przez 5–7 dni. Dzienna dawka może zostać podzielona na dwa podania w ciągu dnia (tj. 25 mg/kg masy ciała dwa razy dziennie).
W celu zapewnienia podania prawidłowej dawki należy możliwie jak najdokładniej określić masę ciała. Poniższa tabela ma służyć jako wskazówka odnośnie podawania produktu w zalecanej dawce, albo 50 mg na kg masy ciała, podawanej raz dziennie, albo, co jest preferowane, podawanej dwa razy dziennie po 25 mg na kg masy ciała.
Liczba tabletek | |||
Dwa razy dziennie | Raz dziennie | ||
Masa ciała (kg) | Rano | Wieczorem | |
0,5 kg | ¼ | - | ¼ |
1 kg | ¼ | ¼ | ½ |
2 kg | ½ | ½ | 1 |
3 kg | ¾ | ¾ | 1 ½ |
4 kg | 1 | 1 | 2 |
5 kg | 1 ¼ | 1 ¼ | 2 ½ |
6 kg | 1 ½ | 1 ½ | 3 |
7 kg | 1 ¾ | 1 ¾ | 3 ½ |
8 kg | 2 | 2 | 4 |



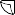 = ¼ tabletki = ½ tabletki = ¾ tabletki = 1 tabletka
= ¼ tabletki = ½ tabletki = ¾ tabletki = 1 tabletka
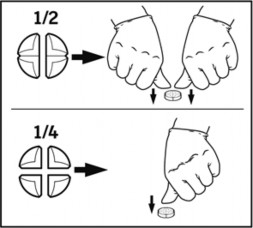
Tabletki można dzielić na 2 lub 4 równe części, w celu zapewnienia właściwego dawkowania. Tabletkę umieścić na płaskiej powierzchni, stroną z oznaczeniem skierowaną do góry, a stroną wypukłą (zaokrągloną) skierowaną do powierzchni.
Połówki: nacisnąć kciukami po obu stronach tabletki. Ćwiartki: nacisnąć kciukiem środek tabletki.
Nie dotyczy.
Przechowywać w miejscu niewidocznym i niedostępnym dla dzieci. Brak specjalnych środków ostrożności dotyczących przechowywania.
Nie używać tego produktu leczniczego weterynaryjnego po upływie terminu ważności podanego na pudełku.
Okres ważności podzielonych tabletek: 3 dni
Specjalne środki ostrożności dotyczące stosowania u zwierząt:
Ze względu na prawdopodobną zmienność (w czasie, geograficzną) występowania bakterii opornych na metronidazol zalecane jest pobieranie próbek bakteriologicznych i wykonywanie badań wrażliwości.
W miarę możliwości produkt należy stosować wyłącznie w oparciu o badanie wrażliwości.
Produkt leczniczy weterynaryjny powinien być stosowany zgodnie z urzędowymi, krajowymi i lokalnymi przepisami dotyczącymi stosowania antybiotyków.
W bardzo rzadkich przypadkach mogą wystąpić objawy neurologiczne, szczególnie po przedłużonym leczeniu metronidazolem.
Specjalne środki ostrożności dla osób podających produkt leczniczy weterynaryjny zwierzętom: Metronidazol wykazuje potwierdzone właściwości mutagenne i genotoksyczne u zwierząt laboratoryjnych i u ludzi. Metronidazol jest potwierdzonym czynnikiem kancerogennym u zwierząt laboratoryjnych i ma potencjalne działanie kancerogenne u ludzi. Brak jest jednak wystarczających dowodów na kancerogenność metronidazolu u ludzi.
Metronidazol może mieć szkodliwy wpływ na nienarodzone dziecko.
Podczas podawania produktu należy nosić nieprzepuszczalne rękawice, aby uniknąć kontaktu produktu ze skórą.
Aby uniknąć przypadkowego połknięcia, szczególnie przez dziecko, niezużyte tabletki i części tabletek należy włożyć z powrotem do otwartego blistra, następnie z powrotem do zewnętrznego opakowania i przechowywać w miejscu niewidocznym i niedostępnym dla dzieci. Po przypadkowym połknięciu, należy niezwłocznie zwrócić się o pomoc lekarską oraz przedstawić lekarzowi ulotkę informacyjną lub etykietę. Po kontakcie z tabletkami dokładnie umyć ręce.
Metronidazol może powodować reakcje nadwrażliwości. W przypadku znanej nadwrażliwości na metronidazol należy unikać kontaktu z produktem leczniczym weterynaryjnym.
Ciąża:
W badaniach na zwierzętach laboratoryjnych uzyskano niespójne wyniki, jeśli chodzi
o teratogenne/embriotoksyczne działanie metronidazolu. Z tego względu stosowanie tego produktu w czasie ciąży nie jest zalecane.
Laktacja:
Metronidazol jest wydalany z mlekiem, dlatego stosowanie w czasie laktacji nie jest zalecane.
Interakcje z innymi produktami leczniczymi i inne rodzaje interakcji:
Metronidazol może wpływać hamująco na degradację innych leków w wątrobie, takich jak fenytoina, cyklosporyna i warfaryna.
Cymetydyna może zmniejszać metabolizm wątrobowy metronidazolu, prowadząc do podwyższonego stężenia metronidazolu w surowicy.
Fenobarbital może zwiększać metabolizm wątrobowy metronidazolu, prowadząc do obniżonego stężenia metronidazolu w surowicy.
Przedawkowanie (objawy, sposób postępowania przy udzielaniu natychmiastowej pomocy, odtrutki): Występowanie działań niepożądanych jest bardziej prawdopodobne przy dawkach i długości leczenia przekraczających zalecany schemat dawkowania. W razie wystąpienia objawów neurologicznych należy przerwać leczenie i wdrożyć leczenie objawowe pacjenta.
Z NIEGO ODPADÓW, JEŚLI MA TO ZASTOSOWANIE
Niewykorzystany produkt leczniczy weterynaryjny lub jego odpady należy usunąć w sposób zgodny z obowiązującymi przepisami.
Pudełko tekturowe zawierające 1, 2, 5, 10, 25 lub 50 blistrów po 10 tabletek. Niektóre wielkości opakowań mogą nie być dostępne w obrocie.
W celu uzyskania informacji na temat niniejszego produktu leczniczego weterynaryjnego, należy kontaktować się z lokalnym przedstawicielem podmiotu odpowiedzialnego:
LIVISTO Sp. z o.o.
ul. Chwaszczyńska 198a PL – 81-571 Gdynia











