Spis treści:
- NAZWA I ADRES PODMIOTU ODPOWIEDZIALNEGO ORAZ WYTWÓRCY ODPOWIEDZIALNEGO ZA ZWOLNIENIE SERII, JEŚLI JEST INNY
- NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
- ZAWARTOŚĆ SUBSTANCJI CZYNNEJ (-CH) I INNYCH SUBSTANCJI
- WSKAZANIA LECZNICZE
- PRZECIWWSKAZANIA
- DZIAŁANIA NIEPOŻĄDANE
- DOCELOWE GATUNKI ZWIERZĄT
- DAWKOWANIE DLA KAŻDEGO GATUNKU, DROGA(-I) I SPOSÓB PODANIA
- ZALECENIA DLA PRAWIDŁOWEGO PODANIA
- OKRES(-Y) KARENCJI
- SPECJALNE ŚRODKI OSTROŻNOŚCI PODCZAS PRZECHOWYWANIA
- SPECJALNE OSTRZEŻENIA
- SPECJALNE ŚRODKI OSTROŻNOŚCI DOTYCZĄCE USUWANIA NIEZUŻYTEGO PRODUKTU LECZNICZEGO WETERYNARYJNEGO LUB POCHODZĄCYCH Z NIEGO ODPADÓW, JEŚLI MA TO ZASTOSOWANIE
- DATA ZATWIERDZENIA LUB OSTATNIEJ ZMIANY TEKSTU ULOTKI
- INNE INFORMACJE
B. ULOTKA INFORMACYJNA
ULOTKA INFORMACYJNA:
Vomend vet 5 mg tabletki do rozgryzania i żucia dla psów
NAZWA I ADRES PODMIOTU ODPOWIEDZIALNEGO ORAZ WYTWÓRCY ODPOWIEDZIALNEGO ZA ZWOLNIENIE SERII, JEŚLI JEST INNY
NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
ZAWARTOŚĆ SUBSTANCJI CZYNNEJ (-CH) I INNYCH SUBSTANCJI
WSKAZANIA LECZNICZE
PRZECIWWSKAZANIA
DZIAŁANIA NIEPOŻĄDANE
bardzo często (więcej niż 1 na 10 leczonych zwierząt wykazujących działanie(a) niepożądane)
często (więcej niż 1, ale mniej niż 10 na 100 leczonych zwierząt)
niezbyt często (więcej niż 1, ale mniej niż 10 na 1000 leczonych zwierząt)
rzadko (więcej niż 1, ale mniej niż 10 na 10 000 leczonych zwierząt)
bardzo rzadko (mniej niż 1 na 10 000 leczonych zwierząt włączając pojedyncze raporty).
DOCELOWE GATUNKI ZWIERZĄT
DAWKOWANIE DLA KAŻDEGO GATUNKU, DROGA(-I) I SPOSÓB PODANIA
ZALECENIA DLA PRAWIDŁOWEGO PODANIA
OKRES(-Y) KARENCJI
SPECJALNE ŚRODKI OSTROŻNOŚCI PODCZAS PRZECHOWYWANIA
SPECJALNE OSTRZEŻENIA
SPECJALNE ŚRODKI OSTROŻNOŚCI DOTYCZĄCE USUWANIA NIEZUŻYTEGO PRODUKTU LECZNICZEGO WETERYNARYJNEGO LUB POCHODZĄCYCH Z NIEGO ODPADÓW, JEŚLI MA TO ZASTOSOWANIE
DATA ZATWIERDZENIA LUB OSTATNIEJ ZMIANY TEKSTU ULOTKI
INNE INFORMACJE
Podmiot odpowiedzialny:
Dechra Regulatory B.V. Handelsweg 25
5531 AE Bladel
Holandia
Wytwórca odpowiedzialny za zwolnienie serii: Lelypharma B.V.
Zuiveringsweg 42
8243 PZ Lelystad
Holandia
Vomend vet 5 mg tabletki do rozgryzania i żucia dla psów metoklopramidu chlorowodorek
Każda tabletka zawiera:
Substancja czynna:
Metoklopramid (jako chlorowodorek jednowodny) 4,46 mg
(co odpowiada 5,0 mg metoklopramidu chlorowodorku)
Tabletka do rozgryzania i żucia
Jasnobrązowa z brązowym plamkami, aromatyzowana, okrągła i wypukła tabletka o średnicy 6 mm z
linią podziału w kształcie krzyża po jednej stronie. Tabletki można podzielić na 2 lub 4 równe części.
Złagodzenie objawów, takich jak częste wymioty, rozszerzenie żołądka, przewlekłe zapalenie żołądka, refluks dwunastniczo-żołądkowy i biegunka związane z obniżoną perystaltyką przewodu pokarmowego.
Nie stosować w przypadkach krwawienia z przewodu pokarmowego, perforacji lub niedrożności przewodu pokarmowego.
Nie stosować u zwierząt ze stwierdzoną nadwrażliwością na substancję czynną lub na dowolną substancję pomocniczą.
Senności i biegunki występowały bardzo rzadko.
U psów występowanie działań neurologicznych (pobudzenie, ataksja, nienaturalne pozycje i (lub) ruchy, prostracja, drżenia i agresja, wokalizacja) zgłaszano bardzo rzadko. Obserwowane działania są przemijające i ustępują po przerwaniu leczenia.
Częstotliwość występowania działań niepożądanych przedstawia się zgodnie z poniższą regułą:
W razie zaobserwowania działań niepożądanych, również niewymienionych w ulotce informacyjnej, lub w przypadku podejrzenia braku działania produktu, poinformuj o tym lekarza weterynarii.
Można również zgłosić działania niepożądane poprzez krajowy system raportowania (www.urpl.gov.pl).
Psy 
Podanie doustne.
Zalecana dawka to 0,22 mg metoklopramidu (co odpowiada 0,25 mg metoklopramidu chlorowodorku) na kg masy ciała, 4 razy na dzień.
Poniższa tabela jest przeznaczona jako wskazówka przy podawaniu produktu:
Masa ciała kg | Dawka mg/zwierzę* | Vomend vet 5 g | Vomend vet 10 g | |
5-7,5 | 1,25 |
| ||
>7,5-12,5 | 2,5 |
| LUB |
|
>12,5-17,5 | 3,75 |
| ||
>17,5-22,5 | 5 |
| LUB |
|
>22,5-27,5 | 6,25 |
| ||
>27,5-32,5 | 7,5 | LUB |
| |
>32,5-37,5 | 8,75 | |||
>37,5-45 | 10 |
| LUB |
|
>45-55 | 12,5 |
| LUB |
|
>55-65 | 15 |
| LUB | |
>65-75 | 17,5 |
| LUB | |
>75-85 | 20 |
| LUB |
|









= ¼ tabletki  = ½ tabletki
= ½ tabletki  = ¾ tabletki
= ¾ tabletki  = 1 tabletka
= 1 tabletka
* dawka w mg metoklopramidu chlorowodorku na zwierzę na podanie.
Tabletki można dzielić na 2 lub 4 równe części w celu zapewnienia właściwego dawkowania. Tabletkę umieścić na płaskiej powierzchni ze stroną z linią podziału skierowaną do góry i stroną wypukłą (zaokrągloną) skierowaną do powierzchni.
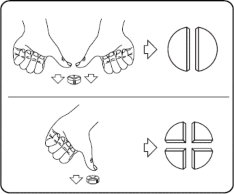
2 równe części: nacisnąć kciukami po obu stronach tabletki.
4 równe części: nacisnąć kciukiem w połowie tabletki.
Przechowywać w miejscu niewidocznym i niedostępnym dla dzieci. Brak specjalnych środków ostrożności dotyczących przechowywania.
Nie używać tego produktu leczniczego weterynaryjnego po upływie terminu ważności podanego na pudełku po upływie {Termin ważności}. Termin ważności oznacza ostatni dzień danego miesiąca. Okres ważności podzielonych tabletek po pierwszym otwarciu opakowania bezpośredniego: 3 dni. Niezużyte części tabletek należy włożyć z powrotem do otwartego blistra i pudełka.
Specjalne ostrzeżenia dla każdego z docelowych gatunków zwierząt:
Nie stosować u psów o masie ciała poniżej 5 kg.
Specjalne środki ostrożności dotyczące stosowania u zwierząt
Unikać podawania zwierzętom z zaburzeniami drgawkowymi, np. padaczką, lub urazem głowy. Ponieważ metoklopramid może zwiększać poziom prolaktyny, należy zachować ostrożność podczas stosowania u psów z ciążą urojoną.
Specjalne środki ostrożności dla osób podających produkt leczniczy weterynaryjny zwierzętom: Produkt może powodować działania neurologiczne po przypadkowym spożyciu, zwłaszcza przez dzieci.
Dzieci nie powinny mieć styczności z produktem leczniczym weterynaryjnym. Niezużyte części tabletki należy umieścić z powrotem w blistrze i pudełku oraz przechowywać ostrożnie poza zasięgiem dzieci i zawsze zużywać podczas następnego podania.
Po przypadkowym połknięciu należy niezwłocznie zwrócić się o pomoc lekarską oraz przedstawić lekarzowi ulotkę informacyjną lub opakowanie.
Ciąża i laktacja:
Bezpieczeństwo produktu leczniczego weterynaryjnego stosowanego w czasie ciąży i laktacji nie zostało określone. Do stosowania jedynie po dokonaniu przez lekarza weterynarii oceny bilansu korzyści/ryzyka wynikającego ze stosowania produktu.
Interakcje z innymi produktami leczniczymi i inne rodzaje interakcji:
W przypadkach zapalenia żołądka należy unikać jednoczesnego podawania leków antycholinergicznych (atropiny), ponieważ mogą znosić działanie metoklopramidu na perystaltykę przewodu pokarmowego.
W przypadkach jednoczesnej biegunki nie ma przeciwwskazań do stosowania leków antycholinergicznych.
Jednoczesne stosowanie metoklopramidu z neuroleptykami pochodnymi fenotiazyny (acepromazyna)
i butyferonu zwiększa ryzyko działania neurologicznego (patrz punkt Działania niepożądane). Metoklopramid może nasilać działanie produktów wpływających depresyjnie na ośrodkowy układ nerwowy. W przypadku jednoczesnego stosowania zaleca się użycie najmniejszej dawki metoklopramidu, aby uniknąć nadmiernej sedacji.
Przedawkowanie (objawy, sposób postępowania przy udzielaniu natychmiastowej pomocy, odtrutki):
W przypadku przedawkowania nie są znane inne działania niepożądane niż te opisane w punkcie Działania niepożądane.
Leków nie należy usuwać do kanalizacji ani wyrzucać do śmieci. O sposoby usunięcia niepotrzebnych leków zapytaj lekarza weterynarii. Pomogą one chronić środowisko.
Blistry OPA/ALU/PVC//ALU zawierające 10 tabletek.
Pudełko tekturowe zawierające 1 lub 10 blistrów.
Niektóre wielkości opakowań mogą nie być dostępne w obrocie.





























