Spis treści:
- NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
- SKŁAD JAKOŚCIOWY I ILOŚCIOWY
- POSTAĆ FARMACEUTYCZNA
- SZCZEGÓŁOWE DANE KLINICZNE
- WŁAŚCIWOŚCI FARMAKOLOGICZNE
- DANE FARMACEUTYCZNE
- NAZWA I ADRES PODMIOTU ODPOWIEDZIALNEGO
- NUMER(-Y) POZWOLENIA NA DOPUSZCZENIE DO OBROTU
- DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU
- DATA OSTATNIEJ AKTUALIZACJI TEKSTU CHARAKTERYSTYKI PRODUKTU LECZNICZEGO WETERYNARYJNEGO
[Version 8.1, 01/2017]
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
SKŁAD JAKOŚCIOWY I ILOŚCIOWY
POSTAĆ FARMACEUTYCZNA
SZCZEGÓŁOWE DANE KLINICZNE
Docelowe gatunki zwierząt
Wskazania lecznicze dla poszczególnych docelowych gatunków zwierząt
Przeciwwskazania
Specjalne ostrzeżenia dla każdego z docelowych gatunków zwierząt
Specjalne środki ostrożności dotyczące stosowania
Działania niepożądane (częstotliwość i stopień nasilenia)
Interakcje z innymi produktami leczniczymi i inne rodzaje interakcji
Dawkowanie i droga(i) podawania
Przedawkowanie (objawy, sposób postępowania przy udzielaniu natychmiastowej pomocy, odtrutki), jeśli konieczne
Okres(-y) karencji
WŁAŚCIWOŚCI FARMAKOLOGICZNE
Właściwości farmakodynamiczne
Właściwości farmakokinetyczne
DANE FARMACEUTYCZNE
Wykaz substancji pomocniczych
Główne niezgodności farmaceutyczne
Okres ważności
Specjalne środki ostrożności podczas przechowywania
Rodzaj i skład opakowania bezpośredniego
Specjalne środki ostrożności dotyczące usuwania niezużytego produktu leczniczego weterynaryjnego lub pochodzących z niego odpadów
NAZWA I ADRES PODMIOTU ODPOWIEDZIALNEGO
NUMER(-Y) POZWOLENIA NA DOPUSZCZENIE DO OBROTU
DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU
DATA OSTATNIEJ AKTUALIZACJI TEKSTU CHARAKTERYSTYKI PRODUKTU LECZNICZEGO WETERYNARYJNEGO
Exspot, 715 mg/ml, roztwór do nakrapiania dla psów
1 dawka (1 ml) produktu zawiera:
Substancja czynna:
permetryna (cis:trans = 40:60) 715 mg
Wykaz wszystkich substancji pomocniczych, patrz punkt 6.1.
Roztwór do nakrapiania Przejrzysty, ciemnożółty roztwór.
Pies
Produkt przeznaczony jest do stosowania u psów w zapobieganiu i zwalczaniu infestacji pcheł (Ctenocephalides felis) i kleszczy (Ixodes ricinus, Rhipicephalus sanguineus). Zabezpiecza przed reinfestacją w okresie do 4 tygodni po podaniu.
Nie stosować w przypadkach nadwrażliwości na substancję czynną lub na dowolną substancję pomocniczą.
Nie stosować u szczeniąt w wieku poniżej 2 tygodni. Nie stosować częściej niż co 7 dni.
Nie stosować u kotów.
Nie stosować na uszkodzoną skórę psa.
W celu uniknięcia przenoszenia inwazji wszystkie psy przebywające w gospodarstwie domowym powinny zostać poddane leczeniu.
W niekorzystnych warunkach przytwierdzanie się pojedynczych pasożytów po zastosowaniu produktu nie może zostać wykluczone. W konsekwencji nie można całkowicie wykluczyć przeniesienia choroby zakaźnej przenoszonej przez wektory.
Specjalne środki ostrożności dotyczące stosowania u zwierząt
Należy zapobiegać wzajemnemu lizaniu sierści przez leczone zwierzęta po podaniu produktu. Zwierzęta poddane leczeniu należy trzymać osobno do czasu wyschnięcia miejsca podania produktu. Należy unikać kąpania psów/zanurzenia w wodzie w ciągu 2 dni od zastosowania produktu.
Produkt leczniczy weterynaryjny przeznaczony jest wyłącznie do podawania zewnętrznego.
Pchły oraz ich postacie rozwojowe występują w otoczeniu zwierząt (legowiska, budy, dywany, tapicerka mebli). Miejsca te powinny być poddawane regularnemu czyszczeniu (np. za pomocą odkurzacza) i działaniu odpowiednich preparatów owadobójczych.
Permetryna jest skrajnie toksyczna dla kotów. Aby zapobiec przypadkowemu narażeniu kotów na ekspozycję na produkt, należy trzymać koty z dala od psów, które zostały poddane leczeniu do momentu wyschnięcia miejsca podania produktu. Należy zapewnić, że koty nie będą poddawać toalecie miejsca podania na skórze psów poddanych leczeniu. Jeśli dojdzie do czyszczenia przez koty miejsca podania produktu na skórze psa, należy natychmiast skorzystać z pomocy lekarza weterynarii. Ponieważ permetryna jest toksyczna dla organizmów wodnych, leczonym psom nie należy pozwalać na kontakt z jakimkolwiek rodzajem wód powierzchniowych przez okres co najmniej 24 godzin od podania produktu.
Specjalne środki ostrożności dla osób podających produkt leczniczy weterynaryjny zwierzętom Osoby o stwierdzonej nadwrażliwości na którykolwiek składnik produktu powinny unikać kontaktu z produktem.
Unikać bezpośredniego kontaktu produktu ze skórą i spojówkami. W razie konieczności natychmiast spłukać pozostałości produktu bieżącą wodą.
Po podaniu produktu umyć ręce.
W przypadku częstego podawania produktu przez jedną osobę zwierzętom wskazane jest używanie rękawiczek ochronnych.
Nie dotykać miejsca podania produktu przez 3-6 godzin. Zaleca się podawać produkt wieczorem.
Leczone psy nie powinny spać z ludźmi (szczególnie dziećmi).
Zwierzęta leczone należy trzymać przez 1 godzinę z dala od źródeł ognia.
Bardzo rzadko w miejscu podania obserwowano występowanie skórnych reakcji nadwrażliwości takich jak zaczerwienienie, swędzenie, zapalenie skóry, egzema i utrata włosów.
Bardzo rzadko donoszono o występowaniu zmian w zachowaniu (pobudzenie, letarg), objawów żołądkowo-jelitowych (nadmierne ślinienie się, biegunka, wymioty, utrata apetytu) oraz objawów neurologicznych (ataksja, drżenia mięśniowe, drgawki lub niedowład).
W przypadku wystąpienia powyższych objawów zalecane jest dokładne umycie zwierzęcia (wykąpanie) oraz zwrócenie się o pomoc medyczną do lekarza weterynarii, jeśli objawy się utrzymują.
4.7. Stosowanie w ciąży, laktacji lub w okresie nieśności
Ciąża i laktacja:
W związku z brakiem danych dotyczących psów nie zaleca się stosowania w czasie ciąży i laktacji.
Nieznane
Dawkowanie:
Psom o masie ciała do 15 kg podać jedną dawkę produktu (715 mg permetryny) na skórę między łopatkami.
Psom o masie powyżej 15 kg podać dwie dawki produktu (1,43 g permetryny) - jedną dawkę na skórę między łopatkami, drugą dawkę na skórę u nasady ogona.
Podawać bezpośrednio na powierzchnię skóry. Nie wcierać produktu w skórę. Sposób podania:
Wyłącznie do miejscowego podania zewnętrznego (spot-on). Otworzyć jedną saszetkę i wyjąć pipetę.
Krok 1:
W celu ułatwienia podania pies powinien stać. Należy trzymać pipetę pionowo jedną ręką, z daleka od twarzy, drugą ręką otworzyć pipetę zaginając ją i odłamując jej końcówkę.
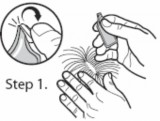
Krok 2: Należy rozgarnąć włosy, tak aby ukazała się skóra, przytknąć końcówkę pipety do skóry pomiędzy łopatkami.
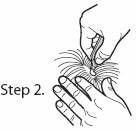
Krok 3 (małe psy): Zdecydowanie ścisnąć pipetę podając jej całą zawartość bezpośrednio na skórę.
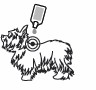
Krok 3 (większe psy): Cała zawartość pipety powinna zostać podana w równej objętości w dwu miejscach zlokalizowanych w różnych miejscach podania wzdłuż linii grzbietowej od łopatek do podstawy ogona.
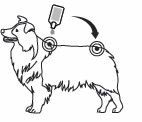
Nie były obserwowane żadne objawy uboczne u psów po zastosowaniu dawki czterokrotnie większej niż zalecana. W przypadku wystąpienia objawów przedawkowania w postaci podrażnienia skóry, psa należy wykąpać przy użyciu szamponu.
Nie dotyczy
Grupa farmakoterapeutyczna: Środki przeciwko ektopasożytom, środki owadobójcze i repelenty. Kod ATCvet: QP53AC04
Permetryna jest syntetycznym pyretroidem. Zaburza przewodnictwo nerwowe poprzez blokowanie kanałów sodowych, co prowadzi do depolaryzacji błony komórek nerwowych i zahamowania przewodnictwa impulsów pasożyta.
Permetryna jest łatwo i szybko metabolizowana, a następnie wydalana przez organizm ssaków. W ciągu 48 godzin od doustnego podania psom 85% permetryny zostaje wydalone wraz z kałem i moczem. U stawonogów procesy te zachodzą dużo wolniej.
Propylen-GlycolMethyl-Ether (Dowanol PM)
Nieznane
Okres ważności produktu leczniczego weterynaryjnego zapakowanego do sprzedaży: 4 lata. Okres ważności po pierwszym otwarciu opakowania bezpośredniego: zużyć natychmiast.
Przechowywać w temperaturze poniżej 25°C. Nie zamrażać. Chronić przed światłem.
Aplikator spot-on (pipeta) w formie blistra z folii PP/COC/PP i Aluminium/PP umieszczony w zewnętrznej saszetce PET/LDPE/Aluminium/LLDPE zawierający 1 ml produktu.
Pudełko tekturowe zawierające 6 pojedynczo pakowanych w saszetki aplikatorów spot-on.
Niewykorzystany produkt leczniczy weterynaryjny lub jego odpady należy usunąć w sposób zgodny z obowiązującymi przepisami.
Produkt Exspot nie powinien się przedostawać do cieków wodnych, ponieważ może być niebezpieczny dla ryb i innych organizmów wodnych.
Produkty zawierające permetrynę są toksyczne dla pszczół.
Intervet International B.V. Wim de Körverstraat 35 5831 AN Boxmeer Holandia
210/96
/ DATA PRZEDŁUŻENIA POZWOLENIA
Data wydania pierwszego pozwolenia na dopuszczenie do obrotu: 04/01/1996. Data przedłużenia pozwolenia: 07/12/2000, 15/03/2006, 01/10/2007.
ZAKAZ WYTWARZANIA, IMPORTU, POSIADANIA, SPRZEDAŻY, DOSTAWY I/LUB STOSOWANIA
Nie dotyczy










