Spis treści:
- NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
- SKŁAD JAKOŚCIOWY I ILOŚCIOWY
- POSTAĆ FARMACEUTYCZNA
- SZCZEGÓŁOWE DANE KLINICZNE
- WŁAŚCIWOŚCI FARMAKOLOGICZNE
- DANE FARMACEUTYCZNE
- PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU
- NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
- DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU/DATA PRZEDŁUŻENIA POZWOLENIA
- DATA ZATWIERDZENIA LUB CZĘŚCIOWEJ ZMIANY TEKSTU CHARAKTERYSTYKI PRODUKTU LECZNICZEGO
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
SKŁAD JAKOŚCIOWY I ILOŚCIOWY
POSTAĆ FARMACEUTYCZNA
SZCZEGÓŁOWE DANE KLINICZNE
Docelowe gatunki zwierząt
Wskazania lecznicze dla poszczególnych docelowych gatunków zwierząt
Przeciwwskazania
Specjalne ostrzeżenia dla każdego z docelowych gatunków zwierząt
Specjalne środki ostrożności dotyczące stosowania
Specjalne środki ostrożności dotyczące stosowania u zwierząt Zwierzęta należy dokładnie zważyć przed leczeniem.
Nie określono bezpieczeństwa produktu u psów poniżej 12. tygodnia życia czy też u psów o masie ciała poniżej 1,5 kg.
Należy zachować ostrożność, aby uniknąć przedostania się zawartości pipetki do oka lub do jamy ustnej leczonych psów. W szczególności należy zapobiegać lizaniu miejsca zastosowania produktu przez leczone zwierzę lub przez inne zwierzęta.
Produkt ten jest bardzo trujący dla kotów i może spowodować ich śmierć. Wynika to z fizjologii kotów, których organizm nie jest w stanie metabolizować niektórych związków, w tym permetryny. W razie przypadkowego kontaktu produktu ze skórą kota należy umyć zwierzę szamponem lub mydłem i niezwłocznie zasięgnąć porady lekarza weterynarii. Aby zapobiec przypadkowej ekspozycji kotów na działanie produktu, należy trzymać leczone psy w odosobnieniu od kotów do czasu, aż miejsce zastosowania produktu wyschnie. Ważnym jest by upewnić się, że koty nie będą lizały miejsca zastosowania produktu u psa. W przypadku ekspozycji tego rodzaju należy natychmiast zasięgnąć porady lekarza weterynarii.
Nie stosować produktu u królików i kotów.

Specjalne środki ostrożności dla osób podających produkt leczniczy weterynaryjny zwierzętom
Produkt może działać neurotoksycznie. Produkt może być szkodliwy w przypadku połknięcia. Należy unikać połknięcia produktu na skutek kontaktu rąk z jamą ustną. Po przypadkowym połknięciu należy niezwłocznie zwrócić się o pomoc lekarską oraz przedstawić lekarzowi ulotkę informacyjną lub opakowanie.
Produkt ten może powodować podrażnienie oczu i błon śluzowych. Dlatego należy unikać kontaktu produktu z jamą ustną i oczami, tj. kontaktu rąk z jamą ustną i rąk z oczami. W razie przypadkowego kontaktu produktu z oczami należy natychmiast dokładnie przemyć oczy wodą. Jeśli podrażnienie oka utrzymuje się, należy zwrócić się o pomoc lekarską oraz przedstawić lekarzowi ulotkę informacyjną lub opakowanie.
Unikać kontaktu produktu ze skórą. W przypadku gdy wystąpi kontakt ze skórą należy natychmiast przemyć zanieczyszczone miejsce wodą z mydłem.
Po użyciu produktu należy dokładnie umyć ręce.
Nie należy jeść, pić ani palić podczas stosowania produktu leczniczego weterynaryjnego.
Osoby o znanej nadwrażliwości (alergii) na fipronil, permetrynę lub którąkolwiek z substancji pomocniczych powinny unikać kontaktu z produktem leczniczym weterynaryjnym, ponieważ w bardzo rzadkich przypadkach może on powodować u niektórych osób podrażnienie dróg oddechowych i reakcje skórne.
W przypadku wystąpienia objawów należy niezwłocznie zwrócić się o pomoc lekarską oraz przedstawić lekarzowi ulotkę informacyjną lub opakowanie.
Leczone zwierzęta nie powinny być dotykane do czasu wyschnięcia miejsca aplikacji produktu i przez około 12 godzin po jego zastosowaniu; w tym czasie dzieci także nie powinny bawić się ze zwierzętami. Dlatego zaleca się, aby produkt stosować o wczesnej porze wieczornej lub w późnych godzinach popołudniowych, aby zminimalizować kontakt z leczonym zwierzęciem. W dniu zastosowania produktu leczone zwierzęta nie powinny spać z właścicielami, a szczególnie z dziećmi.
Pipetki należy przechowywać w oryginalnym opakowaniu. Aby uniemożliwić dzieciom uzyskanie dostępu do zużytych pipetek, należy je niezwłocznie usunąć w odpowiedni sposób.
Inne środki ostrożności
Działania niepożądane (częstotliwość i stopień nasilenia)
bardzo często (więcej niż 1 na 10 leczonych zwierząt wykazujących działanie(a) niepożądane)
często (więcej niż 1, ale mniej niż 10 na 100 leczonych zwierząt)
niezbyt często (więcej niż 1, ale mniej niż 10 na 1000 leczonych zwierząt)
rzadko (więcej niż 1, ale mniej niż 10 na 10000 leczonych zwierząt)
bardzo rzadko (mniej niż 1 na 10000 leczonych zwierząt, włączając pojedyncze raporty).
Stosowanie w ciąży, laktacji lub w okresie nieśności
Interakcje z innymi produktami leczniczymi i inne rodzaje interakcji
Dawkowanie i droga podawania
Przedawkowanie (objawy, sposób postępowania przy udzielaniu natychmiastowej pomocy, odtrutki), jeśli konieczne
Okres(-y) karencji
WŁAŚCIWOŚCI FARMAKOLOGICZNE
Właściwości farmakodynamiczne
Właściwości farmakokinetyczne
DANE FARMACEUTYCZNE
Wykaz substancji pomocniczych
Główne niezgodności farmaceutyczne
Okres ważności
Specjalne środki ostrożności podczas przechowywania
Rodzaj i skład opakowania bezpośredniego
Specjalne środki ostrożności dotyczące usuwania niezużytego produktu leczniczego weterynaryjnego lub pochodzących z niego odpadów
PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU
NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU/DATA PRZEDŁUŻENIA POZWOLENIA
DATA ZATWIERDZENIA LUB CZĘŚCIOWEJ ZMIANY TEKSTU CHARAKTERYSTYKI PRODUKTU LECZNICZEGO
Effitix 402 mg/3600 mg roztwór do nakrapiania dla bardzo dużych psów Efficanix 402 mg/3600 mg spot-on solution for very big dogs (SE)
Każda pipetka 6,6 ml zawiera:
Substancje czynne:
Fipronil 402,6 mg
Permetryna 3597,0 mg
Substancje pomocnicze:
Butylohydroksyanizol (E320) 1,32 mg Butylohydroksytoluen (E321) 0,66 mg
Wykaz wszystkich substancji pomocniczych, patrz punkt 6.1.
Roztwór do nakrapiania Klarowny, żółty roztwór
Psy
Zwalczanie inwazji pcheł i/lub kleszczy u psów, a także odstraszanie (zapobieganie żerowaniu) muchówek i/lub komarów.
Pchły:
Leczenie i zapobieganie inwazji pcheł (Ctenocephalides felis). Pchły przebywające na psie są zabijane w ciągu 24 godzin po zastosowaniu produktu. Jedno zastosowanie zapewnia trwałą ochronę przed nową inwazją dorosłymi postaciami pcheł przez cztery tygodnie. Produkt można stosować w ramach strategii zwalczania alergicznego pchlego zapalenia skóry (APZS), wcześniej zdiagnozowanego przez lekarza weterynarii.
Kleszcze:
Leczenie inwazji kleszczy Ixodes ricinus.
Jedno zastosowanie zapewnia stałą ochronę przed inwazją kleszczy (Ixodes ricinus, Dermacentor reticulatus i Rhipicephalus sanguineus) przez okres czterech tygodni. W przypadku obecności kleszczy Dermacentor reticulatus lub Rhipicephalus sanguineus podczas stosowania produktu może nie dojść do ich zabicia w ciągu pierwszych 48 godzin.
Muchówki i komary:
Jedno zastosowanie zapewnia odstraszanie (zapobieganie żerowaniu) muchówek (Phlebotomus perniciosus) oraz komarów (Culex pipiens, Aedes aegypti) przez cztery tygodnie.
Nie stosować w przypadkach nadwrażliwości na substancje czynne lub na dowolną substancję pomocniczą. Nie stosować u królików i kotów, ponieważ mogą wystąpić działania niepożądane, a nawet śmierć (patrz też punkt 4.5i).
Nie stosować u zwierząt chorych (np. choroby układowe, gorączka) lub ozdrowieńców.
Produkt leczniczy weterynaryjny zachowuje skuteczność po ekspozycji na światło słoneczne lub gdy zwierzę zmoknie podczas deszczu.
Należy unikać częstych kąpieli lub mycia szamponem psów, u których zastosowano produkt, ponieważ może to niekorzystnie wpływać na jego skuteczność.
U psa z inwazją pcheł może wystąpić reakcja alergiczna na ślinę pcheł, określana jako alergiczne pchle zapalenie skóry (APZS). Jeżeli u psa wystąpią: zapalenie skóry, świąd, ślady po ukąszeniu, nadmierne drapanie się, czy też kiedy pies jest niespokojny, należy zasięgnąć porady lekarza weterynarii aby sprawdzić, czy u psa nie występuje APZS.
Aby zapobiegać ponownej inwazji kolejnymi pchłami zaleca się zastosowanie leczenia u wszystkich psów przebywających w gospodarstwie domowym. Należy też zastosować odpowiednie produkty u innych zwierząt przebywających z tym samym gospodarstwie domowym. Pchły często zanieczyszczają kosze, legowiska zwierząt oraz inne miejsca odpoczynku zwierząt, jak dywany, meble tapicerowane, które w przypadku intensywnej inwazji na początku procesu zwalczania należy potraktować odpowiednimi środkami owadobójczymi oraz należy je regularnie odkurzać.
Mogą pojawić się pojedyncze kleszcze lub wystąpić pojedyncze ukąszenia muchówek bądź komarów. Dlatego w niekorzystnych warunkach nie można wykluczyć przeniesienia chorób zakaźnych przez te pasożyty.
Badania wykazały, że produkt zapobiega żerowaniu muchówek i komarów przez cztery tygodnie. Dlatego w przypadku krótkotrwałych podróży (trwających mniej niż 4 tygodnie) do obszarów endemicznych zaleca się zastosowanie leczenia bezpośrednio przed spodziewaną ekspozycją. W przypadku dłuższej ekspozycji (tj. u zwierząt żyjących na obszarach endemicznych lub w przypadku podróży trwających dłużej niż 4 tygodnie) schemat leczenia powinien być prowadzony na podstawie lokalnych danych epidemiologicznych.
Fipronil i permetryna mogą wykazywać niekorzystny wpływ na organizmy wodne. Psy nie powinny pływać w zbiornikach wodnych przez 2 dni po zastosowaniu produktu.
Produkt może mieć niekorzystny wpływ na malowane, lakierowane lub inne powierzchnie bądź sprzęty w gospodarstwie domowym. Należy odczekać do czasu wyschnięcia miejsca zastosowania produktu, zanim zezwoli się na kontakt z takimi materiałami.
Po zastosowaniu produktu obserwowano przemijające reakcje skórne w miejscu zastosowania (świąd, rumień, wyłysienia), a także bardzo rzadko uogólniony świąd. Bardzo rzadko obserwowano zmiany zachowania (nadpobudliwość/niepokój), zaburzenia neurologiczne (osowiałość, drżenia mięśni, drgawki, niezborność) oraz wymioty.
W przypadku lizania sierści może wystąpić przemijające nadmierne ślinienie.
Częstość występowania działań niepożądanych przedstawia się zgodnie z poniższą regułą:
Badania laboratoryjne u psów z użyciem fipronilu i permetryny nie wykazały działania teratogennego ani embriotoksycznego. Bezpieczeństwo produktu leczniczego weterynaryjnego stosowanego w czasie ciąży i
laktacji u suk nie zostało określone. Produkt można stosować w czasie ciąży i laktacji jedynie po dokonaniu przez lekarza weterynarii oceny bilansu korzyści/ryzyka.
Nieznane
Tylko do użytku zewnętrznego. Przez nakrapianie
Dawkowanie:
Masa ciała psa | Fipronil (mg) | Permetryna (mg) |
1,5–4 kg | 26,8 | 240 |
4–10 kg | 67 | 600 |
10–20 kg | 134 | 1200 |
20–40 kg | 268 | 2400 |
40–60 kg | 402 | 3600 |
Zalecana minimalna dawka wynosi 6,7 mg fipronilu/kg m.c. i 60 mg permetryny/kg m.c.
W przypadku psów o masie ciała >60 kg należy stosować odpowiednią kombinację pipetek. Sposób podawania:
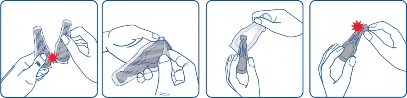
Wyjąć pipetkę z opakowania zewnętrznego. Trzymać pipetkę czubkiem do góry. Postukać w wąską część pipetki aby upewnić się, że cała jej zawartość znajduje się w jej głównej części. Odłamać czubek pipetki wzdłuż wyznaczonej linii.
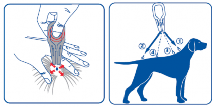
Odgarnąć sierść zwierzęcia tak, aby odsłonić skórę. Umieścić końcówkę pipetki bezpośrednio na odsłoniętej skórze i delikatnie nacisnąć ją kilka razy w celu uwolnienia jej zawartości w dwóch do czterech różnych miejscach, w zależności od masy ciała zwierzęcia, na grzbiecie zwierzęcia od łopatki do podstawy ogona.
Na przykład u psów o masie ciała poniżej 20 kg produkt należy nanieść w dwóch miejscach, natomiast u psów o masie ciała powyżej 20 kg produkt należy nanieść w 2–4 miejscach.
System kontrolowanego zatrzymywania kropli. 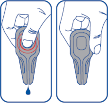 Schemat stosowania:
Schemat stosowania:
Stosowanie produktu powinno wynikać ze zdiagnozowanej inwazji lub ryzyka inwazji pcheł i/lub kleszczy, jak również z konieczności odstraszania (zapobiegania żerowaniu) muchówek i/lub komarów.
W zależności od zagrożenia pasożytami lekarz weterynarii może zalecić powtórzenie leczenia. Odstęp czasu między kolejnym zastosowaniem produktu powinien wynosić co najmniej 4 tygodnie.
Wykazano bezpieczeństwo stosowania produktu przy zastosowaniu dawek 5-krotnie wyższych od maksymalnej zalecanej dawki u zdrowych 12-tygodniowych szczeniąt, leczonych 3 razy w odstępach co 3 tygodnie.
W razie przedawkowania może jednak wzrastać ryzyko wystąpienia działań niepożądanych (patrz
punkt 4.6), a zatem u zwierząt należy zawsze stosować produkt przy użyciu pipetki odpowiedniej do masy ciała zwierzęcia.
Nie dotyczy
Grupa farmakoterapeutyczna: produkty do zwalczania pasożytów zewnętrznych, do stosowania miejscowego.
Kod ACTvet: QP53AC54 (permetryna, połączenia substancji czynnych)
Jest to przeznaczony do stosowania miejscowego produkt zabijający pasożyty zewnętrzne, zawierający fipronil i permetrynę. Takie połączenie działa jako środek owadobójczy, roztoczobójczy, a także odstraszający muchówki i komary.
Fipronil jest związkiem owadobójczym i roztoczobójczym należącym do grupy fenylopirazoli. Fipronil i jego metabolit, sulfon fipronilu, działają na kanały chlorkowe bramkowane ligandem, w szczególności bramkowane neuroprzekaźnikiem o nazwie kwas gamma-aminomasłowy (GABA), jak też odczulające (D) i nieodczulające (N) kanały bramkowane glutaminianem (Glu, występujące tylko u bezkręgowców kanały chlorkowe bramkowane ligandem); blokuje on w ten sposób pre- i postsynaptyczny przepływ jonów chlorkowych przez błony komórkowe. Prowadzi to do niekontrolowanej aktywności ośrodkowego układu nerwowego i śmierci owadów lub roztoczy.
Permetryna należy do pyretroidowych związków roztoczobójczych i owadobójczych klasy I, jak też ma działanie odstraszające. Pyretroidy działają u kręgowców i bezkręgowców na kanały sodowe zależne od potencjału. Pyretroidy są tak zwanymi „blokerami otwartego kanału”, wpływającymi na kanały sodowe poprzez spowolnienie zarówno aktywacji, jak i właściwości inaktywujących, co prowadzi do nadmiernego pobudzenia i śmierci pasożyta.
Produkt ten zapewnia natychmiastowe i stałe działanie owadobójcze przeciwko pchłom (Ctenocephalides felis), natychmiastowe działanie roztoczobójcze przeciwko kleszczom Ixodes ricinus i stałe działanie roztoczobójcze przeciwko kleszczom (Rhipicephalus sanguineus, Dermacentor reticulatus, Ixodes ricinus), a także działanie odstraszające (zapobiegające żerowaniu) muchówki (Phlebotomus perniciosus) i komary (Culex pipiens, Aedes aegypti).
Wykazano w warunkach eksperymentalnych, że u psów na co najmniej 2 dni przed ekspozycją na kleszcze produkt pośrednio redukował ryzyko przeniesienia Babesia canis canis z zakażonych kleszczy Dermacentor reticulatus przez okres do 28 dni po zastosowaniu, zmniejszając w ten sposób ryzyko wystąpienia babeszjozy u leczonych psów.
Głównym metabolitem fipronilu jest jego pochodna sulfonowa, która również wykazuje właściwości owadobójcze i roztoczobójcze.
Po miejscowym zastosowaniu u psów w normalnych warunkach użytkowania:
Permetryna i fipronil, a także jego główny metabolit, ulegają dystrybucji w sierści psa w ciągu jednego dnia po zastosowaniu. Stężenie fipronilu, sulfonu fipronilu i permetryny w sierści zmniejsza się z czasem, lecz związki te pozostają wykrywalne przez co najmniej 35 dni po zastosowaniu produktu.
Maksymalne stężenie fipronilu w osoczu występuje po 5 dniach, natomiast maksymalne stężenie jego aktywnego metabolitu po około 14 dniach. Stężenia pozostają w zakresie oznaczalnym przez około 35 dni. Permetryna charakteryzuje się bardzo niskim stopniem wchłaniania ogólnoustrojowego.
Butylohydroksyanizol (E320) Butylohydroksytoluen (E321) Alkohol benzylowy (E1519)
Glikolu dietylenowego monoetylowy eter
Nie dotyczy
Okres ważności produktu leczniczego weterynaryjnego zapakowanego do sprzedaży: 3 lata. Okres ważności po pierwszym otwarciu opakowania bezpośredniego: zużyć natychmiast.
Przechowywać w temperaturze poniżej 30°C.
Blister należy przechowywać w opakowaniu zewnętrznym w celu ochrony przed światłem.
Przezroczyste, wielowarstwowe, plastikowe, jednodawkowe pipetki zawierające 6,6 ml, otrzymywane przez kształtowanie termiczne przezroczystego denka (poliakrylonitryl-metakrylan lub polietylen-alkohol etylowinylowy-polietylen/polipropylen/kopolimer cyklicznej olefiny/polipropylen) i zamknięte przez zgrzewanie z wieczkiem (poliakrylonitryl-metakrylan lub polietylen-alkohol etylowinylowy-polietylen/ aluminium/polietylen-tereftalan).
Pudełka zawierają pojedyncze pipetki umieszczone w kolorowych blistrach wykonanych z polipropylenu/kopolimeru cyklicznej olefiny/ polipropylenu i zamknięte wieczkiem wykonanym z polietylenu-tereftalanu/aluminium/polipropylenu.
Pudełka po 1, 4, 24 lub 60 pipetek.
Niektóre wielkości opakowań mogą nie być dostępne w obrocie.
Niewykorzystany produkt leczniczy weterynaryjny lub jego odpady należy usunąć w sposób zgodny z obowiązującymi przepisami.
Nie należy zanieczyszczać stawów, cieków wodnych lub kanałów produktem leczniczym weterynaryjnym ani pustym pojemnikiem, ponieważ może to być niebezpieczne dla ryb i innych organizmów wodnych.
VIRBAC
1ère avenue 2065m LID 06516 Carros
Francja
2536/16
16.05.2016
02/2017










