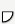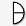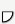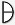Spis treści:
- NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
- SKŁAD JAKOŚCIOWY I ILOŚCIOWY
- POSTAĆ FARMACEUTYCZNA
- SZCZEGÓŁOWE DANE KLINICZNE
- WŁAŚCIWOŚCI FARMAKOLOGICZNE
- DANE FARMACEUTYCZNE
- NAZWA I ADRES PODMIOTU ODPOWIEDZIALNEGO
- NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
- DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU
- DATA OSTATNIEJ AKTUALIZACJI TEKSTU CHARAKTERYSTYKI PRODUKTU LECZNICZEGO WETERYNARYJNEGO
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
SKŁAD JAKOŚCIOWY I ILOŚCIOWY
POSTAĆ FARMACEUTYCZNA
SZCZEGÓŁOWE DANE KLINICZNE
Docelowe gatunki zwierząt
Wskazania lecznicze dla poszczególnych docelowych gatunków zwierząt
Przeciwwskazania
Specjalne ostrzeżenia dla każdego z docelowych gatunków zwierząt
Specjalne środki ostrożności dotyczące stosowania Specjalne środki ostrożności dotyczące stosowania u zwierząt
Działania niepożądane (częstotliwość i stopień nasilenia)
Stosowanie w ciąży i/lub laktacji.
Interakcje z innymi produktami leczniczymi i inne rodzaje interakcji
Dawkowanie i droga podawania
Przedawkowanie (objawy, sposób postępowania przy udzielaniu natychmiastowej pomocy, odtrutki), jeśli konieczne
Okres karencji
WŁAŚCIWOŚCI FARMAKOLOGICZNE
DANE FARMACEUTYCZNE
Wykaz substancji pomocniczych
Główne niezgodności farmaceutyczne
Okres ważności
Rodzaj i skład opakowania bezpośredniego
Specjalne środki ostrożności dotyczące usuwania niezużytego produktu leczniczego
NAZWA I ADRES PODMIOTU ODPOWIEDZIALNEGO
NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU
DATA OSTATNIEJ AKTUALIZACJI TEKSTU CHARAKTERYSTYKI PRODUKTU LECZNICZEGO WETERYNARYJNEGO
Amoxibactin vet 50 mg tabletki dla psów i kotów
Amoxibactin 50 mg tablets for dogs and cats [AT, BE, CY, CZ, EL, ES, FR, HR, HU, IE, IT, LU, NL, PT, RO, SI, SK, UK]
Amoxibactin vet 50 mg tablets for dogs and cats [DK, FI, IS, NO, SE, EE, LT, LV]
1 tabletka zawiera:
Substancja czynna:
Amoksycylina 50 mg (co odpowiada 57,50 mg amoksycyliny trójwodnej) Wykaz wszystkich substancji pomocniczych, patrz punkt 6.1.
Tabletka
Biała lub biaława z brązowymi kropkami, okrągła i wypukła, aromatyzowana tabletka z linią podziału w kształcie krzyża z jednej strony.
Tabletki można podzielić na połowy i ćwiartki.
Psy i koty
Leczenie pierwotnych i wtórnych zakażeń dróg oddechowych, takich jak zapalenie błon śluzowych nosa wywołane przez Pasteurella spp. i Streptococcus spp. i odoskrzelowe zapalenie płuc wywołane przez Pasteurella spp., Escherichia coli i ziarniaki Gram-dodatnie.
Leczenie pierwotnych zakażeń układu moczowo-płciowego, takich jak odmiedniczkowe zapalenie nerek, i zakażeń dolnego odcinka układu moczowego wywołanych przez Escherichia coli, Proteus spp. i ziarniaki Gram-dodatnie, zapalenie śluzówki macicy wywołane przez Escherichia coli, Streptococcus canis i Proteus spp., zapalenie pochwy jako skutek zakażeń mieszanych.
Leczenie zapalenia gruczołu mlekowego wywołanego przez ziarniaki Gram-dodatnie i Escherichia coli.
Leczenie miejscowych zakażeń skóry wywołanych przez Streptococcus spp.
Nie stosować w przypadkach nadwrażliwości na penicyliny lub inne substancje z grupy β-laktamów lub na dowolną substancję pomocniczą.
Nie podawać myszoskoczkom, kawiom domowym, chomikom, królikom i szynszylom.
Nie stosować u zwierząt z poważnymi zaburzeniami czynności nerek z towarzyszącą anurią i oligurią.
Brak
U zwierząt z zaburzeniami czynności wątroby i nerek należy zachować ostrożność przy doborze dawkowania, a stosowanie produktu powinno być poddane przez lekarza weterynarii ocenie stosunku korzyści/ryzyka.
Zaleca się zachowanie ostrożności podczas stosowania u małych zwierząt roślinożernych innych niż
wymienione w punkcie 4.3.
Z powodu prawdopodobnej zmienności (w czasie, geograficznej) występowania oporności bakterii na
amoksycylinę zalecane jest pobieranie próbek bakteriologicznych i badanie lekowrażliwości. Odnotowano zwiększoną oporność na leki przeciwdrobnoustrojowe wśród izolatów E. coli, w tym wielolekoopornych E. coli. W przypadku podejrzenia oporności na wiele leków na podstawie badań wrażliwości należy podjąć specjalne środki ostrożności.
W miarę możliwości produkt należy stosować wyłącznie w oparciu o badanie lekowrażliwości. Stosowanie produktu w inny sposób niż podany w ChPLW może zwiększać występowanie bakterii opornych na amoksycylinę i zmniejszać skuteczność leczenia innymi beta-laktamowymi lekami przeciwdrobnoustrojowymi lub innymi klasami leków przeciwdrobnoustrojowych ze względu na potencjalną oporność krzyżową.
Podczas stosowania produktu należy uwzględnić oficjalne, krajowe i regionalne wytyczne dotyczące
polityki przeciwdrobnoustrojowej.
Tabletki są aromatyzowane. Aby uniknąć przypadkowego połknięcia, tabletki należy przechowywać poza zasięgiem zwierząt.
Specjalne środki ostrożności dla osób podających produkt leczniczy weterynaryjny zwierzętom Penicyliny i cefalosporyny mogą wywoływać reakcje nadwrażliwości (uczulenie) po wstrzyknięciu, inhalacji, połknięciu lub kontakcie ze skórą. Nadwrażliwość na penicyliny może prowadzić do reakcji krzyżowych na cefalosporyny i na odwrót. Reakcje alergiczne na te substancje mogą być czasami poważne.
Nie posługiwać się produktem w przypadku stwierdzonego uczulenia lub zalecenia, aby nie pracować
z takimi produktami.
Produkt należy stosować z dużą ostrożnością w celu uniknięcia ekspozycji, przestrzegając wszystkich zalecanych środków ostrożności.
W przypadku wystąpienia objawów po ekspozycji, takich jak wysypka skórna, należy zwrócić się o pomoc lekarską i przedstawić lekarzowi niniejsze ostrzeżenie. Obrzęk twarzy, warg lub oczu lub trudności z oddychaniem są poważniejszymi objawami i wymagają pilnej pomocy medycznej.
Należy umyć ręce po podaniu tabletek.
Łagodne objawy żołądkowo-jelitowe (biegunka i wymioty) mogą wystąpić bardzo rzadko (mniej niż 1 na 10000 leczonych zwierząt, włączając pojedyncze raporty) po podaniu produktu. Reakcje nadwrażliwości (alergiczne reakcje skórne, anafilaksja) mogą występować bardzo rzadko. W takich przypadkach należy przerwać podawanie i zastosować leczenie objawowe.
Bezpieczeństwo produktu leczniczego weterynaryjnego stosowanego w czasie ciąży i laktacji nie zostało określone.
Badania laboratoryjne u szczurów nie wykazały działania teratogennego, toksycznego dla płodu bądź
szkodliwego dla samicy.
Do stosowania jedynie po dokonaniu przez lekarza weterynarii oceny bilansu korzyści/ryzyka wynikającego ze stosowania produktu.
Chloramfenikol, makrolidy, sulfonamidy i tetracykliny mogą hamować działanie przeciwbakteryjne penicylin z powodu szybkiego początku działania bakteriostatycznego. Należy rozważyć potencjał alergicznej reaktywności krzyżowej z innymi penicylinami.
Penicyliny mogą nasilać działanie aminoglikozydów.
Do podania doustnego psom i kotom.
W celu zapewnienia prawidłowego dawkowania należy jak najdokładniej ustalić masę ciała, aby uniknąć podawania za małych dawek.
Dawkowanie
Zalecana dawka wynosi 10 mg amoksycyliny na kg masy ciała, dwa razy na dobę przez minimum
5 kolejnych dni. Większość rutynowych przypadków odpowiada na leczenie po 5-7 dniach leczenia. Jeśli po 5-7 dniach nie obserwuje się poprawy, należy przeprowadzić ponowną ocenę rozpoznania. W przypadku chorób przewlekłych lub nawracających może być wymagany dłuższy czas trwania leczenia.
Poniższa tabela służy jako wskazówka odnośnie podawania produktu w dawce standardowej 10 mg na


kg masy ciała dwa razy na dobę.
Liczba tabletek dwa razy na dobę | |||
Masa ciała (kg) | Amoksycylina 50 mg dla psów i kotów | Amoksycylina 250 mg dla psów | Amoksycylina 500 mg dla psów |
1-1,25 |
| ||
>1,25-2,5 |
| ||
>2,5-3,75 |
| ||
>3,75-5 |
| ||
>5-6,25 |
| lub | |
>6,25-12,5 |
| lub | |
>12,5-18,75 |
| ||
>18,75-25 |
| lub | |
>25-31,25 |
| ||
>31,25-37,5 |
| lub | |
>37,5-50 |
| lub | |
>50-62,5 |
| ||
>62,5-75 |
| ||




= ¼ tabletki 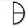 = ½ tabletki
= ½ tabletki  = ¾ tabletki
= ¾ tabletki  = 1 tabletka
= 1 tabletka
Tabletki można dzielić na połowy lub ćwiartki w celu zapewnienia dokładnego dawkowania. Tabletkę umieścić na płaskiej powierzchni ze stroną z linią podziału skierowaną do góry i stroną wypukłą (zaokrągloną) skierowaną do powierzchni.
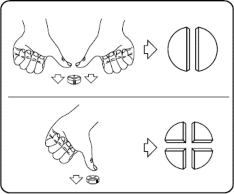
Połówki: nacisnąć kciukami po obu stronach tabletki. Ćwiartki: nacisnąć kciukiem w środku tabletki.
W przypadku przedawkowania nie są znane inne działania niepożądane niż te opisane w punkcie 4.6.
Nie dotyczy.
Grupa farmakoterapeutyczna: leki przeciwbakteryjne do stosowania ogólnoustrojowego. Penicyliny
o rozszerzonym spektrum działania.
Kod ATCvet: QJ01CA04
5.1. Właściwości farmakodynamiczne Ogólne właściwości
Amoksycylina jest antybiotykiem beta-laktamowym, a jej struktura zawiera wspólny dla wszystkich penicylin pierścień beta-laktamowy i pierścień tiazolidynowy. Antybiotyki beta-laktamowe zapobiegają tworzeniu się ścian komórkowych bakterii poprzez zakłócanie końcowego etapu syntezy peptydoglikanu. Hamują one aktywność enzymów transpeptydaz katalizujących wiązanie poprzeczne jednostek polimerowych glikopeptydów, które tworzą ściany komórkowe. Mają one działanie bakteriobójcze, ale powodują lizę tylko rosnących komórek. Antybiotyki beta-laktamowe można nazwać antybiotykami zależnymi od czasu.
Spektrum działania przeciwdrobnoustrojowego
Amoksycylina jest antybiotykiem o szerokim spektrum działania i jest na ogół aktywna przeciw niektórym bakteriom Gram-ujemnym i większości bakterii Gram-dodatnich (Germ-vet 2007), np. wrażliwym na penicyliny Pasteurella spp., Proteus spp, Streptococcus spp., E. coli i ziarniakom Gram-dodatnim.
Oporność
Amoksycylina jest oporna na kwasy, ale nie jest oporna na działanie beta-laktamaz, które mogą hydrolizować cząsteczki, powodując otwarcie struktury pierścienia beta-laktamowego i prowadząc do braku działania antybiotyku.
Większość bakterii Gram-ujemnych jest w istocie oporna na wiele leków beta-laktamowych. Wynika
to częściowo z mechanizmu działania leku i budowy błony bakterii.
Nabyta oporność na leki beta-laktamowe w izolatach klinicznych może być związana z aktywnością beta-laktamaz określoną przez plazmidy lub mutacjami miejsc genu w chromosomie. W niektórych szczepach mutacja jednoetapowa może być odpowiedzialna za oporność, podczas gdy w innych szczepach oporność może być spowodowana kilkoma mutacjami.
Występowanie nabytej oporności może być duże u E. coli.
5.2 Właściwości farmakokinetyczne
Amoksycylina jest dobrze wchłaniana po podaniu doustnym. U psów biodostępność ogólnoustrojowa wynosi 60-70%. Amoksycylina ma względnie małą pozorną objętość dystrybucji, niski stopień wiązania przez białka osocza (34% u psów) i krótki okres półtrwania eliminacji ze względu na aktywne wydalanie kanalikowe przez nerki.
Po absorpcji największe stężenia są wykrywane w nerkach (mocz) i żółci, a następnie wątrobie, płucach, sercu i śledzionie.
Dystrybucja amoksycyliny do płynu mózgowo-rdzeniowego jest niska, chyba że występuje zapalenie
opon.
Magnezu stearynian
Celuloza mikrokrystaliczna Krzemionka koloidalna, bezwodna Karboksymetyloskrobia sodowa (typ A) Laktoza jednowodna
Drożdże (suszone)
Aromat drobiowy
Nie dotyczy.
Okres ważności produktu leczniczego weterynaryjnego zapakowanego do sprzedaży: 3 lata.
6.4. Specjalne środki ostrożności podczas przechowywania
Nie przechowywać w temperaturze powyżej 30C.
Wszelkie niewykorzystane tabletki należy włożyć do otwartego blistra i zużyć w ciągu 4 dni.
Blister – Aluminium/PCV/PE/PVDC.
Pudełko tekturowe zawierające 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 25 lub 50 blistrów po 10 tabletek. Pudełko tekturowe zawierające 10 opakowań jednostkowych, każde zawierające 1 blister po 10 tabletek.
Niektóre wielkości opakowań mogą nie być dostępne w obrocie.
weterynaryjnego lub pochodzących z niego odpadów
Niewykorzystany produkt leczniczy weterynaryjny lub jego odpady należy usunąć w sposób zgodny z obowiązującymi przepisami.
Le Vet. Beheer B.V. Wilgenweg 7
3421 TV Oudewater Holandia
2858/19
/ DATA PRZEDŁUŻENIA POZWOLENIA
Data wydania pierwszego pozwolenia na dopuszczenie do obrotu: 03.04.2019r. Data przedłużenia pozwolenia: