Spis treści:
- NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
- SK AD JAKO
 CIOWY I ILO
CIOWY I ILO CIOWY
CIOWY - POSTA
 FARMACEUTYCZNA
FARMACEUTYCZNA - SZCZEGÓ OWE DANE KLINICZNE
- W A
 CIWO
CIWO CI FARMAKOLOGICZNE
CI FARMAKOLOGICZNE - DANE FARMACEUTYCZNE
- NAZWA I ADRES PODMIOTU ODPOWIEDZIALNEGO
- NUMER(-Y) POZWOLENIA NA DOPUSZCZENIE DO OBROTU
- DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU
- DATA OSTATNIEJ AKTUALIZACJI TEKSTU CHARAKTERYSTYKI PRODUKTU LECZNICZEGO WETERYNARYJNEGO
[Version 8.1, 01/2017]
ANEKS I
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
SK AD JAKO
 CIOWY I ILO
CIOWY I ILO CIOWY
CIOWYPOSTA
 FARMACEUTYCZNA
FARMACEUTYCZNASZCZEGÓ OWE DANE KLINICZNE
Docelowe gatunki zwierz t
Wskazania lecznicze dla poszczególnych docelowych gatunków zwierz t
Przeciwwskazania
Specjalne ostrze enia dla ka dego z docelowych gatunków zwierz t
Specjalne rodki ostro no ci dotycz ce stosowania
Dzia ania niepo
 dane (cz sto i stopie nasilenia)
dane (cz sto i stopie nasilenia)bardzo cz sto (wi cej ni 1 na 10 leczonych zwierz t wykazuj cych dzia anie(a) niepo dane)
cz sto (wi cej ni 1, ale mniej ni 10 na 100 leczonych zwierz t)
niezbyt cz sto (wi cej ni 1, ale mniej ni 10 na 1000 leczonych zwierz t)
rzadko (wi cej ni 1, ale mniej ni 10 na 10000 leczonych zwierz t)
bardzo rzadko (mniej ni 1 na 10000 leczonych zwierz t, w
 czaj c pojedyncze raporty).
czaj c pojedyncze raporty).Interakcje z innymi produktami leczniczymi i inne rodzaje interakcji
Dawkowanie i droga podawania
Przedawkowanie (objawy, sposób post powania przy udzielaniu natychmiastowej pomocy, odtrutki), je li konieczne
Okresy karencji
W A
 CIWO
CIWO CI FARMAKOLOGICZNE
CI FARMAKOLOGICZNEW a ciwo ci farmakodynamiczne
W a ciwo ci farmakokinetyczne
DANE FARMACEUTYCZNE
Wykaz substancji pomocniczych
G ówne niezgodno ci farmaceutyczne
Okres wa no ci
Specjalne rodki ostro no ci podczas przechowywania
Rodzaj i sk ad opakowania bezpo redniego
Specjalne rodki ostro no ci dotycz ce usuwania niezu ytego produktu leczniczego weterynaryjnego lub pochodz cych z niego odpadów
NAZWA I ADRES PODMIOTU ODPOWIEDZIALNEGO
NUMER(-Y) POZWOLENIA NA DOPUSZCZENIE DO OBROTU
DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU
DATA OSTATNIEJ AKTUALIZACJI TEKSTU CHARAKTERYSTYKI PRODUKTU LECZNICZEGO WETERYNARYJNEGO

Alfaxan Multidose 10 mg/ml roztwór do wstrzykiwa dla psów i kotów
Ka dy ml roztworu zawiera:
Substancja czynna:
Alfaksalon 10 mg
Substancje pomocnicze:
Etanol 150 mg
Chlorokrezol 1 mg Benzetoniowy chlorek 0,2 mg
Wykaz wszystkich substancji pomocniczych, patrz punkt 6.1.
Roztwór do wstrzykiwa Klarowny, bezbarwny roztwór
Psy i koty
Jako produkt znieczulaj cy do stosowania w indukcji znieczulenia przed podaniem znieczulenia wziewnego.
Jako jedyny produkt znieczulaj cy w celu indukcji i podtrzymania znieczulenia w celu przeprowadzenia badania lub zabiegu chirurgicznego.
Nie stosowa w skojarzeniu z innymi produktami znieczulaj cymi podawanymi do ylnie. Nie stosowa w przypadkach nadwra liwo ci na substancj czynn , lub na dowoln substancj pomocnicz .
W a ciwo ci przeciwbólowe alfaksalonu s ograniczone, w zwi zku z czym nale y zapewni odpowiedni analgezj oko ooperacyjn w przypadku bolesnych zabiegów.
Specjalne rodki ostro no ci dotycz ce stosowania u zwierz t
Nie wykazano bezpiecze stwa produktu leczniczego weterynaryjnego dla zwierz t w wieku poni ej 12 tygodni.
W fazie postindukcyjnej cz sto wyst puje przej ciowy bezdech, w szczególno ci u psów - szczegó owe informacje na ten temat znajduj si w punkcie 4.6. W takich przypadkach nale y
zastosowa intubacj dotchawiczn i poda tlen. Nale y dysponowa urz dzeniami umo liwiaj cymi prowadzenie przerywanej wentylacji nadci nieniowej. Aby zminimalizowa mo liwo wyst pienia bezdechu, produkt leczniczy weterynaryjny nale y podawa przez powolne wstrzykni cie do ylne, a nie jako bolus. Jako najlepsz praktyk w procedurach znieczulenia zaleca si stosowanie uprzednio za o onego cewnika do ylnego (wenflonu).

W szczególno ci podczas stosowania wi kszych dawek produktu leczniczego weterynaryjnego mo e wyst pi , zale na od dawki, depresja oddechowa. Nale y stosowa tlen i (lub) przerywan wentylacj nadci nieniow w celu zapobiegania zagro eniu hipoksemi i hiperkapni . Powinno to mie szczególne znaczenie w przypadkach znieczulenia wi cego si z dodatkowym ryzykiem oraz za ka dym razem, kiedy czas trwania znieczulenia jest wyd u ony.
Zarówno u psów jak i u kotów przerwa w podawaniu znieczulenia poprzez przerywane podawanie w bolusie mo e wymaga wyd u enia o ponad 20% lub dawka podtrzymuj ca podawana w formie infuzji do ylnej mo e wymaga obni enia o ponad 20%, je li przep yw krwi w w trobie jest istotnie pomniejszony lub wyst puje silny uraz komórek w trobowych.
U kotów i psów z niewydolno ci nerek dawki stosowane w fazie indukcji i utrzymania znieczulenia mog wymaga ograniczenia.
Podobnie jak w przypadku wszystkich produktów do znieczulenia ogólnego:
Przed podaniem produktu znieczulaj cego nale y upewni si , czy pacjent jest na czczo. Podobnie jak w przypadku wszystkich do ylnych produktów znieczulaj cych nale y zachowa ostro no u zwierz t z niewydolno ci serca lub uk adu oddechowego lub u zwierz t z hipowolemi lub os abionych.
Doradza si dodatkowy monitoring i zwracanie szczególnej uwagi na parametry oddechowe u zwierz t starszych lub je li istnieje dodatkowy stres fizjologiczny w wyniku wcze niej istniej cej choroby, wstrz su lub cesarskiego ci cia.
Po indukcji znieczulenia zaleca si stosowanie rurki dotchawiczej w celu zapewnienia dro no ci dróg oddechowych.
Zaleca si suplementacj tlenem w okresie utrzymywania w stanie znieczulenia.
Mo e wyst pi ostra niewydolno oddechowa – nale y rozwa y wentylacj p uc tlenem, je li saturacja hemoglobiny tlenem (SpO2%) spada poni ej 90% lub je li bezdech utrzymuje si d u ej ni 60 sekund.

W przypadku wykrycia zaburze rytmu serca najwy szym priorytetem jest wentylacja dróg oddechowych tlenem, a nast pnie podanie odpowiednich leków nasercowych lub interwencja.
Podczas wybudzania nie nale y przenosi zwierz t ani im przeszkadza . Mo e to prowadzi do wyst pienia ruchów wios owych, drgania mi ni lub bardziej gwa townych ruchów. Takich reakcji nale y unika , jednak s one nieistotne z klinicznego punktu widzenia. Wybudzanie ze znieczulenia powinno odbywa si w odpowiednim miejscu i pod odpowiednim nadzorem. Zastosowanie
ni lub bardziej gwa townych ruchów. Takich reakcji nale y unika , jednak s one nieistotne z klinicznego punktu widzenia. Wybudzanie ze znieczulenia powinno odbywa si w odpowiednim miejscu i pod odpowiednim nadzorem. Zastosowanie
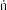
w premedykacji benzodiazepin jako jedynego leku mo e zwi ksza prawdopodobie stwo wyst pienia pobudzenia psychoruchowego.
Specjalne rodki ostro no ci dla osób podaj cych produkt leczniczy weterynaryjny zwierz tom
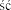
Ten produkt jest lekiem uspokajaj cym, nale y zachowa ostro no , aby unikn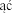 przypadkowego wstrzykni cia leku samemu sobie (samoiniekcji).
przypadkowego wstrzykni cia leku samemu sobie (samoiniekcji).
Ig a powinna pozostawa zabezpieczona do momentu wykonywania iniekcji.
Je li dojdzie do przypadkowego podania leku samemu sobie (samoiniekcji), nale y natychmiast
zasi gn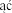 porady lekarskiej oraz pokaza mu Charakterystyk produktu leczniczego weterynaryjnego, ulotk lub opakowanie. W przypadku kontaktu ze skór lub oczami produkt mo e powodowa
porady lekarskiej oraz pokaza mu Charakterystyk produktu leczniczego weterynaryjnego, ulotk lub opakowanie. W przypadku kontaktu ze skór lub oczami produkt mo e powodowa
podra nienia.
Produkt nale y natychmiast sp uka ze skóry i z oczu wod .


W badaniach klinicznych prowadzonych z wykorzystaniem produktu leczniczego weterynaryjnego, bezdech w fazie indukcji znieczulenia, definiowany jako przerwa w oddychaniu trwaj ca 30 sekund lub d u ej, wyst powa bardzo cz sto u psów i kotów. 44% psów i 19% kotów do wiadcza o bezdechu po podaniu znieczulenia. redni czas trwania bezdechu u tych zwierz t wynosi 100 sekund u psów
i 60 sekund u kotów. W takiej sytuacji nale y zastosowa intubacj dotchawiczn i poda tlen.

:

Cz sto wyst powania dzia a niepo danych przedstawia si zgodnie z poni sz regu
danych przedstawia si zgodnie z poni sz regu
4.7. Stosowanie w ci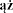 y, laktacji lub w okresie nie no ci
y, laktacji lub w okresie nie no ci
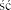

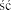
Bezpiecze stwa produktu leczniczego weterynaryjnego nie ustalono w przypadkach zamierzonej kontynuacji ci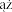 y lub podczas laktacji. Nie oceniano wp ywu produktu na p odno . Badania przy wykorzystaniu alfaksalonu na ci
y lub podczas laktacji. Nie oceniano wp ywu produktu na p odno . Badania przy wykorzystaniu alfaksalonu na ci arnych myszach, szczurach i królikach nie wykaza y jednak szkodliwego wp ywu na przebieg ci y u leczonych zwierz t ani na wydajno reprodukcyjn ich potomstwa. Produkt nale y stosowa u ci
arnych myszach, szczurach i królikach nie wykaza y jednak szkodliwego wp ywu na przebieg ci y u leczonych zwierz t ani na wydajno reprodukcyjn ich potomstwa. Produkt nale y stosowa u ci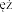 arnych zwierz t zgodnie z ocen ryzyka i korzy ci dokonan przez lekarza weterynarii. Produkt bezpiecznie stosowano u psów w celu indukcji znieczulenia przed porodem rozwi zanym cesarskim ci ciem. W tych badaniach nie stosowano premedykacji, podawano dawk 1-2 mg/kg (tj. nieco ni sz ni zwyk a dawka wynosz ca 3 mg/kg, patrz punkt 4.9), a produkt by skutecznie podawany zgodnie z zaleceniami.
arnych zwierz t zgodnie z ocen ryzyka i korzy ci dokonan przez lekarza weterynarii. Produkt bezpiecznie stosowano u psów w celu indukcji znieczulenia przed porodem rozwi zanym cesarskim ci ciem. W tych badaniach nie stosowano premedykacji, podawano dawk 1-2 mg/kg (tj. nieco ni sz ni zwyk a dawka wynosz ca 3 mg/kg, patrz punkt 4.9), a produkt by skutecznie podawany zgodnie z zaleceniami.
Wykazano, e produkt leczniczy weterynaryjny jest bezpieczny podczas stosowania w skojarzeniu z nast puj cymi kategoriami produktów stosowanych w premedykacji:
Kategoria leków | Przyk ady |
Fenotiazyny | Acepromazyny maleinian |
Antycholinergiki | Atropiny siarczan |
Benzodiazepiny | Diazepam, Midazolamu chlorowodorek |
Agoni ci receptora alfa-2- adrenergicznego | Ksylazyny chlorowodorek, Medetomidyny chlorowodorek |
Opioidy | Metadon, morfiny siarczan, butorfanolu winian, buprenorfiny chlorowodorek |
Niesteroidowe leki przeciwzapalne | Karprofen, meloksykam |
Nale y oczekiwa , e równoczesne podawanie z innymi produktami dzia aj cymi depresyjnie na dzia anie centralnego uk adu nerwowego nasili dzia anie depresyjne tego produktu leczniczego weterynaryjnego, wymagaj c przerwania dalszego podawania produktu leczniczego weterynaryjnego po osi gni ciu wymaganej g boko ci znieczulenia.
Dodatkowe stosowanie jednego produktu do premedykacji lub skojarzenia takich produktów cz sto zmniejsza wymagan do podania dawk tego produktu leczniczego weterynaryjnego.
Premedykacja przy zastosowaniu agonistów receptora alfa-2-adrenergicznego, takich jak ksylazyna
i medetomidyna mo e znacznie wyd u y czas trwania znieczulenia w sposób zale ny od dawki. Aby skróci czas wybudzania, mo e by po dane odwrócenie dzia ania tych produktów u ywanych do premedykacji.
dane odwrócenie dzia ania tych produktów u ywanych do premedykacji.

Benzodiazepin nie nale y stosowa samodzielnie do premedykacji u psów i kotów, gdy mo e to pogorszy jako znieczulenia u niekórych pacjentów. Benzodiazepiny mo na bezpiecznie
i skutecznie stosowa w skojarzeniu z innymi produktami do premedykacji oraz z tym produktem leczniczym weterynaryjnym. Patrz punkt 4.3.
Podanie do ylne. Indukcja znieczulenia:
Dawka indukcyjna produktu leczniczego weterynaryjnego opiera si na danych otrzymanych

z kontrolowanych bada laboratoryjnych oraz bada terenowych i odpowiada ilo ci leku wymaganej do zapewnienia odpowiedniego poziomu znieczulenia u 9 na 10 pacjentów (tj. 90. percentyl).
Do indukcji znieczulenia zaleca si stosowanie nast puj cych dawek:
PSY | KOTY | |||
Bez premedykacji | Z premedykacj | Bez premedykacji | Z premedykacj | |
mg/kg | 3 | 2 | 5 | 5 |
ml/kg | 0,3 | 0,2 | 0,5 | 0,5 |
Odpowiedni dawk nale y pobra do strzykawki dozuj cej. Nale y kontynuowa podawanie leku, dopóki lekarz nie uzna, e g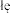 boko znieczulenia jest wystarczaj ca do wykonania intubacji dotchawiczej lub do czasu podania ca ej dawki. Niezb dne tempo iniekcji mo na osi gn poprzez podanie jednej czwartej (¼) obliczonej dawki co 15 sekund, tak aby ca kowita dawka, je li b dzie wymagana, zosta a podana w ci gu pierwszych 60 sekund. Je li, 60 sekund po podaniu ca ej pierwszej dawki indukcyjnej, nadal nie mo na przeprowadzi intubacji, mo na poda kolejn podobn dawk , aby osi gn
boko znieczulenia jest wystarczaj ca do wykonania intubacji dotchawiczej lub do czasu podania ca ej dawki. Niezb dne tempo iniekcji mo na osi gn poprzez podanie jednej czwartej (¼) obliczonej dawki co 15 sekund, tak aby ca kowita dawka, je li b dzie wymagana, zosta a podana w ci gu pierwszych 60 sekund. Je li, 60 sekund po podaniu ca ej pierwszej dawki indukcyjnej, nadal nie mo na przeprowadzi intubacji, mo na poda kolejn podobn dawk , aby osi gn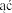 po
po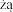 dany efekt.
dany efekt.
Podtrzymanie znieczulenia:
Po indukcji znieczulenia tym produktem leczniczym weterynaryjnym zwierz mo na zaintubowa


i podtrzymywa znieczulenie z zastosowaniem równie tego produktu leczniczego weterynaryjnego lub wziewnego produktu znieczulaj cego. Dawki podtrzymuj ce produktu leczniczego weterynaryjnego mo na podawa jako dodatkowe bolusy lub jako infuzja do ylna podawana ze sta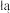 pr dko ci . Produkt leczniczy weterynaryjny by bezpiecznie i skutecznie stosowany zarówno u psów i kotów podczas zabiegów trwaj cych do godziny. Poni sze dawki sugerowane do utrzymania znieczulenia opieraj si na danych uzyskanych z kontrolowanych bada laboratoryjnych i bada terenowych oraz stanowi redni dawk leku wymagan do zapewnienia znieczulenia u psa lub kota. Rzeczywista dawka b dzie jednak uzale niona od reakcji danego pacjenta.
pr dko ci . Produkt leczniczy weterynaryjny by bezpiecznie i skutecznie stosowany zarówno u psów i kotów podczas zabiegów trwaj cych do godziny. Poni sze dawki sugerowane do utrzymania znieczulenia opieraj si na danych uzyskanych z kontrolowanych bada laboratoryjnych i bada terenowych oraz stanowi redni dawk leku wymagan do zapewnienia znieczulenia u psa lub kota. Rzeczywista dawka b dzie jednak uzale niona od reakcji danego pacjenta.
Do podtrzymania znieczulenia zaleca si stosowanie nast puj cych dawek:
PSY | KOTY | |||
Bez premedykacji | Z premedykacj | Bez premedykacji | Z premedykacj | |
Dawka wlewu podawanego ze sta | ||||
mg/kg/godzin | 8 - 9 | 6 - 7 | 10 - 11 | 7 - 8 |
mg/kg/minut | 0,13 - 0,15 | 0,10 - 0,12 | 0,16 - 0,18 | 0,11 - 0,13 |
ml/kg/minut | 0,013 - 0,015 | 0,010 - 0,012 | 0,016 - 0,018 | 0,011 - 0,013 |
Dawka bolusa podawanego co 10 minut w celu utrzymania znieczulenia | ||||
mg/kg | 1,3 - 1,5 | 1,0 - 1,2 | 1,6 - 1,8 | 1,1 - 1,3 |
ml/kg | 0,13 - 0,15 | 0,10 - 0,12 | 0,16 - 0,18 | 0,11 - 0,13 |
W przypadku podtrzymywania znieczulenia za pomoc tego produktu leczniczego weterynaryjnego podczas zabiegów trwaj cych od ponad 5 do 10 minut, ig motylkow lub cewnik do ylny (wenflon) mo na pozostawi w yle, aby móc nast pnie wstrzykiwa niewielkie ilo ci produktu leczniczego weterynaryjnego w celu podtrzymania wymaganej g boko ci i czasu trwania znieczulenia.
boko ci i czasu trwania znieczulenia.
W wi kszo ci przypadków redni czas wybudzania przy zastosowaniu tego produktu leczniczego weterynaryjnego u ytego do podtrzymania znieczulenia b dzie d u szy ni w przypadku stosowania gazu wziewnego jako produktu do podtrzymania znieczulenia.
Wykazano siln tolerancj na przedawkowanie stosuj c do 10-krotno ci zalecanej dawki równej 2 mg/kg u psów (tj. do 20 mg/kg) oraz do 5-krotno ci zalecanej dawki równej 5 mg/kg u kotów (tj. do 25 mg/kg). U psów i kotów podawanie tych nadmiernych dawek w ci gu 60 sekund powoduje bezdech i chwilowe obni enie redniego t tniczego ci nienia krwi. Obni enie ci nienia krwi nie zagra a yciu ani nie jest rekompensowane zmianami t tna. Zwierz ta te mo na leczy wy cznie za pomoc przerywanej wentylacji nadci nieniowej (je li jest wymagana) przy zastosowaniu powietrza atmosferycznego lub, najlepiej, tlenu. Wybudzenie nast puje szybko i bez resztkowego dzia ania.
cznie za pomoc przerywanej wentylacji nadci nieniowej (je li jest wymagana) przy zastosowaniu powietrza atmosferycznego lub, najlepiej, tlenu. Wybudzenie nast puje szybko i bez resztkowego dzia ania.
Nie dotyczy.
Grupa farmakoterapeutyczna: inne ogólne produkty znieczulaj ce, alfaksalon. Kod ATCvet: QN01AX05.


Alfaksalon (3- -hydroksy-5- -pregnano-11,20-dion) to neuroaktywna cz steczka steroidowa o w a ciwo ciach znieczulenia ogólnego. G ównym mechanizmem dzia ania znieczulaj cego
alfaksalonu jest modulacja transportu jonów chlorkowych przez b on komórek nerwowych wywo ana poprzez wi zanie si alfaksalonu z receptorami GABAA.
U kotów po podaniu pojedynczej dawki do ylnej alfaksalonu wynosz cej 5 mg/kg masy cia a, redni okres pó trwania w fazie eliminacji z osocza (t1/2) wynosi w przybli eniu 45 minut. Klirens osoczowy wynosi 25 ml/kg/min. Pozorna obj to dystrybucji wynosi 1,8 l/kg.
U psów po podaniu pojedynczej dawki do ylnej alfaksalonu wynosz cej 2 mg/kg masy cia a, redni okres pó trwania w fazie eliminacji z osocza (t1/2) wynosi w przybli eniu 25 minut. Klirens osoczowy wynosi 59 ml/kg/min. Pozorna obj to dystrybucji wynosi 2,4 l/kg.
U psów i kotów eliminacja alfaksalonu wykazuje nieliniow farmakokinetyk (zale n od dawki).
Badania in vitro kocich i psich hepatocytów wykazuj , e alfaksalon podlega zarówno metabolizmowi fazy I (zale nej od cytochromu P450) i fazy II (zale nej od sprz gania). Zarówno u psów jak i u kotów w fazie I powstaje pi (5 metabolitów alfakskalonu ) tych samych u obu gatunków. Metabolity fazy II obserwowane u kotów to alfaksalonu siarczan i alfaksolonu glukuronid, podczas gdy u psów obserwowany jest alfaksolonu glukuronid.
(5 metabolitów alfakskalonu ) tych samych u obu gatunków. Metabolity fazy II obserwowane u kotów to alfaksalonu siarczan i alfaksolonu glukuronid, podczas gdy u psów obserwowany jest alfaksolonu glukuronid.
Jest prawdopodobne, e metabolity alfaksolonu zostan wyeliminowane z organizmów psów i kotów drog w trobow (z ka em) lub drog nerkow , podobnie jak ma to miejsce u innych gatunków.
Hydroksypropylobetadeks Sodu chlorek
Disodu fosforan bezwodny Potasu diwodorofosforan Chlorokrezol
Benzetoniowy chlorek Etanol

Sodu wodorotlenek (do regulacji pH) Kwas solny st ony (do regulacji pH) Woda do wstrzykiwa
ony (do regulacji pH) Woda do wstrzykiwa
Poniewa nie wykonywano bada dotycz cych zgodno ci, tego produktu leczniczego weterynaryjnego nie wolno miesza z innymi produktami leczniczymi weterynaryjnymi.
Okres wa no ci produktu leczniczego weterynaryjnego zapakowanego do sprzeda y: 3 lata. Okres wa no ci po pierwszym otwarciu opakowania bezpo redniego: 28 dni.
Przechowywa w temperaturze poni ej 25°C.
Przechowywa fiolk w opakowaniu zewn trznym w celu ochrony przed wiat em.
Fiolka szklana o pojemno ci 10 lub 20 ml zamkni ta korkiem z gumy bromobutylowej z wieczkiem aluminiowym, w tekturowym pude ku.
Niektóre wielko ci opakowa mog nie by dost pne w obrocie.
Niewykorzystany produkt leczniczy weterynaryjny lub jego odpady nale y usun w sposób zgodny z obowi zuj cymi przepisami.
w sposób zgodny z obowi zuj cymi przepisami.
Jurox (Ireland) Limited The Black Church
St. Marys Place Dublin D07 P4AX Irlandia.
/ DATA PRZED U ENIA POZWOLENIA
ENIA POZWOLENIA
Data wydania pierwszego pozwolenia na dopuszczenie do obrotu: <{DD/MM/RRRR}> <{DD miesi c RRRR}.>
Data przed u enia pozwolenia: <{DD/MM/RRRR}> <{DD miesi c RRRR}.>
<{MM/RRRR}>
<{DD/MM/RRRR}>
<{DD miesi c RRRR}>
ZAKAZ WYTWARZANIA, IMPORTU, POSIADANIA, SPRZEDA Y, DOSTAWY I/LUB STOSOWANIA
Y, DOSTAWY I/LUB STOSOWANIA
<Nie dotyczy>