Spis treści:
- NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
- SKŁAD JAKOŚCIOWY I ILOŚCIOWY
- POSTAĆ FARMACEUTYCZNA
- SZCZEGÓŁOWE DANE KLINICZNE
- WŁAŚCIWOŚCI FARMAKOLOGICZNE
- DANE FARMACEUTYCZNE
- NAZWA I ADRES PODMIOTU ODPOWIEDZIALNEGO
- NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
- DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU / DATA PRZEDŁUŻENIA POZWOLENIA
- DATA OSTATNIEJ AKTUALIZACJI TEKSTU CHARAKTERYSTYKI PRODUKTU LECZNICZEGO WETERYNARYJNEGO
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
SKŁAD JAKOŚCIOWY I ILOŚCIOWY
POSTAĆ FARMACEUTYCZNA
SZCZEGÓŁOWE DANE KLINICZNE
Docelowe gatunki zwierząt
Wskazania lecznicze dla poszczególnych docelowych gatunków zwierząt
Przeciwwskazania
Specjalne ostrzeżenia dla każdego z docelowych gatunków zwierząt
Specjalne środki ostrożności dotyczące stosowania
Działania niepożądane (częstotliwość i stopień nasilenia)
Stosowanie w ciąży, laktacji lub w okresie nieśności
Interakcje z innymi produktami leczniczymi i inne rodzaje interakcji
Dawkowanie i droga podawania
Przedawkowanie (objawy, sposób postępowania przy udzielaniu natychmiastowej pomocy, odtrutki), jeśli konieczne
Okres karencji
WŁAŚCIWOŚCI FARMAKOLOGICZNE
Właściwości farmakodynamiczne
Właściwości farmakokinetyczne
DANE FARMACEUTYCZNE
Wykaz substancji pomocniczych
Główne niezgodności farmaceutyczne
Okres ważności
Rodzaj i skład opakowania bezpośredniego
Specjalne środki ostrożności dotyczące usuwania niezużytego produktu leczniczego weterynaryjnego lub pochodzących z niego odpadów
NAZWA I ADRES PODMIOTU ODPOWIEDZIALNEGO
NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU / DATA PRZEDŁUŻENIA POZWOLENIA
DATA OSTATNIEJ AKTUALIZACJI TEKSTU CHARAKTERYSTYKI PRODUKTU LECZNICZEGO WETERYNARYJNEGO
Kelevo 800 mikrogramów tabletki dla psów Kelevo 800 μg tablets for dogs
Kelevo 800 microgram tablets for dogs (AT, DE)
Każda tabletka zawiera:
Substancja czynna:
Lewotyroksyna sodowa 800 µg (co odpowiada 778 μg lewotyroksyny)
Substancje pomocnicze:
Wykaz wszystkich substancji pomocniczych, patrz punkt 6.1.
Tabletka.
Biała do białawej, okrągła, wypukła tabletka z brązowymi plamkami i liniami podziału w kształcie krzyża po jednej stronie. Tabletki mogą być podzielone na 2 lub 4 równe części.
Psy.
Leczenie pierwotnej i wtórnej niedoczynności tarczycy.
Nie stosować u psów z niewyrównaną niewydolnością nadnerczy.
Nie stosować w przypadkach stwierdzonej nadwrażliwości na lewotyroksynę sodową lub na dowolną substancję pomocniczą.
Rozpoznanie niedoczynności tarczycy należy potwierdzić odpowiednimi badaniami.
Specjalne środki ostrożności dotyczące stosowania u zwierząt
Nagły wzrost zapotrzebowania na tlen w tkankach obwodowych oraz chronotropowe działanie lewotyroksyny sodowej mogą powodować nadmierne obciążenie niewydolnego serca, powodując dekompensację i objawy zastoinowej niewydolności serca.
Zwierzęta z niedoczynnością tarczycy, u których występuje jednocześnie niedoczynność kory nadnerczy, mają ograniczoną zdolność metabolizowania lewotyroksyny sodowej, przez co występuje u nich zwiększone ryzyko wystąpienia tyreotoksykozy. Aby uniknąć przełomu nadnerczowego, przed rozpoczęciem podawania lewotyroksyny sodowej należy u tych zwierząt zastosować stabilizujące leczenie glikokortykosteroidami i mineralokortykosteroidami. Następnie, po powtórnym badaniu tarczycy, zalecane jest wprowadzanie lewotyroksyny stopniowo, zaczynając od 25% wielkości zwykłej dawki, zwiększając ją o 25% co dwa tygodnie, aż do czasu uzyskania optymalnej stabilizacji. Stopniowe wprowadzanie leczenia jest również zalecane u zwierząt cierpiących na inne schorzenia współistniejące, w szczególności choroby serca, cukrzycę i niewydolność nerek lub wątroby.
Specjalne środki ostrożności dla osób podających produkt leczniczy weterynaryjny zwierzętom Produkt zawiera lewotyroksynę sodową w wysokim stężeniu i może być szkodliwy po połknięciu, w szczególności dla dzieci. Kobiety w ciąży powinny ostrożnie obchodzić się z tym produktem.
Niezużyte części tabletek należy umieścić z powrotem w otwartym blistrze, który należy następnie włożyć do opakowania zewnętrznego przechowywać poza zasięgiem dzieci; należy je zawsze zużyć przy kolejnym podaniu.
W razie przypadkowego połknięcia, należy niezwłocznie zwrócić się o pomoc lekarską oraz pokazać lekarzowi ulotkę informacyjną lub etykietę.
Po podaniu tabletek należy umyć ręce.
Początkowo może wystąpić zaostrzenie objawów skórnych, z nasilonym świądem spowodowanym złuszczaniem starych komórek naskórka.
Bezpieczeństwo produktu leczniczego weterynaryjnego stosowanego u ciężarnych i karmiących suk nie zostało ustalone, z tego względu stosowanie produktu u tych zwierząt powinno być oparte na ocenie bilansu korzyści/ryzyka dokonanej przez prowadzącego lekarza weterynarii. Należy jednak pamiętać, że lewotyroksyna jest substancją endogenną, a hormony tarczycy mają kluczowe znaczenie dla rozwoju płodu, szczególnie w początkowym okresie ciąży. Niedoczynność tarczycy w czasie ciąży może prowadzić do ciężkich powikłań takich jak śmierć płodów i zwiększenie śmiertelności okołoporodowej. W czasie ciąży dawka podtrzymująca lewotyroksyny sodowej może wymagać dostosowania. Z tego względu ciężarne suki powinny być regularnie monitorowane od zapłodnienia aż do kilku tygodni po porodzie.
Szereg leków może zaburzać wiązanie hormonów tarczycy w osoczu i w tkankach lub modyfikować ich metabolizm (np.: barbiturany, leki zobojętniające sok żołądkowy, sterydy anaboliczne, diazepam, furosemid, mitotan, fenylobutazon, fenytoina, propranolol, wysokie dawki salicylanów
i sulfonamidów). Należy wziąć pod uwagę ich właściwości podczas leczenia zwierząt otrzymujących jednocześnie inne leki.
Estrogeny mogą zwiększać zapotrzebowanie na hormony tarczycy.
Ketamina może wywoływać częstoskurcz i nadciśnienie u pacjentów otrzymujących hormony tarczycy.
Lewotyroksyna nasila działanie katecholamin i sympatykomimetyków.
Zwiększenie dawki naparstnicy może być konieczne u pacjentów z wyrównaną wcześniej zastoinową niewydolnością serca, u których uzupełniane są niedobory hormonów tarczycy. Po leczeniu niedoczynności tarczycy u pacjentów ze współistniejącą cukrzycą zalecane jest ścisłe monitorowanie kontroli cukrzycy.
U większości pacjentów leczonych długotrwale wysokimi dziennymi dawkami glikokortykosteroidów stężenia T4 w surowicy będą bardzo niskie lub niewykrywalne, wartości T3 będą również poniżej normy.
Podanie doustne.
Zalecana dawka początkowa dla psów wynosi 20 μg lewotyroksyny sodowej na kg masy ciała dziennie, podawane w pojedynczej dawce lub w dwóch równych dawkach podzielonych.
Z uwagi na różnice w szybkości wchłaniania i metabolizmie konieczna może być modyfikacja dawki w celu uzyskania pełnej odpowiedzi klinicznej. Dawka początkowa i częstotliwość podawania są jedynie punktem wyjścia. Leczenie powinno być wysoce zindywidualizowane i dostosowane
do wymagań konkretnego zwierzęcia, szczególnie u małych psów, na podstawie obserwacji prowadzonej przez lekarza weterynarii.
U psów obecność pożywienia może wpływać na wchłanianie lewotyroksyny sodowej. Z tego względu godziny podawania leku i ich odniesienie do pory karmienia powinny być codziennie takie same.
Informacja dla prowadzącego lekarza weterynarii
W przypadku małych psów zaleca się stosowanie tabletek o mniejszej mocy 200 μg przy rozpoczynaniu leczenia oraz przy późniejszym dostosowywaniu dawki, ponieważ umożliwia to dokładniejsze dawkowanie i dostosowanie dawki.
Monitorowanie terapeutyczne
Dawka powinna być dostosowana na podstawie odpowiedzi klinicznej i poziomu tyroksyny w osoczu.
W celu odpowiedniego monitorowania terapii można wykonać pomiary stężenia T4 w osoczu
w najniższym punkcie krzywej (tuż przed podaniem) oraz wartości szczytowych (około czterech godzin po podaniu). U zwierząt przyjmujących odpowiednią dawkę szczytowe stężenie T4 w osoczu powinno znajdować się w górnym zakresie normy (około 30–47 nmol/l), a stężenie minimalne powinno przekraczać około 19 nmol/l. Jeżeli poziomy T4 znajdują się poza tym zakresem, dawka lewotyroksyny może być zmieniana z przyrostem od 50 do 200 μg, aż do uzyskania u pacjenta klinicznie prawidłowej czynności tarczycy oraz poziomu T4 w osoczu mieszczącego się w zakresie wartości referencyjnych. Stężenie T4 w osoczu można ponownie zmierzyć dwa tygodnie po zmianie dawki, jednak równie ważnym czynnikiem w indywidualnym wyznaczaniu dawki jest poprawa kliniczna, która może nastąpić dopiero po upływie czterech do ośmiu tygodni. Po zoptymalizowaniu dawki, monitorowanie kliniczne i biochemiczne można przeprowadzać co 6–12 miesięcy.
W celu zapewnienia dokładnego dawkowania tabletki można podzielić na 2 lub 4 równe części. Należy położyć tabletkę na płaskiej powierzchni, stroną z oznaczeniem skierowaną do góry, a stroną wypukłą (zaokrągloną) do powierzchni.
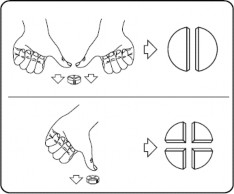
Połówki: nacisnąć kciukami po obu stronach tabletki. Ćwiartki: nacisnąć kciukiem środek tabletki.
Po podaniu zbyt wysokiej dawki może wystąpić tyreotoksykoza. Tyreotoksykoza jako efekt uboczny umiarkowanie zwiększonej suplementacji rzadko występuje u psów, ponieważ ten gatunek wykazuje zdolność do katabolizowania i wydalania hormonów tarczycy. Po przypadkowym połknięciu większej ilości produktu leczniczego weterynaryjnego można ograniczyć szybkość wchłaniania poprzez wywołanie wymiotów i jednorazowe, doustne podanie węgla aktywowanego i siarczanu magnezu.
W przypadku ostrego przedawkowania u psów objawy kliniczne stanowią rozwinięcie fizjologicznych skutków działania hormonu. Ostre przedawkowanie lewotyroksyny może spowodować wymioty, biegunkę, hiperaktywność, nadciśnienie, osowiałość, tachykardię, zwiększoną częstość oddechów, duszność oraz nieprawidłową reakcję źrenic na światło.
Po długotrwałej, nadmiernej suplementacji u psów teoretycznie mogą wystąpić objawy kliniczne nadczynności tarczycy, takie jak: nadmierne pragnienie, wielomocz, dyszenie, utrata masy ciała bez anoreksji, a także tachykardia i(lub) nerwowość. W razie stwierdzenia tych objawów należy zbadać stężenie T4 w surowicy, w celu potwierdzenia rozpoznania i natychmiast przerwać suplementację. Po ustąpieniu objawów (co może potrwać dni lub tygodnie), ponownym ustaleniu dawki hormonów tarczycy i po pełnym wyzdrowieniu zwierzęcia można wznowić podawanie w niższej dawce, ze ścisłym monitorowaniem zwierzęcia.
Nie dotyczy.
Grupa farmakoterapeutyczna: hormony tarczycy Kod ATCvet: QH03AA01
Lewotyroksyna jest syntetycznym homologiem naturalnie występującego hormonu, tyroksyny (T4). Jest przekształcana w bardziej aktywną biologicznie trijodotyroninę (T3). T3 wiąże się ze swoistymi receptorami błony plazmatycznej, mitochondriów i chromatyny, co powoduje zmiany w transkrypcji DNA i syntezie białek. Z tego powodu rozpoczęcie działania jest powolne.
Lewotyroksyna sodowa wpływa na metabolizm węglowodanów, białek, tłuszczów, witamin, kwasów nukleinowych i jonów. Stymuluje zużycie tlenu i powoduje zwiększenie aktywności metabolicznej poprzez zwiększenie liczby mitochondriów. Następuje stymulacja syntezy białek i zwiększenie zużycia węglowodanów. Pobudzany jest metabolizm tłuszczów.
Po przyjęciu doustnym wchłanianie z przewodu pokarmowego wynosi od 10 do 50% u psów; Cmax jest osiągane w ciągu 4–12 godzin po podaniu u psów. Po podaniu 20 mikrogramów substancji czynnej na kg 57 psom z niedoczynnością tarczycy, poziom tyroksyny (T4) w osoczu w większości przypadków wzrósł do wartości prawidłowych (20–46 nmol). Po wchłonięciu do krwiobiegu T4 ulega odjodowaniu do T3 w tkankach obwodowych. U psów ponad 50% tyroksyny wytwarzanej każdego dnia jest wydalane z kałem. Okres półtrwania w surowicy u zdrowych psów wynosi od 10 do
16 godzin. U psów z niedoczynnością tarczycy jest on dłuższy.
Wapnia wodorofosforan dwuwodny Magnezu stearynian
Celuloza mikrokrystaliczna Kroskarmeloza sodowa Aromat drożdży
Nie dotyczy.
Okres ważności produktu leczniczego weterynaryjnego zapakowanego do sprzedaży: 2 lata Okres ważności podzielonych tabletek: 4 dni
6.4. Specjalne środki ostrożności podczas przechowywania
Nie przechowywać w temperaturze powyżej 30°C.
Części podzielonych tabletek należy umieścić z powrotem w blistrze i zawsze zużyć przy kolejnym podaniu.
Blister z aluminium – PVC / PE / PVDC, każdy zawierający 10 lub 25 tabletek. Wielkości opakowań:
Pudełko tekturowe zawierające 50 tabletek.
Pudełko tekturowe zawierające 100 tabletek. Pudełko tekturowe zawierające 250 tabletek.
Niektóre wielkości opakowań mogą nie być dostępne w obrocie.
Niewykorzystany produkt leczniczy weterynaryjny lub jego odpady należy usunąć w sposób zgodny z obowiązującymi przepisami.
LIVISTO Int’l, S.L.
Av. Universitat Autònoma, 29
08290 Cerdanyola del Vallès (Barcelona) Hiszpania
3125/21
Data wydania pierwszego pozwolenia na dopuszczenie do obrotu: 16/08/2021
01/2022
ZAKAZ WYTWARZANIA, IMPORTU, POSIADANIA, SPRZEDAŻY, DOSTAWY I/LUB STOSOWANIA
Nie dotyczy.










