Spis treści:
Ulotka dołączona do opakowania: informacja dla rodziców i opiekunów
Curosurf, 80 mg/ml, zawiesina do stosowania dotchawiczego i dooskrzelowego
(Poractant alfa)
Frakcja fosfolipidów z płuc świni
Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać.
W razie jakichkolwiek wątpliwości należy zwrócić się do lekarza.
Jeśli u pacjenta wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione w tej ulotce, należy powiedzieć o tym lekarzowi lub pielęgniarce. Patrz punkt 3.
Spis treści ulotki:
Dawkowanie:
infekcja
krwawienie do mózgu
powietrze w klatce piersiowej spowodowane uszkodzeniem płuc
spowolnienie czynności serca
niskie ciśnienie krwi
przewlekła choroba płuc
zmniejszona ilość tlenu w organizmie
zwiększona ilość tlenu w organizmie
niebieskie zabarwienie skóry lub dziąseł spowodowane niedoborem tlenu
zatrzymanie oddychania
powikłania w następstwie umieszczenia rurek w płucach
obniżenie aktywności mózgowej
Podczas podawania leku Curosurf przez cienki cewnik były raportowane niektóre łagodne i krótkotrwałe działania niepożądane: bradykardia, bezdech, zmniejszenie wysycenia krwi tlenem, piana na ustach, kaszel, dławienie się i kichanie.
Zgłaszanie działań niepożądanych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione w ulotce, należy powiedzieć o tym lekarzowi, farmaceucie lub pielęgniarce.
Działania niepożądane można zgłaszać bezpośrednio do Departamentu Monitorowania Niepożądanych Działań Produktów Leczniczych Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych, Al. Jerozolimskie 181C, 02-222 Warszawa,
tel.: + 48 22 49 21 301, faks: + 48 22 49 21 309, e-mail: ndl@urpl.gov.pl.
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Dzięki zgłaszaniu działań niepożądanych można będzie zgromadzić więcej informacji na temat bezpieczeństwa stosowania leku.
4. JAK PRZECHOWYWAĆ LEK CUROSURF
Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Przechowywać w lodówce w temperaturze od 2°C do 8°C, przechowywać w oryginalnym opakowaniu w celu ochrony przed światłem. Przed podaniem dziecku, należy podgrzać do temperatury pokojowej.
Nie otwarte i nie użyte fiolki produktu Curosurf, które zostały ogrzane do temperatury pokojowej, w ciągu 24 godzin można umieścić z powrotem w lodówce w celu późniejszego użycia. Leku nie należy ogrzewać do temperatury pokojowej i umieszczać w lodówce więcej niż jeden raz.
Nie stosować tego leku po upływie terminu ważności zamieszczonego na pudełku i fiolce. Termin ważności oznacza ostatni dzień podanego miesiąca.
Jeden pojemnik należy wykorzystać raz, a pozostałości wyrzucić. Szpital powinien zapewnić bezpieczne usunięcie niewykorzystanych pozostałości Curosurf.
Leków nie należy wyrzucać do kanalizacji. Należy zapytać farmaceutę, jak usunąć leki, których się już nie używa. Takie postępowanie pomoże chronić środowisko
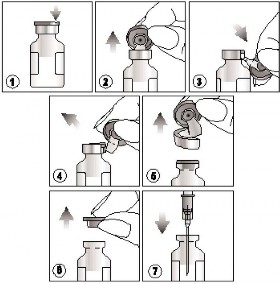
Odnaleźć nacięcie znajdujące się na kolorowym, plastikowym kapslu,
Unieść kapsel w miejscu nacięcia i pociągnąć go do góry,
Pociągnąć w dół plastikową część kapsla razem z jego częścią aluminiową,
i 5) Usunąć cały kapsel ściągając aluminiowy pierścień
Lekarz dobiera odpowiednią dawkę leku, w zależności od masy ciała dziecka. Jeżeli dziecku podaje się Curosurf, aby zapobiec wystąpieniu RDS, lek należy podać w ciągu 15 minut po urodzeniu. Jeżeli dziecku podaje się Curosurf w celu leczenia RDS, lek należy podać jak najszybciej po zdiagnozowaniu schorzenia. Jeżeli dziecko potrzebuje dodatkowej dawki leku Curosurf, podaje się ją 12 godzin po podaniu pierwszej dawki. W razie konieczności, po kolejnych 12 godzinach można podać trzecią dawkę.
Stosowanie leku Curosurf u wcześniaków z niewydolnością wątroby lub nerek nie było badane.
Sposób podawania leku:
Curosurf podawany jest dziecku w inkubatorze przez lekarza lub pielęgniarkę. Lek zostanie podgrzany do temperatury pokojowej, a następnie podany przy pomocy strzykawki poprzez rurkę intubacyjną do tchawicy dziecka. W tym celu niezbędne może być odłączenie dziecka na kilka minut od respiratora.
Może zostać również zastosowana metoda mniej inwazyjnego podania surfaktantu przez cienki cewnik (LISA – ang. Less Invasive Surfactant Administration).
Curosurf zawiera sód
Lek zawiera mniej niż 1 mmol (23 mg) sodu w jednej fiolce, to znaczy lek uznaje się za „wolny od sodu“.
3. MOŻLIWE DZIAŁANIA NIEPOŻĄDANE
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią.Możliwe działania niepożądane zostały wymienione poniżej w zależności od częstości występowania:
W przypadku wątpliwości dotyczących działań niepożądanych, należy skontaktować się z lekarzem.
Niezbyt często (występują u mniej niż 1 na 100
pacjentów):
Rzadko (występują u mniej niż 1 na 1000
pacjentów):
Ponadto zgłoszono następujące działania niepożądane:
5. ZAWARTOŚĆ OPAKOWANIA I INNE INFORMACJE
Co zawiera lek Curosurf
- Substancją czynną jest mieszanina lipidów i protein otrzymywanych z pęcherzyków płucnych świni.
- Pozostałe składniki to: sodu chlorek, woda do wstrzykiwań, wodorowęglan sodu (do regulacji pH).
Jak wygląda lek Curosurf i co zawiera opakowanie
Lek Curosurf jest to sterylna zawiesina. Jest on dostępny w jednorazowych szklanych fiolkach o pojemności 5 ml, zawierających 1,5 ml (120 mg) lub
3 ml (240 mg) frakcji fosfolipidów pochodzących z pęcherzyków płucnych świni. Każdy ml sterylnej zawiesiny zawiera 80 mg frakcji fosfolipidów z pęcherzyków płucnych świni. W jednym opakowaniu znajdują się 2 fiolki po 1,5 ml zawiesiny lub 1 fiolka po 3 ml zawiesiny leku Curosurf.
Nie wszystkie wielkości opakowań muszą znajdować się w obrocie.
Podmiot odpowiedzialny:
Chiesi Farmaceutici S.p.A, Via Palermo 26/A, 43 122 Parma, Włochy.
Wytwórca:
Chiesi Farmaceutici S.p.A, Via San Leonardo 96 - Via Palermo 26/A, 43 122 Parma, Włochy. Chiesi Pharmaceuticals GmbH, Gonzagagasse 16/16, A-1010 Wiedeń, Austria.
W celu uzyskania bardziej szczegółowych informacji, należy zwrócić się do przedstawiciela podmiotu odpowiedzialnego w Polsce:
Chiesi Poland Sp. z o.o., Al. Jerozolimskie 134, 02-305 Warszawa tel.: (22) 620 14 21, faks: (22) 652 37 79, e-mail: info-pl@chiesi.com

Data ostatniej aktualizacji ulotki:

Prosimy przeczytać informację na odwrocie ulotki
Jak pobrać produkt?
6) i 7) Zdjąć gumowy korek przed pobraniem zawartości fiolki.
Do jednorazowego użytku. Niewykorzystaną zawiesinę, jaka pozostała w fiolce, należy wyrzucić. Nie przechowywać niewykorzystanej zawiesiny do ponownego stosowania.
Wszelkie resztki niewykorzystanego produktu lub jego odpady należy usunąć w sposób zgodny z przepisami.