Spis treści:
- Co to jest lek Duosol nie zawierający potasu i w jakim celu się go stosuje
- Informacje ważne przed zastosowaniem leku Duosol nie zawierającego potasu Leku Duosol nie zawierającego potasu nie należy stosować, jeżeli:
- Jak stosować lek Duosol nie zawierający potasu
- Możliwe działania niepożądane
- Jak przechowywać lek Duosol nie zawierający potasu
- Zawartość opakowania i inne informacje Co zawiera lek Duosol nie zawierający potasu
Ulotka dołączona do opakowania: informacja dla pacjenta Duosol nie zawierający potasu, roztwór do hemofiltracji
Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta
Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać.
W razie jakichkolwiek wątpliwości należy zwrócić się do lekarza lub farmaceuty.
Jeśli u pacjenta wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione w tej ulotce, należy powiedzieć o tym lekarzowi lub farmaceucie. Patrz punkt 4.
Spis treści ulotki
Co to jest lek Duosol nie zawierający potasu i w jakim celu się go stosuje
Duosol nie zawierający potasu to roztwór do hemofiltracji. Lek ten jest przeznaczony do stosowania u pacjentów z ostrą niewydolnością nerek, u których nerki nie są w stanie usuwać z krwi produktów przemiany materii. Proces hemofiltracji ciągłej polega na usuwaniu z organizmu produktów przemiany materii, które w normalnych warunkach są wydalane przez nerki. Roztwór wyrównuje równowagę płynów i zapewnia uzupełnienie utraconych soli (elektrolitów).
Informacje ważne przed zastosowaniem leku Duosol nie zawierającego potasu Leku Duosol nie zawierającego potasu nie należy stosować, jeżeli:
u pacjenta występuje nieprawidłowo niskie stężenie potasu we krwi (hipokaliemia);
u pacjenta występuje niskie stężenie kwasów we krwi (zasadowica metaboliczna).
Zabieg hemofiltracji nie powinien być stosowany w następujących przypadkach:
niewydolność nerek w połączeniu z bardzo intensywnymi procesami metabolicznymi (hiperkatabolizm); w takim przypadku nagromadzonych produktów przemiany materii nie można przez dłuższy czas usuwać poprzez hemofiltrację;
niewystarczający przepływ krwi z dostępu żylnego;
wszelkie stany, w których występuje podwyższone ryzyko krwotoku, ponieważ pacjent otrzymuje leki zapobiegające tworzeniu się skrzepów (antykoagulacja układowa).
Ostrzeżenia i środki ostrożności
Przed rozpoczęciem stosowania leku Duosol nie zawierającego potasu należy omówić to z lekarzem lub farmaceutą.
Przed i w trakcie hemofiltracji należy monitorować ciśnienie krwi, równowagę płynów, równowagę soli (elektrolitów), równowagę kwasowo-zasadową oraz czynność nerek. Należy regularnie sprawdzać stężenie cukru oraz fosforanów we krwi.
Przed i w trakcie hemofiltracji należy poza tym monitorować stężenie potasu we krwi.
Lek Duosol nie zawierający potasu a inne leki
Należy powiedzieć lekarzowi lub farmaceucie o wszystkich lekach przyjmowanych przez pacjenta obecnie lub ostatnio, a także o lekach, które pacjent planuje przyjmować.
Stężenie innych leków we krwi może ulec zmniejszeniu w trakcie hemofiltracji i lekarz weźmie to pod uwagę.
Poprzez stosowanie odpowiednich dawek roztworu do hemofiltracji i dokładny monitoring można uniknąć wystąpienia interakcji z innymi lekami.
Uwzględnione będą następujące interakcje:
Infuzje podawane w ramach intensywnej opieki medycznej mogą zmienić skład krwi i stan płynów pacjenta.
Toksyczne działania niektórych leków stosowanych w leczeniu osłabienia serca (leki zawierające naparstnicę) mogą nie być widoczne, gdy stężenie potasu lub magnezu jest zbyt wysokie lub stężenie wapnia jest zbyt niskie. Jeśli stężenia te są korygowane przez hemofiltrację, mogą wówczas wystąpić działania toksyczne i spowodować na przykład zaburzenia rytmu serca. Jeśli u pacjenta występuje niskie stężenie potasu lub wysokie stężenie wapnia we krwi, wówczas naparstnica może mieć działanie toksyczne w dawkach niższych niż zwykle stosowane w leczeniu.
Podawanie witaminy D i leków zawierających wapń może zwiększyć ryzyko zbyt wysokiego stężenia wapnia we krwi (hiperkalcemii).
Dodatkowe stosowanie wodorowęglanu sodu może zwiększyć ryzyko nieprawidłowo niskiego stężenia kwasów we krwi (zasadowicy metabolicznej).
Ciąża, karmienie piersią i wpływ na płodność
Jeśli pacjentka jest w ciąży lub karmi piersią, przypuszcza że może być w ciąży, lub gdy planuje mieć dziecko, powinna poradzić się lekarza lub farmaceuty przed otrzymaniem tego leku.
Brak danych dotyczących stosowania roztworów do hemofiltracji u kobiet w okresie ciąży. Ponieważ jednak wszystkie składniki tego leku są substancjami występującymi naturalnie, które tylko zastępują te same substancje utracone z organizmu podczas hemofiltracji, nie należy spodziewać się żadnych zagrożeń dla dziecka w czasie ciąży i karmienia piersią i nie należy spodziewać się żadnego wpływu na płodność.
Prowadzenie pojazdów i obsługiwanie maszyn
Lek ten jest zwykle podawany pacjentom unieruchomionym w szpitalu/na oddziale dializy. Wyklucza to prowadzenie pojazdów i obsługiwanie maszyn.
Jak stosować lek Duosol nie zawierający potasu
Możliwe działania niepożądane
Jak przechowywać lek Duosol nie zawierający potasu
Zawartość opakowania i inne informacje Co zawiera lek Duosol nie zawierający potasu
Lek ten będzie podawany pacjentowi tylko pod nadzorem lekarza z doświadczeniem w technikach hemofiltracji.
Lekarz zadecyduje o odpowiedniej dawce dla pacjenta, biorąc pod uwagę stan kliniczny, masę ciała i warunki metaboliczne. O ile nie zalecono inaczej, u pacjentów wszystkich grup wiekowych zaleca się szybkość filtracji 20-25 ml/kg masy ciała na godzinę, aby zapewnić eliminację tych substancji, które normalnie są wydalane z moczem.
Pacjentowi podawany jest gotowy do użycia roztwór do hemofiltracji przez rurki aparatu do hemofiltracji (tzw. obieg pozaustrojowy) za pomocą pompy infuzyjnej.
Leczenie ostrej niewydolności nerek prowadzone jest przez ograniczony okres czasu i kończy się w momencie przywrócenia czynności nerek.
Zastosowanie większej niż zalecana dawki leku Duosol nie zawierającego potasu
Po podawaniu zalecanych dawek tego leku nie odnotowano przypadków zagrażających życiu. W razie
potrzeby, podawanie można w każdej chwili przerwać.
Niewłaściwe równoważenie ilości płynów może prowadzić do obecności zbyt dużej lub zbyt małej ilości wody w organizmie (przewodnienie lub odwodnienie). Stany te objawiają się zmianami ciśnienia krwi lub szybkości tętna.
Do przedawkowania wodorowęglanu może dojść, gdy podawana jest zbyt duża ilość roztworu do hemofiltracji. Może to prowadzić do nieprawidłowo niskiego stężenia kwasów we krwi (zasadowicy metabolicznej), mniejszej ilości wapnia rozpuszczonego we krwi (zmniejszenia stężenia zjonizowanego wapnia) albo skurczy mięśni (tężyczki).
Przedawkowanie może powodować zastoinową niewydolność serca i (lub) zastój krwi w płucach oraz może powodować zmiany równowagi soli (elektrolitów) i równowagi kwasowo-zasadowej.
Lekarz zdecyduje o odpowiednim leczeniu.
W razie jakichkolwiek dalszych wątpliwości związanych ze stosowaniem tego leku należy zwrócić się do lekarza lub farmaceuty.
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią. Nie odnotowano dotychczas żadnych działań niepożądanych związanych ze stosowaniem tego leku,
możliwe są jednak następujące działania niepożądane. Częstość występowania tych działań niepożądanych jest nieznana (nie może być określona na podstawie dostępnych danych):
Nadmiar lub niedobór wody w organizmie (przewodnienie lub odwodnienie), nieprawidłowe stężenie soli (elektrolitów), niskie stężenie fosforanu we krwi (hipofosfatemia), wysokie stężenie cukru we krwi (hiperglikemia), nieprawidłowo niskie stężenie kwasów we krwi (zasadowica metaboliczna), zbyt wysokie lub niskie ciśnienie krwi (nadciśnienie, niedociśnienie), nudności, wymioty i skurcze mięśni.
Zgłaszanie działań niepożądanych
Po dopuszczeniu produktu leczniczego do obrotu istotne jest zgłaszanie podejrzewanych działań niepożądanych. Umożliwia to nieprzerwane monitorowanie stosunku korzyści do ryzyka stosowania produktu leczniczego. Osoby należące do fachowego personelu medycznego powinny zgłaszać wszelkie podejrzewane działania niepożądane za pośrednictwem Departamentu Monitorowania Niepożądanych Działań Produktów Leczniczych Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych
i Produktów Biobójczych, Al. Jerozolimskie 181C, 02-222 Warszawa Tel.: + 48 22 49 21 301
Faks: + 48 22 49 21 309
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Dzięki zgłaszaniu działań niepożądanych można będzie zgromadzić więcej informacji na temat bezpieczeństwa stosowania tego leku.
Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Nie należy stosować tego leku po upływie terminu ważności zamieszczonego na worku i pudełku po:
„Termin ważności”. Termin ważności oznacza ostatni dzień podanego miesiąca.
Warunki przechowywania
Nie przechowywać w temperaturze powyżej 25°C. Nie przechowywać w lodówce ani nie zamrażać.
Warunki przechowywania po przygotowaniu roztworu gotowego do użycia
Zmieszany produkt powinien być wykorzystany natychmiast. Produkt po zmieszaniu zachowuje stabilność fizyczną i chemiczną przez 24 godziny w temperaturze 25°C.
Substancje czynne: | Mniejsza komora Roztwór elektrolitów | Większa komora Roztwór wodorowęglanu | ||
555 ml zawiera | na 1000 ml | 4445 ml zawiera | na 1000 ml | |
sodu chlorek | 2,34 g | 4,21 g | 27,47 g | 6,18 g |
wapnia chlorek dwuwodny | 1,10 g | 1,98 g | — | — |
magnezu chlorek sześciowodny | 0,51 g | 0,91 g | — | — |
glukoza jednowodna co odpowiada glukozie bezwodnej | 5,49 g 5,0 g | 9,90 g 9,0 g | — | — |
sodu wodorowęglan | — | — | 15,96 g | 3,59 g |
Elektrolity: | [mmol/ komorę] | [mmol/l] | [mmol/ komorę] | [mmol/l] |
Na+ | 40,0 | 72 | 660 | 149 |
Ca2+ | 7,5 | 13,5 | — | — |
Mg2+ | 2,5 | 4,5 | — | — |
Cl | 75,0 | 135 | 470 | 106 |
HCO3 | — | — | 190 | 42.8 |
teoretyczna osmolarność [mOsm/l] | 275 | 297 | ||
Skład gotowego do użycia roztworu do hemofiltracji po zmieszaniu:
1000 ml gotowego do użycia roztworu do hemofiltracji zawiera [mmol/l]: Na+ 140
Ca++ 1,5
Mg++ 0,5
Cl- 109
HCO3- 35,0
glukoza bezwodna 5,6 (co odp. 1,0 g)
Teoretyczna osmolarność [mOsm/l] 292
pH 7,0–8,0
Pozostałe składniki to:
Roztwór elektrolitów (mniejsza komora)
kwas solny 25% (do ustalania pH), woda do wstrzykiwań
Roztwór wodorowęglanu (większa komora)
dwutlenek węgla (do ustalania pH), woda do wstrzykiwań
Jak wygląda lek Duosol nie zawierający potasu i co zawiera opakowanie
Roztwór do hemofiltracji
Przezroczysty i bezbarwny roztwór, pozbawiony widocznych cząstek
Lek ten jest dostarczany w worku dwukomorowym. Poprzez zmieszanie obu roztworów po otwarciu przegrody pomiędzy komorami otrzymuje się gotowy do użycia roztwór do hemofiltracji.
2 worki po 5000 ml (worki dwukomorowe, 4445 ml i 555 ml) w tekturowym pudełku
Podmiot odpowiedzialny i wytwórca
B. Braun Avitum AG Schwarzenberger Weg 73-79 34212 Melsungen
Niemcy
Ten produkt leczniczy jest dopuszczony do obrotu w krajach członkowskich Europejskiego Obszaru Gospodarczego pod następującymi nazwami:
Czechy: Duosol bez kalia
Estonia: Duosol ilma kaaliumita, hemofiltratsioonilahus
Finlandia: Duosol sine Kalium hemofiltraationeste
Włochy: Duosol senza potassio soluzione per emofiltrazione
Łotwa: Duosol bez kālija šķīdums hemofiltrācijai
Litwa: Duosol K 0 hemofiltracijos tirpalas Niemcy, Luksemburg: Duosol ohne Kalium Hämofiltrationslösung Polska: Duosol nie zawierający potasu
Słowenia: Duosol brez kalija raztopina za hemofiltracijo
Hiszpania: Priosol sin Potasio solución para hemofiltración
Holandia: Duosol zonder Kalium, oplossing voor hemofiltratie Wielka Brytania: Duosol without Potassium solution for haemofiltration
Data ostatniej aktualizacji ulotki: 20.06.2019
Informacje przeznaczone wyłącznie dla fachowego personelu medycznego:
Instrukcja przygotowania gotowego do użycia roztworu do hemofiltracji
Przed użyciem należy poddać pojemnik i roztwór kontroli wzrokowej. Roztwór do hemofiltracji wolno stosować tylko wtedy, gdy pojemnik (zewnętrzne opakowanie ochronne oraz worek dwukomorowy), przegroda pomiędzy komorami oraz złącza są nieuszkodzone i nienaruszone, a roztwór jest przezroczysty, bezbarwny oraz pozbawiony widocznych cząstek.
Zewnętrzne opakowanie ochronne zdjąć bezpośrednio przed użyciem.
1
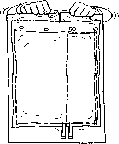
Zdjąć zewnętrzne opakowanie ochronne.
2.
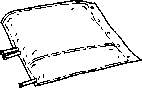
Rozprostować worek i położyć go na czystej, płaskiej powierzchni.
3.
Nacisnąć mniejszą komorę worka obiema dłońmi, w taki sposób, aby w pełni otworzyła się przegroda pomiędzy komorami na jej całej długości.
4.
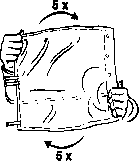
Zapewnić dokładne wymieszanie zawartości, obracając worek pięciokrotnie w obie strony.

Podawanie gotowego do użycia roztworu do hemofiltracji
Roztwór do hemofiltracji należy ogrzewać w przybliżeniu do temperatury ciała przy pomocy zintegrowanego lub zewnętrznego podgrzewacza. W żadnym wypadku nie wolno podawać roztworu, jeśli jest poniżej temperatury pokojowej.
Podczas stosowania tego produktu leczniczego zaobserwowano w rzadkich przypadkach wytrącanie białego osadu węglanu wapnia w przewodach, szczególnie w pobliżu pompy i urządzenia grzewczego. Dlatego podczas hemofiltracji należy ściśle kontrolować wizualnie roztwór w przewodach infuzyjnych co 30 minut w celu zapewnienia, że roztwór znajdujący się w przewodach jest przezroczysty i wolny od wytrąceń.
Wytrącenia mogą wystąpić również ze znacznym opóźnieniem po rozpoczęciu leczenia. Jeśli zauważy się wytrącenia, należy natychmiast wymienić roztwór i przewody infuzyjne oraz dokładnie monitorować pacjenta.
Do jednorazowego użytku. Niewykorzystaną zawartość roztworu i wszelkie uszkodzone pojemniki należy wyrzucić.











