Spis treści:
- NAZWA PRODUKTU LECZNICZEGO
- SKŁAD JAKOŚCIOWY I ILOŚCIOWY
- POSTAĆ FARMACEUTYCZNA
- SZCZEGÓŁOWE DANE KLINICZNE
- WŁAŚCIWOŚCI FARMAKOLOGICZNE
- DANE FARMACEUTYCZNE
- PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU
- NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
- DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU / DATA PRZEDŁUŻENIA POZWOLENIA
- DATA ZATWIERDZENIA LUB CZĘŚCIOWEJ ZMIANY TEKSTU CHARAKTERYSTYKI PRODUKTU LECZNICZEGO
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
NAZWA PRODUKTU LECZNICZEGO
SKŁAD JAKOŚCIOWY I ILOŚCIOWY
POSTAĆ FARMACEUTYCZNA
SZCZEGÓŁOWE DANE KLINICZNE
Wskazania do stosowania
Dawkowanie i sposób podawania
Przeciwwskazania
Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania
Interakcje z innymi produktami leczniczymi i inne rodzaje interakcji
Wpływ na płodność, ciążę i laktację
Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn
Działania niepożądane
Przedawkowanie
WŁAŚCIWOŚCI FARMAKOLOGICZNE
Właściwości farmakodynamiczne
Właściwości farmakokinetyczne
Przedkliniczne dane o bezpieczeństwie
DANE FARMACEUTYCZNE
Wykaz substancji pomocniczych
Niezgodności farmaceutyczne
Okres ważności
Specjalne środki ostrożności podczas przechowywania
Rodzaj i zawartość opakowania
Specjalne środki ostrożności dotyczące usuwania
PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU
NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU / DATA PRZEDŁUŻENIA POZWOLENIA
DATA ZATWIERDZENIA LUB CZĘŚCIOWEJ ZMIANY TEKSTU CHARAKTERYSTYKI PRODUKTU LECZNICZEGO
Hedelix, 40 mg/5 ml, syrop
100 ml syropu zawiera 0,8 g wyciągu gęstego z Hedera helix L., folium (liść bluszczu pospolitego)
(2,2 – 2,9:1); rozpuszczalnik ekstrakcyjny: etanol 96% (V/V); glikol propylenowy; woda (45:2:53) m/m/m.
Substancja pomocnicza o znanym działaniu: sorbitol (E 420) Produkt leczniczy nie zawiera etanolu (alkohol)
Pełny wykaz substancji pomocniczych, patrz punkt 6.1.
Syrop
Hedelix jest klarownym, żółtawo-brązowym roztworem.
Produkt leczniczy roślinny stosowany jako lek wykrztuśny w produktywnym (tzw. mokrym) kaszlu.
Dawkowanie:
O ile lekarz nie zaleci inaczej, zalecane jest następujące dawkowanie:
Młodzież, dorośli i osoby w podeszłym wieku:
5 ml 3 razy na dobę.
Dzieci w wieku 6-11 lat:
2,5 ml 4 razy na dobę.
Dzieci w wieku 2-5 lat:
2,5 ml 3 razy na dobę.
Stosowanie u dzieci w wieku poniżej 2 lat jest przeciwwskazane (patrz: pkt. 4.3 Przeciwwskazania). Czas stosowania
Jeśli w czasie stosowania tego leku objawy utrzymują się dłużej niż tydzień, należy skonsultować się z lekarzem lub farmaceutą.
Sposób podawania:
Podanie doustne
W celu umożliwienia dokładnego dawkowania do produktu leczniczego dołączono łyżeczkę polipropylenową lub strzykawkę dozującą.
Instrukcja użycia strzykawki dozującej:
Dokładna podziałka konieczna do odmierzania odpowiedniej dawki jest wydrukowana na strzykawce dozującej
1. 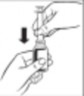 2.
2. 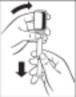 3.
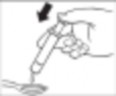
3. 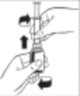 4.
4. 

Nadwrażliwość na substancję czynną, rośliny z rodziny araliowatych (Araliaceae) lub jakikolwiek składnik produktu wymieniony w pkt. 6.1..
Stosowanie u dzieci w wieku poniżej 2 lat z powodu ryzyka nasilenia objawów ze strony układu oddechowego.
Nie należy stosować leku u osób z zaburzeniami syntezy bursztynianu argininy (choroba metaboliczna cyklu mocznikowego). [W pojedynczym przypadku u pięcioletniego dziecka z przypuszczalnym zaburzeniem syntezy bursztynianu argininy obserwowano powtórne wywołanie epizodu objawów, związanego czasowo ze stosowaniem identycznego produktu leczniczego.]
Utrzymujący się lub nawracający kaszel u dzieci w wieku od 2 do 4 lat wymaga zdiagnozowania przed zastosowaniem leku.
Jeśli pojawi się duszność, gorączka lub ropna plwocina należy skonsultować się z lekarzem lub farmaceutą.
Jednoczesne stosowanie z opiatowymi środkami przeciwkaszlowymi, takimi jak kodeina lub dekstrometorfan nie jest zalecane bez kontroli medycznej.
Zalecana jest ostrożność u pacjentów z nieżytem żołądka lub wrzodem żołądka.
Lek w 5 ml zawiera 1,75 g sorbitolu (co odpowiada 0,44 g fruktozy) i stanowi około 0,15 jednostek węglowodanowych.
Nie należy stosować u pacjentów z rzadką wrodzoną nietolerancją fruktozy.
Ze względu na zawartość wyciągu roślinnego, syrop Hedelix może tworzyć osad w butelce. Osad może powodować zmętnienie roztworu, a smak może ulegać niewielkim zmianom.
Nie zgłaszano.
Nie ustalono bezpieczeństwa stosowania w okresie ciąży i laktacji. Ze względu na brak wystarczających danych stosowanie w okresie ciąży i laktacji nie jest zalecane.
Nie przeprowadzono badań dotyczących wpływu na zdolność prowadzenia pojazdów i obsługiwania maszyn.
Do określenia częstości występowania działań niepożądanych przyjęto następującą klasyfikację MedDRA: bardzo często (1/10);
często (1/100 do <1/10);
niezbyt często (1/1 000 do <1/100); rzadko (1/10 000 do <1/1 000); bardzo rzadko (<1/10 000);
częstość nieznana (nie może być określona na podstawie dostępnych danych).
Zaburzenia układu immunologicznego:
Częstość nieznana: reakcje alergiczne (pokrzywka, wysypka skórna, duszność).
Zaburzenia żołądka i jelit:
Częstość nieznana: zaburzenia żołądkowo-jelitowe (nudności, wymioty, biegunka).
Jeśli wystąpią inne działania niepożądane niż wymienione powyżej należy skontaktować się z lekarzem lub farmaceutą.
Zgłaszanie podejrzewanych działań niepożądanych
Po dopuszczeniu produktu leczniczego do obrotu istotne jest zgłaszanie podejrzewanych działań
niepożądanych. Umożliwia to nieprzerwane monitorowanie stosunku korzyści do ryzyka stosowania produktu leczniczego. Osoby należące do fachowego personelu medycznego powinny zgłaszać wszelkie podejrzewane działania niepożądane za pośrednictwem:
Departamentu Monitorowania Niepożądanych Działań Produktów Leczniczych Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych
i Produktów Biobójczych, Al. Jerozolimskie 181C, 02-222 Warszawa Tel: + 48 22 49 21 301
Fax: + 48 22 49 21 309
Strona internetowa: https://smz.ezdrowie.gov.pl
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Przedawkowanie może powodować nudności, wymioty, biegunkę i pobudzenie. Należy zastosować leczenie objawowe i wspomagające.
Opisano jeden przypadek dziecka w wieku 4 lat, u którego wystąpiła biegunka i agresja po przypadkowym zażyciu wyciągu z bluszczu w ilości odpowiadającej 1,8 g substancji roślinnej, co odpowiada około 88 ml syropu Hedelix.
Grupa farmakoterapeutyczna: leki wykrztuśne, (Hederae helicis folium)
Kod ATC: R05CA12
Mechanizm działania nie jest znany.
Brak danych.
Test Amesa dla substancji czynnej produktu leczniczego Hedelix nie wykazał potencjalnej mutagenności. Brak danych na temat genotoksyczności, rakotwórczości i toksycznego wpływu na rozród preparatów z liści bluszczu pospolitego.
Makrogologlicerolu hydroksystearynian, olejek anyżowy, hydroksyetyloceluloza, sorbitol (roztwór 70%) (E 420), glikol propylenowy, glicerol, woda oczyszczona.
Nie dotyczy.
3 lata.
Okres ważności po pierwszym otwarciu: 6 miesięcy
Nie stosować po upływie terminu ważności.
Przechowywać w miejscu niewidocznym i niedostępnym dla dzieci. Przechowywać w temperaturze poniżej 25° C.
Butelka z barwnego szkła z łyżeczką polipropylenową w tekturowym pudełku lub butelka ze szkła
brązowego z łącznikiem z PE i zakrętką PP z wkładką uszczelniającą PET i pierścieniem gwarancyjnym PE wraz ze strzykawką dozującą z PP/PE w tekturowym pudełku.
100 ml
200 ml
Brak specjalnych wymagań.
Fortis Pharmaceuticals Sp. z o. o. ul. Mickiewicza 29,
40-085 Katowice Polska
R/3676
Data wydania pierwszego pozwolenia na dopuszczenie do obrotu: 21 czerwiec 1995 Data ostatniego przedłużenia pozwolenia: 07 sierpień 2014











