Spis treści:
- NAZWA PRODUKTU LECZNICZEGO
- SKŁAD JAKOŚCIOWY I ILOŚCIOWY
- POSTAĆ FARMACEUTYCZNA
- SZCZEGÓŁOWE DANE KLINICZNE
- WŁAŚCIWOŚCI FARMAKOLOGICZNE
- DANE FARMACEUTYCZNE
- PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU
- NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
- DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU I DATA PRZEDŁUŻENIA POZWOLENIA
- DATA ZATWIERDZENIA LUB CZĘŚCIOWEJ ZMIANY TEKSTU CHARAKTERYSTYKI PRODUKTU LECZNICZEGO
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
NAZWA PRODUKTU LECZNICZEGO
SKŁAD JAKOŚCIOWY I ILOŚCIOWY
POSTAĆ FARMACEUTYCZNA
SZCZEGÓŁOWE DANE KLINICZNE
Wskazania do stosowania
Dawkowanie i sposób podawania
Jeśli implant podskórny nie zostanie założony zgodnie z instrukcjami oraz zostanie założony w niewłaściwym dniu, może to doprowadzić do niezamierzonej ciąży (patrz punkt 4.2 Jak zakładać Implanon NXT oraz Kiedy zakładać Implanon NXT).
Implant podskórny założony głębiej niż podskórnie (głębokie założenie) może być niewyczuwalny palpacyjnie, co może utrudnić jego lokalizację i (lub) usunięcie (patrz punkt 4.2 W jaki sposób usunąć Implanon NXT” oraz punkt 4.4).
Iniekcja: implant podskórny należy założyć w dniu, w którym wypada następna iniekcja.
Tabletka zawierająca tylko progestagen: pacjentka może przejść z tabletki zawierającej tylko progestagen na stosowanie implantu podskórnego Implanon NXT w dowolnym dniu miesiąca. Implant podskórny powinien być założony w ciągu 24 godzin od przyjęcia ostatniej tabletki.
Implant podskórny i (lub) system terapeutyczny domaciczny uwalniający progestagen (IUS): należy założyć implant podskórny w tym samym dniu, w którym poprzedni implant podskórny lub IUS jest usuwany.
Jeśli implant podskórny został założony w sposób zalecany, nie jest konieczne stosowanie dodatkowych metod antykoncepcji. Jeśli termin założenia implantu podskórnego odbiega
od zalecanego, należy doradzić kobiecie stosowanie przez 7 dni po założeniu implantu podskórnego metody barierowej. Jeśli miał miejsce stosunek płciowy, należy upewnić się, że pacjentka nie jest
w ciąży.
Po aborcji lub poronieniu
W pierwszym trymestrze ciąży: implant podskórny powinien być założony w ciągu pierwszych 5 dni po poronieniu lub aborcji w pierwszym trymestrze ciąży.
W drugim trymestrze ciąży: implant podskórny należy zakładać w 21. do 28. dnia po poronieniu w drugim trymestrze ciąży.
Jeśli implant podskórny został założony w sposób zalecany, nie jest konieczne stosowanie dodatkowych metod antykoncepcji. Jeśli termin założenia implantu podskórnego odbiega
od zalecanego, należy doradzić kobiecie stosowanie przez 7 dni po założeniu implantu podskórnego metody barierowej. Jeśli miał miejsce stosunek płciowy, należy upewnić się, że pacjentka nie jest
w ciąży.
Po porodzie
Kobiety nie karmiące piersią: implant podskórny należy zakładać w 21. do 28. dnia po porodzie. Jeśli implant podskórny został założony w sposób zalecany, nie jest konieczne stosowanie dodatkowych metod antykoncepcji. Jeśli implant podskórny został założony później niż 28 dni po porodzie, należy doradzić kobiecie stosowanie przez 7 dni po założeniu implantu podskórnego metody barierowej. Jeśli miał miejsce stosunek płciowy, należy upewnić się, że pacjentka nie jest w ciąży.
Karmienie piersią: implant podskórny należy założyć cztery tygodnie po porodzie (patrz punkt 4.6). Należy doradzić kobiecie stosowanie metody barierowej przez 7 dni po założeniu
implantu podskórnego. Jeśli miał miejsce stosunek płciowy, należy upewnić się, że pacjentka nie jest w ciąży.
Jak zakładać Implanon NXT
Aby zapewnić skuteczne działanie oraz niepowikłane usunięcie implantu podskórnego Implanon NXT, konieczne jest prawidłowe i ostrożne jego podskórne założenie w ramię ręki niedominującej, zgodnie z instrukcją. Fachowy personel medyczny oraz pacjentka powinni móc sprawdzić obecność implantu podskórnego palpacyjnie po jego wprowadzeniu.
Implant podskórny należy umieścić podskórnie bezpośrednio pod skórę po wewnętrznej stronie górnej części ramienia ręki niedominującej.
Implant podskórny założony głębiej niż podskórnie (głębokie założenie) może być niewyczuwalny palpacyjnie, co może utrudnić jego lokalizację i (lub) usunięcie (patrz punkt
Procedura zakładania implantu podskórnego
Aby upewnić się, że implant podskórny został założony bezpośrednio pod skórę, fachowy personel medyczny powinien ustawić się w taki sposób, aby widział przesuwanie się wprowadzanej igły obserwując aplikator z boku, a nie znad ramienia. Obserwowane z boku miejsce założenia oraz ruchy igły bezpośrednio pod skórą będą wyraźnie widoczne.
W celach poglądowych na rycinach przedstawiono wewnętrzną stronę lewego ramienia.
Należy położyć pacjentkę na plecach z odwróconym na zewnątrz ramieniem ręki niedominującej, zgiętej w łokciu tak, aby jej ręka była pod głową (lub w pozycji najbliższej temu położeniu) (Rycina 1).
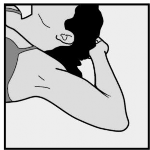
Rycina 1
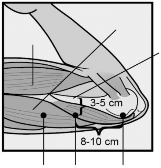
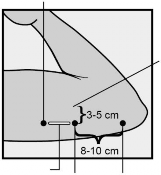
Zidentyfikować miejsce założenia implantu podskórnego znajdujące się po wewnętrznej stronie górnej części ramienia ręki niedominującej. Miejsce założenia znajduje się nad mięśniem trójgłowym ramienia w odległości około 8-10 cm od nadkłykcia przyśrodkowego kości ramiennej i 3-5 cm do tyłu (poniżej) od bruzdy (rowka) między mięśniem dwugłowym (bicepsem)
a mięśniem trójgłowym ramienia (tricepsem) (Ryciny 2a, 2b oraz 2c). Takie umiejscowienie pozwala ominąć duże naczynia krwionośne i nerwy leżące w obrębie bruzdy. Jeśli założenie implantu podskórnego w tym miejscu jest niemożliwe (np. u kobiet ze szczupłymi ramionami), należy go umieścić możliwie jak najdalej do tyłu od bruzdy.
Zaznaczyć markerem chirurgicznym dwa oznaczenia: pierwsze oznaczenie, to miejsce, gdzie implant podskórny zostanie wprowadzony, drugie, znajduje się 5 centymetrów dalej od pierwszego oznaczenia (w kierunku barku) (Ryciny 2a i 2b). Drugie oznaczenie (znak wskazujący) będzie wyznaczało kierunek wprowadzenia implantu podskórnego podczas zakładania.
Miejsce
Znak wskazujący
Bruzda
Biceps
Triceps
Bruzda
P D P D
Znak
Miejsce
Nadkłykcie
założenia Miejsce
Nadkłykcie
wskazujący
wprowadzenia przyśrodkowe
implantu wprowadzenia przyśrodkowe podskórnego implantu
podskórnego
implantu podskórnego
Rycina 2a Rycina 2b
P, proksymalnie (w kierunku barku); D, dystalnie (w kierunku łokcia)
pośrodkowy
Żyła odłokciowa
ramienny
Biceps
Obszar bruzdy
Kość ramienna
Nerw łokciowy
Implant
Nerw Mięsień
Okolica boczna
Okolica przyśrodkowa
podskórny po wprowadzeniu
Triceps
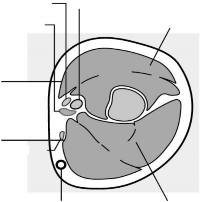
Rycina 2c
Przekrój górnej części lewego ramienia, widok od strony łokcia Okolica przyśrodkowa (wewnętrzna) ramienia
Okolica boczna (zewnętrzna) ramienia
Po zaznaczeniu ramienia, należy potwierdzić prawidłowe położenie miejsca założenia po wewnętrznej części ramienia.
Przemyć skórę środkiem dezynfekującym od miejsca wprowadzenia implantu podskórnego do znaku wskazującego.
Podać znieczulenie (np. przy pomocy znieczulenia w sprayu lub wstrzyknąć 2 ml 1% roztworu lidokainy bezpośrednio pod skórę, wzdłuż „kanału wprowadzania implantu podskórnego”).
Wyjąć z blistra sterylny jednorazowy aplikator, zawierający Implanon NXT. Przed użyciem należy wizualnie sprawdzić, czy nie doszło do naruszenia opakowania (np. rozerwania, przebicia). Jeżeli opakowanie ma widoczne uszkodzenie, które mogło wpłynąć na sterylność, nie należy stosować aplikatora.
Przytrzymać aplikator tuż przy igle, w miejscu gdzie jego powierzchnia jest chropowata. Usunąć osłonkę z igły zsuwając ją poziomo z igły w kierunku wskazanym strzałką (Rycina 3). Jeśli osłonki z igły nie można łatwo usunąć, nie należy stosować aplikatora. Należy sprawdzić wzrokowo obecność implantu podskórnego, który powinien być widoczny w postaci białego pręcika w zakończeniu igły. Nie dotykać fioletowego suwaka dopóki igła nie zostanie w pełni
wprowadzona pod skórę, ponieważ doprowadziłoby to do cofnięcia się igły a tym samym do przedwczesnego wypadnięcia implantu podskórnego z aplikatora.
Jeśli fioletowy suwak zostanie przedwcześnie zwolniony, należy zacząć procedurę od nowa, używając nowego aplikatora.
Fioletowy suwak
(Nie należy jeszcze dotykać)
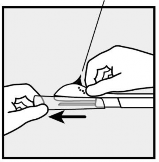
Rycina 3
Wolną ręką, należy naciągnąć skórę wokół miejsca założenia implantu podskórnego w kierunku łokcia (Rycina 4).
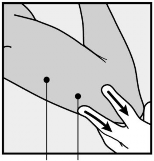
P D
Znak wskazujący Miejsce założenia
implantu podskórnego
Rycina 4
Implant podskórny należy założyć podskórnie bezpośrednio pod skórę (patrz punkt 4.4). Aby upewnić się, że implant podskórny został założony bezpośrednio pod skórę, należy ustawić się w taki sposób, aby móc widzieć przesuwanie się wprowadzanej igły obserwując aplikator z boku, a nie znad ramienia. Miejsce założenia oraz ruchy igły tuż pod skórą można wyraźnie zobaczyć patrząc z boku (patrz Rycina 6).
Wprowadzić pod niewielkim kątem (mniejszym niż 30) samą końcówkę igły (Rycina 5a).
Wprowadzić sam czubek igły (ukośnie ścięty otwór w końcówce) tuż pod skórę (ale nie dalej) (Rycina 5b). Jeśli igła zostanie wkłuta głębiej, należy ją wycofać, tak, aby pod skórą znajdował się tylko jej czubek.

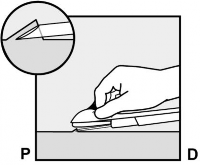
Rycina 5a Rycina 5b
Opuścić aplikator do pozycji niemal poziomej. Aby ułatwić umieszczenie implantu podskórnego pod skórą, należy unieść skórę przy pomocy igły, wprowadzając delikatnie igłę na całą jej długość (Rycina 6). Może pojawić się niewielki opór, ale nie należy stosować siły. Jeśli igła nie zostanie wprowadzona na całą jej długość, implant podskórny nie będzie poprawnie założony.
Jeśli końcówka igły wyjdzie ze skóry zanim igła zostanie wprowadzona w całości, należy ją wycofać i skorygować jej położenie pod skórą, aby dokończyć procedurę zakładania implantu.
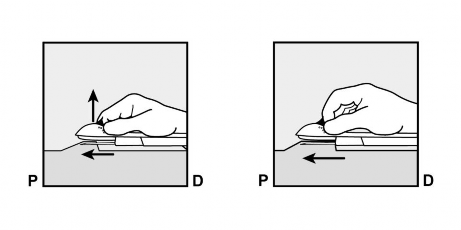
Rycina 6 Rycina 7
Trzymać aplikator równolegle do powierzchni skóry i wprowadzić igłę na całą jej długość (Rycina 7). W razie potrzeby można ustabilizować aplikator wolną ręką.
W celu odblokowania fioletowego suwaka należy go delikatnie przesunąć w dół (Rycina 8a). Przesunąć suwak w tył do jego zatrzymania.
Nie należy ruszać (
 ) aplikatorem w czasie przesuwania fioletowego suwaka (Rycina 8b). Teraz implant podskórny znajduje się pod skórą, a igła jest zablokowana wewnątrz aplikatora.
) aplikatorem w czasie przesuwania fioletowego suwaka (Rycina 8b). Teraz implant podskórny znajduje się pod skórą, a igła jest zablokowana wewnątrz aplikatora.Aplikator można teraz usunąć (Rycina 8c).
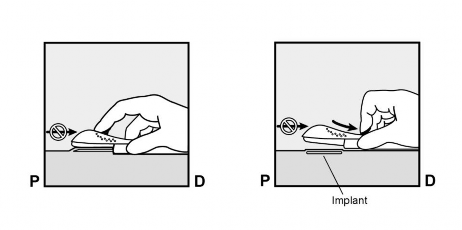
Rycina 8a Rycina 8b

Rycina 8c
Jeśli aplikator podczas całego zabiegu nie jest trzymany w tej samej pozycji lub jeśli fioletowy suwak nie zostanie przesunięty w tył do oporu, implant podskórny nie będzie prawidłowo założony i może wystawać z miejsca założenia.
Jeśli implant podskórny wystaje z miejsca założenia, należy go usunąć i przeprowadzić nową procedurę w tym samym miejscu, używając nowego aplikatora. Nie wolno wpychać wystającego implantu podskórnego z powrotem w nacięcie.
Nałożyć mały przylegający bandaż w miejscu założenia implantu podskórnego.
Zawsze należy sprawdzić obecność implantu podskórnego palpacyjnie natychmiast po jego wprowadzeniu. Powinniśmy być w stanie zlokalizować palpacyjnie oba końce 4 cm implantu podskórnego (Rycina 9). Patrz punkt poniżej „Jeśli po założeniu nie można wyczuć implantu podskórnego palpacyjnie”.
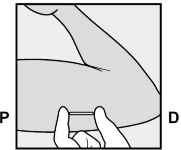
Rycina 9
Należy poinformować pacjentkę, aby sprawdzała palpacyjnie obecność implantu podskórnego.
Nałożyć sterylny gazik oraz opatrunek uciskowy, aby nie dopuścić do powstania zasinienia
w miejscu wprowadzenia implantu podskórnego. Pacjentka może usunąć opatrunek uciskowy po 24 godzinach, natomiast przylegający gazik po 3-5 dniach od założenia implantu podskórnego.
Należy wypełnić Kartę Ostrzeżeń dla Pacjenta i przekazać ją pacjentce. Należy również wypełnić naklejkę i dołączyć ją do karty pacjentki. Jeśli stosowane są elektroniczne karty pacjenta, informacja z naklejki również powinna być w nich zawarta.
Aplikator jest przeznaczony do jednorazowego użycia i należy go zutylizować w odpowiedni sposób, zgodnie z lokalnymi przepisami, dotyczącymi obchodzenia się z odpadami niebezpiecznymi dla środowiska.
Jeśli po założeniu nie można wyczuć implantu podskórnego palpacyjnie:
W przypadku, gdy implantu podskórnego nie można wyczuć palpacyjnie lub istnieją wątpliwości, czy został założony może to oznaczać, że implant podskórny nie został założony lub został umieszczony głęboko:
Należy sprawdzić aplikator. Igła powinna być całkowicie cofnięta, a jedynie fioletowe zakończenie obturatora powinno być widoczne.
Należy zastosować inne metody w celu potwierdzenia obecności implantu podskórnego. Ponieważ implant podskórny nie przepuszcza promieni rentgenowskich odpowiednie metody lokalizowania to dwuwymiarowe prześwietlenie rentgenowskie oraz tomografia komputerowa (ang. CT scan, Computerized Tomography). Można wykorzystać ultrasonografię (ang. USS, Ultrasound Scanning) z zastosowaniem głowicy liniowej o dużej częstotliwości (10 MHz lub większej) lub rezonans magnetyczny (ang. MRI, Magnetic Resonance Imaging). Jeśli nie można wyczuć implantu podskórnego wykorzystując powyższe metody obrazowania, należy zmierzyć stężenie etonogestrelu we krwi pacjentki. W takim przypadku należy zwrócić się
do podmiotu odpowiedzialnego, który dostarczy stosowną instrukcję postępowania (protokół).
Do czasu potwierdzenia obecności implantu podskórnego Implanon NXT, pacjentka musi stosować niehormonalną metodę antykoncepcji.
Implanty podskórne umieszczone głęboko należy zlokalizować i usunąć jak najszybciej, aby uniknąć możliwości przemieszczenia się ich w odległe miejsce (patrz punkt 4.4).
W jaki sposób usunąć Implanon NXT
Implant podskórny może usunąć w warunkach aseptycznych wyłącznie fachowy personel medyczny, który dobrze zna tę technikę usuwania. Osoby nieobeznane z techniką usuwania implantu podskórnego powinny zwrócić się do podmiotu odpowiedzialnego w celu uzyskania dodatkowych informacji.
Przed rozpoczęciem procedury usuwania implantu podskórnego, fachowy personel medyczny powinien ocenić umiejscowienie implantu podskórnego. Implant podskórny należy zlokalizować w ramieniu palpacyjnie.
Jeśli implant podskórny jest niewyczuwalny palpacyjnie, należy sprawdzić w Karcie Ostrzeżeń dla Pacjenta lub w dokumentacji medycznej, w którym ramieniu znajduje się implant podskórny. Jeśli nie da się wyczuć implantu podskórnego, mógł zostać umiejscowiony głęboko lub przemieścić się. Należy mieć wzgląd na to, że implant podskórny może leżeć w pobliżu naczyń krwionośnych i nerwów.
Niewyczuwalne palpacyjnie implanty podskórne może usunąć wyłącznie fachowy personel medyczny, który ma doświadczenie w usuwaniu głęboko położonych implantów podskórnych i dobrze zna metody lokalizowania implantu podskórnego oraz budowę anatomiczną ramienia. Należy zwrócić się do podmiotu odpowiedzialnego w celu uzyskania dodatkowych informacji.
Jeśli implant podskórny jest niewyczuwalny palpacyjnie, patrz punkt poniżej „Lokalizacja i usuwanie niewyczuwalnego palpacyjnie implantu podskórnego”.
Procedura dotycząca usuwania implantu podskórnego wyczuwalnego palpacyjnie
W celach poglądowych na rycinach przedstawiono wewnętrzną stronę lewego ramienia.
Należy ułożyć pacjentkę na plecach na stole. Ramię należy ułożyć zgięte w łokciu z dłonią ułożoną pod głową (lub w pozycji najbliższej temu położeniu) (Patrz Rycina 10).
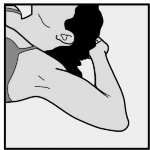
Rycina 10
Zlokalizować implant podskórny palpacyjnie. Popchnąć w dół koniec implantu podskórnego znajdujący się najbliżej barku (Rycina 11), aby go ustabilizować; powinno pojawić się wybrzuszenie wskazujące końcówkę implantu podskórnego położoną najbliżej łokcia. Jeśli końcówka nie uniesie się w górę, usunięcie implantu podskórnego może być trudne
i procedurę powinien przeprowadzić fachowy personel medyczny mający doświadczenie w usuwaniu implantów podskórnych położonych głębiej. Należy zwrócić się do podmiotu odpowiedzialnego w celu uzyskania dodatkowych informacji.
Zaznaczyć np. markerem chirurgicznym dalszy koniec (koniec znajdujący się bliżej łokcia).
Oczyścić miejsce roztworem antyseptycznym.
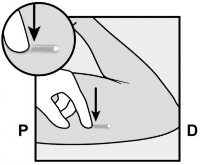
Rycina 11
P, proksymalnie (w kierunku barku); D, dystalnie (w kierunku łokcia)
Znieczulić miejsce planowanego nacięcia, np. podając 0,5 do 1 ml 1% roztworu lidokainy (Rycina 12). Podać środek znieczulający pod implant podskórny, aby implant podskórny znajdował się blisko powierzchni skóry. Wstrzyknięcie środka do miejscowego znieczulenia nad implantem podskórnym może utrudnić jego usunięcie.
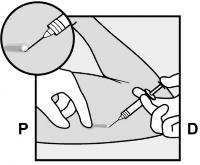
Rycina 12
Należy pchnąć koniec implantu podskórnego znajdujący się najbliżej barku (Rycina 13) w dół, aby go ustabilizować w czasie całego zabiegu. Rozpoczynając od miejsca leżącego nad końcem implantu podskórnego położonego najbliżej łokcia, wykonać podłużne nacięcie (równolegle do implantu podskórnego) o długości 2 mm w kierunku łokcia. Uważać, aby nie naciąć końca implantu podskórnego.
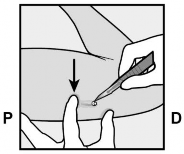
Rycina 13
Koniec implantu podskórnego powinien wyłonić się z nacięcia. Jeśli się nie pojawi, delikatnie pchnąć implant podskórny w kierunku miejsca nacięcia, aż jego koniec będzie widoczny. Uchwycić implant podskórny kleszczykami i wyciągnąć go, jeśli to możliwe (Rycina 14).
W razie potrzeby delikatnie usunąć tkanki, które przywarły do końcówki implantu podskórnego, oddzielając je na tępo. Jeśli po oddzieleniu tkanek końcówka implantu podskórnego nie zostanie odsłonięta, naciąć otoczkę z tkanek, a następnie wyjąć implant podskórny kleszczykami (Ryciny 15 i 16).
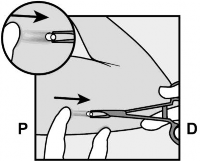
Rycina 14
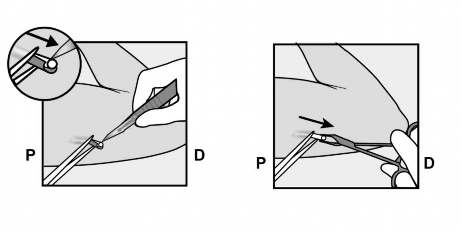
Rycina 15 Rycina 16
Jeśli implant podskórny nie jest widoczny w miejscu nacięcia, należy delikatnie wprowadzić kleszczyki (najlepiej zakrzywione kleszczyki naczyniowe Halsteada z końcami skierowanymi ku górze) powierzchownie w miejscu nacięcia (Rycina 17).
Należy delikatnie uchwycić implant podskórny, a następnie przełożyć kleszczyki do drugiej ręki (Rycina 18).
Za pomocą innych kleszczyków starannie rozdzielić tkankę otaczającą implant podskórny (Rycina 19). Wówczas implant podskórny można usunąć.
Jeżeli nie można uchwycić implantu podskórnego, należy przerwać zabieg i skierować pacjentkę do lekarza mającego doświadczenie w wykonywaniu skomplikowanych zabiegów usunięcia implantu podskórnego lub zwrócić się do podmiotu odpowiedzialnego.
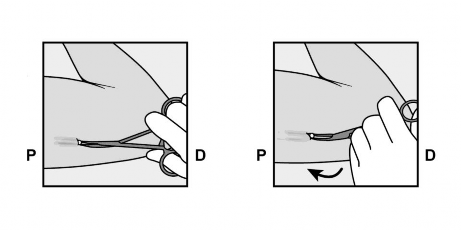
Rycina 17 Rycina 18
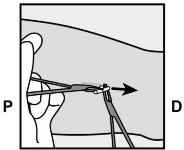
Rycina 19
Potwierdzić, że cały implant podskórny o długości 4 cm został usunięty mierząc jego długość. Zgłaszano przypadki złamań implantu podskórnego znajdującego się w ramieniu pacjentki. W niektórych przypadkach zgłaszano trudności z usunięciem złamanego implantu podskórnego. W przypadku usunięcia części implantu podskórnego (mniej niż 4 cm), pozostały fragment należy usunąć, postępując zgodnie z instrukcją podaną w tym punkcie.
Jeśli pacjentka chciałaby kontynuować stosowanie implantu Implanon NXT, nowy implant podskórny można wprowadzić bezpośrednio po usunięciu poprzedniego używając tego samego nacięcia pod warunkiem, że miejsce nacięcia jest prawidłowo położone (patrz punkt 4.2 Jak wymieniać Implanon NXT).
Po usunięciu implantu podskórnego, zamknąć miejsce nacięcia jałowymi plastrami do zamykania ran. Nałożyć sterylny gazik oraz opatrunek uciskowy, aby nie dopuścić do powstania zasinienia. Pacjentka może usunąć opatrunek uciskowy po 24 godzinach natomiast jałowe plastry do zamykania ran po 3-5 dniach od założenia implantu podskórnego.
Lokalizacja i usuwanie niewyczuwalnego palpacyjnie implantu podskórnego
W rzadkich przypadkach zgłaszano przemieszczenie implantu podskórnego; zwykle jest to niewielkie przemieszczenie w stosunku do miejsca pierwotnej lokalizacji (patrz także punkt 4.4), ale może spowodować, że wykrycie pierwotnego umiejscowienia implantu metodą palpacyjną będzie niemożliwe. Implant podskórny, który został umieszczony głęboko lub przemieścił się, może nie być wyczuwalny metodą palpacyjną i dlatego, jak opisano poniżej w celu jego zlokalizowania konieczne może być wykorzystanie technik obrazowych.
Przed próbą usunięcia implantu podskórnego niewyczuwalnego palpacyjnie zawsze należy najpierw go zlokalizować. Ponieważ implant podskórny nie przepuszcza promieni rentgenowskich, odpowiednie metody jego lokalizowania to dwuwymiarowe prześwietlenie rentgenowskie oraz tomografia komputerowa (CT). Można wykorzystać ultrasonografię (USS) z zastosowaniem głowicy
liniowej o dużej częstotliwości (10 MHz lub większej) lub rezonans magnetyczny (MRI). Po zlokalizowaniu implantu podskórnego w ramieniu, powinien go usunąć fachowy personel medyczny, który ma doświadczenie w usuwaniu głęboko położonych implantów podskórnych i dobrze zna budowę anatomiczną ramienia. Należy rozważyć wykorzystanie ultrasonografu w czasie wykonywania zabiegu usunięcia implantu podskórnego.
Jeśli po wielu próbach implantu podskórnego nie uda się zlokalizować w ramieniu, należy rozważyć zastosowanie metod obrazowych klatki piersiowej, ponieważ w wyjątkowo rzadkich przypadkach zgłaszano przemieszczenie implantu podskórnego do naczyń płucnych. Jeśli implant podskórny zostanie zlokalizowany w klatce piersiowej, w celu jego usunięcia konieczne może być przeprowadzenie zabiegu operacyjnego lub zastosowanie metod wewnątrznaczyniowych; należy skonsultować się z fachowym personelem medycznym, zaznajomionym z anatomią klatki piersiowej.
Jeśli w jakimkolwiek momencie te metody obrazowania zawiodą, w celu zlokalizowania implantu podskórnego można zmierzyć stężenie etonogestrelu we krwi. Należy skontaktować się z podmiotem odpowiedzialnym w celu uzyskania dalszych wskazówek.
Jeśli implant przemieścił się w obrębie ramienia, usunięcie może wymagać drobnego zabiegu chirurgicznego z większym nacięciem lub zabiegu chirurgicznego w sali operacyjnej. Procedura usunięcia implantu podskórnego założonego głęboko powinna być przeprowadzona ostrożnie, aby uniknąć uszkodzenia struktury nerwu lub naczyń krwionośnych w ramieniu.
Niewyczuwalne palpacyjnie i głęboko umieszczone implanty podskórne powinien usuwać fachowy personel medyczny, który dobrze zna budowę anatomiczną ramienia i procedury usuwania głęboko położonych implantów podskórnych.
Zdecydowanie nie zaleca się przeprowadzania zwiadowczego zabiegu chirurgicznego bez wcześniejszego ustalenia lokalizacji implantu podskórnego.
Należy skontaktować się z podmiotem odpowiedzialnym w celu otrzymania dalszych wskazówek.
Jak wymieniać Implanon NXT
Po usunięciu poprzedniego implantu podskórnego nowy może być założony od razu, jak to opisano w punkcie 4.2 Jak zakładać Implanon NXT.
Nowy implant podskórny można założyć w to samo ramię i często poprzez to samo nacięcie, przez które był usuwany poprzedni implant podskórny, pod warunkiem że miejsce nacięcia jest prawidłowo położone, tj. znajduje się w odległości 8-10 cm od nadkłykcia przyśrodkowego kości ramiennej,
3-5 cm do tyłu (poniżej) od bruzdy (rowka) (patrz punkt 4.2 „Jak zakładać Implanon NXT”). Jeśli wykorzystywane będzie to samo nacięcie, należy znieczulić miejsce zakładania implantu podskórnego poprzez wstrzyknięcie leku znieczulającego (np. 2 ml 1% roztworu lidokainy) bezpośrednio pod skórę, blisko nacięcia wzdłuż „kanału wprowadzenia implantu podskórnego” oraz przestrzegać instrukcji.
Przeciwwskazania
Implanon NXT, 68 mg, implant podskórny
Implanon NXT to nieprzepuszczający promieni rentgenowskich, nie ulegający biodegradacji, zawierający jedynie progestagen giętki pręcik znajdujący się w sterylnym, gotowym do jednorazowego użycia, aplikatorze.
Każdy nieprzepuszczający promieni rentgenowskich implant podskórny zawiera 68 mg etonogestrelu
(Etonogestrelum); współczynnik uwalniania wynosi od 60 do 70 µg/dobę w tygodniu 5. do 6.
i zmniejsza się do około 35 do 45 µg/dobę pod koniec pierwszego roku, a następnie do około 30 do 40 µg/dobę pod koniec drugiego roku i do około 25 do 30 µg/dobę pod koniec trzeciego roku.
Aplikator zaprojektowano tak, aby można go było używać jedną ręką oraz w celu ułatwienia poprawnego podskórnego podawania implantu.
Pełny wykaz substancji pomocniczych, patrz punkt 6.1.
Implant podskórny.
Nieprzepuszczający promieni rentgenowskich, nie ulegający biodegradacji biały lub prawie biały, miękki, giętki pręcik o długości 4 cm i średnicy 2 mm.
Antykoncepcja.
Bezpieczeństwo i skuteczność stosowania produktu leczniczego określono u kobiet w wieku 18 – 40 lat.
Dawkowanie
1 implant, zakładany podskórnie, mogący pozostawać pod skórą przez 3 lata.
Dzieci i młodzież
Nie określono bezpieczeństwa stosowania ani skuteczności implantu podskórnego Implanon NXT u młodzieży w wieku poniżej 18 lat.
Sposób podawania
Przed zastosowaniem implantu podskórnego Implanon NXT należy upewnić się, że pacjentka nie jest w ciąży.
Zdecydowanie zaleca się, aby implant podskórny Implanon NXT był zakładany i usuwany wyłącznie przez fachowy personel medyczny (ang. HCPs, Healthcare Professionals), który ukończył szkolenie dotyczące stosowania aplikatora implantu podskórnego Implanon NXT oraz technik jego zakładania i usuwania, a także, aby implant był zakładany lub usuwany
pod odpowiednim nadzorem.
Przed założeniem implantu należy starannie przeczytać instrukcję zakładania i usuwania implantu podskórnego w punkcie 4.2 Jak zakładać Implanon NXT oraz Jak usuwać Implanon NXT.
Filmy instruktażowe przedstawiające sposób zakładania i usuwania implantu podskórnego są dostępne na stronie internetowej www.implanonnxtvideos.eu. W razie jakichkolwiek pytań prosimy zwrócić się do podmiotu odpowiedzialnego, firmy Organon Polska Sp. z o.o., nr telefonu: + 48 22 105 50 01.
W przypadku wątpliwości dotyczących czynności niezbędnych do bezpiecznego założenia i (lub) usunięcia implantu podskórnego Implanon NXT nie należy podejmować prób założenia i (lub) usunięcia implantu.
Jak stosować Implanon NXT
Implanon NXT jest środkiem antykoncepcyjnym o długim czasie działania. Implant zakłada się podskórnie i może pozostawać pod skórą przez 3 lata. Implant podskórny należy usunąć nie później niż po upływie 3 lat od daty założenia implantu podskórnego. Należy poinformować pacjentkę,
że może ona w każdej chwili poprosić o usunięcie implantu podskórnego Implanon NXT. Fachowy personel medyczny zaznajomiony z techniką przeprowadzania takiego zabiegu może rozważyć wcześniejsze usunięcie implantu podskórnego u kobiet z większą masą ciała (patrz punkt 4.4).
Niezwłoczne założenie następnego implantu podskórnego po usunięciu poprzedniego zapewnia stałą ochronę antykoncepcyjną. Jeśli pacjentka zrezygnuje ze stosowania implantu podskórnego Implanon NXT i wciąż chce mieć zapewnioną ochronę antykoncepcyjną, należy zalecić jej inne metody antykoncepcyjne.
Opakowanie implantu podskórnego Implanon NXT zawiera przeznaczoną dla pacjentki Kartę Ostrzeżeń dla Pacjenta, w której należy zapisać numer serii implantu podskórnego. Fachowy personel medyczny umieszcza w Karcie Ostrzeżeń dla Pacjenta datę założenia implantu podskórnego, w które ramię implant podskórny został założony oraz zaplanowaną datę jego usunięcia.
Należy poinformować pacjentki, aby Kartę Ostrzeżeń dla Pacjenta przechowywały w bezpiecznym miejscu i pokazywały ją podczas każdej wizyty związanej ze stosowaniem implantu podskórnego. Karta Ostrzeżeń dla Pacjenta zawiera również instrukcje dla pacjentki, aby od czasu do czasu delikatnie dotykała implantu podskórnego, tak aby upewnić się, że pacjentka wyczuwa jego lokalizację. Należy poinformować pacjentki, aby jak najszybciej skontaktowały się z lekarzem, jeśli
w dowolnym momencie nie mogą wyczuć implantu podskórnego. W opakowaniu znajduje się również naklejka przeznaczona dla fachowego personelu medycznego, służąca do zanotowania numeru serii.
Informacje te powinny zostać uwzględnione w elektronicznej dokumentacji medycznej pacjenta, jeżeli jest wykorzystywana.
Podstawę do pomyślnego stosowania, a później również usunięcia implantu podskórnego Implanon NXT stanowi prawidłowe i ostrożne umieszczenie implantu podskórnego pod skórą, zgodnie z instrukcjami.
Implant podskórny Implanon NXT powinien być założony podskórnie BEZPOŚREDNIO POD SKÓRĘ w wewnętrzną stronę ramienia ręki niedominującej. Miejsce założenia znajduje się nad
mięśniem trójgłowym ramienia w odległości około 8-10 cm od nadkłykcia przyśrodkowego kości ramiennej i 3-5 cm do tyłu (poniżej) od bruzdy (rowka) pomiędzy bicepsem, a mięśniem trójgłowym ramienia. Takie umiejscowienie pozwala ominąć duże naczynia krwionośne oraz nerwy leżące
w obrębie bruzdy (rowka) i w jej pobliżu (patrz Ryciny 2a, 2b oraz 2c).
Obecność implantu podskórnego należy sprawdzić palpacyjnie natychmiast po jego założeniu.
W przypadku, gdy obecności implantu podskórnego nie można stwierdzić palpacyjnie lub, gdy jego obecność budzi wątpliwości patrz punkt 4.2 Jak zakładać Implanon NXT, podpunkt „Jeśli po założeniu nie można wyczuć implantu podskórnego palpacyjnie”.
Kiedy zakładać Implanon NXT
WAŻNE: Przed założeniem implantu podskórnego należy upewnić się, że pacjentka nie jest w ciąży.
Termin założenia implantu podskórnego zależy od dotychczas stosowanej metody antykoncepcji: Jeżeli w ciągu poprzedniego miesiąca nie była stosowana antykoncepcja hormonalna
Implant podskórny należy zakładać pomiędzy 1. a 5. dniem cyklu miesiączkowego, nawet jeśli kobieta
wciąż krwawi (1 dzień cyklu jest pierwszym dniem krwawienia miesiączkowego).
Jeśli implant podskórny został założony w sposób zalecany, nie jest konieczne stosowanie dodatkowych metod antykoncepcji. Jeśli termin założenia implantu podskórnego odbiega od zalecanego, należy doradzić kobiecie stosowanie przez 7 dni po założeniu implantu podskórnego metody barierowej. Jeśli miał miejsce stosunek płciowy, należy upewnić się, że pacjentka nie jest w ciąży.
Zastąpienie implantem podskórnym Implanon NXT innej hormonalnej metody antykoncepcji
Zmiana ze złożonej antykoncepcji hormonalnej (złożone doustne środki antykoncepcyjne, system terapeutyczny dopochwowy lub system transdermalny)
Preferuje się, aby implant podskórny zakładać w następnym dniu po przyjęciu ostatniej tabletki zawierającej substancje czynne stosowanego dotychczas złożonego doustnego środka antykoncepcyjnego lub w dniu usunięcia systemu terapeutycznego dopochwowego lub systemu transdermalnego. Należy założyć implant podskórny najpóźniej w następnym dniu po planowej przerwie w stosowaniu doustnego środka antykoncepcyjnego, systemu terapeutycznego dopochwowego, systemu transdermalnego lub tabletek zawierających placebo w ramach poprzedniego cyklu stosowania złożonych hormonalnych środków antykoncepcyjnych, kiedy należałoby rozpocząć następny cykl stosowania. Nie wszystkie metody antykoncepcyjne (system transdermalny, system terapeutyczny dopochwowy) są dostępne w każdym kraju.
Jeśli implant podskórny został założony w sposób zalecany, nie jest konieczne stosowanie dodatkowych metod antykoncepcji. Jeśli termin założenia implantu podskórnego odbiega od zalecanego, należy doradzić kobiecie stosowanie przez 7 dni po założeniu implantu podskórnego metody barierowej. Jeśli miał miejsce stosunek płciowy, należy upewnić się, że pacjentka nie jest w ciąży.
Zmiana z antykoncepcji hormonalnej, zawierającej wyłącznie progestagen (tabletki zawierające tylko progestagen, iniekcje, implant, system terapeutyczny domaciczny uwalniający progestagen
[ang. IUS])
Istnieje kilka metod antykoncepcji zawierających tylko progestagen, w związku z tym założenie implantu podskórnego powinno być wykonane następująco:
Nadwrażliwość na substancję czynną lub na którąkolwiek substancję pomocniczą wymienioną w punkcie 6.1.
Występowanie obecnie żylnej choroby zakrzepowo-zatorowej.
Występowanie lub podejrzenie nowotworów złośliwych zależnych od hormonów płciowych.
Występowanie guzów wątroby (łagodnych lub złośliwych) obecnie lub w wywiadzie.
Występowanie obecnie lub w wywiadzie ciężkich chorób wątroby, do czasu powrotu wskaźników czynności wątroby do normy.
Krwawienie z dróg rodnych o nieznanej przyczynie.
Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania
Interakcje z innymi produktami leczniczymi i inne rodzaje interakcji
Wpływ na płodność, ciążę i laktację
Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn
Działania niepożądane
Przedawkowanie
Jeśli u pacjentki stwierdzona jest którakolwiek z chorób i (lub) czynników ryzyka wymienionych poniżej, korzyści ze stosowania progestagenu należy wyważyć względem potencjalnego ryzyka
i przedyskutować to z kobietą przed podjęciem przez nią decyzji o założeniu implantu podskórnego Implanon NXT. W przypadku nasilenia, zaostrzenia lub pojawienia się po raz pierwszy któregokolwiek ze stanów opisanych poniżej kobieta powinna skontaktować się z fachowym personelem medycznym. Fachowy personel medyczny zadecyduje wówczas, czy zaprzestać stosowania implantu Implanon NXT.
Rak piersi
Ryzyko raka piersi zwiększa się generalnie z wiekiem. W czasie stosowania złożonych doustnych środków antykoncepcyjnych ryzyko rozpoznania raka piersi w niewielkim stopniu wzrasta.
Zwiększone ryzyko stopniowo zmniejsza się w ciągu 10 lat od zaprzestania stosowania doustnych środków antykoncepcyjnych i nie jest związane z długością okresu ich stosowania, ale z wiekiem kobiety w czasie, gdy je stosowała. Spodziewaną liczbę zdiagnozowanych przypadków raka piersi na 10 000 kobiet, które stosują złożone doustne środki antykoncepcyjne (do 10 lat po zaprzestaniu ich stosowania), w porównaniu z grupą kobiet nigdy niestosujących takich produktów leczniczych, wyliczono dla odpowiadających grup wiekowych w tym samym przedziale czasu na: 4,5/4 (16-19 lat), 17,5/16 (20-24 lata), 48,7/44 (25-29 lat), 110/100 (30-34 lata), 180/160 (35-39 lat) i 260/230
(40-44 lata). Ryzyko u kobiet stosujących środki antykoncepcyjne, zawierające wyłącznie progestageny, jest prawdopodobnie porównywalne do przypadku kobiet, stosujących złożone doustne środki antykoncepcyjne. Jednakże w przypadku tych produktów leczniczych, dane w mniejszym stopniu pozwalają na wyciągnięcie wniosków. Zwiększenie ryzyka związanego z doustnymi środkami antykoncepcyjnymi jest niewielkie, w porównaniu z ryzykiem zachorowania na raka piersi przez całe życie. Nowotwory piersi zdiagnozowane u kobiet stosujących doustne produkty antykoncepcyjne są zwykle mniej zaawansowane niż u kobiet niestosujących doustnej antykoncepcji. Zwiększone ryzyko, obserwowane u kobiet stosujących doustne środki antykoncepcyjne, może wiązać się z wcześniejszą diagnozą, biologicznym działaniem doustnych środków antykoncepcyjnych lub skojarzeniem obu tych czynników.
Choroba wątroby
W przypadku wystąpienia ostrych lub przewlekłych zaburzeń czynności wątroby, kobietę należy skierować do specjalisty.
Zakrzepowe i inne zaburzenia naczyniowe
Badania epidemiologiczne wykazały związek pomiędzy stosowaniem złożonych doustnych środków antykoncepcyjnych (estrogen + progestagen) ze zwiększoną zachorowalnością na żylną chorobę zakrzepowo–zatorową (zakrzepicę żył głębokich oraz zatorowość płucną) i tętnicze zaburzenia zakrzepowo–zatorowe (zawał mięśnia sercowego i udar mózgu). Kliniczne znaczenie tych obserwacji dla etonogestrelu (biologicznie czynnego metabolitu desogestrelu), progestagenowego środka antykoncepcyjnego bez dodatku składnika estrogenowego jest nieznane.
Ograniczone dane epidemiologiczne nie wskazują na istnienie zwiększonego ryzyka wystąpienia żylnej choroby zakrzepowo–zatorowej lub tętniczych zaburzeń zakrzepowo-zatorowych u kobiet stosujących implant, jednakże w okresie po wprowadzeniu produktu leczniczego do obrotu zgłaszano przypadki tych chorób u kobiet stosujących implanty etonogestrelu. Zaleca się dokonanie oceny czynników zwiększających ryzyko wystąpienia żylnej choroby zakrzepowo–zatorowej lub tętniczych zaburzeń zakrzepowo-zatorowych. Kobiety z chorobą zakrzepowo-zatorową w wywiadzie należy przestrzec przed możliwością nawrotu choroby. W przypadku wystąpienia zakrzepicy implant podskórny należy usunąć. Usunięcie implantu podskórnego należy rozważyć także w przypadku długotrwałego unieruchomienia wskutek operacji lub choroby.
Podwyższone ciśnienie tętnicze
Jeśli w czasie stosowania implantu podskórnego Implanon NXT dojdzie do rozwoju nadciśnienia lub jeśli znaczące zwiększenie wartości ciśnienia tętniczego nie odpowiada w sposób zadowalający na leczenie przeciwnadciśnieniowe, należy zaprzestać stosowania implantu podskórnego Implanon NXT.
Metabolizm węglowodanów
Stosowanie środków antykoncepcyjnych zawierających progestageny może wpływać na obwodową insulinooporność oraz tolerancję glukozy. Dlatego kobiety z cukrzycą należy starannie monitorować w pierwszych miesiącach stosowania implantu podskórnego Implanon NXT.
Ostuda
W rzadkich przypadkach może wystąpić ostuda, szczególnie u kobiet, u których wystąpiła ona
w okresie ciąży. W czasie stosowania implantu podskórnego Implanon NXT kobiety z tendencją do ostudy powinny unikać ekspozycji na słońce i promieniowanie ultrafioletowe.
Masa ciała
Działanie antykoncepcyjne implantu podskórnego Implanon NXT zależy od stężenia etonogestrelu
w osoczu, które jest odwrotnie proporcjonalne do masy ciała i zmniejsza się wraz z upływem czasu po wprowadzeniu implantu podskórnego. Doświadczenie kliniczne, w trzecim roku stosowania u kobiet z większą masą ciała jest ograniczone. Dlatego nie można wykluczyć, że skuteczność antykoncepcyjna u tych kobiet w trzecim roku stosowania implantu podskórnego będzie zmniejszona w porównaniu z grupą kobiet o prawidłowej masie ciała. Fachowy personel medyczny może, zatem rozważyć wcześniejszą wymianę implantu podskórnego u kobiet z nadwagą.
Powikłania w czasie zakładania implantu podskórnego
Zgłaszano przypadki przemieszczenia się implantu podskórnego w obrębie ramienia względem pierwotnego umiejscowienia, które mogły być związane z głębokim założeniem implantu podskórnego (patrz punkt 4.2 Jak zakładać Implanon NXT) lub siły zewnętrznego działania (np. manipulacji przy implancie lub uprawiania sportów kontaktowych). Po wprowadzeniu produktu leczniczego do obrotu zgłaszano także rzadkie przypadki zlokalizowania implantu podskórnego
w naczyniach krwionośnych ramienia oraz w tętnicy płucnej, które mogły być związane z głębokim założeniem implantu podskórnego lub umieszczeniem go wewnątrz naczynia. W przypadkach, gdy implant podskórny przemieścił się w obrębie ramienia względem pierwotnego umiejscowienia, zlokalizowanie implantu podskórnego może być trudniejsze, a usunięcie może wymagać drobnego zabiegu chirurgicznego z większym nacięciem lub zabiegu chirurgicznego w sali operacyjnej.
W przypadkach, gdy implant podskórny przemieścił się do tętnicy płucnej, konieczne może być zastosowanie metod wewnątrznaczyniowych lub przeprowadzenie zabiegu chirurgicznego (patrz punkt 4.2 Jak usuwać Implanon NXT). Jeżeli w jakimkolwiek czasie implant podskórny jest niewyczuwalny palpacyjnie, należy go zlokalizować i zaleca się usunięcie implantu podskórnego tak szybko, jak to tylko możliwe z medycznego punktu widzenia. Jeśli implant podskórny nie zostanie usunięty, działanie antykoncepcyjne oraz ryzyko działań niepożądanych progestagenu mogą trwać przez dłuższy okres czasu, niż życzy sobie tego kobieta.
Implant podskórny może ulec wysunięciu, szczególnie, jeśli nie został wprowadzony zgodnie
z instrukcjami podanymi w punkcie 4.2 Jak zakładać Implanon NXT lub wskutek miejscowego stanu zapalnego.
Torbiele jajników
Przy stosowaniu hormonalnych środków antykoncepcyjnych o małych dawkach może dojść do nadmiernego rozwoju pęcherzyków jajnikowych, tak, że osiągną one rozmiary większe niż
w prawidłowym cyklu. Zazwyczaj, powiększone pęcherzyki zanikają samoistnie. Często nie dają objawów; w pewnych przypadkach mogą być przyczyną łagodnego bólu brzucha. Rzadko wymagają interwencji chirurgicznej.
Ciąża pozamaciczna
Ochrona przed ciążą pozamaciczną, jaką dają tradycyjne środki antykoncepcyjne zawierające tylko progestagen, nie jest tak duża, jak w przypadku złożonych doustnych środków antykoncepcyjnych, co jest związane z częstszym występowaniem owulacji. Pomimo, że Implanon NXT będzie hamował owulację, ciążę pozamaciczną należy brać pod uwagę w diagnostyce różnicowej u kobiet
z zatrzymaniem miesiączki i bólami brzucha.
Zaburzenia psychiczne
Obniżony nastrój i depresja to dobrze znane działania niepożądane stosowania hormonalnych środków antykoncepcyjnych (patrz punkt 4.8). Depresja może mieć ciężki przebieg i jest dobrze znanym czynnikiem ryzyka zachowań samobójczych i samobójstw. Jeśli u pacjentki wystąpią zmiany nastroju lub objawy depresji, również krótko po rozpoczęciu leczenia, zaleca się, aby skonsultował się
z lekarzem.
Inne warunki
W okresie ciąży i stosowania hormonów płciowych zgłaszano występowanie następujących chorób, ale nie ustalono ich związku ze stosowaniem progestagenów: żółtaczka i (lub) świąd związany
z cholestazą; kamica żółciowa; porfiria; toczeń rumieniowaty układowy; zespół
hemolityczno-mocznicowy; pląsawica Sydenhama; opryszczka ciężarnych; utrata słuchu związana z otosklerozą oraz (dziedziczny) obrzęk naczynioruchowy.
Badanie lekarskie i (lub) wizyta u lekarza
Przed założeniem lub wymianą implantu podskórnego Implanon NXT należy zebrać kompletny wywiad lekarski (w tym wywiad rodzinny) oraz upewnić się, że pacjentka nie jest w ciąży. Należy zmierzyć ciśnienie krwi oraz przeprowadzić badanie przedmiotowe, uwzględniając przeciwwskazania (patrz punkt 4.3) oraz ostrzeżenia (patrz punkt 4.4). Zaleca się, aby kobieta zgłosiła się na badanie kontrolne 3 miesiące po założeniu implantu podskórnego Implanon NXT. W czasie badania kontrolnego należy wykonać pomiar ciśnienia krwi oraz zapytać pacjentkę, czy ma jakiekolwiek pytania lub skargi oraz czy wystąpiły jakiekolwiek działania niepożądane. Częstość i rodzaj następnych badań okresowych należy dostosować w sposób indywidualny, według oceny klinicznej. Implant podskórny powinien być wyczuwalny palpacyjnie podczas każdej wizyty kontrolnej. Należy poinformować pacjentki, że jeśli nie mogą wyczuć implantu podskórnego, powinny jak najszybciej skontaktować się z lekarzem, w dowolnym momencie między wizytami kontrolnymi.
Należy poinformować pacjentkę, że Implanon NXT nie chroni przed zakażeniem HIV (AIDS) i innymi chorobami przenoszonymi drogą płciową.
Zmniejszona skuteczność podczas jednoczesnego stosowania innych produktów leczniczych W przypadku jednoczesnego stosowania produktów leczniczych zmniejszających stężenie
etonogestrelu w osoczu skuteczność implantu Implanon NXT może się zmniejszyć (patrz punkt 4.5).
Zmiana profilu krwawień z dróg rodnych
W czasie stosowania implantu Implanon NXT kobiety mogą zaobserwować zmiany w krwawieniu miesiączkowym, których nie da się przewidzieć przed założeniem implantu podskórnego. Zmiana dotyczy pojawienia się nieregularnych krwawień miesiączkowych (brak krwawień miesiączkowych, rzadko występujące, częste lub ciągłe krwawienia miesiączkowe), intensywności krwawień miesiączkowych (zwiększona lub zmniejszona) lub czasu trwania krwawienia miesiączkowego. Brak krwawień miesiączkowych odnotowano u 1 na 5 kobiet natomiast u innych 1 na 5 kobiet odnotowano częste i (lub) przedłużające się krwawienia miesiączkowe. Na podstawie przebiegu krwawień miesiączkowych w czasie pierwszych trzech miesięcy większość kobiet może określić przebieg kolejnych. Informacja, poradnictwo oraz stosowanie kalendarzyka krwawień miesiączkowych może poprawić stopień akceptacji przez kobietę nowego profilu krwawień. Ocena krwawienia z dróg rodnych powinna być przeprowadzona ad hoc i może uwzględniać badanie w celu wykluczenia choroby ginekologicznej lub upewnienia się, że pacjentka nie jest w ciąży.
Złamanie lub wygięcie implantu in situ
Zgłaszano przypadki złamania lub wygięcia implantu podskórnego znajdującego się w ramieniu pacjentki, co mogło być spowodowane przez działanie sił zewnętrznych. Zgłaszano również przypadki przemieszczania się fragmentu złamanego implantu podskórnego w obrębie ramienia. Dane in vitro wskazują, że w razie złamania lub wygięcia implantu podskórnego szybkość uwalniania etonogestrelu może być nieznacznie zwiększona. Nie jest spodziewane, by zmiana ta miała jakiekolwiek znaczenie kliniczne.
Jednak w razie złamania implantu podskórnego należy go usunąć i ważne jest, by podczas usuwania implantu podskórnego w ciele pacjentki nie pozostała żadna jego część (patrz punkt 4.2, w którym
zamieszczono procedury dotyczące usuwania implantu podskórnego wyczuwalnego palpacyjnie lub niewyczuwalnego palpacyjnie).
Uwaga: W celu określenia potencjalnych interakcji, należy zapoznać się z informacjami dotyczącymi jednocześnie stosowanych produktów leczniczych.
Wpływ innych produktów leczniczych na implant podskórny Implanon NXT
Mogą występować interakcje z produktami leczniczymi, które indukują enzymy mikrosomalne, co może skutkować zwiększeniem klirensu hormonów płciowych i może prowadzić do wystąpienia krwawienia miesiączkowego i (lub) zmniejszenia skuteczności antykoncepcyjnej.
Postępowanie
Indukcja enzymów może być widoczna już po kilku dniach leczenia. Maksymalna indukcja enzymów jest na ogół widoczna w ciągu kilku tygodni. Po przerwaniu leczenia, indukcja enzymów może utrzymywać się przez około 4 tygodnie.
Pacjentki podczas leczenia produktami leczniczymi indukującymi enzymy wątrobowe lub produktami ziołowymi należy poinformować, że skuteczność implantu podskórnego Implanon NXT może być zmniejszona. Usunięcie implantu podskórnego nie jest konieczne, ale w celu utrzymania maksymalnej ochrony pacjentkę należy poinformować, o konieczności stosowania dodatkowej, niehormonalnej metody antykoncepcji w czasie jednoczesnego podawania produktu leczniczego oraz przez 28 dni po zakończeniu leczenia.
W literaturze opisano następujące interakcje (głównie ze złożonymi środkami antykoncepcyjnymi, ale w niektórych przypadkach także ze środkami antykoncepcyjnymi zawierającymi wyłącznie progestagen w tym implantem Implanon NXT):
Substancje zwiększające klirens hormonalnych środków antykoncepcyjnych (zmniejszona skuteczność antykoncepcyjna poprzez indukcję enzymów) np.:
Barbiturany, bosentan, karbamazepina, fenytoina, prymidon, ryfampicyna oraz produkty lecznicze stosowane w zakażeniach wirusem HIV/HCV, takie jak rytonawir, efawirenz, boceprewir, newirapina, oraz prawdopodobnie także felbamat, gryzeofulwina, okskarbazepina, topiramat oraz produkty zawierające ziele dziurawca zwyczajnego (Hypericum perforatum).
Substancje wywierające różny wpływ na klirens hormonalnych środków antykoncepcyjnych Jednoczesne podawanie z hormonalnymi środkami antykoncepcyjnymi wielu połączeń inhibitorów proteazy HIV i nienukleozydowych inhibitorów odwrotnej transkryptazy w tym połączeń
z inhibitorami wirusa zapalenia wątroby typu C (HCV), może zwiększać lub zmniejszać stężenie progesteronu, w tym etonogestrelu. W niektórych przypadkach wpływ netto tych zmian może mieć znaczenie kliniczne.
Dlatego też przepisując jednocześnie stosowane produkty lecznicze przeciwko HIV/HCV, należy wziąć pod uwagę możliwe interakcje oraz odpowiednie zalecenia. W przypadku jakichkolwiek wątpliwości, u kobiet w trakcie leczenia inhibitorami proteazy lub nienukleozydowymi inhibitorami odwrotnej transkryptazy należy stosować dodatkową, mechaniczną metodę antykoncepcji.
Substancje zmniejszające klirens hormonalnych środków antykoncepcyjnych (inhibitory enzymów) Jednoczesne podawanie silnych (np. ketokonazol, itrakonazol, klarytromycyna) lub umiarkowanych (np. flukonazol, diltiazem, erytromycyna) inhibitorów CYP3A4 może zwiększać stężenie progesteronu, w tym etonogestrelu.
Wpływ implantu Implanon NXT na inne produkty lecznicze
Hormonalne środki antykoncepcyjne mogą wpływać na metabolizm niektórych, innych substancji czynnych. W związku z tym, ich stężenie w osoczu i tkankach może być zwiększone (np. cyklosporyny) lub zmniejszone (np. lamotryginy).
Badania laboratoryjne
Dane uzyskane dla złożonych doustnych środków antykoncepcyjnych wykazały, że steroidy mogą wpływać na wyniki niektórych badań laboratoryjnych, w tym biochemiczne parametry czynności wątroby, tarczycy, nadnerczy i nerek, stężenie białek (nośnikowych) w osoczu, np. globuliny wiążące kortykosteroidy oraz frakcje lipidowo-lipoproteinowe, parametry metabolizmu węglowodanów oraz parametry koagulacji i fibrynolizy. Zmiany te zwykle pozostają w granicach normy. Nie wiadomo, do jakiego stopnia dotyczy to środków antykoncepcyjnych, zawierających wyłącznie progestageny.
Ciąża
Stosowanie implantu podskórnego Implanon NXT jest przeciwwskazane w okresie ciąży. Jeśli w czasie stosowania implantu podskórnego Implanon NXT kobieta zajdzie w ciążę, implant podskórny należy usunąć. Badania na zwierzętach wykazały, że bardzo duże dawki substancji o działaniu progestagennym mogą powodować maskulinizację płodów żeńskich. Obszerne badania epidemiologiczne nie potwierdziły zwiększonego ryzyka wad wrodzonych u dziecka, jeżeli kobieta stosowała doustne środki antykoncepcyjne przed zajściem w ciążę, ani wpływu teratogennego tych produktów, stosowanych w sposób niezamierzony w okresie ciąży. Chociaż prawdopodobnie dotyczy to wszystkich doustnych środków antykoncepcyjnych, nie jest jasne, czy dotyczy także implantu Implanon NXT.
Dane uzyskane w badaniach z zakresu bezpieczeństwa farmakoterapii dla różnych produktów zawierających etonogestrel i dezogestrel (etonogestrel jest metabolitem dezogestrelu) również nie wskazują na zwiększone ryzyko.
Karmienie piersią
Dane kliniczne wskazują, że Implanon NXT nie wpływa na wydzielanie oraz jakość pokarmu kobiecego (stężenie białka, laktozy i tłuszczu). Jednakże niewielkie ilości etonogestrelu są wydzielane do mleka kobiecego. Przyjmując dobowe spożycie mleka na 150 ml/kg mc., średnia dobowa dawka etonogestrelu, jaką spożywałoby niemowlę, wynosi około 27 ng/kg mc./dobę po jednym miesiącu uwalniania etonogestrelu z implantu podskórnego. Odpowiada to w przybliżeniu 2,2% dobowej dawki u matki, wyliczonej względem masy ciała oraz około 0,2% szacowanej bezwzględnej dobowej dawki u matki. Stężenie etonogestrelu w mleku kobiecym w okresie karmienia piersią zmniejsza się wraz
z upływem czasu.
Istnieją ograniczone dane z długoterminowej obserwacji z udziałem 38 dzieci, których matki miały założony implant podskórny pomiędzy 4. a 8. tygodniem po porodzie. Dzieci te były karmione piersią przez okres średnio 14 miesięcy, zaś obserwowane były do 36. miesiąca życia. Ocena wzrastania oraz rozwoju fizycznego i psychomotorycznego nie wykazała różnic w porównaniu do dzieci karmionych piersią, których matki stosowały system terapeutyczny domaciczny (n=33). Niemniej jednak rozwój
i wzrost dziecka należy starannie obserwować. W oparciu o dostępne dane, Implanon NXT można stosować w okresie karmienia piersią i powinien być założony w czwartym tygodniu po porodzie.
W oparciu o profil farmakodynamiczny oczekuje się, że implant podskórny Implanon NXT nie ma wpływu lub wywiera nieistotny wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn.
W czasie stosowania implantu Implanon NXT kobiety mogą zaobserwować zmiany w krwawieniu miesiączkowym, których nie da się przewidzieć przed założeniem implantu podskórnego. Zmiana dotyczy pojawienia się nieregularnych krwawień miesiączkowych (brak krwawień miesiączkowych, rzadko występujące, częste lub ciągłe krwawienia miesiączkowe), intensywności krwawień (zwiększona lub zmniejszona) lub czasu trwania krwawienia miesiączkowego. Brak krwawień miesiączkowych odnotowano u 1 na 5 kobiet, natomiast u kolejnych 1 na 5 kobiet odnotowano częste
i (lub) przedłużające się krwawienia miesiączkowe. Rzadko odnotowano obfite krwawienia miesiączkowe. Zgłaszane w badaniach klinicznych zmiany w krwawieniach miesiączkowych były najczęstszym powodem zaprzestania terapii (około 11%). Na podstawie przebiegu krwawień miesiączkowych w czasie pierwszych trzech miesięcy większość kobiet może określić przebieg kolejnych.
Zgłaszane w badaniach klinicznych możliwe działania niepożądane wymieniono w tabeli poniżej:
Klasyfikacja układów i narządów MedDRA1 | Bardzo często ( 1/10) | Często (≥ 1/100 do < 1/10) | Niezbyt często ( 1/1000 do < 1/100) |
Zakażenia i zarażenia pasożytnicze | zakażenia pochwy | zapalenie gardła, katar, zakażenie układu moczowego | |
Zaburzenia układu immunologicznego | nadwrażliwość | ||
Zaburzenia metabolizmu i odżywiania | zwiększenie apetytu | ||
Zaburzenia psychiczne | chwiejność emocjonalna, obniżony nastrój, nerwowość, zmniejszone libido | niepokój, bezsenność | |
Zaburzenia układu nerwowego | bóle głowy | zawroty głowy | migrena, senność |
Zaburzenia naczyniowe | uderzenia gorąca | ||
Zaburzenia żołądka i jelit | ból brzucha, nudności, wzdęcia | wymioty, zaparcia, biegunka | |
Zaburzenia skóry i tkanki podskórnej | trądzik | łysienie | nadmierne owłosienie, wysypka, świąd |
Zaburzenia mięśniowo- szkieletowe i tkanki łącznej | bóle pleców, bóle stawów, bóle mięśni, bóle kostno-mięśniowe | ||
Zaburzenia nerek i dróg moczowych | dyzuria | ||
Zaburzenia układu rozrodczego i piersi | tkliwość piersi, ból piersi, nieregularne krwawienia miesiączkowe | bolesne krwawienia miesiączkowe, torbiele jajników | nadmierna wydzielina z dróg rodnych, dyskomfort w obrębie sromu i pochwy, mlekotok, powiększenie piersi, świąd narządów płciowych |
Zaburzenia ogólne i stany w miejscu podania | ból w miejscu wprowadzenia implantu podskórnego, reakcja w miejscu wprowadzenia implantu podskórnego, uczucie zmęczenia, objawy grypopodobne, bóle | gorączka, obrzęki | |
Badania diagnostyczne | zwiększenie masy ciała | zmniejszenie masy ciała |
1W celu opisania pewnych działań niepożądanych wymieniono najbardziej odpowiednie terminy klasyfikacji MedDRA (wersja 10.1). Nie wymieniono synonimów oraz pokrewnych działań niepożądanych związanych z przyjmowaniem implantu podskórnego Implanon NXT, ale powinny one także być brane pod uwagę.
Po wprowadzeniu produktu leczniczego do obrotu, w rzadkich przypadkach, zaobserwowano znamienne klinicznie zwiększenie ciśnienia tętniczego. Odnotowano również występowanie łojotoku. Mogą wystąpić reakcje anafilaktyczne, pokrzywka, obrzęk naczynioruchowy, pogorszenie się obrzęku naczynioruchowego i (lub) pogorszenie się dziedzicznego obrzęku naczynioruchowego.
Następujące działania niepożądane występowały w związku z procedurą zakładania i usuwania implantu:
W czasie zakładania i usuwania implantu podskórnego może dojść do powstania zasinienia, w tym krwiaków w niektórych przypadkach, niewielkiego miejscowego podrażnienia, a także może wystąpić ból lub świąd.
Założenie implantu może powodować reakcje wazowagalne (takie jak niedociśnienie, zawroty głowy lub omdlenia).
W miejscu zakładania implantu podskórnego może dochodzić do procesów zwłóknienia, może dojść do formowania blizn lub rozwinięcia ropnia. Mogą wystąpić parestezje lub objawy przypominające parestezje. Zgłaszano przypadki zewnętrznego wydalenia implantu podskórnego lub jego przemieszczenia w tym, w rzadkich przypadkach przemieszczenia do klatki piersiowej. W rzadkich przypadkach implanty podskórne zlokalizowano w naczyniach krwionośnych, w tym w tętnicy płucnej. W niektórych przypadkach, gdy implant podskórny zlokalizowano w tętnicy płucnej zgłaszano ból w klatce piersiowej i (lub) zaburzenia oddychania (takie jak duszność, kaszel, krwioplucie); w innych przypadkach nie zgłaszano żadnych objawów (patrz punkt 4.4). W przypadku nieprzestrzegania zaleceń (patrz punkt 4.2) implant podskórny może zostać założony nieprawidłowo; mogą także pojawić się trudności ze zlokalizowaniem i usunięciem implantu podskórnego. W czasie usuwania implantu podskórnego może być konieczny zabieg chirurgiczny.
W rzadkich przypadkach odnotowano ciążę pozamaciczną (patrz punkt 4.4).
U kobiet stosujących złożone doustne środki antykoncepcyjne mogą wystąpić liczne (ciężkie) działania niepożądane. Są to: żylna choroba zakrzepowo-zatorowa, tętnicze zaburzenia zakrzepowo-zatorowe, nowotwory zależne od hormonów (np. rak wątroby, rak piersi) oraz ostuda. Niektóre działania niepożądane zostały bardziej szczegółowo opisane w punkcie 4.4.
Zgłaszanie podejrzewanych działań niepożądanych
Po dopuszczeniu produktu leczniczego do obrotu istotne jest zgłaszanie podejrzewanych działań niepożądanych. Umożliwia to nieprzerwane monitorowanie stosunku korzyści do ryzyka stosowania produktu leczniczego. Osoby należące do fachowego personelu medycznego powinny zgłaszać wszelkie podejrzewane działania niepożądane za pośrednictwem Departamentu Monitorowania Niepożądanych Działań Produktów Leczniczych Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych:
Al. Jerozolimskie 181C, 02-222 Warszawa, Tel.: + 48 22 49 21 301, Faks: + 48 22 49 21 309, Strona internetowa: https://smz.ezdrowie.gov.pl.
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Przed założeniem nowego implantu podskórnego poprzedni zawsze należy usunąć. Brak danych dotyczących przedawkowania etonogestrelu. Generalnie nie zgłaszano ciężkiego szkodliwego działania po przedawkowaniu środków antykoncepcyjnych.
WŁAŚCIWOŚCI FARMAKOLOGICZNE
Właściwości farmakodynamiczne
Właściwości farmakokinetyczne
Przedkliniczne dane o bezpieczeństwie
Grupa farmakoterapeutyczna: Hormonalne środki antykoncepcyjne do stosowania ogólnego, progestageny, kod ATC: G03AC08.
Mechanizm działania
Implanon NXT jest nie ulegającym biodegradacji, nie przepuszczającym promieni rentgenowskich, zawierającym etonogestrel implantem podskórnym do stosowania podskórnego, znajdującym się
w sterylnym, gotowym do jednorazowego użycia aplikatorze. Etonogestrel jest biologicznie czynnym metabolitem dezogestrelu, progestagenu wchodzącego w skład wielu doustnych środków antykoncepcyjnych. Strukturalnie jest to pochodna 19-nortestosteronu, która wykazuje duże powinowactwo do receptorów progesteronu w narządach docelowych. Działanie antykoncepcyjne etonogestrelu polega przede wszystkim na hamowaniu owulacji. Owulacje nie są obserwowane
w pierwszych dwóch latach stosowania implantu podskórnego i bardzo rzadko w trzecim roku. Poza hamowaniem owulacji etonogestrel powoduje zmiany w śluzie szyjkowym, co utrudnia migrację plemników.
Skuteczność kliniczna i bezpieczeństwo stosowania
Badania kliniczne przeprowadzono u kobiet w wieku 18 – 40 lat. Chociaż nie przeprowadzono bezpośredniego porównania, skuteczność antykoncepcyjna okazała się co najmniej porównywalna ze stwierdzaną dla doustnych środków antykoncepcyjnych. W trakcie badań klinicznych nie zaobserwowano ciąż w trakcie 35 057 cyklów z ekspozycją na Implanon NXT; ustalony indeks Pearl’a wynosi 0,00 (granice 95% przedziału ufności: 0,00-0,14). Należy jednak uświadomić sobie, że w praktyce żadna metoda nie może być uważana za skuteczną w 100%. Wysoka skuteczność antykoncepcyjna zależy między innymi od tego, że w przeciwieństwie do doustnych środków antykoncepcyjnych, nie opiera się na regularnym przyjmowaniu tabletek. Działanie antykoncepcyjne etonogestrelu jest odwracalne, co potwierdza szybki powrót prawidłowego cyklu miesiączkowego po usunięciu implantu podskórnego. Chociaż etonogestrel hamuje owulację, aktywność jajników nie jest całkowicie hamowana. Średnie stężenia estradiolu mieszczą się powyżej wartości obserwowanych we wczesnej fazie folikularnej. W dwuletnim badaniu, w którym porównywano mineralną gęstość kości u 44 kobiet stosujących Implanon NXT i w grupie kontrolnej 29 kobiet stosujących system terapeutyczny domaciczny, nie zaobserwowano niekorzystnego wpływu na masę kostną. Nie stwierdzono znamiennego klinicznie wpływu na metabolizm lipidów. Stosowanie środków antykoncepcyjnych zawierających progestageny może wpływać na insulinooporność oraz tolerancję glukozy. W badaniach klinicznych wykazano również, że u kobiet stosujących Implanon NXT krwawienia miesiączkowe są mniej bolesne.
Wchłanianie
Po założeniu implantu podskórnego, etonogestrel szybko wchłania się do krążenia. Stężenia hamujące owulację osiągane są w ciągu 1 doby. Maksymalne stężenia w surowicy (pomiędzy 472 a 1270 pg/ml) osiągane są w ciągu 1 do 13 dni. Tempo uwalniania produktu leczniczego z implantu podskórnego zmniejsza się w czasie. W rezultacie stężenia w surowicy szybko zmniejszają się w ciągu pierwszych kilku miesięcy. Pod koniec pierwszego roku średnie stężenie wynosi około 200 pg/ml (zakres
150-261 pg/ml) i powoli spada do 156 pg/ml (zakres 111-202 pg/ml) pod koniec trzeciego roku. Obserwowaną zmienność stężeń w surowicy można przypisać częściowo wpływowi zmian masy ciała.
Dystrybucja
Etonogestrel jest w 95,5-99% związany z białkami osocza, głównie albuminami i w mniejszym stopniu z globuliną wiążącą hormony płciowe. Centralne i całkowite objętości dystrybucji wynoszą, odpowiednio, 27 l i 220 l i podlegają dużym wahaniom w czasie stosowania implantu podskórnego Implanon NXT.
Metabolizm
Etonogestrel podlega hydroksylacji i redukcji. Metabolity są sprzęgane do postaci siarczanów
i glukuronianów. Badania na zwierzętach pokazują, że krążenie jelitowo-wątrobowe prawdopodobnie nie wpływa na progestagenową aktywność etonogestrelu.
Eliminacja
Po dożylnym podaniu etonogestrelu okres półtrwania w fazie eliminacji wynosi w przybliżeniu 25 godzin, a klirens około 7,5 l/godz. Zarówno klirens, jak i okres półtrwania w fazie eliminacji pozostają stałe w okresie leczenia. Zarówno etonogestrel jak i jego metabolity w postaci wolnych
steroidów, jak i związków sprzężonych, wydalane są z moczem i kałem w proporcji 1,5:1. Po podaniu etonogestrelu kobietom w okresie karmienia piersią, jest on wydzielany do mleka, przy czym współczynnik mleko/surowica wynosi 0,44-0,50 w czasie pierwszych czterech miesięcy. U kobiet karmiących piersią, średnie przenoszenie etonogestrelu do organizmu niemowlęcia wynosi około 0,2% dobowej dawki u matki (2,2% wartości normalizowane na kg masy ciała). Stężenia wykazują stopniowe i statystycznie znamienne zmniejszenie w czasie.
Badania toksykologiczne nie ujawniły żadnych innych działań niż te, które można wytłumaczyć na podstawie hormonalnych właściwości etonogestrelu, niezależnie od drogi jego podawania.
DANE FARMACEUTYCZNE
Wykaz substancji pomocniczych
Niezgodności farmaceutyczne
Okres ważności
Specjalne środki ostrożności podczas przechowywania
Rodzaj i zawartość opakowania
Specjalne środki ostrożności dotyczące usuwania i przygotowania produktu leczniczego do stosowania
Implant podskórny
Rdzeń: Etylenu i octanu winylu kopolimer (28% octanu winylu) Baru siarczan
Magnezu stearynian
Warstwa wierzchnia: Etylenu i octanu winylu kopolimer (15% octanu winylu)
Nie dotyczy.
5 lat
Implanon NXT nie powinien być zakładany po terminie ważności zamieszczonym na opakowaniu.
Brak szczególnych środków ostrożności dotyczących warunków przechowywania produktu leczniczego.
Przechowywać w oryginalnym opakowaniu.
Blister zawiera 1 implant podskórny (o długości 4 cm i 2 mm średnicy) w igle ze stali nierdzewnej, w sterylnym gotowym do jednorazowego użycia aplikatorze. Aplikator pakowany pojedynczo
w blister z folii PETG, powlekany folią HDPE. Zawartość blistra jest sterylna, chyba że opakowanie zostało uszkodzone lub otwarte.
Wielkości opakowań: tekturowe pudełko zawierające 1 blister, tekturowe pudełko zawierające 5 blistrów.
Nie wszystkie wielkości opakowań muszą znajdować się w obrocie.
Patrz punkt 4.2.
Aplikator przeznaczony jest do jednorazowego użycia.
Wszelkie niewykorzystane resztki produktu leczniczego lub jego odpady należy usunąć zgodnie z lokalnymi przepisami.
PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU
Organon Polska Sp. z o.o. ul. Marszałkowska 126/134 00-008 Warszawa
NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
21319
DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU I DATA PRZEDŁUŻENIA POZWOLENIA
Data wydania pierwszego pozwolenia na dopuszczenie do obrotu: 10 lipca 2013 r. Data ostatniego przedłużenia pozwolenia: 20 listopada 2013 r.
DATA ZATWIERDZENIA LUB CZĘŚCIOWEJ ZMIANY TEKSTU CHARAKTERYSTYKI PRODUKTU LECZNICZEGO
26/04/2023











