Spis treści:
- NAZWA PRODUKTU LECZNICZEGO
- SKŁAD JAKOŚCIOWY I ILOŚCIOWY
- POSTAĆ FARMACEUTYCZNA
- SZCZEGÓŁOWE DANE KLINICZNE
- WŁAŚCIWOŚCI FARMAKOLOGICZNE
- DANE FARMACEUTYCZNE
- PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU
- NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
- DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU I DATA PRZEDŁUŻENIA POZWOLENIA
- DATA ZATWIERDZENIA LUB CZĘŚCIOWEJ ZMIANY TEKSTU
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
NAZWA PRODUKTU LECZNICZEGO
SKŁAD JAKOŚCIOWY I ILOŚCIOWY
POSTAĆ FARMACEUTYCZNA
SZCZEGÓŁOWE DANE KLINICZNE
Wskazania do stosowania
Dawkowanie i sposób podawania
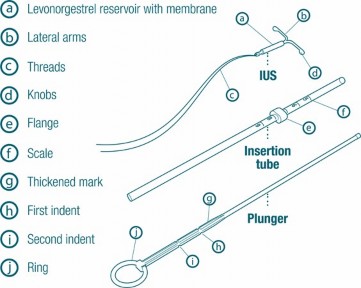
zbiornik lewonorgestrelu z
membraną
ramiona
nitki
wybrzuszenie
kołnierz
skala
odcinek pogrubiony z oznakowaniem
pierwsze przewężenie
drugie przewężenie
pierścień
Przeciwwskazania
Ciąża lub podejrzenie ciąży;
Istniejące lub nawracające stany zapalne narządów miednicy;
Infekcje dolnego odcinka dróg rodnych;
Poporodowe zapalenie błony śluzowej macicy;
Infekcje macicy po poronieniu w ciągu ostatnich trzech miesięcy;
Zapalenie szyjki macicy; dysplazja nabłonka szyjki macicy;
Podejrzenie lub występowanie nowotworu złośliwego szyjki lub trzonu macicy;
Nowotwór wątroby lub inne ostre lub ciężkie choroby wątroby;
Wrodzone lub nabyte nieprawidłowości w budowie macicy, w tym włókniakomięśniaki zniekształcające jamę macicy;
Niezdiagnozowane, nietypowe krwawienia z macicy;
Stany, które sprzyjają rozwojowi infekcji;
Podejrzenie lub występowanie nowotworów zależnych od hormonów, takich jak nowotwór piersi (patrz punkt 4.4);
Nowotwory złośliwe dotyczące krwi lub białaczki za wyjątkiem okresu remisji;
Niedawno przebyta choroba trofoblastu, gdy utrzymuje się podwyższony poziom hCG;
Nadwrażliwość na substancje czynną lub którąkolwiek substancję pomocniczą wymienioną
Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania
migrena, migrena ogniskowa z asymetrycznymi ubytkami pola widzenia lub innymi objawami
wskazującymi na przemijające niedokrwienie mózgu,
wyjątkowo silny ból głowy lub nietypowo częsty ból głowy,
żółtaczka,
znaczne zwiększenie ciśnienia tętniczego krwi,
nowotwory złośliwe dotyczące krwi lub białaczki w okresie remisji,
długotrwałe leczenie kortykosteroidami,
występowanie w przeszłości objawów czynnościowych torbieli jajnika,
występująca obecnie lub przebyta w przeszłości, ciężka choroba tętnic, jak np. udar mózgu lub zawał serca,
ciężkie lub liczne czynniki ryzyka rozwoju choroby tętnic,
zakrzepica tętnic lub jakakolwiek obecnie występująca choroba zatorowa,
ostra żylna choroba zakrzepowo-zatorowa.
u kobiet z obfitymi krwawieniami miesiączkowymi w wywiadzie (w tym kobiet, które stosują
system Levosert w leczeniu obfitych krwawień miesiączkowych)
u kobiet z większym niż prawidłowy BMI (ang. Body Mass Index – wskaźnik masy ciała) w momencie zakładania systemu; ryzyko to zwiększa się stopniowo wraz ze zwiększaniem BMI.
Interakcje z innymi produktami leczniczymi i inne rodzaje interakcji
Wpływ na płodność, ciążę i laktację
Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn
Działania niepożądane
Przedawkowanie
WŁAŚCIWOŚCI FARMAKOLOGICZNE
Właściwości farmakodynamiczne
zapobieganie wzrostowi endometrium,
zagęszczenie śluzu szyjkowego zapobiega przedostawaniu się plemników przez kanał szyjki
macicy,
zahamowanie owulacji u niektórych kobiet.
Właściwości farmakokinetyczne
Przedkliniczne dane o bezpieczeństwie
DANE FARMACEUTYCZNE
Wykaz substancji pomocniczych
Niezgodności farmaceutyczne
Okres ważności
Specjalne środki ostrożności podczas przechowywania
Rodzaj i zawartość opakowania
Specjalne środki ostrożności dotyczące usuwania i przygotowania produktu leczniczego
PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU
NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU I DATA PRZEDŁUŻENIA POZWOLENIA
DATA ZATWIERDZENIA LUB CZĘŚCIOWEJ ZMIANY TEKSTU
Levosert, 52 mg (20 mikrogramów/24 h), system terapeutyczny domaciczny
Substancją czynną jest lewonorgestrel (LNG).
System terapeutyczny domaciczny zawiera 52 mg lewonorgestrelu. Uwalniana początkowo dawka lewonorgestrelu wynosi około 20 mikrogramów. Dawka ta stopniowo zmniejsza się do około 8,6 mikrogramów/dzień po 6 latach stosowania. Średnia szybkość uwalniania LNG in vivo wynosi około 14,3 mikrograma/dzień przez okres 6 lat.
Pełny wykaz substancji pomocniczych, patrz punkt 6.1
System terapeutyczny domaciczny (ang. Intrauterine system – IUS).
Produkt leczniczy składa się z aplikatora i systemu terapeutycznego domacicznego zawierającego lewonorgestrel, znajdującego się na końcu aplikatora. Aplikator składa się z rurki wprowadzającej, tłoczka, kołnierzyka, szkieletu (korpusu) i suwaka. Wkładka składa się z białego lub prawie białego cylindra zawierającego hormon, zlokalizowanego na szkielecie w kształcie litery T i pokrytego nieprzezroczystą membraną, która reguluje uwalnianie lewonorgestrelu. Szkielet w kształcie litery T ma pętlę na końcu pionowego trzonu i dwa poziome ramiona na drugim końcu. Nitki służące do usuwania systemu są dołączone do pętli.
Leczenie nadmiernych krwawień miesiączkowych. Produkt leczniczy Levosert może być szczególnie skuteczny jako antykoncepcja (odwracalna) u kobiet, u których występują nadmierne krwawienia miesiączkowe.
U kobiet w wieku rozrodczym, produkt leczniczy Levosert należy założyć do jamy macicy w ciągu siedmiu dni od wystąpienia krwawienia miesiączkowego. System można wymienić na nowy
w dowolnym dniu cyklu.
Założenie poporodowe: W celu zredukowania ryzyka perforacji, założenie poporodowe należy przełożyć do czasu całkowitej inwolucji macicy. Nie należy zakładać systemu wcześniej niż po upływie sześciu tygodni od porodu. W przypadku wystąpienia u pacjentki nadmiernego krwawienia poporodowego i (lub) bólu, przed założeniem systemu należy wykluczyć infekcję lub inne przyczyny. Produkt leczniczy Levosert można także założyć natychmiast po poronieniu w pierwszym trymestrze
ciąży.
Produkt leczniczy Levosert zachowuje skuteczność przez 6 lat we wskazaniu do antykoncepcji oraz przez 5 lat we wskazaniu do redukowania nadmiernych krwawień miesiączkowych. System Levosert należy usunąć po 5 lub 6 latach stosowania, zgodnie ze wskazaniami.
Jeśli pacjentka chce kontynuować stosowanie tej samej metody, to po usunięciu poprzedniego systemu można od razu założyć nowy. W takim przypadku nie jest konieczne stosowanie dodatkowej ochrony.
Produkt leczniczy Levosert nie był badany u pacjentek w wieku poniżej 16 lat. Produktu leczniczego Levosert nie należy stosować przed wystąpieniem pierwszej miesiączki.
Zaburzenia czynności wątroby
Produkt leczniczy Levosert jest przeciwwskazany u pacjentek, u których występuje rak wątroby lub inna ciężka choroba wątroby (patrz punkt 4.3).
Instrukcje dotyczące stosowania i przechowywania
System Levosert jest dostarczany w sterylnym opakowaniu, które należy otworzyć tuż przed założeniem systemu. Rozpakowany system powinien być zakładany w warunkach aseptycznych. W przypadku uszkodzenia sterylnego opakowania, system należy wyrzucić (patrz punkt 6.6).
Stanowczo zaleca się, aby system Levosert był zakładany tylko przez lekarzy i (lub) pracowników służby zdrowia z doświadczeniem w zakładaniu systemu terapeutycznego domacicznego zawierającego lewonorgestrel i (lub), którzy odbyli odpowiednie szkolenia z zakładania systemu terapeutycznego domacicznego zawierającego lewonorgestrel.
W przypadku trudności przy zakładaniu i (lub) silnego bólu lub krwawienia podczas lub po założeniu systemu, patrz punkt 4.4.
System Levosert jest dostępny w sterylnym opakowaniu sterylizowanym tlenkiem etylenu. Nie należy go ponownie sterylizować. System można zastosować tylko jeden raz. Jeśli wewnętrzne opakowanie jest uszkodzone lub otwarte, nie należy stosować produktu leczniczego. Nie należy stosować po ostatnim dniu miesiąca wskazanego na etykiecie.
System Levosert jest zakładany do jamy macicy z wykorzystaniem załączonego aplikatora, zgodnie z instrukcjami dotyczącymi zakładania systemu.
Poniższa instrukcja dotycząca zakładania znajduje się w pudełku zawierającym terapeutyczny system domaciczny.
Należy uważnie przeczytać poniższą instrukcję do stosowania, ponieważ mogą występować różnice w typie systemu w porównaniu z wcześniej stosowanymi terapeutycznymi systemami domacicznymi.
IUS
IUS - system wewnątrzmaciczny Insertion tube – rurka wprowadzająca Plunger - tłoczek
w punkcie 6.1.
Przed założeniem systemu należy zebrać pełny wywiad lekarski, w tym rodzinny. Należy przeprowadzić badanie fizykalne z uwzględnieniem wyników wywiadu oraz przeciwwskazań
i ostrzeżeń. Należy przeprowadzić pomiar tętna i ciśnienia krwi oraz oburęczne badanie miednicy
w celu ustalenia położenia macicy. Pacjentkę należy ponownie zbadać po upływie sześciu tygodni od założenia sytemu, a następne badania należy przeprowadzić, jeśli będzie to klinicznie uzasadnione
i dostosowane indywidualnie do stanu pacjentki. Przed założeniem systemu należy sprawdzić, czy pacjentka nie jest w ciąży i wyleczyć infekcje dróg rodnych. Pacjentkę należy poinformować, że system Levosert nie chroni przed zakażeniem wirusem HIV (AIDS) i innymi chorobami przenoszonymi drogą płciową (należy odnieść się do punktu znajdującego się poniżej, dotyczącego infekcji narządów miednicy).
Kobiety należy zachęcać do udziału w badaniach przesiewowych szyjki macicy i piersi, odpowiednio do ich wieku.
Stany, w których system Levosert można stosować ostrożnie
System Levosert może być stosowany z ostrożnością po specjalistycznej konsultacji lub należy rozważyć usunięcie systemu, w przypadku występowania któregokolwiek z następujących stanów lub wystąpienia ich po raz pierwszy w czasie leczenia:
Produkt leczniczy Levosert należy stosować ostrożnie u kobiet z wrodzonymi wadami serca lub wadami zastawek serca, zwiększającymi ryzyko zapalenia wsierdzia.
Nieregularne krwawienia mogą maskować pewne objawy związane z występowaniem polipów lub raka endometrium, dlatego w razie ich wystąpienia należy rozważyć odpowiednie działania diagnostyczne.
Kobiety stosujące system Levosert należy zachęcać do rzucenia palenia.
Ostrzeżenia i środki ostrożności dotyczące założenia i (lub) usunięcia systemu
Informacje ogólne: Zakładaniu oraz usuwaniu systemu może towarzyszyć niewielki ból i krwawienie. W przypadku trudności przy zakładaniu i (lub) silnego bólu lub krwawienia podczas lub po założeniu systemu, należy natychmiast przeprowadzić badanie fizykalne i ultrasonograficzne w celu wykluczenia perforacji trzonu lub szyjki macicy (patrz także ”Perforacja”).
Zabieg może wywołać omdlenie na skutek reakcji wazowagalnej lub napad padaczkowy u chorych na padaczkę. W przypadku wczesnych objawów reakcji wazowagalnej, może być konieczne przerwanie zakładania lub usunięcie systemu. W celu przywrócenia przepływu krwi przez mózg, jeśli to konieczne, kobieta powinna leżeć, z obniżoną głową i z nogami uniesionymi pionowo do góry. Należy utrzymywać drożność dróg oddechowych. Utrzymująca się bradykardia może być kontrolowana przez dożylne podanie atropiny. Można podać tlen, jeśli jest dostępny.
Perforacja: Najczęściej podczas zakładania może dojść do przebicia trzonu lub szyjki macicy, przy czym fakt ten może zostać wykryty dopiero w późniejszym czasie. Może to być związane z silnym bólem lub ciągłym krwawieniem. Jeżeli podejrzewa się perforację, należy jak najszybciej usunąć system; może w tym celu być konieczne wykonanie zabiegu operacyjnego.
Częstość występowania perforacji podczas lub po założeniu produktu leczniczego Levosert wynosiła 0,1% w badaniu klinicznym, w którym nie uczestniczyły kobiety karmiące piersią.
W szeroko zakrojonym prospektywnym, porównawczym, nieinterwencyjnym badaniu kohortowym z udziałem kobiet stosujących antykoncepcję wewnątrzmaciczną (n=61448) częstość występowania perforacji wyniosła 1,3 przypadku (95% CI: 1,1–1,6) na 1000 założeń w całej kohorcie objętej badaniem, 1,4 przypadku (95% CI: 1,1–1,8) na 1000 założeń w kohorcie kobiet stosujących inny system zawierający lewonorgestrel i 1,1 przypadku (95% CI: 0,7–1,6) na 1000 założeń w kohorcie
kobiet stosujących wkładkę zawierającą miedź. W badaniu tym wykazano, że zarówno karmienie piersią podczas zakładania jak i zakładania do 36 tygodni po urodzeniu wiązały się ze zwiększonym ryzykiem perforacji (patrz tabela 1). Wspomniane czynniki ryzyka były niezależne od rodzaju zastosowanej antykoncepcji wewnątrzmacicznej.
Tabela 1: Częstość występowania perforacji na 1000 założeń w całej kohorcie ze stratyfikacją ze względu na karmienie piersią i czas, od porodu do założenia (wieloródki)
Karmienie piersią w terminie zakładania | Niekarmienie piersią w terminie zakładania | |
Założenie ≤36 tygodni po | 5,6 | 1,7 |
porodzie | (95% CI: 3,9-7,7; n=6047 założeń) | (95% CI: 0,8-3,1; n=5927 |
założeń) | ||
Założenie >36 tygodni po | 1,6 | 0,7 |
porodzie | (95% CI: 0,0-9,1; n=608 założeń) | (95% CI: 0,5-1.1; n=41910 |
założeń) |
Po wydłużeniu okresu obserwacji do 5 lat w podgrupie w niniejszym badaniu (N = 39 009 kobiet, którym założono system zawierający lewonorgestrel lub wkładkę zawierającą miedź, u 73% z tych kobiet dostępne były informacje dotyczące pełnego 5-letniego okresu obserwacji), częstość występowania perforacji wykrytej w dowolnym momencie w ciągu całego 5-letniego okresu wyniosła 2,0 (95% CI: 1,6 – 2,5) na 1000 założeń. Potwierdzono, że karmienie piersią w momencie założenia i poród w okresie 36 tygodni przed założeniem były czynnikami ryzyka również w podgrupie obserwowanej przez maksymalnie 5 lat.
Ryzyko perforacji ściany macicy może być większe w przypadku założeń poporodowych (patrz punkt 4.2), u kobiet karmiących oraz u kobiet z trwale tyłopochyloną macicą.
Ponowne badanie lekarskie powinno zostać przeprowadzone zgodnie z wytycznymi podanymi
w punkcie zatytułowanym „Badanie lekarskie” powyżej, przy czym wytyczne te należy dostosować do wskazań klinicznych u kobiet z czynnikami ryzyka perforacji.
Infekcje narządów miednicy: U kobiet stosujących wkładki zawierające miedź ryzyko zakażenia narządów miednicy jest największe w pierwszym miesiącu po założeniu, a następnie maleje.
Znanymi czynnikami ryzyka infekcji narządów miednicy są kontakty seksualne z wieloma partnerami, częste stosunki seksualne oraz młody wiek. Infekcje narządów miednicy mogą mieć poważne konsekwencje, ponieważ mogą wpływać na płodność i zwiększać ryzyko ciąży pozamacicznej. Podobnie jak w przypadku innych zabiegów ginekologicznych lub chirurgicznych, również po założeniu systemu terapeutycznego domacicznego może dojść do rozwoju ciężkiego zakażenia lub sepsy (w tym sepsy wywołanej przez paciorkowce grupy A), choć jest to niezmiernie rzadkie zjawisko.
U kobiet stosujących system Levosert, u których występują objawy przedmiotowe i podmiotowe sugerujące infekcję narządów miednicy, zaleca się wykonanie badań bakteriologicznych i obserwację, gdy wystąpią nawet nieznaczne objawy wskazujące na infekcję oraz należy wdrożyć odpowiednią antybiotykoterapię. Nie ma potrzeby usuwania systemu Levosert, o ile objawy ustąpią w ciągu następnych 72 godzin lub jeśli pacjentka poprosi o usunięcie systemu. System Levosert należy usunąć, jeśli dochodzi do nawracających infekcji błony śluzowej macicy, narządów miednicy mniejszej lub jeśli występuje ostry stan zapalny.
Komplikacje, które mogą prowadzić do niepowodzenia metody
Samoistne wydalenie systemu: W badaniach klinicznych systemów terapeutycznych domacicznych Levosert we wskazaniu do stosowania w antykoncepcji, częstość wypadania systemu była niewielka (<4% założonych systemów) i występowała w takim samym stopniu jak notowany dla innych wkładek wewnątrzmacicznych i systemów terapeutycznych domacicznych. Objawami całkowitego lub częściowego wypadnięcia systemu Levosert mogą być krwawienie lub ból. Do wydalenia systemu z jamy macicy może również dojść bez wiedzy pacjentki, co prowadzi do utraty ochrony
antykoncepcyjnej. Ponieważ Levosert zmniejsza obfitość krwawień miesiączkowych, nasilenie tych krwawień może być objawem wypadnięcia systemu.
Ryzyko wypadnięcia jest zwiększone
Należy poinformować pacjentkę o możliwych objawach wypadnięcia oraz o sposobie sprawdzenia nici systemu Levosert oraz doradzić, aby skontaktowała się z lekarzem, jeśli nitki nie są wyczuwalne. Należy stosować mechaniczne środki antykoncepcyjne (takie jak prezerwatywa) do czasu potwierdzenia lokalizacji systemu Levosert.
Częściowe wypadnięcie może zmniejszyć skuteczność działania systemu Levosert.
W przypadku częściowego wypadnięcia systemu Levosert należy go usunąć. Nowy system należy założyć od razu po usunięciu poprzedniego, pod warunkiem upewnienia się, że pacjentka nie jest w ciąży.
Brak nitek w ujściu szyjki macicy: Jeśli podczas badania kontrolnego nitki służące do usuwania systemu nie są widoczne w ujściu szyjki macicy, należy w pierwszej kolejności sprawdzić, czy pacjentka nie jest w ciąży. Nitki mogły schować się do kanału szyjki lub do jamy macicy i mogą się pojawić dopiero w czasie następnego krwawienia miesiączkowego. Jeśli nitek nie można znaleźć – mogły zerwać się, system mógł zostać wydalony, lub w rzadkich przypadkach może on znajdować się poza macicą w następstwie perforacji. W celu upewnienia się o prawidłowym umiejscowieniu systemu można wykonać badanie USG, a pacjentce należy zalecić w tym czasie stosowanie alternatywnej metody antykoncepcji. Jeśli badanie USG nie powiodło się, a jednocześnie nic nie wskazuje na samoistne wydalenie, należy przeprowadzić badanie radiologiczne jamy brzusznej w celu wykluczenia obecności systemu poza macicą.
Nieregularności w krwawieniach
Nieregularne krwawienia: Stosowanie systemu Levosert powoduje zazwyczaj znaczną redukcję krwawienia miesiączkowego w ciągu 3 do 6 miesięcy leczenia. Obfite krwawienie miesiączkowe lub nieoczekiwane krwawienie może wskazywać na wydalenie systemu. Jeżeli utrzymuje się krwotok miesiączkowy, kobietę należy ponownie zbadać. Ocenę jamy macicy należy wykonać za pomocą badania ultrasonograficznego. Należy rozważyć również biopsję endometrium.
Ryzyko u kobiet przed menopauzą
Ponieważ nieregularne krwawienia i (lub) plamienia mogą wystąpić w pierwszych miesiącach leczenia u kobiet przed menopauzą, przed założeniem systemu Levosert należy sprawdzić, czy nie występują stany patologiczne endometrium.
Kiedy należy sprawdzić, czy kobiety w wieku rozrodczym nie są w ciąży: Należy wziąć pod uwagę możliwość ciąży, jeśli miesiączka nie wystąpiła w ciągu 6 tygodni od początku poprzedniego krwawienia. Należy również wykluczyć wydalenie systemu. Nie ma potrzeby powtórzenia testu ciążowego u niemiesiączkujących kobiet, o ile nie występują inne objawy. U kobiet w wieku rozrodczym, skąpe krwawienie i (lub) brak krwawienia może pojawiać się stopniowo u około 20% pacjentek, które stosują produkt leczniczy Levosert.
Porada dotycząca leczenia krwotoku miesiączkowego: Stosowanie systemu Levosert powoduje zazwyczaj znaczną redukcję krwawienia miesiączkowego w ciągu 3 do 6 miesięcy leczenia. Jeżeli w tym czasie nie zostanie istotnie zmniejszona utrata krwi, należy rozważyć alternatywne sposoby leczenia.
Inne zagrożenia związane ze stosowaniem
Ciąża pozamaciczna: Bezwzględne ryzyko ciąży pozamacicznej u pacjentek stosujących system terapeutyczny domaciczny zawierający lewonorgestrel jest małe. Jednak, jeśli kobieta zajdzie w ciążę po umieszczeniu systemu Levosert w macicy, względne ryzyko ciąży pozamacicznej jest zwiększone. Należy wziąć pod uwagę prawdopodobieństwo ciąży pozamacicznej w przypadku wystąpienia bólu w podbrzuszu, szczególnie, gdy towarzyszy on zatrzymaniu krwawienia miesiączkowego lub pojawieniu się krwawień u kobiet niemiesiączkujących.
W przeprowadzonym badaniu klinicznym, ogólna częstość występowania ciąż pozamacicznych podczas stosowania systemu Levosert wynosiła około 0,12 na 100 kobieto-lat. Kobiety rozważające zastosowanie systemu Levosert powinny zostać poinformowane na temat objawów podmiotowych, objawów przedmiotowych i zagrożeń związanych z ciążą pozamaciczną. U kobiet, które zaszły
w ciążę podczas stosowania systemu Levosert, należy brać pod uwagę możliwość ciąży
pozamacicznej i przeprowadzić odpowiednią diagnostykę w tym kierunku.
U kobiet z przebytą ciążą pozamaciczną, po zabiegach chirurgicznych w obrębie jajowodów lub
z zakażeniem narządów miednicy mniejszej zwiększa się ryzyko wystąpienia ciąży pozamacicznej. Nie jest znane ryzyko wystąpienia ciąży pozamacicznej u kobiet z przebytą ciążą pozamaciczną, które stosują system Levosert. Prawdopodobieństwo wystąpienia ciąży pozamacicznej należy rozważyć
w przypadku wystąpienia bólu w podbrzuszu, szczególnie w powiązaniu z brakiem krwawienia miesiączkowego lub jeśli krwawienie pojawi się u kobiet niemiesiączkujących. Ciąża pozamaciczna może wymagać przeprowadzenia zabiegu chirurgicznego i może wiązać się z utratą płodności.
Torbiele jajników: Cykle owulacyjne z pęknięciem pęcherzyka jajnikowego występują zazwyczaj
u kobiet w wieku rozrodczym. Czasami atrezja pęcherzyka jest opóźniona i folikulogeneza może być kontynuowana. Tych powiększonych pęcherzyków nie można rozróżnić klinicznie od torbieli jajnika. W większości przypadków pęcherzyki te nie dają żadnych objawów, czasem jednak mogą powodować ból w obrębie miednicy lub ból w czasie stosunku.
W badaniu klinicznym z zastosowaniem systemu Levosert, w którym uczestniczyło 280 kobiet
z nadmiernymi krwawieniami miesiączkowymi, spośród których 141 stosowało system Levosert, występowanie torbieli jajników (objawowych i bezobjawowych) zgłaszano u 9,9% pacjentek w ciągu 12 miesięcy od założenia systemu. W badaniu klinicznym systemu Levosert, w którym uczestniczyło 1751 pacjentek, objawowe torbiele jajników występowały u około 4,5% kobiet używających systemu Levosert przez ponad 6 lat oraz u 0,3% kobiet, które zaprzestały stosowania systemu Levosert z powodu torbieli jajników.
W większości przypadków powiększone torbiele jajników zanikają samoistnie w ciągu dwóch do
trzech miesięcy obserwacji. Jeśli to nie nastąpi, zaleca się regularne badania kontrolne USG
i wdrożenie postępowania diagnostyczno-leczniczego. Rzadko konieczne jest leczenie chirurgiczne.
Obniżony nastrój i depresja to dobrze znane działania niepożądane stosowania hormonalnych środków antykoncepcyjnych (patrz punkt 4.8). Depresja może mieć ciężki przebieg i jest dobrze znanym czynnikiem ryzyka zachowań samobójczych i samobójstw. Jeśli u pacjentki wystąpią zmiany nastroju lub objawy depresji, również krótko po rozpoczęciu leczenia, zaleca się, aby skonsultowała się z lekarzem.
Rak piersi
Ryzyko u kobiet przed menopauzą
W metaanalizie 54 badań epidemiologicznych wykazano, że u kobiet przyjmujących złożone doustne środki antykoncepcyjne, głównie stosujących złożone doustne środki antykoncepcyjne zawierające estrogen i progestagen, nieznacznie zwiększa się względne ryzyko (ang. Relative Risk, RR = 1,24) zachorowania na raka piersi. To zwiększone ryzyko stopniowo zanika w ciągu 10 lat od zaprzestania stosowania złożonego doustnego środka antykoncepcyjnego. Ponieważ rak piersi występuje rzadko
u kobiet w wieku poniżej 40 lat, zwiększenie liczby rozpoznanych przypadków tej choroby u kobiet stosujących obecnie lub w przeszłości złożone doustne środki antykoncepcyjne jest niewielkie wobec ryzyka raka piersi w czasie całego życia.
Ryzyko wystąpienia raka piersi u pacjentek stosujących środki antykoncepcyjne zawierające tylko progestagen (tabletki antykoncepcyjne zawierające tylko progestagen, implanty i zastrzyki), w tym system Levosert, jest prawdopodobnie podobne do tego, które związane jest ze stosowaniem złożonych doustnych środków antykoncepcyjnych. Jednakże, dla środków antykoncepcyjnych zawierających tylko progestagen, dowody dotyczą znacznie mniejszej liczby pacjentek i są mniej rozstrzygające niż w przypadku złożonych doustnych środków antykoncepcyjnych.
Tolerancja glukozy: Ponieważ małe dawki lewonorgestrelu mogą wpływać na tolerancję glukozy,
u kobiet chorujących na cukrzycę stosujących system Levosert należy kontrolować stężenie glukozy
we krwi.
Antykoncepcja postkoitalna: produkt leczniczy Levosert nie jest wskazany do stosowania jako
postkoitalny środek antykoncepcyjny.
Rama w kształcie litery T systemu Levosert zawiera siarczan baru, dzięki czemu system jest widoczny podczas obrazowania rentgenowskiego.
Metabolizm progestagenów może być zwiększony podczas jednoczesnego stosowania substancji znanych jako indukujące enzymy metabolizujące produkty lecznicze, szczególnie enzymy cytochromu P450, takie jak produkty lecznicze przeciwdrgawkowe (np. fenobarbital, fenytoina, karbamazepina) oraz przeciwzakaźne (np. gryzeofulwina, ryfampicyna, ryfabutyna, newirapina, efawirenz). Z drugiej strony, substancje znane jako hamujące enzymy metabolizujące produkty lecznicze (np. itrakonazol, ketokonazol) mogą zwiększać stężenie lewonorgestrelu w surowicy. Nie jest znany wpływ wyżej wymienionych produktów leczniczych na skuteczność antykoncepcyjną, ale nie uważa się go za szczególnie istotny ze względu na miejscowy mechanizm działania systemu Levosert.
Stosowanie systemu Levosert jest przeciwwskazane w czasie ciąży lub w razie podejrzenia, że pacjentka jest w ciąży. Jeśli pacjentka zaszła w ciążę pomimo założonego systemu Levosert (patrz punkt 5), należy upewnić się, że pacjentka nie jest w ciąży pozamacicznej (patrz punkt 4.4) i usunąć system tak szybko, jak to możliwe, ponieważ może być zwiększone ryzyko komplikacji w ciąży (poronienie, przedwczesny poród, infekcja, sepsa). Usuwanie systemu Levosert lub badanie jamy macicy może również doprowadzić do samoistnego poronienia. Jeśli systemu nie można usunąć z jamy macicy lub jeśli pacjentka chce utrzymać ciążę, pacjentkę należy poinformować o ryzyku.
Następnie taką ciążę należy prowadzić pod szczególną kontrolą lekarza. Pacjentkę należy poinformować, że wszelkie objawy sugerujące komplikacje ciąży, np. ściskający ból brzucha z gorączką, należy natychmiast zgłosić lekarzowi.
Miejscowa ekspozycja na lewonorgestrel
Ponadto nie można wykluczyć zwiększonego ryzyka wirylizacji płodów żeńskich z powodu wewnątrzmacicznego narażenia na działanie lewonorgestrelu. Odnotowano pojedyncze przypadki maskulinizacji zewnętrznych narządów płciowych płodów żeńskich w następstwie miejscowego narażenia na lewonorgestrel podczas ciąży z założonym systemem terapeutycznym domacicznym uwalniającym lewonorgestrel.
Po zastosowaniu systemu terapeutycznego domacicznego zawierającego lewonorgestrel, lewonorgestrel jest wydzielany w bardzo małych ilościach do mleka matki. Ponieważ nie stwierdzono żadnego ryzyka dla dziecka, podczas stosowania systemu Levosert można kontynuować karmienie piersią.
Podczas stosowania systemu terapeutycznego domacicznego zawierającego lewonorgestrel u kobiet karmiących piersią, rzadko występowały krwawienia z macicy.
Stosowanie systemu terapeutycznego domacicznego zawierającego lewonorgestrel nie wpływa na
płodność kobiety po jego usunięciu.
Produkt leczniczy Levosert nie wpływa na zdolność prowadzenia pojazdów i obsługiwania maszyn.
Działania niepożądane obserwuje się najczęściej w pierwszych miesiącach po założeniu systemu i przemijają podczas stosowania z upływem czasu.
Bardzo częste działania niepożądane (występujące u ponad 10% pacjentek) obejmują: krwawienia
z pochwy i (lub) macicy, takie jak: plamienia, skąpe krwawienia lub jego brak (patrz punkt 5.1) oraz
łagodne torbiele jajników.
Określenie częstości występowania łagodnych torbieli jajnika zależało od zastosowanej metody diagnostycznej. W badaniach klinicznych, u 12% pacjentek stosujących system terapeutyczny domaciczny zawierający lewonorgestrel, obserwowano powiększone pęcherzyki jajnikowe, jednak większość z nich nie dawała objawów i zanikała w okresie trzech miesięcy.
W tabeli poniżej przedstawiono działania niepożądane według klasyfikacji układów i narządów MedDRA (MedDRA SOCs). Częstość występowania jest oparta na danych z badań klinicznych.
Klasyfikacja układów i narządów | Działania niepożądane | |||
Bardzo często: ≥ 1/10 | Często: ≥ 1/100 do 1 < 10 | Niezbyt często: ≥ 1/1000 do 1 < 100 | Rzadko: ≥ 1/10000 do 1 < 1000 | |
Zakażenia i zarażenia pasożytnicze | Zakażenia bakteryjne pochwy, zakażenia grzybicze pochwy i sromu | |||
Zaburzenia układu immunologicznego | Nadwrażliwość, w tym wysypka, pokrzywka i obrzęk naczynioruchowy | |||
Zaburzenia psychiczne | Nastroje depresyjne, nerwowość, zmniejszone libido | |||
Zaburzenia układu nerwowego | Ból głowy, migrena, stan przedomdleniowy | Omdlenia | ||
Zaburzenia naczyniowe | Zawroty głowy | |||
Zaburzenia żołądka i jelit | Ból brzucha i (lub) dyskomfort w jamie brzusznej, nudności, wzdęcia brzucha, wymioty | |||
Zaburzenia skóry i tkanki podskórnej | Trądzik | Łysienie, hirsutyzm, świąd, wyprysk, ostuda i (lub) nadmierna pigmentacja skóry | Wysypka, pokrzywka | |
Zaburzenia mięśniowo- szkieletowe i tkanki łącznej | Ból pleców | |||
Zaburzenia układu rozrodczego i piersi | Krwawienia z macicy i (lub) pochwy, w tym plamienie, skąpe miesiączki, brak miesiączki, łagodne torbiele jajników | Ból w miednicy, bolesne miesiączkowanie, upławy, zapalenie sromu i pochwy, tkliwość piersi, ból piersi, dyspareunia, kurcze macicy | Perforacja macicy* Choroby zapalne miednicy, zapalenie błony śluzowej trzonu macicy, zapalenie szyjki macicy, rozmaz normalny klasy II Papanicolaou | |
Ciąża, połóg i okres okołoporodowy | Ciąża pozamaciczna | |||
Zaburzenia ogólne i stany w miejscu podania | Ból podczas zakładania systemu, krwawienie podczas zakładania systemu | Wypadnięcie systemu wewnątrzmacicz nego | Obrzęk | |
Badania diagnostyczne | Wzrost masy ciała |
* Podana częstość oparta została na szeroko zakrojonym, prospektywnym, porównawczym, nieinterwencyjnym badaniu kohortowym z udziałem kobiet stosujących antykoncepcję wewnątrzmaciczną, w którym wykazano, że karmienie piersią w czasie zakładania antykoncepcji wewnątrzmacicznej oraz zakładanie antykoncepcji wewnątrzmacicznej do 36 tygodnia po porodzie są niezależnymi czynnikami ryzyka perforacji (patrz punkt 4.4). W badaniach klinicznych z antykoncepcją wewnątrzmaciczną z lewonorgestrelem, z których wykluczono kobiety karmiące piersią, częstość perforacji została określona jako „rzadka”.
Zakażenia i zarażenia pasożytnicze
Po założeniu systemu terapeutycznego domacicznego opisywano przypadki sepsy (w tym sepsy
wywołanej przez paciorkowce z grupy A) (patrz punkt 4.4).
Ciąża, połóg i okres okołoporodowy
Jeśli kobieta zajdzie w ciążę po umieszczeniu systemu Levosert w macicy, względne prawdopodobieństwo ciąży pozamacicznej jest zwiększone (patrz punkt „Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania” i „Wpływ na płodność, ciążę i laktację”).
Zaburzenia układu rozrodczego i piersi
U kobiet stosujących domaciczny system terapeutyczny zawierający lewonorgestrel, zgłaszano przypadki raka piersi (częstość nieznana, patrz punkt 4.4).
Następujące reakcje niepożądane zgłaszano jako mające związek z procedurą założenia lub usunięcia systemu Levosert: ból, krwawienie oraz związana z założeniem systemu reakcja wazowagalna z zawrotami głowy i omdleniami (patrz punkt 4.4). Procedura może również wywołać drgawki u pacjentek z padaczką.
Zgłaszanie podejrzewanych działań niepożądanych
Po dopuszczeniu produktu leczniczego do obrotu istotne jest zgłaszanie podejrzewanych działań niepożądanych. Umożliwia to nieprzerwane monitorowanie stosunku korzyści do ryzyka stosowania produktu leczniczego. Osoby należące do fachowego personelu medycznego powinny zgłaszać wszelkie podejrzewane działania niepożądane za pośrednictwem Departamentu Monitorowania Niepożądanych Działań Produktów Leczniczych Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych
Al. Jerozolimskie 181C
PL-02 222 Warszawa
Tel.: + 48 22 49 21 301
Faks: + 48 22 49 21 309
Strona internetowa: https://smz.ezdrowie.gov.pl
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Grupa farmakoterapeutyczna: Wewnątrzmaciczne środki antykoncepcyjne, plastikowy system
terapeutyczny domaciczny z progestagenem, kod ATC: G02BA03
Lewonorgestrel jest progestagenem szeroko stosowanym w ginekologii: jako składnik progestagenowy w doustnych środkach antykoncepcyjnych, w hormonalnej terapii zastępczej bądź samodzielnie w antykoncepcji progestagenowej doustnej (minitabletki) lub implantach podskórnych. Lewonorgestrel może być także podawany bezpośrednio do jamy macicy w postaci systemu terapeutycznego domacicznego uwalniającego hormon. Metoda ta pozwala na stosowanie bardzo małej dawki dobowej, gdyż hormon uwalniany jest bezpośrednio do narządu docelowego.
Mechanizm działania systemu terapeutycznego domacicznego zawierającego lewonorgestrel opiera się głównie na działaniu hormonalnym, co powoduje następujące zmiany:
Fizyczna obecność systemu w macicy może również wywierać niewielki wpływ na działanie
antykoncepcyjne.
Skuteczność kliniczna
Badanie dotyczące antykoncepcji
Po założeniu systemu zgodnie z instrukcją, produkt leczniczy Levosert zapewnia ochronę antykoncepcyjną. Skuteczność antykoncepcyjną systemu Levosert oceniano w dużym badaniu klinicznym. Całkowity odsetek występowania ciąży, obliczony jako wskaźnik Pearla, u kobiet
w wieku od 16 do 35 lat (włącznie) wynosił 0,15 (95% CI: 0,02, 0,55) pod koniec pierwszego roku oraz 0,18 (95% CI: 0,08, 0,33) pod koniec szóstego roku. Po upływie jednego roku u 19% kobiet stosujących Levosert wystąpił brak miesiączkowania, u 27% pod koniec drugiego roku stosowania, u 37% pod koniec trzeciego roku, u 37% pod koniec czwartego roku i u 40% do końca piątego roku oraz u 40% pod koniec szóstego roku użytkowania.
Zapobieganie wzrostowi śluzówki macicy to najbardziej prawdopodobny mechanizm działania domacicznego systemu terapeutycznego zawierającego lewonorgestrel w zmniejszaniu utraty krwi w przypadku idiopatycznego nadmiernego krwawienia miesiączkowego.
Nadmierne krwawienie miesiączkowe
W badaniu klinicznym z udziałem kobiet z nadmiernym krwawieniem miesiączkowym (≥80 ml
w ciągu jednego cyklu miesiączkowego), stosowanie systemu Levosert związane było ze znaczącym zmniejszeniem utraty krwi spowodowanej miesiączką w ciągu 3 do 6 miesięcy od rozpoczęcia leczenia. Objętość krwawienia miesiączkowego zmniejszyła się o 88% u kobiet z nadmiernym krwawieniem miesiączkowym po 3 miesiącach stosowania, natomiast podczas całego badania (12 miesięcy) utrzymywało się zmniejszenie krwawienia o 82%.W przypadku nadmiernych krwawień wywołanych przez włókniaki podśluzówkowe skuteczność leczenia może być mniejsza. Zmniejszone krwawienie przyczynia się do wzrostu poziomu hemoglobiny we krwi u pacjentek,
u których występują nadmierne krwawienia miesiączkowe.
W warunkach in vivo, początkowa szybkość uwalniania lewonorgestrelu z systemu Levosert wynosząca 20,1 mikrogramów/dobę spada do 17,5 mikrogramów/dobę podczas pierwszego roku, oraz 8,6 mikrogramów/dobę podczas szóstego roku. Lewonorgestrel jest uwalniany bezpośrednio do jamy macicy, a jego stężenie w osoczu jest małe (252 ± 123 pg/ml siedem dni po założeniu systemu oraz 93
± 45 pg/ml po sześciu latach), co powoduje jedynie nieznaczne działanie ogólnoustrojowe. Farmakokinetyka lewonorgestrelu była szeroko badana i opisywana w literaturze. Okres półtrwania został oszacowany na 20 godzin, chociaż niektóre badania wykazały znacznie krótszy - 9 godzin, a inne dłuższy - 80 godzin. Inną ważną obserwacją, choć jest ona zgodna z doświadczeniami dotyczącymi innych syntetycznych steroidów, są znaczne różnice w tempie klirensu metabolicznego wśród badanych osób, nawet gdy lewonorgestrel został podany drogą dożylną. Lewonorgestrel silnie wiąże się z białkami (głównie z globuliną wiążącą hormony płciowe [SHBG]) i jest intensywnie metabolizowany do wielu nieaktywnych metabolitów.
Niekliniczne badania nad bezpieczeństwem nie wykazały znaczącego ryzyka dla ludzi poza informacjami zawartymi w innych punktach Charakterystyki Produktu Leczniczego. Dane te pochodzą z konwencjonalnych badań farmakologicznych dotyczących bezpieczeństwa, toksyczności wielokrotnego podania, genotoksyczności, potencjału rakotwórczego i toksycznego wpływu na reprodukcję i rozwój.
Polidimetylosiloksan (PDMS) zbiornik Polidimetylosiloksan (PDMS) membrana
Rama w kształcie litery T z polietylenu z dodatkiem 20-24 % baru siarczanu Nić z polipropylenu
Ftalocyjanina miedzi, niebieska
5 lat.
Przechowywać w oryginalnym opakowaniu. Przechowywać blister w zewnętrznym kartoniku w celu ochrony przed światłem.
Jeden domaciczny system terapeutyczny zawierający lewonorgestrel jest pakowany w termicznie ukształtowany blister z poliestru ze zdzieralnym wieczkiem z polietylenu-Tyvek.
do stosowania
Ponieważ technika zakładania systemu różni się od techniki zakładania wkładek wewnątrzmacicznych, należy położyć szczególny nacisk na szkolenie dotyczące prawidłowej techniki zakładania. Specjalne instrukcje dotyczące zakładania systemu znajdują się w opakowaniu.
System Levosert jest dostarczany w sterylnym opakowaniu, które należy otworzyć tuż przed założeniem systemu. Każdy system powinien być zakładany w warunkach aseptycznych.
W przypadku uszkodzenia sterylnego opakowania system należy wyrzucić zgodnie z lokalnymi przepisami dotyczącymi odpadów medycznych. W ten sam sposób należy postąpić z usuniętym systemem Levosert i aplikatorem. Zewnętrzne opakowanie tekturowe i wewnętrzne opakowanie typu blister można potraktować jako zwykłe odpady.
GEDEON RICHTER POLSKA Sp. z o.o.
ul. Ks. J. Poniatowskiego 5 05-825 Grodzisk Mazowiecki
21336
Data wydania pierwszego pozwolenia na dopuszczenie do obrotu: 17.07.2013 r.
Data przedłużenia pozwolenia: 03.12.2018 r.
CHARAKTERYSTYKI PRODUKTU LECZNICZEGO
24.06.2022 r.











