Spis treści:
- NAZWA PRODUKTU LECZNICZEGO
- SKŁAD JAKOŚCIOWY I ILOŚCIOWY
- POSTAĆ FARMACEUTYCZNA
- SZCZEGÓŁOWE DANE KLINICZNE
- WŁAŚCIWOŚCI FARMAKOLOGICZNE
- DANE FARMACEUTYCZNE
- PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA
- NUMER(-Y) POZWOLENIA(Ń) NA DOPUSZCZENIE DO OBROTU
- DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU I DATA PRZEDŁUŻENIA POZWOLENIA
- DATA ZATWIERDZENIA LUB CZĘŚCIOWEJ ZMIANY TEKSTU
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
NAZWA PRODUKTU LECZNICZEGO
SKŁAD JAKOŚCIOWY I ILOŚCIOWY
POSTAĆ FARMACEUTYCZNA
SZCZEGÓŁOWE DANE KLINICZNE
Wskazania do stosowania
Dawkowanie i sposób podawania
Przeciwwskazania
Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania
Interakcje z innymi produktami leczniczymi i inne rodzaje interakcji
Wpływ na płodność, ciążę i laktację
Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn
Działania niepożądane
Przedawkowanie
WŁAŚCIWOŚCI FARMAKOLOGICZNE
Właściwości farmakodynamiczne
Właściwości farmakokinetyczne
Przedkliniczne dane o bezpieczeństwie
DANE FARMACEUTYCZNE
Wykaz substancji pomocniczych
Niezgodności farmaceutyczne
Okres ważności
Specjalne środki ostrożności podczas przechowywania
Rodzaj i zawartość opakowania
Specjalne środki ostrożności dotyczące usuwania
PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA
NUMER(-Y) POZWOLENIA(Ń) NA DOPUSZCZENIE DO OBROTU
DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU I DATA PRZEDŁUŻENIA POZWOLENIA
DATA ZATWIERDZENIA LUB CZĘŚCIOWEJ ZMIANY TEKSTU
Febuxostat MSN, 80 mg, tabletki powlekane
Każda tabletka zawiera 80 mg febuksostatu (w postaci febuksostatu półwodnego). Substancje pomocnicze o znanym działaniu:
Każda tabletka zawiera 76,50 mg laktozy (jednowodnej).
Każda tabletka zawiera 4,77 mg sodu.
Pełny wykaz substancji pomocniczych, patrz punkt 6.1.
Tabletka powlekana.
Żółte, w kształcie kapsułki (około 17 mm długości i 6 mm szerokości), obustronnie wypukłe (około 5 mm grubości) tabletki powlekane z wytłoczonym po jednej stronie symbolem „80” i gładkie po drugiej stronie.
Leczenie przewlekłej hiperurykemii w chorobach, w których wystąpiło już odkładanie się złogów moczanowych (w tym guzki dnawe i (lub) zapalenie stawów dnawe czynne lub w wywiadzie).
Ten produkt leczniczy jest wskazany do stosowania u dorosłych.
Dawkowanie
Zalecana doustna dawka febuksostatu to 80 mg raz na dobę, niezależnie od spożycia posiłku. Jeśli po 2-4 tygodniach leczenia stężenie kwasu moczowego w surowicy krwi jest > 6 mg/dl (357 μmol/l), można rozważyć zastosowanie febuksostatu w dawce 120 mg raz na dobę.
Działanie febuksostatu jest na tyle szybkie, że umożliwia kontrolę stężenia kwasu moczowego w surowicy po 2 tygodniach. Celem terapeutycznym jest zmniejszenie i utrzymanie stężenia kwasu moczowego w surowicy krwi na poziomie poniżej 6 mg/dl (357 μmol/l).
Zaleca się profilaktykę przeciw zaostrzeniom dny moczanowej przez co najmniej 6 miesięcy (patrz punkt 4.4.).
Osoby w wieku podeszłym
Nie jest wymagana modyfikacja dawki produktu u osób w podeszłym wieku (patrz punkt 5.2).
Zaburzenia czynności nerek
Skuteczność i bezpieczeństwo stosowania nie zostały w pełni ocenione u pacjentów z ciężkimi zaburzeniami czynności nerek (klirens kreatyniny <30 ml/min, patrz punkt 5.2).
Nie ma konieczności modyfikacji dawki produktu u pacjentów z łagodnymi lub umiarkowanymi zaburzeniami czynności nerek.
Zaburzenia czynności wątroby
Skuteczność i bezpieczeństwo stosowania febuksostatu nie zostały zbadane u pacjentów z ciężkimi zaburzeniami czynności wątroby (klasa C wg Childa-Pugha).
Zalecana dawka u pacjentów z łagodnymi zaburzeniami wątroby to 80 mg. Dostępne są ograniczone informacje dotyczące pacjentów z umiarkowanymi zaburzeniami czynności wątroby.
Dzieci i młodzież
Nie ustalono bezpieczeństwa stosowania i skuteczności febuksostatu u dzieci w wieku poniżej 18 lat. Brak jest dostępnych danych.
Sposób podawania Podanie doustne
Febuxostat MSN należy przyjmować doustnie i można go przyjmować z jedzeniem lub bez jedzenia.
Nadwrażliwość na substancję czynną lub na którąkolwiek substancję pomocniczą wymienioną w
punkcie 6.1 (patrz również punkt 4.8).
Zaburzenia sercowo-naczyniowe
Podczas opracowywania produktu oraz w jednym badaniu po dopuszczeniu do obrotu (CARES) u pacjentów z istniejącymi uprzednio ciężkimi chorobami układu sercowo-naczyniowego (np. zawał mięśnia sercowego, udar lub niestabilna dławica piersiowa), leczonych febuksostatem obserwowano większą liczbę zgonów z przyczyn sercowo-naczyniowych w porównaniu do pacjentów leczonych allopurynolem.
Jednakże w kolejnym badaniu po dopuszczeniu do obrotu (FAST), odsetek występowania zdarzeń sercowo-naczyniowych zarówno nie prowadzących do zgonu jak i prowadzących do zgonu był podobny w przypadku febuksostatu oraz allopurynolu.
Leczenie w tej grupie pacjentów należy prowadzić z zachowaniem ostrożności i regularnie ich monitorować.
Bardziej szczegółowe informacje dotyczące bezpieczeństwa sercowo-naczyniowego febuksostatu znajdują się w punkcie 4.8 i punkcie 5.1.
Alergia i (lub) nadwrażliwość na produkt leczniczy
Po wprowadzeniu produktu do obrotu odnotowano rzadkie przypadki wystąpienia ciężkich reakcji alergicznych i (lub) nadwrażliwości, w tym zagrażającego życiu zespołu Stevensa-Johnsona, toksycznego martwiczego oddzielania się naskórka oraz ostrych reakcji anafilaktycznych i (lub) wstrząsu. W większości przypadków reakcje te występowały podczas pierwszych miesięcy leczenia febuksostatem. U niektórych pacjentów (nie u wszystkich) wcześniej występowały zaburzenia czynności nerek i (lub) nadwrażliwość na allopurynol. Ciężkie reakcje nadwrażliwości, w tym reakcja polekowa z eozynofilią i objawami ogólnymi (ang. DRESS - Drug Reaction with Eosinophilia and Systemic Symptoms) były w niektórych przypadkach związane z gorączką, zaburzeniami hematologicznymi, zaburzeniami czynności nerek lub wątroby.
Pacjentów należy poinformować o objawach przedmiotowych i podmiotowych oraz ściśle monitorować w kierunku wystąpienia objawów reakcji alergicznych i (lub) reakcji nadwrażliwości (patrz punkt 4.8). Leczenie febuksostatem należy natychmiast przerwać w razie wystąpienia ciężkich reakcji alergicznych i (lub) nadwrażliwości, w tym zespołu Stevensa-Johnsona, ponieważ wczesne
odstawienie produktu jest związane z lepszym rokowaniem. Jeżeli u pacjenta wystąpiła reakcja alergiczna i (lub) nadwrażliwości, w tym zespół Stevensa-Johnsona i ostra reakcja anafilaktyczna i (lub) wstrząs, ponowne leczenie febuksostatem u tego pacjenta jest niedopuszczalne.
Ostre napady dny (zaostrzenie dny moczanowej)
Leczenia febuksostatem nie należy rozpoczynać do chwili całkowitego ustąpienia ostrego napadu dny moczanowej. Zaostrzenie dny moczanowej może wystąpić w trakcie rozpoczynania leczenia wskutek zmian stężenia kwasu moczowego w surowicy, wynikających z uwolnienia moczanu ze złogów w tkankach (patrz punkty 4.8 i 5.1). Podczas rozpoczynania leczenia febuksostatem zaleca się profilaktykę lekami z grupy NLPZ lub kolchicyną przeciw zaostrzeniom dny moczanowej przez co najmniej 6 miesięcy (patrz punkt 4.2).
W razie wystąpienia zaostrzenia dny w trakcie leczenia febuksostatem, produktu nie należy odstawiać. Zaostrzenie dny moczanowej można równocześnie leczyć w sposób odpowiedni dla danego pacjenta. Stałe leczenie febuksostatem zmniejsza częstość i nasilenie zaostrzeń dny.
Odkładanie się złogów ksantyny
U pacjentów ze znacznie przyspieszonym tempem wytwarzania moczanu (np. nowotwór złośliwy i leczenie przeciwnowotworowe, zespół Lescha-Nyhana) bezwzględne stężenie ksantyny w moczu może w rzadkich przypadkach wzrosnąć na tyle, że możliwe będzie odkładanie się jej złogów w drogach moczowych. Ze względu na brak doświadczenia dotyczącego febuksostatu, nie zaleca się stosowania produktu w tych populacjach.
Merkaptopuryna/azatiopryna
Nie zaleca się stosowania febuksostatu u pacjentów leczonych równocześnie merkaptopuryną/ azatiopryną, ponieważ hamowanie oksydazy ksantynowej przez febuksostat może powodować zwiększenie stężenia merkaptopuryny/azatiopryny w osoczu, co może prowadzić do poważnej toksyczności.
Jeśli nie można uniknąć równoczesnego stosowania obu tych leków, zaleca się zmniejszenie dawki merkaptopuryny/azatiopryny do 20% lub mniej wcześniej zalecanej dawki, w celu uniknięcia możliwych reakcji hematologicznych (patrz punkty 4.5 i 5.3).
Pacjentów należy ściśle monitorować, a następnie należy skorygować dawkę merkaptopuryny/azatiopryny na podstawie oceny odpowiedzi terapeutycznej i wystąpienia ewentualnych objawów toksycznych.
Pacjenci po przeszczepach narządów
Ponieważ brak doświadczenia dotyczącego stosowania produktu u pacjentów po przeszczepach narządów, nie zaleca się stosowania febuksostatu u takich pacjentów (patrz punkt 5.1).
Teofilina
U zdrowych ochotników jednoczesne podanie febuksostatu w dawce 80 mg i pojedynczej dawki 400 mg teofiliny nie wykazało jakiejkolwiek interakcji farmakokinetycznej (patrz punkt 4.5). Febuksostat w dawce 80 mg może być stosowany u pacjentów leczonych równocześnie teofiliną bez ryzyka wystąpienia podwyższenia stężenia teofiliny w osoczu. Brak danych dla febuksostatu w dawce 120 mg.
Zaburzenia wątroby
W trakcie połączonych badań klinicznych fazy 3 zaobserwowano łagodne zaburzenia w testach czynnościowych wątroby u pacjentów leczonych febuksostatem (5,0%). Wykonanie testu czynnościowego wątroby jest zalecane przed rozpoczęciem leczenia febuksostatem, a następnie okresowo w oparciu o ocenę kliniczną (patrz punkt 5.1).
Zaburzenia tarczycy
W długotrwałych, otwartych badaniach rozszerzonych zaobserwowano zwiększone stężenia TSH (>5,5 μIU/ml) u pacjentów długotrwale leczonych febuksostatem (5,5%). Konieczna jest ostrożność podczas stosowania febuksostatu u pacjentów z zaburzeniami czynności tarczycy (patrz punkt 5.1).
Laktoza i sód
Tabletki febuksostatu zawierają laktozę. Pacjenci z rzadkimi, dziedzicznie występującymi zaburzeniami, takimi jak nietolerancja galaktozy, niedobór laktazy lub zespół złego wchłaniania glukozy-galaktozy, nie powinni stosować tego produktu.
Ten produkt leczniczy zawiera mniej niż 1 mmol sodu (23 mg) w 80 mg tabletce powlekanej, to
znaczy zasadniczo „nie zawiera sodu”.
Merkaptopuryna/azatiopryna
W oparciu o mechanizm działania hamującego aktywność oksydazy ksantynowej - XO przez febuksostat, nie zaleca się jednoczesnego stosowania tych leków. Hamowanie oksydazy ksantynowej (XO) przez febuksostat może powodować zwiększenie stężenia tych leków w osoczu, co prowadzi do mielotoksyczności.
W przypadku łącznego stosowania z febuksostatem, dawkę merkaptopuryny/azatiopryny należy zmniejszyć do 20% poprzednio przepisanej dawki lub mniejszej (patrz punkty 4.4 i 5.3).
Adekwatność proponowanego dostosowania dawki, w oparciu o modele i symulowaną analizę danych z badań przedklinicznych na szczurach, została potwierdzona wynikami badania klinicznego interakcji między lekami u zdrowych ochotników otrzymujących 100 mg azatiopryny w monoterapii i zmniejszoną dawkę azatiopryny (25 mg) w połączeniu z febuksostatem (40 lub 120 mg).
Nie przeprowadzono badań interakcji febuksostatu z innymi cytotoksycznymi środkami chemioterapeutycznymi. Nie są dostępne żadne dane dotyczące bezpieczeństwa stosowania febuksostatu w trakcie innego leczenia cytotoksycznego.
Rosiglitazon/substraty CYP2C8
Wykazano, iż febuksostat jest słabym inhibitorem CYP2C8 in vitro. W badaniu, w którym wzięli udział zdrowi ochotnicy jednoczesne podanie 120 mg febuksostatu na dobę i pojedynczej dawki 4 mg rosiglitazonu doustnie nie miało wpływu na farmakokinetykę rosiglitazonu i jego metabolitu N- desmetyl rosiglitazonu, co wskazuje że febuksostat nie jest inhibitorem CYP2C8 in vivo. W związku z tym nie jest wymagana jakakolwiek zmiana dawkowania podczas jednoczesnego podawania febuksostatu i rosiglitazonu lub innych substratów CYP2C8.
Teofilina
Przeprowadzono badanie interakcji z zastosowaniem febuksostatu u zdrowych ochotników, aby ocenić czy hamowanie XO może prowadzić do wzrostu stężenia teofiliny w osoczu, tak jak zgłaszano dla innych inhibitorów XO. Wyniki badania wykazały, iż jednoczesne podanie febuksostatu w dawce 80 mg raz na dobę z pojedynczą dawką 400 mg teofiliny nie ma wpływu na farmakokinetykę lub bezpieczeństwo stosowania teofiliny. Z tego względu nie zaleca się zachowania szczególnej ostrożności w przypadku jednoczesnego podawania febuksostatu w dawce 80 mg oraz teofiliny. Brak danych dla febuksostatu w dawce 120 mg.
Naproksen i inne inhibitory glukuronidacji
Metabolizm febuksostatu zależy od enzymów glukuronylotransferaza (UGT). Produkty lecznicze, które hamują glukuronidację, takie jak leki z grupy NLPZ i probenecyd, mogą teoretycznie wpływać na eliminację febuksostatu. U zdrowych uczestników badań jednoczesne stosowanie febuksostatu i naproksenu w dawce 250 mg dwa razy na dobę było związane ze zwiększoną ekspozycją na febuksostat (Cmax 28%, AUC 41% i t1/2 26%). W badaniach klinicznych stosowanie naproksenu lub innych leków z grupy NLPZ/inhibitorów COX-2 nie było związane z żadnym klinicznie istotnym zwiększeniem częstości zdarzeń niepożądanych.
Febuksostat może być podawany jednocześnie z naproksenem bez konieczności modyfikacji dawki febuksostatu lub naproksenu.
Leki indukujące glukuronidację
Leki silnie indukujące enzymy UGT mogą potencjalnie prowadzić do zwiększenia metabolizmu i zmniejszenia skuteczności febuksostatu. Z tego względu zaleca się kontrolowanie stężenia kwasu moczowego w surowicy krwi przez 1-2 tygodnie po rozpoczęciu leczenia silnym lekiem indukującym glukuronidację. Z drugiej strony, przerwanie leczenia lekiem indukującym może doprowadzić do zwiększonych stężeń febuksostatu w osoczu.
Kolchicyna/indometacyna/hydrochlorotiazyd/warfaryna
Febuksostat może być podawany jednocześnie z kolchicyną lub indometacyną bez konieczności modyfikacji dawki febuksostatu lub drugiej równocześnie stosowanej substancji czynnej.
Nie jest wymagana modyfikacja dawki febuksostatu w przypadku jednoczesnego podawania z hydrochlorotiazydem.
Nie jest konieczna modyfikacja dawki warfaryny w przypadku jednoczesnego podawania z febuksostatem. Podawanie febuksostatu (80 mg lub 120 mg raz na dobę) jednocześnie z warfaryną nie wpływało na farmakokinetykę warfaryny u zdrowych ochotników. Wskaźnik INR i aktywność czynnika krzepnięcia VII również nie uległy zmianie po jednoczesnym podawaniu febuksostatu.
Dezypramina/substraty CYP2D6
Wykazano, że febuksostat jest słabym inhibitorem CYP2D6 in vitro. W badaniu zdrowych uczestników dawka 120 mg febuksostatu na dobę powodowała zwiększenie o 22% wartości AUC dla dezypraminy, substratu CYP2D6, wskazując na potencjalne słabe działanie hamujące febuksostatu na enzym CYP2D6 w warunkach in vivo. Z tego względu nie należy się spodziewać, że jednoczesne podawanie febuksostatu z innymi substratami CYP2D6 będzie wymagać modyfikacji dawki tych leków.
Leki zobojętniające sok żołądkowy
Wykazano, że jednoczesne zażycie leku zobojętniającego sok żołądkowy, zawierającego wodorotlenek magnezu i wodorotlenek glinu, opóźnia wchłanianie febuksostatu (o około 1 godzinę) i wywołuje zmniejszenie o 32% stężenia Cmax, natomiast nie zaobserwowano znaczącej zmiany wartości AUC. Z tego względu febuksostat można przyjmować niezależnie od stosowania leków zobojętniających sok żołądkowy.
Ciąża
Z danych otrzymanych z bardzo ograniczonej liczby przypadków stosowania produktu leczniczego w okresie ciąży nie wynika szkodliwe działanie febuksostatu na przebieg ciąży lub stan zdrowia płodu i (lub) noworodka. Badania na zwierzętach nie wykazują bezpośredniego lub pośredniego szkodliwego wpływu na przebieg ciąży, rozwój zarodka lub płodu, lub przebieg porodu (patrz punkt 5.3).
Potencjalne zagrożenie dla człowieka nie jest znane. Febuksostatu nie należy stosować w okresie ciąży.
Karmienie piersią
Nie wiadomo, czy febuksostat przenika do mleka kobiet karmiących piersią. Badania na zwierzętach wykazały przenikanie tej substancji czynnej do mleka i zaburzenia rozwoju karmionych młodych. Nie można wykluczyć ryzyka u niemowlęcia karmionego piersią. Febuksostatu nie należy stosować w okresie karmienia piersią.
Płodność
W badaniach reprodukcji u zwierząt z użyciem dawek do 48 mg/kg/dobę, nie wykazano zależnego od dawki niekorzystnego wpływu na płodność (patrz punkt 5.3). Wpływ febuksostatu na płodność u ludzi nie jest znany.
Zgłaszano związane ze stosowaniem febuksostatu reakcje niepożądane, takie jak senność, zawroty głowy, parestezje i niewyraźne widzenie. Pacjenci powinni zachować ostrożność przed podjęciem decyzji o prowadzeniu pojazdów, obsługiwania maszyn lub podejmowania niebezpiecznych czynności do chwili, gdy będą w dostatecznym stopniu pewni, że febuksostat nie wpływa niekorzystnie na ich zdolność wykonywania tych czynności.
Podsumowanie profilu bezpieczeństwa
Najczęściej zgłaszane reakcje niepożądane w badaniach klinicznych (4072 pacjentów leczonych co najmniej jedną dawką – 10 mg do 300 mg) w badaniach dotyczących bezpieczeństwa stosowania produktu leczniczego po wydaniu pozwolenia (badanie FAST: 3001 pacjentów leczonych co najmniej jedną dawką od 18 mg do 120 mg) oraz po wprowadzeniu produktu do obrotu to objawy dny moczanowej, zaburzenia czynności wątroby, biegunka, nudności, ból głowy, zawroty głowy, duszność, wysypka, świąd, ból stawów, ból mięśni, ból kończyn, obrzęk i zmęczenie. Te działania niepożądane miały przeważnie łagodne lub umiarkowane nasilenie. Po wprowadzeniu produktu do obrotu zgłaszano rzadkie przypadki reakcji nadwrażliwości na febuksostat, niektóre z nich związane były z objawami ogólnoustrojowymi oraz rzadkie przypadki nagłego zgonu z przyczyn sercowo- naczyniowych.
Tabelaryczny wykaz działań niepożądanych
Poniżej wymienione są często (≥1/100 do <1/10), niezbyt często (≥1/1000 do <1/100) i rzadko (≥1/10000 do <1/1000) występujące reakcje niepożądane, zgłaszane u pacjentów leczonych febuksostatem.
W obrębie każdej grupy o określonej częstości występowania działania niepożądane są wymienione zgodnie ze zmniejszającym się nasileniem.
Tabela 1: Działania niepożądane związane z leczeniem w badaniach klinicznych fazy 3, długotrwałych badaniach rozszerzonych, badaniach dotyczących bezpieczeństwa stosowania produktu leczniczego po wydaniu pozwolenia oraz po wprowadzeniu do obrotu
Zaburzenia krwi i układu chłonnego | Rzadko Pancytopenia, trombocytopenia, agranulocytoza*, niedokrwistość# |
Zaburzenia układu immunologicznego | Rzadko Reakcja anafilaktyczna*, nadwrażliwość na produkt* |
Zaburzenia endokrynologiczne | Niezbyt często Zwiększona aktywność TSH, niedoczynność tarczycy# |
Zaburzenia oka | Niezbyt często Niewyraźne widzenie Rzadko Niedrożność tętnicy siatkówki# |
Zaburzenia metabolizmu i odżywiania | Często*** Zaostrzenie dny moczanowej Niezbyt często Cukrzyca, hiperlipidemia, zmniejszenie apetytu, zwiększenie masy ciała Rzadko Zmniejszenie masy ciała, nasilony apetyt, jadłowstręt |
Zaburzenia psychiczne | Niezbyt często |
Zmniejszone libido, bezsenność Rzadko Nerwowość, nastrój depresyjny#, zaburzenia snu# | |
Zaburzenia układu nerwowego | Często Ból głowy, zawroty głowy Niezbyt często Parestezje, niedowład połowiczy, senność, letarg#, zaburzenia smaku, niedoczulica, osłabienie węchu Rzadko Utrata smaku#, uczucie pieczenia# |
Zaburzenia ucha i błędnika | Niezbyt często Szumy uszne Rzadko Zawroty głowy pochodzenia błędnikowego# |
Zaburzenia serca | Niezbyt często Migotanie przedsionków, kołatanie serca, nieprawidłowy zapis EKG, arytmia# Rzadko Nagły zgon z przyczyn sercowo-naczyniowych |
Zaburzenia naczyniowe | Niezbyt często Nadciśnienie tętnicze, zaczerwienienie, uderzenia gorąca Rzadko Zapaść krążeniowa# |
Zaburzenia układu oddechowego klatki piersiowej i śródpiersia | Często Duszność Niezbyt często Zapalenie oskrzeli, zakażenie górnych dróg oddechowych, infekcja dolnych dróg oddechowych#, kaszel, wodnista wydzielina z nosa# Rzadko Zapalenie płuc# |
Zaburzenia żołądka i jelit | Często Biegunka**, nudności Niezbyt często Ból brzucha, ból w górnej części brzucha#, wzdęcia, refluks żołądkowo-przełykowy, wymioty, suchość błony śluzowej jamy ustnej, niestrawność, zaparcie, częste wypróżnianie, wzdęcia z oddawaniem gazów, dyskomfort żołądkowo-jelitowy, owrzodzenie jamy ustnej, obrzęk warg#, zapalenie trzustki Rzadko Perforacja układu pokarmowego#, zapalenie jamy ustnej# |
Zaburzenia wątroby i dróg żółciowych | Często Nieprawidłowa czynność wątroby** Niezbyt często Kamica żółciowa Rzadko Zapalenie wątroby, żółtaczka*, uszkodzenie wątroby*, zapalenie pęcherzyka żółciowego# |
Zaburzenia skóry i tkanki podskórnej | Często Wysypka (w tym różne rodzaje wysypki występujące z mniejszą częstością, patrz poniżej), świąd Niezbyt często Zapalenie skóry, pokrzywka, zmiana zabarwienia skóry, uszkodzenie skóry, wybroczyny, wysypka plamkowa, wysypka |
grudkowo-plamkowa, wysypka grudkowa, nadmierne pocenie się, łysienie, wyprysk#, rumień, poty nocne#, łuszczyca#, swędząca wysypka# Rzadko Toksyczne martwicze oddzielanie się naskórka*, zespół Stevensa- Johnsona*, obrzęk naczynioruchowy*, reakcje na lek z eozynofilią i objawami ogólnoustrojowymi*, uogólniona wysypka (ciężka)*, wysypka złuszczająca, wysypka grudkowa, wysypka pęcherzykowa, wysypka krostkowa, wysypka rumieniowata, wysypka odropodobna | |
Zaburzenia mięśniowo- szkieletowe i tkanki łącznej | Często Ból stawów, ból mięśni, ból kończyn# Niezbyt często Zapalenie stawów, bóle mięśniowo-stawowe, osłabienie mięśni, kurcze mięśni, nadmierne napięcie mięśni, zapalenie kaletki, obrzęk stawów#, ból pleców, sztywność mięśniowo-stawowa#, sztywność stawów# Rzadko Rabdomioliza*, zespół stożka rotatorów#, zespół bólu wielomięśniowego# |
Zaburzenia nerek i dróg moczowych | Niezbyt często Niewydolność nerek, kamica nerkowa, krwiomocz, częstomocz, białkomocz, parcie na mocz, zakażenie dróg moczowych# Rzadko Cewkowo-śródmiąższowe zapalenie nerek* |
Zaburzenia układu rozrodczego i piersi | Niezbyt często Zaburzenia wzwodu |
Zaburzenia ogólne i stany w miejscu podania | Często Obrzęk, zmęczenie Niezbyt często Ból w klatce piersiowej, dyskomfort w klatce piersiowej, ból#, złe samopoczucie# Rzadko Pragnienie, uczucie gorąca# |
Badania diagnostyczne | Niezbyt często Zwiększenie aktywności amylazy we krwi, zmniejszenie liczby płytek krwi, zmniejszenie liczby białych krwinek, zmniejszenie liczby limfocytów, zwiększenie stężenia kreatyniny we krwi, zmniejszenie stężenia hemoglobiny, zwiększenie stężenia mocznika we krwi, zwiększenie stężenia trójglicerydów we krwi, zwiększenie stężenia cholesterolu we krwi, zmniejszenie stężenia hematokrytu, zwiększenie aktywności dehydrogenazy mleczanowej we krwi, zwiększenie stężenia potasu we krwi, zwiększenie INR# Rzadko Zwiększenie stężenia glukozy we krwi, wydłużony czas kaolinowo-kefalinowy, zmniejszenie liczby czerwonych krwinek, zwiększenie aktywności aminotransferazy alaninowej, zwiększenie aktywności fosfokinazy kreatynowej we krwi* |
Urazy, zatrucia i powikłania po zabiegach | Niezbyt często Urazy# |
* Działania niepożądane, zgłoszone po wprowadzeniu produktu leczniczego do obrotu.
** Związana z leczeniem, biegunka niezakaźna i nieprawidłowe wyniki testów czynnościowych wątroby zaobserwowane w połączonych badaniach fazy 3 są częstsze u pacjentów jednocześnie leczonych kolchicyną.
*** Patrz punkt 5.1 w celu zapoznania się z informacjami dotyczącymi częstości przypadków zaostrzenia dny moczanowej w poszczególnych randomizowanych, kontrolowanych badaniach fazy 3.
# Reakcje niepożądane związane z leczeniem w badaniach dotyczących bezpieczeństwa stosowania produktu leczniczego po wydaniu pozwolenia.
Opis wybranych działań niepożądanych
Po wprowadzeniu produktu do obrotu odnotowano rzadkie przypadki wystąpienia ciężkich reakcji nadwrażliwości, w tym zespołu Stevensa-Johnsona, toksyczne martwicze oddzielanie się naskórka i reakcji anafilaktycznych/wstrząsu, po przyjęciu febuksostatu. Zespół Stevensa-Johnsona i toksyczne martwicze oddzielanie się naskórka charakteryzują się nasilającą się wysypką skórną z pęcherzami lub uszkodzeniem błon śluzowych i podrażnieniem oczu. Reakcji nadwrażliwości na febuksostat mogą towarzyszyć następujące objawy: reakcje skórne w postaci naciekowych zmian grudkowo- plamkowych, uogólnionych lub złuszczających wysypek, uszkodzenie skóry, obrzęk twarzy, gorączka, nieprawidłowości w składzie krwi takie jak trombocytopenia i eozynofilia oraz zmiany w obrębie pojedynczych organów lub wielonarządowe (wątroba i nerki, w tym cewkowo-śródmiąższowe zapalenie nerek) (patrz punkt 4.4).
Objawy dny moczanowej obserwowano często wkrótce po rozpoczęciu leczenia i podczas pierwszych miesięcy leczenia. Następnie, częstość zaostrzeń dny moczanowej malała z upływem czasu. Zaleca się stosowanie leczenia profilaktycznego przeciw dnie (patrz punkt 4.2 i 4.4).
Zgłaszanie podejrzewanych działań niepożądanych
Po dopuszczeniu produktu leczniczego do obrotu istotne jest zgłaszanie podejrzewanych działań niepożądanych. Umożliwia to nieprzerwane monitorowanie stosunku korzyści do ryzyka stosowania produktu leczniczego. Osoby należące do fachowego personelu medycznego powinny zgłaszać wszelkie podejrzewane działania niepożądane za pośrednictwem Departamentu Monitorowania Niepożądanych Działań Produktów Leczniczych Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych: Al. Jerozolimskie 181C, 02-222 Warszawa,
tel.: + 48 22 49 21 301, faks: + 48 22 49 21 309, strona internetowa: https://smz.ezdrowie.gov.pl Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
W przypadku przedawkowania należy zastosować u pacjentów leczenie objawowe i podtrzymujące.
Grupa farmakoterapeutyczna: Produkty przeciw dnie moczanowej, leki hamujące wytwarzanie kwasu moczowego, kod ATC: M04AA03.
Mechanizm działania
Kwas moczowy jest końcowym produktem metabolizmu puryny u ludzi i jest wytwarzany w kaskadzie hipoksantyna → ksantyna → kwas moczowy. Oba etapy w powyższych transformacjach są katalizowane przez oksydazę ksantynową (XO). Febuksostat jest pochodną 2-aryltiazolu i osiąga swoje działanie terapeutyczne polegające na zmniejszeniu stężenia kwasu moczowego w surowicy krwi poprzez selektywne hamowanie XO. Febuksostat to silny, niepurynowy selektywny inhibitor XO (NP-SIXO) z wartością hamowania Ki in vitro poniżej jednego nanomola. Wykazano, że febuksostat silnie hamuje zarówno utlenione, jak i zredukowane postacie XO. W stężeniach terapeutycznych febuksostat nie hamuje innych enzymów biorących udział w metabolizmie puryny lub pirymidyny, mianowicie deaminazy guaniny, fosforybozylotransferazy hipoksantynowo-guaninowej,
fosforybozylotransferazy orotanowej, dekarboksylazy monofosforanu orotydyny lub fosforylazy nukleozydów purynowych.
Skuteczność i bezpieczeństwo stosowania
Skuteczność kliniczną febuksostatu wykazano w trzech podstawowych badaniach klinicznych 3 fazy (dwa zasadnicze badania APEX i FACT oraz dodatkowe badanie CONFIRMS opisane poniżej), które przeprowadzono z udziałem 1832 pacjentów z hiperurykemią i dną moczanową. W każdym podstawowym badaniu klinicznym 3 fazy febuksostat wykazywał się lepszą zdolnością zmniejszania i utrzymywania stężenia kwasu moczowego w surowicy krwi w porównaniu z allopurynolem.
Pierwszorzędowym punktem końcowym skuteczności w badaniach APEX i FACT był odsetek pacjentów, u których ostatnie 3 comiesięczne wyniki pomiarów stężenia kwasu moczowego w surowicy były mniejsze niż 6,0 mg/dl (357 μmol/l). W dodatkowym badaniu fazy 3 CONFIRMS, którego wyniki zostały udostępnione po uzyskaniu pierwszego pozwolenia na dopuszczenie do obrotu febuksostatu, pierwszorzędowym punktem końcowym skuteczności był odsetek pacjentów, u których wyniki pomiarów stężenia kwasu moczowego w surowicy były mniejsze niż 6,0 mg/dl podczas wizyty końcowej. Do badań tych nie włączono pacjentów po przeszczepach narządów (patrz punkt 4.2).
Badanie APEX: APEX (Allopurinol and Placebo-Controlled Efficacy Study of Febuxostat) było randomizowanym, prowadzonym metodą podwójnie ślepej próby przez okres 28 tygodni, wieloośrodkowym badaniem klinicznym 3 fazy. Dokonano randomizacji tysiąca siedemdziesięciu dwóch (1072) pacjentów: placebo (n=134), febuksostat 80 mg raz na dobę (n=267), febuksostat
120 mg raz na dobę (n=269), febuksostat 240 mg raz na dobę (n=134) lub allopurynol (300 mg raz na dobę [n=258] u pacjentów z wyjściowym stężeniem kreatyniny w surowicy ≤1,5 mg/dl lub 100 mg raz na dobę [n=10] u pacjentów z wyjściowym stężeniem kreatyniny w surowicy w zakresie >1,5 mg/dl i
≤2,0 mg/dl). Jako dawkę oceny bezpieczeństwa zastosowano dawkę 240 mg febuksostatu (2-krotność zalecanej największej dawki).
Badanie APEX wykazało statystycznie istotną przewagę zarówno febuksostatu 80 mg raz na dobę, jak i febuksostatu 120 mg raz na dobę w porównaniu z grupą otrzymującą standardowo stosowane dawki allopurynolu 300 mg (n=258) / 100 mg (n=10) w zakresie zmniejszania stężenia kwasu moczowego w surowicy poniżej 6 mg/dl (357 μmol/l) (patrz Tabela 2 i Wykres 1).
Badanie FACT: FACT (Febuxostat Allopurinol Controlled Trial) było randomizowanym, prowadzonym metodą podwójnie ślepej próby przez okres 52 tygodni, wieloośrodkowym badaniem klinicznym 3 fazy. Dokonano randomizacji siedmiuset sześćdziesięciu (760) pacjentów: febuksostat 80 mg na dobę (n=256), febuksostat 120 mg raz na dobę (n=251) lub allopurynol 300 mg raz na dobę (n=253).
Badanie FACT wykazało statystycznie istotną wyższość zarówno febuksostatu 80 mg raz na dobę, jak i febuksostatu 120 mg raz na dobę w porównaniu z grupą otrzymującą standardowo stosowaną dawkę allopurynolu 300 mg w zakresie zmniejszania i utrzymania stężenia kwasu moczowego w surowicy poniżej 6 mg/dl (357 μmol/l).
W Tabeli 2 podsumowano wyniki dla pierwszorzędowego punktu końcowego:
Tabela 2
Odsetek pacjentów ze stężeniem kwasu moczowego w surowicy <6,0 mg/dl (357 μmol/l) Ostatnie trzy comiesięczne wizyty
Badanie | Allopurynol | ||
Febuksostat | Febuksostat | 300 / | |
80 mg raz na dobę | 120 mg raz na dobę | 100 mg raz na dobę 1 | |
APEX | 48% * | 65% *, # | 22% |
(28 tygodni) | (n=262) | (n=269) | (n=268) |
FACT | 53%* | 62%* | 21% |
(52 tygodnie) | (n=255) | (n=250) | (n=251) |
Wyniki sumaryczne | 51%* | 63%*, # | 22% |
(n=517) | (n=519) | (n=519) |
1 Wyniki od pacjentów otrzymujących 100 mg/dobę (n=10: pacjenci ze stężeniem kreatyniny w surowicy >1,5 i ≤2,0 mg/dl) lub 300 mg/dobę (n=509) zostały zsumowane do analiz.
* p<0,001 w porównaniu z allopurynolem, # p<0,001 w porównaniu z dawką 80 mg
Febuksostat zmniejszał stężenia kwasu moczowego w surowicy szybko i trwale. Zmniejszenie stężenia kwasu moczowego w surowicy do wartości <6,0 mg/dl (357 μmol/l) stwierdzano do wizyty w tygodniu 2, a następnie stężenie to utrzymywało się przez cały okres leczenia. Średnie stężenia kwasu moczowego w surowicy wraz z upływem czasu dla każdej grupy leczenia w dwóch podstawowych badaniach klinicznych 3 fazy są przedstawione na Wykresie 1.
Wykres 1. Średnie stężenia kwasu moczowego w surowicy krwi – połączone wyniki z głównych badań 3 fazy
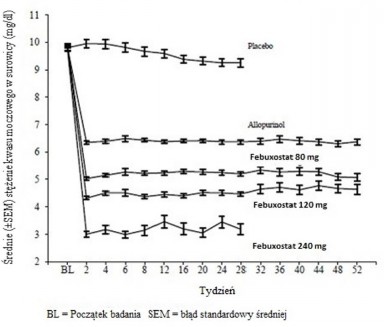
Uwaga: 509 pacjentów otrzymywało allopurynol 300 mg raz na dobę; 10 pacjentów ze stężeniem kreatyniny w surowicy w zakresie >1,5 mg/dl i ≤2,0 mg/dl otrzymywało dawkę 100 mg raz na dobę (10 pacjentów z 268 w badaniu APEX).
Dawkę 240 mg febuksostatu zastosowano w celu oceny bezpieczeństwa stosowania febuksostatu w dawce dwukrotnie większej od zalecanej maksymalnej dawki.
Badanie CONFIRMS – badanie CONFIRMS było randomizowanym, kontrolowanym badaniem klinicznym fazy 3. prowadzonym przez okres 26 tygodni, mającym na celu ocenę bezpieczeństwa stosowania i skuteczności febuksostatu w dawkach 40 mg i 80 mg w porównaniu do allopurynolu w dawce 300 mg lub 200 mg, u pacjentów z dną moczanową i hiperurykemią. Dokonano randomizacji dwóch tysięcy sześćdziesięciu dziewięciu (2269) pacjentów: febuksostat 40 mg raz na dobę (n=757), febuksostat 80 mg raz na dobę (n=756) lub allopurynol w dawce 300 mg lub 200 mg na dobę (n=756). U przynajmniej 65% pacjentów występowały łagodne do umiarkowanych zaburzenia czynności nerek (klirens kreatyniny 30-89 ml/min). Prowadzenie leczenia zapobiegającego zaostrzeniu dny moczanowej było obowiązkowe przez okres 26 tygodni.
Odsetek pacjentów ze stężeniem kwasu moczowego w surowicy <6,0 mg/dl podczas wizyty końcowej (357 μmol/l) wynosił, odpowiednio, 45 % w przypadku febuksostatu w dawce 40 mg, 67% w
przypadku febuksostatu w dawce 80 mg i 42% w przypadku allopurynolu w dawce 300 mg lub 200 mg.
Pierwszorzędowy punkt końcowy w podgrupie pacjentów z zaburzeniami czynności nerek
W badaniu APEX oceniono skuteczność u 40 pacjentów z zaburzeniami czynności nerek (tzn. wyjściowym stężeniem kreatyniny w surowicy w zakresie >1,5 mg/dl i ≤2,0 mg/dl). U pacjentów z niewydolnością nerek, którzy zostali zrandomizowani do otrzymywania allopurynolu, dawkę ograniczono do 100 mg raz na dobę. Pierwszorzędowy punkt końcowy osiągnięto dla febuksostatu u 44% (80 mg raz na dobę), 45% (120 mg raz na dobę) i 60% (240 mg raz na dobę) pacjentów w porównaniu z 0% w grupach otrzymujących allopurynol w dawce 100 mg na dobę i placebo.
Nie odnotowano klinicznie istotnych różnic procentowego zmniejszenia stężenia kwasu moczowego w surowicy u zdrowych uczestników, bez względu na czynność nerek (58% w grupie z prawidłową czynnością nerek i 55% w grupie z ciężkimi zaburzeniami czynności nerek).
W badaniu CONFIRMS dokonano prospektywnej analizy wyników uzyskanych u pacjentów z dną moczanową i zaburzeniem czynności nerek i wykazano, że febuksostat był znacznie bardziej skuteczny w zmniejszaniu stężenia kwasu moczowego w surowicy do <6,0 mg/dl w porównaniu do allopurynolu w dawce 300 mg lub 200 mg u pacjentów z dną moczanową i łagodnymi do umiarkowanych zaburzeniami czynności nerek (65% badanych pacjentów).
Pierwszorzędowy punkt końcowy w podgrupie pacjentów ze stężeniem kwasu moczowego w surowicy
≥10 mg/dl
U około 40% pacjentów (połączone wyniki badań APEX i FACT) stwierdzono początkowe stężenie kwasu moczowego w surowicy ≥10 mg/dl. W tej podgrupie pierwszorzędowy punkt końcowy (stężenie kwasu moczowego w surowicy <6,0 mg/dl podczas ostatnich trzech wizyt) osiągnięto dla febuksostatu u 41% (80 mg raz na dobę), 48% (120 mg raz na dobę) i 66% (240 mg raz na dobę) pacjentów w porównaniu z 9% w grupie leczonej allopurynolem w dawce 300 mg lub 100 mg na dobę i 0% w grupie otrzymującej placebo.
W badaniu CONFIRMS odsetek pacjentów, u których osiągnięto pierwszorzędowy punkt końcowy (stężenie kwasu moczowego w surowicy <6,0 mg/dl podczas wizyty końcowej) u pacjentów z początkowym stężeniem kwasu moczowego w surowicy ≥10 mg/dl, leczonych febuksostatem w dawce 40 mg raz na dobę wynosił odpowiednio 27% (66/249), dla febuksostatu w dawce 80 mg raz na dobę 49% (125/254) i dla allopurynolu w dawce 300 lub 200 mg raz na dobę 31% (72/230).
Wyniki kliniczne: odsetek pacjentów wymagających leczenia z powodu zaostrzenia dny moczanowej Badanie APEX: podczas 8-tygodniowego okresu stosowania leczenia profilaktycznego, odsetek pacjentów wymagających leczenia z powodu zaostrzenia dny moczanowej był większy w grupie otrzymującej febuksostat w dawce 120 mg (36%) w porównaniu do grupy otrzymującej febuksostat w dawce 80 mg (28%), allopurynol 300 mg (23%) i placebo (20%). Zaostrzenie następowało po zakończeniu okresu leczenia profilaktycznego i przemijało stopniowo wraz z upływem czasu. Od 46% do 55% pacjentów otrzymało leczenie z powodu zaostrzenia dny moczanowej od tygodnia 8. do 28.
Zaostrzenie dny moczanowej w ciągu ostatnich 4 tygodni badania (tydzień 24 – 28) zaobserwowano u 15% (febuksostat pacjentów dawce 80 mg, 120 mg) i 14% (allopurynol w dawce 300 mg) i 20% (placebo) badanych.
Badanie FACT: podczas 8-tygodniowego okresu stosowania leczenia zapobiegającego, odsetek pacjentów wymagających leczenia z powodu zaostrzenia dny moczanowej był większy w grupie otrzymującej febuksostat w dawce 120 mg (36%) w porównaniu do grupy otrzymującej febuksostat w dawce 80 mg (22%) i allopurynol 300 mg (21%). Po zakończeniu 8-tygodniowego okresu leczenia profilaktycznego następowało zaostrzenie, które przemijało stopniowo wraz z upływem czasu (64% i 70% pacjentów otrzymało leczenie z powodu zaostrzenia dny moczanowej od tygodnia 8. do 52).
Zaostrzenie dny moczanowej w ciągu ostatnich 4 tygodni badania (tydzień 49 – 52) zaobserwowano u
6-8% (febuksostat w dawce 80 mg, 120 mg) i 11% (allopurynol w dawce 300 mg) badanych.
Odsetek pacjentów wymagających leczenia z powodu zaostrzenia dny moczanowej (badania APEX i FACT) był liczebnie mniejszy w grupach, które osiągnęły średnie stężenie kwasu moczowego w surowicy po rozpoczęciu badania <6,0 mg/dl, <5,0 mg/dl lub <4,0 mg/dl w porównaniu z grupą, która osiągnęła średnie stężenie kwasu moczowego w surowicy po rozpoczęciu badania ≥6,0 mg/dl w trakcie ostatnich 32 tygodni okresu leczenia (odstępy czasowe tydzień 20-24 do tygodnia 49-52).
Podczas badania CONFIRMS procent pacjentów wymagających leczenia z powodu zaostrzenia dny moczanowej (dzień 1 w miesiącu 6) wynosił odpowiednio 31% i 25% w grupach otrzymujących febuksostat i allopurynol. Nie zaobserwowano różnic odsetka pacjentów wymagających leczenia z powodu zaostrzenia dny moczanowej między grupami, w których podawano febuksostat w dawkach 40 mg i 80 mg.
Długotrwałe, otwarte badania rozszerzające
Badanie EXCEL (C02-021): badanie EXCEL było trwającym 3 lata badaniem klinicznym fazy 3., otwartym, wieloośrodkowym, kontrolowanym allopurynolem, rozszerzonym badaniem 3. fazy dotyczącym bezpieczeństwa, przeznaczonym dla pacjentów, którzy ukończyli badanie podstawowe fazy 3. (APEX lub FACT). Do badania włączono 1086 pacjentów: febuksostat 80 mg na dobę (n=649), febuksostat 120 mg na dobę (n=292) i allopurynol w dawce 300 lub 100 mg na dobę [n=145]. Około 69% pacjentów nie wymagało zmiany leczenia w celu osiągnięcia końcowego leczenia podtrzymującego). Pacjenci, u których stężenie kwasu moczowego w surowicy wynosiło <6,0 mg/dl podczas 3 kolejnych badań, zostali wyłączeni z badania.
Stężenie kwasu moczowego w surowicy utrzymywało się na stałym poziomie w czasie całego badania (np. 91% i 93% pacjentów w początkowym etapie leczenia febuksostatem odpowiednio w dawce 80 mg i 120 mg, miało stężenie kwasu moczowego w surowicy <6,0 mg/dl w miesiącu 36.).
Dane pochodzące z trzech lat leczenia wykazały zmniejszenie częstości występowania zaostrzeń dny moczanowej z mniej niż 4% pacjentów wymagających leczenia w związku z zaostrzeniem (tj. ponad 96% pacjentów nie wymagało leczenia w związku z zaostrzeniem) w miesiącach 16-24 i miesiącach 30-36.
U 46% i 38% pacjentów, u których prowadzono leczenie podtrzymujące febuksostatem, odpowiednio, w dawce 80 mg lub 120 mg raz na dobę, podczas wizyty końcowej stwierdzono całkowity zanik wyczuwalnych guzków dnawych, zaobserwowanych na początku leczenia.
Badanie FOCUS (TMX-01-005) było 5-letnim badaniem klinicznym fazy 2, otwartym, wieloośrodkowym, rozszerzającym badaniem dotyczącym bezpieczeństwa stosowania, przeznaczonym dla pacjentów, którzy ukończyli 4-tygodniowy etap podawania febuksostatu w podwójnie zaślepiony sposób w badaniu TMX-00-004.
116 pacjentów zostało włączonych i otrzymało początkowo febuksostat w dawce 80 mg raz na dobę. 62% pacjentów nie wymagało dostosowania dawkowania w celu utrzymania stężenia kwasu moczowego w surowicy <6,0 mg/dl i 38% wymagało dostosowania dawkowania w celu osiągnięcia końcowej dawki podtrzymującej.
Odsetek pacjentów ze stężeniem kwasu moczowego w surowicy <6,0 mg/dl (357 μmol/l) podczas
wizyty końcowej był większy niż 80% (81-100%) dla każdej dawki febuksostatu.
Podczas badań klinicznych 3 fazy obserwowano niewielkie nieprawidłowości w testach czynności wątroby u pacjentów leczonych febuksostatem (5,0%). Podobne wyniki zgłaszano w przypadku allopurynolu (4,2%) (patrz punkt 4.4). Zwiększone wartości TSH (>5,5 μIU/ml) obserwowano u pacjentów leczonych przez długi okres febuksostatem (5,5%) i u pacjentów leczonych allopurynolem (5,8%) w długotrwałych otwartych badaniach rozszerzonych (patrz punkt 4.4).
Długotrwałe badania po wprowadzeniu do obrotu
Badanie CARES było wieloośrodkowym, randomizowanym badaniem z podwójnie ślepą próbą prowadzonym w celu wykazania równoważności, porównującym zdarzenia sercowo-naczyniowe występujące przy stosowaniu febuksostatu i przy stosowaniu allopurynolu u pacjentów z dną moczanową i ciężkimi chorobami układu sercowo-naczyniowego w wywiadzie w tym: zawał mięśnia sercowego, hospitalizacja z powodu niestabilnej dławicy piersiowej, zabiegi rewaskularyzacji naczyń serca lub mózgu, udar, hospitalizacja z powodu przemijającego ataku niedokrwiennego, choroba naczyń obwodowych lub cukrzyca z oznakami powikłań mikro- lub makronaczyniowych. W celu osiągnięcia stężenia kwasu moczowego w surowicy mniejszego niż 6,0 mg/dl, dawkę febuksostatu podawano stopniowo, od 40 mg do 80 mg (niezależnie od czynności nerek) a dawkę allopurynolu zwiększano stopniowo o 100 mg w zakresie od 300 do 600 mg u pacjentów z prawidłową funkcją nerek i łagodnymi zaburzeniami czynności nerek oraz w zakresie dawek od 200 do 400 u pacjentów z umiarkowanymi zaburzeniami czynności nerek.
Pierwszorzędowym punktem końcowym w badaniu CARES był czas przed wystąpieniem pierwszego ciężkiego zdarzenia niepożądanego sercowo-naczyniowego (MACE – Major Adverse Cardiac Events), złożony z nieprowadzącego do zgonu zawału mięśnia sercowego, nieprowadzącego do zgonu udaru, zgonu z przyczyn sercowo-naczyniowych i niestabilnej dławicy piersiowej z nagłą koniecznością rewaskularyzacji wieńcowej. Punkty końcowe (pierwszorzędowy i drugorzędowy) były analizowane w populacji zgodnej z zaplanowanym leczeniem (ITT - intention-to-treat analysis) włączając wszystkie osoby przydzielone przez randomizację, które otrzymały przynajmniej jedną dawkę produktu w badaniu z podwójnie ślepą próbą.
Ogółem 56,6% pacjentów zakończyło badanie przed czasem i 45% pacjentów nie stawiło się na
wszystkie zaplanowane w badaniu wizyty.
W sumie obserwowano 6190 pacjentów średnio przez 32 miesiące przy ekspozycji trwającej średnio 728 dni w grupie pacjentów leczonych febuksostatem (n=3098) i 719 dni w grupie otrzymującej allopurynol (n=3092). Pierwszorzędowy punkt końcowy MACE wystąpił z podobną częstością w grupie febuksostatu i allopurynolu (odpowiednio u 10,8% vs 10,4% pacjentów; hazard względny [HR
– hazard ratio] 1,03; obustronny powtórzony przedział ufności 95 % [CI – confidence interval] 0,89- 1,21.
W analizie poszczególnych składowych MACE odsetek zgonów z przyczyn sercowo-naczyniowych był wyższy w przypadku febuksostatu niż w przypadku allopurynolu (4,3% vs 3,2% pacjentów, HR 1,34; 95% CI 1,03-1,73). Odsetek innych składowych MACE był podobny w grupie febuksostatu i allopurynolu tj. nieprowadzący do zgonu zawał mięśnia sercowego (3,6% vs. 3,8% pacjentów; HR 0,93; 95% CI 0,72-1,21), nie prowadzący do zgonu udar (2,3% vs. 2,3% pacjentów; HR 1,01; 95% CI 0,73-1,41) i nagła rewaskularyzacja z powodu niestabilnej dławicy piersiowej (1,6% vs 1,8% pacjentów, HR 0,86; 95% CI 0,59-1,26). Odsetek śmiertelności ze wszystkich powodów był również wyższy dla febuksostatu niż dla allopurynolu (7,8% vs 6,4% pacjentów; HR 1,22 95% CI 1,01-1,47), co było spowodowane głównie przez wyższy odsetek zgonów z przyczyn sercowo-naczyniowych w tej grupie (patrz punkt 4.4).
Odsetek potwierdzonych hospitalizacji z powodu niewydolności serca, przyjęć do szpitala związanych zaburzeniami rytmu serca nie związanych z niedokrwieniem, żylnymi zaburzeniami zakrzepowozatorowymi i hospitalizacji z powodu przemijającego ataku niedokrwiennego był porównywalny dla febuksostatu i allopurynolu.
Badanie FAST było prospektywnym, randomizowanym, otwartym badaniem z zaślepionym punktem końcowym, prowadzonym w celu porównania profilu bezpieczeństwa dla układu sercowo- naczyniowego, przy stosowaniu febuksostatu i przy stosowaniu allopurynolu u pacjentów z przewlekłą hiperurykemią (w stanach/przypadkach, w których wystąpiło już odkładanie się złogów moczanowych) i czynnikami ryzyka dla układu sercowo-naczyniowego (np. pacjenci w wieku 60 lat lub starsi i z przynajmniej jednym czynnikiem ryzyka dla układu sercowo-naczyniowego).
Zakwalifikowani pacjenci przed randomizacją byli leczeni allopurynolem, w razie potrzeb dostosowywano dawkę, zgodnie z oceną kliniczną, rekomendacjami EULAR (European Alliance of Associations for Rheumatology) i zatwierdzonym dawkowaniem. Pod koniec wstępnej fazy otwartej z zastosowaniem allopurynolu, pacjenci ze stężeniem kwasu moczowego w surowicy krwi <0,36 mmol/l (< 6 mg/dl) lub otrzymujący maksymalną tolerowaną dawkę lub maksymalną dozwoloną dawkę allopurynolu zostali losowo przydzieleni w proporcji 1:1 do grup otrzymujących febuksostat
lub allopurynol. Pierwszorzędowym punktem końcowym w badaniu FAST był czas do pierwszego wystąpienia jakiegokolwiek zdarzenia zawartego w złożonym punkcie końcowym Antiplatelet Trialists’ Collaborative (APTC), który obejmuje: i) hospitalizację z powodu nie prowadzącego do zgonu zawału mięśnia sercowego/dodatniego biomarkera ostrego zespołu wieńcowego (ACS – acute coronary syndrome); ii) nie prowadzący do zgonu udar; iii) zgon związany ze zdarzeniem sercowo- naczyniowym. Analiza pierwotna oparta była na podejściu „on-treatment” (OT).
Ogółem 6128 pacjentów zostało przydzielonych losowo, 3063 do grupy leczonej febuksostatem i 3065 do grupy leczonej allopurynolem.
W analizie pierwotnej OT wykazano równoważność febuksostatu i allopurynolu pod względem częstości występowania pierwszorzędowych punktów końcowych, które wystąpiły u 172 pacjentów (1,72/100 pacjento-lat) w przypadku febuksostatu w porównaniu do 241 pacjentów (2,05/100 pacjento-lat) w przypadku allopurynolu, skorygowany hazard względny [HR – hazard ratio] 0,85 (95% CI: 0,70, 1,03), p<0,001. Analiza pierwotna OT pierwszorzędowych punktów końcowych w podgrupie pacjentów z zawałem mięśnia sercowego, udarem lub ostrym zespołem wieńcowym w wywiadzie nie wykazała istotnych różnic pomiędzy leczonymi grupami: w grupie leczonej febuksostatem było 65 (9,5%) pacjentów, u których wystąpiły zdarzenia i 83 (11,8%) pacjentów, u których wystąpiły zdarzenia w grupie leczonej allopurynolem; skorygowany HR 1,02 (95% CI: 0,74- 1,42); p=0,202.
Leczenie febuksostatem nie było związane ze zwiększeniem częstości występowania zgonu z przyczyn sercowo-naczyniowych lub zgonów ze wszystkich powodów, ogółem ani w podgrupach pacjentów z zawałem mięśnia sercowego, udarem lub ostrym zespołem wieńcowym w wywiadzie. Ogółem, w grupie leczonej febuksostatem było mniej zgonów (62 zgony z powodu zdarzeń sercowo- naczyniowych i 108 zgonów ze wszystkich powodów) niż w grupie leczonej allopurynolem (82 zgony z powodu zdarzeń sercowo-naczyniowych i 174 zgony ze wszystkich powodów).
Odnotowano znaczniejsze obniżenie stężenia kwasu moczowego w przypadku leczenia febuksostatem w porównaniu do leczenia allopurynolu.
U zdrowych uczestników maksymalne stężenia w osoczu krwi (Cmax) i pole pod krzywą stężenia w osoczu w funkcji czasu (AUC) dla febuksostatu zwiększały się proporcjonalnie do dawki, po pojedynczej dawce i dawkach wielokrotnych z zakresu 10 mg do 120 mg. Dla zakresu dawek 120 mg do 300 mg obserwuje się większe niż proporcjonalne zwiększenie wartości AUC dla febuksostatu. Nie stwierdza się istotnej kumulacji leku podczas podawania dawek z zakresu 10 mg do 240 mg co 24 godziny. Dla febuksostatu stwierdzono średni okres półtrwania w końcowej fazie eliminacji (t1/2) wynoszący około 5 do 8 godzin.
Przeprowadzono analizy farmakokinetyczne lub farmakodynamiczne populacji wśród 211 pacjentów z hiperurykemią i dną moczanową leczonych febuksostatem w dawce 40 mg do 240 mg na dobę.
Ogólnie parametry farmakokinetyczne febuksostatu oszacowane w tych analizach są zgodne z parametrami uzyskanymi u zdrowych uczestników, co wskazuje, że zdrowi uczestnicy są reprezentatywni dla oceny farmakokinetyki lub farmakodynamiki w populacji pacjentów z dną moczanową.
Wchłanianie
Febuksostat jest szybko (tmax 1,0-1,5 h) i dobrze wchłaniany (co najmniej 84%). Po jednokrotnym lub wielokrotnym podaniu dawek 80 mg i 120 mg raz na dobę stężenie Cmax wynosiło odpowiednio
2,8-3,2 μg/ml i 5,0-5,3 μg/ml. Bezwzględna dostępność biologiczna febuksostatu w postaci tabletek
nie została zbadana.
Po doustnym podaniu wielokrotnych dawek 80 mg raz na dobę lub pojedynczej dawki 120 mg z posiłkiem o dużej zawartości tłuszczów nastąpiło zmniejszenie wartości Cmax odpowiednio o 49% i 38% oraz zmniejszenie wartości AUC odpowiednio o 18% i 16%. Nie zaobserwowano natomiast żadnej klinicznie istotnej zmiany procentowego zmniejszenia stężenia kwasu moczowego w surowicy
w testach (dawka wielokrotna 80 mg). Z tego względu febuksostat można przyjmować niezależnie od posiłków.
Dystrybucja
Objętość dystrybucji febuksostatu w stanie stacjonarnym (Vss/F) waha się w zakresie od 29 l do 75 l po podaniu doustnym dawek 10-300 mg. Febuksostat wiąże się z białkami osocza w około 99,2% (głównie z albuminami); wskaźnik ten utrzymuje się na stałym poziomie w zakresie stężeń osiąganych za pomocą dawek 80 mg i 120 mg. Czynne metabolity wiążą się z białkami osocza w zakresie od około 82% do 91%.
Metabolizm
Febuksostat jest w znacznym stopniu metabolizowany poprzez koniugację za pośrednictwem transferazy urydylodifosfoglukuronowej (UDPGT) oraz oksydację za pośrednictwem układu cytochromu P450 (CYP). Zidentyfikowano cztery farmakologicznie czynne metabolity hydroksylowe, z których trzy występują w osoczu krwi ludzkiej. Badania in vitro z ludzkimi mikrosomami wątroby wykazały, że te metabolity utleniające są tworzone głównie przez CYP1A1, CYP1A2, CYP2C8 lub CYP2C9, a glukuronid febuksostatu jest tworzony głównie przez UGT 1A1, 1A8 i 1A9.
Eliminacja
Febuksostat jest wydalany zarówno przez wątrobę, jak i nerki. Po podaniu doustnym dawki 80 mg febuksostatu znakowanego radioizotopem 14C około 49% dawki produktu stwierdzano w moczu w postaci niezmienionej (3%), acyloglukuronidu substancji czynnej (30%), jego znanych metabolitów utleniających i ich koniugatów (13%) oraz innych nieznanych metabolitów (3%). Poza wydalaniem w moczu, około 45% dawki leku stwierdzano w kale w postaci niezmienionej (12%),
acyloglukuronidu substancji czynnej (1%), jego znanych metabolitów utleniających i ich koniugatów (25%) oraz innych nieznanych metabolitów (7%).
Zaburzenia czynności nerek
Po wielokrotnym podaniu dawek 80 mg febuksostatu u pacjentów z łagodnymi, umiarkowanymi lub ciężkimi zaburzeniami czynności nerek wartość Cmax febuksostatu nie zmieniała się w porównaniu z pacjentami z prawidłową czynnością nerek. Średnia całkowita wartość AUC dla febuksostatu zwiększała się około 1,8 razy od 7,5 μg⋅h/ml w grupie pacjentów z prawidłową czynnością nerek do 13,2 μg⋅h/ml w grupie pacjentów z ciężkimi zaburzeniami czynności nerek. Wartości Cmax i AUC czynnych metabolitów zwiększały się odpowiednio 2- i 4-krotnie. Nie ma jednak konieczności zmiany dawki produktu u pacjentów z łagodnymi lub umiarkowanymi zaburzeniami czynności nerek.
Zaburzenia czynności wątroby
Po wielokrotnym podaniu dawki 80 mg febuksostatu u pacjentów z łagodnymi (klasa A wg Childa- Pugha) lub umiarkowanymi (klasa B wg Childa-Pugha) zaburzeniami czynności wątroby wartości Cmax i AUC febuksostatu i jego metabolitów nie zmieniały się znacząco w porównaniu z pacjentami z prawidłową czynnością wątroby. Nie przeprowadzono badań wśród pacjentów z ciężkimi zaburzeniami czynności wątroby (klasa C wg Childa-Pugha).
Wiek
Nie zaobserwowano znaczących zmian wartości AUC dla febuksostatu lub jego metabolitów po wielokrotnym podaniu doustnym dawek febuksostatu osobom w podeszłym wieku w porównaniu z młodszymi zdrowymi uczestnikami.
Płeć
Po wielokrotnym, doustnym podaniu dawek febuksostatu stwierdzono większe wartości Cmax i AUC odpowiednio o 24% i 12% u kobiet w porównaniu z mężczyznami. Niemniej wartości Cmax i AUC skorygowane ze względu na masę ciała były podobne dla obu płci. Nie jest wymagana modyfikacja dawki w związku z płcią pacjenta.
Działania toksyczne leku podczas badań nieklinicznych obserwowano zwykle po ekspozycji większej od maksymalnej ekspozycji na lek u człowieka.
W oparciu o modelowanie i analizę symulacyjną danych z badań przedklinicznych na szczurach, w przypadku jednoczesnego stosowania z febuksostatem, dawkę merkaptopuryny/azatiopryny należy zmniejszyć do 20% lub mniej wcześniej zalecanej dawki, w celu uniknięcia możliwych reakcji hematologicznych (patrz punkt 4.4 i 4.5).
Rakotwórczość, mutageneza, zaburzenie płodności
U samców szczurów stwierdzono statystycznie znaczące zwiększenie częstości występowania nowotworów pęcherza moczowego (brodawczak lub rak z komórek nabłonka przejściowego) jedynie z towarzyszącymi złogami ksantyny w grupie otrzymującej duże dawki, odpowiadające około
11-krotności ekspozycji u ludzi. Nie nastąpiło znaczące zwiększenie częstości występowania żadnych innych typów nowotworów u samców albo u samic myszy lub szczurów. Uważa się, że obserwacje te są efektem metabolizmu puryny i składu moczu specyficznego dla gatunku i nie mają znaczenia w praktyce klinicznej.
Standardowy zestaw testów genotoksyczności nie ujawnił żadnych biologicznie istotnych działań genotoksycznych febuksostatu.
Stwierdzono, że febuksostat w dawkach doustnych do 48 mg/kg/dobę nie wpływa na płodność i zdolności rozrodcze u samców i samic szczurów.
Nie zaobserwowano dowodów zaburzenia płodności, działań teratogennych ani innego szkodliwego wpływu na płód w wyniku stosowania febuksostatu. W przypadku toksycznego oddziaływania na matkę dużych dawek i towarzyszącego zmniejszonego wskaźnika odstawienia potomstwa od piersi, dochodziło do ograniczenia rozwoju potomstwa u szczurów po ekspozycji odpowiadającej 4,3- krotności ekspozycji u ludzi. Badania teratologiczne, przeprowadzone na ciężarnych samicach szczurów po ekspozycji odpowiadającej około 4,3-krotności i ciężarnych samicach królików po ekspozycji odpowiadającej około 13-krotności ekspozycji u ludzi nie ujawniły działań teratogennych.
Rdzeń tabletki
Celuloza mikrokrystaliczna (PH 101)
Laktoza jednowodna Kroskarmeloza sodowa Hydroksypropyloceluloza Krzemionka koloidalna uwodniona Magnezu stearynian
Otoczka tabletki (Opadry II Yellow 85F42129) Alkohol poliwinylowy częściowo hydrolizowany Tytanu dwutlenek (E 171)
Makrogol 3350
Talk
Żelaza tlenek żółty (E 172)
Nie dotyczy
3 lata.
Brak specjalnych zaleceń dotyczących przechowywania produktu leczniczego.
Blister Aclar/PVC/Aluminium, pakowany w tekturowe pudełko. Wielkość opakowań: 14, 28, 42, 56, 84 i 98 tabletek powlekanych. Nie wszystkie wielkości opakowań muszą znajdować się w obrocie.
Wszelkie niewykorzystane resztki produktu leczniczego lub jego odpady należy usunąć zgodnie z lokalnymi przepisami.
DOPUSZCZENIE DO OBROTU
Vivanta Generics s.r.o. Třtinová 260/1, Čakovice 196 00 Praga 9 Republika Czeska
Pozwolenie nr: 26204
Data wydania pierwszego pozwolenia na dopuszczenie do obrotu: 2021-01-25
CHARAKTERYSTYKI PRODUKTU LECZNICZEGO
2022-07-20











