Spis treści:
- NAZWA I ADRES PODMIOTU ODPOWIEDZIALNEGO ORAZ WYTWÓRCY ODPOWIEDZIALNEGO ZA ZWOLNIENIE SERII, JEŚLI JEST INNY
- NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
- ZAWARTOŚĆ SUBSTANCJI CZYNNEJ(-CH) I INNYCH SUBSTANCJI
- WSKAZANIA LECZNICZE
- PRZECIWWSKAZANIA
- DZIAŁANIA NIEPOŻĄDANE
- DOCELOWE GATUNKI ZWIERZĄT
- DAWKOWANIE DLA KAŻDEGO GATUNKU, DROGA (-I) I SPOSÓB PODANIA
- ZALECENIA DLA PRAWIDŁOWEGO PODANIA
- OKRES(-Y) KARENCJI
- SPECJALNE ŚRODKI OSTROŻNOŚCI PODCZAS PRZECHOWYWANIA
- SPECJALNE OSTRZEŻENIA, JEŚLI KONIECZNE
- SPECJALNE ŚRODKI OSTROŻNOŚCI DOTYCZĄCE USUWANIA NIEZUŻYTEGO PRODUKTU LECZNICZEGO WETERYNARYJNEGO LUB POCHODZĄCYCH Z NIEGO ODPADÓW, JEŚLI MA TO ZASTOSOWANIE
- DATA ZATWIERDZENIA LUB OSTATNIEJ ZMIANY TEKSTU ULOTKI
- INNE INFORMACJE
B. ULOTKA INFORMACYJNA
ULOTKA INFORMACYJNA
Doxybactin 50 mg tabletki dla psów i kotów
NAZWA I ADRES PODMIOTU ODPOWIEDZIALNEGO ORAZ WYTWÓRCY ODPOWIEDZIALNEGO ZA ZWOLNIENIE SERII, JEŚLI JEST INNY
NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
ZAWARTOŚĆ SUBSTANCJI CZYNNEJ(-CH) I INNYCH SUBSTANCJI
WSKAZANIA LECZNICZE
PRZECIWWSKAZANIA
DZIAŁANIA NIEPOŻĄDANE
bardzo często (więcej niż 1 na 10 leczonych zwierząt wykazujących działanie(a) niepożądane)
często (więcej niż 1, ale mniej niż 10 na 100 leczonych zwierząt)
niezbyt często (więcej niż 1, ale mniej niż 10 na 1000 leczonych zwierząt)
rzadko (więcej niż 1, ale mniej niż 10 na 10000 leczonych zwierząt)
bardzo rzadko (mniej niż 1 na 10000 leczonych zwierząt włączając pojedyncze raporty).
DOCELOWE GATUNKI ZWIERZĄT
DAWKOWANIE DLA KAŻDEGO GATUNKU, DROGA (-I) I SPOSÓB PODANIA
ZALECENIA DLA PRAWIDŁOWEGO PODANIA
OKRES(-Y) KARENCJI
SPECJALNE ŚRODKI OSTROŻNOŚCI PODCZAS PRZECHOWYWANIA
SPECJALNE OSTRZEŻENIA, JEŚLI KONIECZNE
SPECJALNE ŚRODKI OSTROŻNOŚCI DOTYCZĄCE USUWANIA NIEZUŻYTEGO PRODUKTU LECZNICZEGO WETERYNARYJNEGO LUB POCHODZĄCYCH Z NIEGO ODPADÓW, JEŚLI MA TO ZASTOSOWANIE
DATA ZATWIERDZENIA LUB OSTATNIEJ ZMIANY TEKSTU ULOTKI
INNE INFORMACJE
Podmiot odpowiedzialny:
Le Vet Beheer B.V. Wilgenweg 7
3421 TV Oudewater
Holandia
Wytwórca odpowiedzialny za zwolnienie serii: Lelypharma B.V.
Zuiveringsweg 42
8243 PZ Lelystad
Holandia
Genera Inc.
Svetonedeljska cesta 2, Kalinovica 10436 Rakov Potok
Chorwacja
Jedynie miejsce testowania i zwalniania partii produktu będzie wymienione na wydrukowanej ulotce.
Doxybactin 50 mg tabletki dla psów i kotów doksycyklina
Każda tabletka zawiera:
Substancja czynna:
Doksycyklina (w postaci doksycykliny hyklanu) 50 mg
Żółta z brązowymi kropkami, okrągła i wypukła, aromatyzowana tabletka z linią podziału w kształcie krzyża z jednej strony. Tabletki można podzielić na 2 lub 4 równe części.
Leczenie następujących chorób wywołanych przez bakterie wrażliwe na doksycyklinę:
Psy:
Nieżyt nosa (zapalenie błony śluzowej nosa) wywołane przez Bordetella bronchiseptica i Pasteurella
spp.;
Odoskrzelowe zapalenie płuc (zrazikowe zapalenie płuc) wywołane przez Bordetella spp. i
Pasteurella spp.;
Śródmiąższowe zapalenie nerek (zapalenie części tkanek nerkowych) wywołane przez Leptospira spp.
Koty:
Zakażenie dróg oddechowych wywołane przez Bordetella bronchiseptica, Chlamydophila felis i
Pasteurella spp.
Nie stosować w przypadkach nadwrażliwości na tetracykliny lub na dowolną substancję pomocniczą.
Zaburzenia żołądkowo-jelitowe, takie jak wymioty, biegunka i zapalenie przełyku, zgłaszano bardzo rzadko jako działania niepożądane po leczeniu doksycykliną.
U bardzo młodych zwierząt przebarwienie zębów w skutek tworzenia się kompleksu tetracyklina- fosforan wapnia może wystąpić bardzo rzadko.
Reakcje nadwrażliwości, wrażliwość na światło i, w wyjątkowych przypadkach fotodermatoza, mogą
bardzo rzadko wystąpić po ekspozycji na intensywne światło dzienne.
Wiadomo, że w przypadku stosowania innych tetracyklin bardzo rzadko występuje opóźnienie rozwoju kośćca młodych zwierząt (odwracalne po zakończeniu leczenia) i może ono wystąpić po podaniu doksycykliny.
Częstotliwość występowania działań niepożądanych przedstawia się zgodnie z poniższą regułą:
W razie zaobserwowania działań niepożądanych, również niewymienionych w ulotce informacyjnej, lub w przypadku podejrzenia braku działania produktu, poinformuj o tym lekarza weterynarii.
Można również zgłosić działania niepożądane poprzez krajowy system raportowania
(www.urpl.gov.pl)
Psy i koty.
Podanie doustne.
Zalecana dawka dla psów i kotów to 10 mg doksycykliny na kg masy ciała na dobę. W większości rutynowych przypadków oczekuje się odpowiedzi na leczenie po 5-7 dniach leczenia. Leczenie należy kontynuować przez 2-3 dni po uzyskaniu klinicznego wyleczenia w przypadku ostrych zakażeń. W przypadku chorób przewlekłych lub nawracających może być wymagany dłuższy, do 14 dni, czas trwania leczenia. U psów ze śródmiąższowym zapaleniem nerek z powodu leptospirozy zaleca się leczenie przez 14 dni. U kotów z zakażeniami wywołanymi przez C. felis zaleca się leczenie przez minimum 28 dni w celu zapewnienia eliminacji patogenu z organizmu. W celu zapewnienia prawidłowego dawkowania należy jak najdokładniej ustalić masę ciała, aby uniknąć podawania za małych dawek.
Poniższa tabela służy jako wskazówka odnośnie podawania produktu w standardowej dawce 10 mg na
kg masy ciała na dobę.
Masa ciała | Dawka mg | Doxybactin 50 mg | Doxybactin 200 mg | Doxybactin 400 mg |
0,75 kg-1,25 kg | 12,5 |
| - | - | ||
>1,25 kg-2,5 kg | 25 |
| - | - | ||
>2,5 kg-3,75 kg | 37,5 |
| - | - | ||
>3,75 kg-5 kg | 50 |
| - | - | ||
>5 kg-6,25 kg | 62,5 |
| - | - | ||
>6,25 kg-7,5 kg | 75 |
| - | - | ||
>7,5 kg-10 kg | 100 |
| - | - | ||
>10 kg-12,5 kg | 125 |
| - | - | ||
>12,5 kg-15 kg | 150 |
| - | |||
>15 kg-20 kg | 200 | - |
| - | ||
>20 kg-25 kg | 250 |
| oraz |
| - | |
>25 kg-30 kg | 300 | - |
| - | ||
>30 kg-35 kg | 350 | - |
| - | ||
>35 kg-40 kg | 400 | - | - |
| ||
>40 kg-45 kg | 450 |
| oraz |
| ||
>45 kg-50 kg | 500 | - |
| oraz |
| |
>50 kg-60 kg | 600 | - |
| oraz |
| |
>60 kg-70 kg | 700 | - |
| oraz |
| |
>70 kg-80 kg | 800 | - | - |
| ||

= ¼ tabletki  = ½ tabletki
= ½ tabletki  = ¾ tabletki
= ¾ tabletki  = 1 tabletka
= 1 tabletka
Tabletki należy podawać razem z pożywieniem (patrz punkt 12, Specjalne ostrzeżenia). Tabletki można dzielić na 2 lub 4 równe części w celu zapewnienia właściwego dawkowania. Tabletkę umieścić na płaskiej powierzchni ze stroną z linią podziału skierowaną do góry i stroną wypukłą (zaokrągloną) skierowaną do powierzchni.
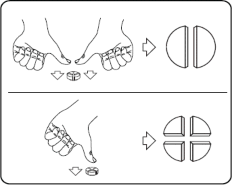
2 równe części: nacisnąć kciukami po obu stronach tabletki. 4 równe części: nacisnąć kciukiem po środku tabletki.
Nie dotyczy.
Przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Przechowywać w temperaturze poniżej 30°C.
Nie używać tego produktu leczniczego weterynaryjnego po upływie terminu ważności podanego na
opakowaniu po terminie ważności (EXP).
Termin ważności oznacza ostatni dzień danego miesiąca.
Okres ważności tabletek podzielonych: 3 dni.
Specjalne środki ostrożności dotyczące stosowania u zwierząt:
Zwierzętom z dysfagią lub chorobami, którym towarzyszą wymioty, produkt należy podawać z zachowaniem ostrożności, ponieważ podawanie tabletek zawierających doksycykliny hyklan zostało powiązane z występowaniem nadżerek przełyku.
W celu zmniejszenia prawdopodobieństwa wystąpienia podrażnienia przełyku i innych żołądkowo-jelitowych działań niepożądanych produkt należy podawać razem z pożywieniem.
Należy zachować szczególną ostrożność podczas podawania produktu zwierzętom z chorobą wątroby, ponieważ u niektórych zwierząt udokumentowano zwiększenie aktywności enzymów wątrobowych po leczeniu doksycykliną.
Młodym zwierzętom produkt należy podawać z zachowaniem ostrożności, ponieważ tetracykliny mogą powodować trwałe przebarwienie zębów w przypadku podawania podczas ich rozwoju.
Piśmiennictwo dotyczące ludzi wskazuje jednak, że w przypadku doksycykliny istnieje mniejsze prawdopodobieństwo spowodowania tych nieprawidłowości niż w przypadku innych tetracyklin, ponieważ doksycyklina ma mniejszą zdolność wiązania wapnia.
Stosowanie produktu powinno opierać się na identyfikacji i badaniu wrażliwości patogenów docelowych. Jeśli nie jest to możliwe, terapia powinna opierać się na informacjach epidemiologicznych i wiedzy o podatności docelowych patogenów na poziomie lokalnym/regionalnym. Stosowanie produktu powinno być zgodne z oficjalną, krajową i regionalną polityką przeciwdrobnoustrojową.
Stosowanie produktu niezgodnie z zaleceniami podanymi w ChPLW może zwiększać występowanie bakterii opornych na doksycyklinę i zmniejszać skuteczność leczenia innymi tetracyklinami z powodu potencjalnej oporności krzyżowej.
Ponieważ tabletki są aromatyzowane, należy przechowywać je poza zasięgiem zwierząt, aby uniknąć przypadkowego połknięcia.
Specjalne środki ostrożności dla osób podających produkt leczniczy weterynaryjny zwierzętom: Tetracykliny mogą powodować reakcje nadwrażliwości (alergiczne).
Osoby o znanej nadwrażliwości na tetracykliny powinny unikać kontaktu z produktem leczniczym
weterynaryjnym.
W przypadku wystąpienia objawów po ekspozycji, takich jak wysypka skórna należy niezwłocznie zwrócić się o pomoc lekarską oraz przedstawić lekarzowi ulotkę informacyjną.
Doksycyklina może powodować zaburzenia żołądkowo-jelitowe po przypadkowym połknięciu, zwłaszcza przez dzieci. W celu uniknięcia przypadkowego połknięcia, zwłaszcza przez dziecko, niezużyte części tabletki należy włożyć z powrotem do otwartego blistra i do pudełka tekturowego. Po przypadkowym połknięciu, zwłaszcza przez dzieci, należy zwrócić się o pomoc lekarską.
Umyć ręce po użyciu.
Ciąża i laktacja:
Bezpieczeństwo produktu leczniczego weterynaryjnego stosowanego w czasie ciąży i laktacji nie zostało określone. Tetracykliny mogą opóźniać rozwój kośćca u płodu (w pełni odwracalne) i powodować przebarwienie zębów mlecznych. Dowody z piśmiennictwa dotyczącego ludzi sugerują jednak, że w przypadku doksycykliny istnieje mniejsze prawdopodobieństwo spowodowania tych nieprawidłowości niż w przypadku innych tetracyklin. Do stosowania jedynie po dokonaniu przez lekarza weterynarii oceny bilansu korzyści/ryzyka wynikającego ze stosowania produktu.
Interakcje z innymi produktami leczniczymi i inne rodzaje interakcji:
Nie podawać jednocześnie z antybiotykami bakteriobójczymi, takimi jak penicyliny i cefalosporyny. Doustnych substancji pochłaniających i substancji zawierających kationy wielowartościowe, takich jak leki zobojętniające kwas żołądkowy i sole żelaza, nie należy stosować na 3 godziny przed do 3 godzin po podaniu doksycykliny. Okres półtrwania doksycykliny ulega skróceniu wskutek jednoczesnego podawania leków przeciwpadaczkowych, takich jak fenobarbital i fenytoina.
Przedawkowanie (objawy, sposób postępowania przy udzielaniu natychmiastowej pomocy, odtrutki): W przypadku przedawkowania nie są spodziewane inne objawy niż te, wymienione w punkcie dotyczącym działań niepożądanych.
Leków nie należy usuwać do kanalizacji ani wyrzucać do śmieci.
O sposoby usunięcia niepotrzebnych leków zapytaj lekarza weterynarii lub farmaceutę. Pomogą one chronić środowisko.
29.11.2022.
Blister Aluminium - PCV/PE/PVDC.
Pudełko tekturowe zawierające 1, 2, 3 lub 10 blistrów po 10 tabletek.
Pudełko tekturowe zawierające 10 oddzielnych pudełek tekturowych, zawierających po 1 blistrze po 10 tabletek.
Niektóre wielkości opakowań mogą nie być dostępne w obrocie.
W celu uzyskania informacji na temat niniejszego produktu leczniczego weterynaryjnego, należy kontaktować się z lokalnym przedstawicielem podmiotu odpowiedzialnego: Dechra Veterinary Products sp. z o.o., ul. Modlińska 61, 03-199 Warszawa, Polska.
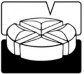
Podzielna tabletka