Spis treści:
- NAZWA I ADRES PODMIOTU ODPOWIEDZIALNEGO ORAZ WYTWÓRCY
- NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
- ZAWARTOŚĆ SUBSTANCJI CZYNNEJ I INNYCH SUBSTANCJI
- WSKAZANIA LECZNICZE
- PRZECIWWSKAZANIA
- DZIAŁANIA NIEPOŻĄDANE
- DOCELOWE GATUNKI ZWIERZĄT
- DAWKOWANIE DLA KAŻDEGO GATUNKU, DROGA I SPOSÓB PODANIA
- ZALECENIA DLA PRAWIDŁOWEGO PODANIA
- OKRES KARENCJI
- SPECJALNE ŚRODKI OSTROŻNOŚCI PODCZAS PRZECHOWYWANIA
- SPECJALNE OSTRZEŻENIA
- SPECJALNE ŚRODKI OSTROŻNOŚCI DOTYCZĄCE USUWANIA NIEZUŻYTEGO PRODUKTU LECZNICZEGO WETERYNARYJNEGO LUB POCHODZĄCYCH Z NIEGO ODPADÓW, JEŚLI MA TO ZASTOSOWANIE
- DATA ZATWIERDZENIA LUB OSTATNIEJ ZMIANY TEKSTU ULOTKI
- INNE INFORMACJE
B. ULOTKA INFORMACYJNA
ULOTKA INFORMACYJNA
Tramadol Domes Pharma 50 mg tabletki dla psów
NAZWA I ADRES PODMIOTU ODPOWIEDZIALNEGO ORAZ WYTWÓRCY
NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
ZAWARTOŚĆ SUBSTANCJI CZYNNEJ I INNYCH SUBSTANCJI
WSKAZANIA LECZNICZE
PRZECIWWSKAZANIA
DZIAŁANIA NIEPOŻĄDANE
bardzo często (więcej niż 1 na 10 leczonych zwierząt wykazujących działanie(a) niepożądane)
często (więcej niż 1, ale mniej niż 10 na 100 leczonych zwierząt)
niezbyt często (więcej niż 1, ale mniej niż 10 na 1000 leczonych zwierząt)
rzadko (więcej niż 1, ale mniej niż 10 na 10000 leczonych zwierząt)
bardzo rzadko (mniej niż 1 na 10000 leczonych zwierząt włączając pojedyncze raporty).
DOCELOWE GATUNKI ZWIERZĄT
DAWKOWANIE DLA KAŻDEGO GATUNKU, DROGA I SPOSÓB PODANIA
ZALECENIA DLA PRAWIDŁOWEGO PODANIA
OKRES KARENCJI
SPECJALNE ŚRODKI OSTROŻNOŚCI PODCZAS PRZECHOWYWANIA
SPECJALNE OSTRZEŻENIA
SPECJALNE ŚRODKI OSTROŻNOŚCI DOTYCZĄCE USUWANIA NIEZUŻYTEGO PRODUKTU LECZNICZEGO WETERYNARYJNEGO LUB POCHODZĄCYCH Z NIEGO ODPADÓW, JEŚLI MA TO ZASTOSOWANIE
DATA ZATWIERDZENIA LUB OSTATNIEJ ZMIANY TEKSTU ULOTKI
INNE INFORMACJE
ODPOWIEDZIALNEGO ZA ZWOLNIENIE SERII, JEŚLI JEST INNY
Podmiot odpowiedzialny:
DOMES PHARMA
3 rue André Citroën 63430 Pont-Du-Chateau Francja
Wytwórca odpowiedzialny za zwolnienie serii: EUROPHARTECH
34 rue Henri Matisse – BP 23 63370 Lempdes
Francja
Tramadol Domes Pharma 50 mg tabletki dla psów Tramadolu chlorowodorek
Każda tabletka zawiera:
Substancja czynna:
Tramadol 43,90 mg
(co odpowiada 50,00 mg tramadolu chlorowodorku)
Biała do kremowej, lekko nakrapiania, okrągła i wypukła tabletka o średnicy 10 mm z liniami podziału w kształcie krzyża.
Tabletki można podzielić na 2 lub 4 równe części.
Do zmniejszania ostrego i przewlekłego łagodnego bólu tkanek miękkich oraz bólu mięśniowo- szkieletowego.
Nie podawać w połączeniu z trójcyklicznymi lekami przeciwdepresyjnymi, inhibitorami
monoaminooksydazy i inhibitorami wychwytu zwrotnego serotoniny.
Nie stosować w przypadkach nadwrażliwości na substancję czynną lub na dowolną substancję pomocniczą.
Nie stosować u zwierząt z padaczką.
Często mogą występować łagodna sedacja i senność, zwłaszcza w przypadku podawania większych dawek.
U psów po podaniu tramadolu niezbyt często obserwuje się nudności i wymioty.
Nadwrażliwość może wystąpić w rzadkich przypadkach. W przypadku wystąpienia nadwrażliwości należy przerwać leczenie.
W bardzo rzadkich przypadkach tramadol może powodować drgawki u psów z niskim progiem
drgawkowym.
Częstotliwość występowania działań niepożądanych przedstawia się zgodnie z poniższą regułą:
W razie zaobserwowania działań niepożądanych, również niewymienionych w ulotce informacyjnej, lub w przypadku podejrzenia braku działania produktu, poinformuj o tym lekarza weterynarii.
Można również zgłosić działania niepożądane poprzez krajowy system raportowania (www.urpl.gov.pl).
Psy.

Do podania doustnego.
Zalecana dawka wynosi 2–4 mg tramadolu chlorowodorku na kg m.c., co 8 godzin lub w miarę
potrzeby, zależnie od natężenia bólu.
Minimalny odstęp czasu między dawkami wynosi 6 godzin. Zalecana maksymalna dawka dobowa wynosi 16 mg/kg. Ponieważ indywidualna odpowiedź na tramadol jest zmienna i zależy częściowo od dawki, wieku zwierzęcia, indywidualnych różnic w zakresie wrażliwości na ból oraz stanu ogólnego, optymalny schemat dawkowania powinien być dostosowany indywidualnie w oparciu o powyższy zakres dawek i odstępy czasowe między kolejnymi podaniami. Pies powinien być regularnie badany przez lekarza weterynarii, w celu oceny, czy konieczne jest uzyskanie dodatkowego efektu przeciwbólowego. Dodatkowe działanie przeciwbólowe można osiągnąć poprzez zwiększanie dawki tramadolu do maksymalnej dawki dobowej i (lub) poprzez zastosowanie analgezji multimodalnej oraz innych odpowiednich produktów przeciwbólowych.

Należy pamiętać, że poniższa tabela dawkowania jest tabelą orientacyjną uwzględniającą najwyższą dawkę wynoszącą 4 mg na kg m.c. Tabela podaje liczbę tabletek do podania przy uwzględnieniu dawki 4 mg tramadolu chlorowodorku na kg m.c.
Masa ciała psa | Dawka 4 mg/kg oraz ilość tabletek produktu na podanie | ||
3,12 kg | 12,5 mg | 1/4 |
|
6,25 kg | 25 mg | 1/2 |
|
9,37 kg | 37,5 mg | 3/4 |
|
12,5 kg | 50 mg | 1 |
|
15,62 kg | 62,5 mg | 1+ 1/4 |
|
18,75 kg | 75 mg | 1 + 1/2 |
|
21,87 kg | 87,5 mg | 1 + 3/4 |
|
25 kg | 100 mg | 2 |
|
> 25 kg | podać dodatkową ¼ tabletki ( ) na każde 3,12 kg m.c. powyżej masy 25 kg | ||

Tabletki można dzielić na 2 równe części, aby zapewnić właściwe dawkowanie.
Tabletkę należy położyć na płaskiej powierzchni linią podziału do góry a wypukłą (zaokrągloną) stroną tabletki do dołu.
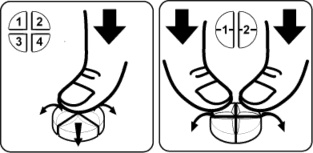
4 równe części: nacisnąć kciukiem środek tabletki.
2 równe części: nacisnąć kciukami z obu stron tabletki.
Nie dotyczy.
Przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Po otwarciu blistra należy umieścić niewykorzystane części tabletki w blistrze i schować blister
z powrotem do pudełka tekturowego.
Brak specjalnych środków ostrożności dotyczących przechowywania.
Nie stosować tego produktu leczniczego weterynaryjnego po upływie terminu ważności zamieszczonego na blistrze i opakowaniu kartonowym po EXP. Termin ważności oznacza ostatni dzień danego miesiąca.
Specjalne środki ostrożności dotyczące stosowania u zwierząt:
Tabletki są aromatyzowane, dlatego należy przechowywać je w miejscu niedostępnym dla zwierząt, aby zapobiec przypadkowemu spożyciu.
Prawidłowe dawkowanie tabletki jest możliwe wyłącznie u psów o wadze powyżej 3,12 kg. Stosować z zachowaniem ostrożności u psów z zaburzeniami czynności nerek lub wątroby. U psów z zaburzoną czynnością wątroby metabolizm tramadolu do aktywnych metabolitów może być upośledzony, skutkując zmniejszoną skutecznością produktu. Jeden z aktywnych metabolitów tramadolu jest wydalany przez nerki, dlatego też schemat dawkowania u psów z zaburzeniami czynności nerek może wymagać dostosowania. Podczas stosowania produktu należy monitorować czynność nerek i wątroby. O ile to możliwe, przerwanie długotrwałego leczenia przeciwbólowego powinno odbywać się stopniowo.
Specjalne środki ostrożności dla osób podających produkt leczniczy weterynaryjny zwierzętom: Tramadol może powodować sedację, nudności i zawroty głowy po przypadkowym połknięciu, zwłaszcza u dzieci.
Aby uniknąć przypadkowego spożycia, w szczególności przez dziecko, niewykorzystane części tabletki należy włożyć z powrotem do otwartego blistra i do pudełka tekturowego oraz przechowywać w bezpiecznym miejscu niewidocznym i niedostępnym dla dzieci. Po przypadkowym połknięciu, w szczególności przez dzieci, należy niezwłocznie zwrócić się o pomoc lekarską oraz pokazać lekarzowi ulotkę informacyjną lub opakowanie. W razie przypadkowego połknięcia przez dorosłych: nie należy prowadzić pojazdów, ponieważ może wystąpić sedacja. Osoby o znanej nadwrażliwości na tramadol lub na dowolną substancję pomocniczą powinny unikać kontaktu
z produktem leczniczym weterynaryjnym. Należy umyć ręce po podaniu produktu.
Ciąża, laktacja i płodność:
W badaniach laboratoryjnych prowadzonych odpowiednio na myszach i (lub) szczurach oraz królikach, tramadol:
‐ nie wykazał działania teratogennego, toksycznego dla płodu, szkodliwego dla samicy.
‐ nie wykazał żadnego negatywnego działania na potomstwo w okresie okołoporodowym
i poporodowym.
‐ stosowany w dawkach terapeutycznych nie skutkował niekorzystnym działaniem na parametry reprodukcyjne oraz płodność samców i samic.
Do stosowania jedynie po dokonaniu przez lekarza weterynarii oceny bilansu korzyści/ryzyka wynikającego ze stosowania produktu.
Interakcje z innymi produktami leczniczymi i inne rodzaje interakcji:
Jednoczesne podawanie tego produktu z lekami działającymi depresyjnie na ośrodkowy układ
nerwowy może nasilać działanie na OUN oraz skutkować depresją oddechową.
Produkt może nasilać działanie leków, które obniżają próg drgawkowy. Leki o działaniu hamującym (np. cymetydyna i erytromycyna) lub indukującym (np. karbamazepina) metabolizm z udziałem CYP450, mogą mieć wpływ na działanie przeciwbólowe tego produktu. Znaczenie kliniczne tej interakcji nie zostało jeszcze w pełni zbadane. Połączenie produktu z kombinacjami agonistów/antagonistów (np. buprenorfina, butorfanol) nie jest wskazane, ponieważ działanie przeciwbólowe czystego agonisty teoretycznie ulec obniżeniu może w takim układzie.
Patrz również Przeciwwskazania.
Przedawkowanie (objawy, sposób postępowania przy udzielaniu natychmiastowej pomocy, odtrutki): W przypadku zatrucia tramadolem istnieje prawdopodobieństwo wystąpienia objawów podobnych do tych obserwowanych w przypadku zatruć innymi lekami przeciwbólowymi działającymi ośrodkowo (opioidami). Obejmują one w szczególności zwężenie źrenic, wymioty, zapaść sercowo- naczyniową, zaburzenia świadomości włącznie ze śpiączką, drgawki, depresję oddechową włącznie z zatrzymaniem oddechu.
Ogólne sposoby postępowania w nagłych przypadkach: utrzymanie drożności dróg oddechowych, podtrzymywanie pracy serca i układu oddechowego stosownie do objawów. Wywołanie wymiotów w celu opróżnienia żołądka jest odpowiednim zabiegiem, chyba, że zwierzę wykazuje obniżenie świadomości, w którym to przypadku można rozważać płukanie żołądka. Odtrutką w przypadku depresji oddechowej jest nalokson. Niemniej, nalokson może nie być przydatny we wszystkich
przypadkach przedawkowania tramadolu, ponieważ może jedynie częściowo znieść niektóre z jego
działań. W przypadku drgawek należy podać diazepam.
Leków nie należy usuwać do kanalizacji ani wyrzucać do śmieci.
O sposoby usunięcia niepotrzebnych leków zapytaj lekarza weterynarii. Pomogą one chronić środowisko.
Wielkości opakowań:
Pudełko tekturowe zawierające 10 tabletek Pudełko tekturowe zawierające 30 tabletek Pudełko tekturowe zawierające 60 tabletek Pudełko tekturowe zawierające 100 tabletek
Niektóre wielkości opakowań mogą nie być dostępne w obrocie.
Numer pozwolenia na dopuszczenie do obrotu:
Klasyfikacja produktu leczniczego pod względem wydawania: Wydawany z przepisu lekarza - Rp.

Podzielna tabletka.























