Spis treści:
[Wersja 8.1,01/2017]
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
Ekyflogyl 1,8 mg/ml + 8,7 mg/ml
2. 
Jeden mililitr zawiera
Substancje czynne:
Prednizolon (jako octan) 1,8 mg 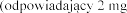 prednizolonu octanu)
prednizolonu octanu)
Lidokaina (jako chlorowodorek jednowodny) 8,7 mg
Substancja pomocnicza:
Dimetylosulfotlenek 968 mg
Wykaz wszystkich substancji pomocniczych, patrz punkt 6.1.
3. 
klarowna, lepka ciecz
4. 
4.1 
Konie
4.2
 iowo- szkieletowymi.
iowo- szkieletowymi.
Przeciwwskazania
Specjaln
Interakcje z innymi produktami leczniczymi i inne rodzaje interakcji
Dawkowanie i droga podawania
a przy udzielaniu natychmiastowej pomocy,
Okres(-y) karencji
erek.

Brak.
Nie  miejscowo na
miejscowo na
obszarze stosowania.
Podanie
szar.
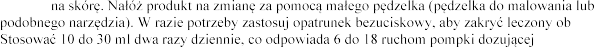

ci od charakteru zmiany.


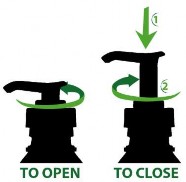


odtru
Tkanki jadalne: 10 dni
5.  E
E
Grupa farmakoterapeutyczna: Inne stosowane miejscowo 
 a
a
Kod ATC vet: QM02AX99
5.1 

Prednizolon jest syntetycznym glukokortykostero a
zcie zapobiega depolimeryzacji
mukopolisacharydów.
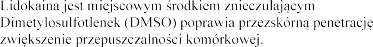
substancji czynnych przez
5.2 etyczne
.

podaniu
absorpcji. W przypadku zaburzonej lidok
kró

absorpcji. W przypadku zaburzonej
w w
w fazie eliminacji

DANE FARMACEUTYCZNE
Wykaz substancji pomocniczych
6.4.
PODMIOT ODPOWIEDZIALNY
NUMER(-Y) POZWOLENIA NA DOPUSZCZENIE DO OBROTU
DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU
DATA OSTATNIEJ AKTUALIZACJI TEKSTU
Dimetylosulfotlenek Hydroksyetyloceluloza Woda oczyszczona
ra
opakowaniu
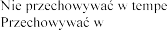

turze pow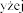 .
.
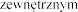 w celu ochrony
w celu ochrony 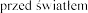 .
.
Butelka
ylenu.
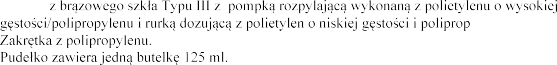
6.5 Rodzaj 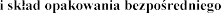
adów

6.6
3 lata
Niewykorzystany produkt leczniczy weterynaryjny l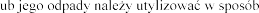
AUDEVARD
42-46 rue Médéric
92110 CLICHY
Francja
3003/20
Data wydania pierwszego pozwolenia na dopuszczenie do obrotu: 31/07/2020
11/03/2021











