Spis treści:
- Co to jest Fulvestrant Sandoz i w jakim celu się go stosuje
- Informacje ważne przed zastosowaniem leku Fulvestrant Sandoz Kiedy nie stosować leku Fulvestrant Sandoz
- Jak stosować Fulvestrant Sandoz
- Możliwe działania niepożądane
- Jak przechowywać Fulvestrant Sandoz
- Zawartość opakowania i inne informacje Co zawiera Fulvestrant Sandoz
Ulotka dołączona do opakowania: informacja dla pacjenta
Fulvestrant Sandoz, 250 mg/5 ml, roztwór do wstrzykiwań w ampułko-strzykawce
Fulvestrantum
Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać.
W razie jakichkolwiek wątpliwości należy zwrócić się do lekarza, farmaceuty lub pielęgniarki.
Lek ten przepisano ściśle określonej osobie. Nie należy go przekazywać innym. Lek może zaszkodzić innej osobie, nawet jeśli objawy jej choroby są takie same.
Jeśli u pacjenta wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione w tej ulotce, należy powiedzieć o tym lekarzowi, farmaceucie lub pielęgniarce. Patrz punkt 4.
Spis treści ulotki:
Co to jest Fulvestrant Sandoz i w jakim celu się go stosuje
Fulvestrant Sandoz zawiera substancję czynną fulwestrant, należący do leków blokujących działanie receptorów estrogenowych.
Estrogeny, żeńskie hormony płciowe, mogą w niektórych przypadkach uczestniczyć w rozwoju raka piersi.
Fulvestrant Sandoz jest stosowany:
jako jedyny lek w leczeniu kobiet po menopauzie z pewnym rodzajem raka piersi, tzw. rakiem piersi z obecnością receptorów estrogenowych, który jest miejscowo zaawansowany lub rozprzestrzenił się do innych części ciała (przerzuty),
w skojarzeniu z palbocyklibem w leczeniu kobiet z pewnym rodzajem raka piersi, tzw. rakiem piersi z obecnością receptorów hormonalnych, bez nadmiernej ekspresji receptora ludzkiego naskórkowego czynnika wzrostu 2, który jest miejscowo zaawansowany lub rozprzestrzenił się do innych części ciała (przerzuty). Kobiety przed menopauzą będą również otrzymywać lek zwany agonistą hormonu uwalniającego hormon luteinizujący (LHRH).
Gdy lek Fulvestrant Sandoz podaje się razem z palbocyklibem, ważne jest, aby przeczytać także ulotkę dołączoną do opakowania leku zawierającego palbocyklib. W razie jakichkolwiek pytań dotyczących palbocyklibu należy zwrócić się do lekarza prowadzącego.
Informacje ważne przed zastosowaniem leku Fulvestrant Sandoz Kiedy nie stosować leku Fulvestrant Sandoz
jeśli pacjentka ma uczulenie na fulwestrant lub którykolwiek z pozostałych składników tego leku (wymienionych w punkcie 6);
jeśli pacjentka jest w ciąży lub karmi piersią;
jeśli pacjentka ma ciężkie zaburzenia czynności wątroby.
Ostrzeżenia i środki ostrożności
Przed zastosowaniem leku Fulvestrant Sandoz należy omówić to z lekarzem, farmaceutą lub
pielęgniarką, jeśli którykolwiek z poniższych problemów zdrowotnych dotyczy pacjentki:
zaburzenia czynności nerek lub wątroby;
mała liczba płytek krwi (uczestniczących w procesie krzepnięcia) lub zaburzenia krwawienia;
występująca w przeszłości choroba zakrzepowa;
osteoporoza (zmniejszona gęstość kości);
choroba alkoholowa.
Dzieci i młodzież
Fulvestrant Sandoz nie jest przeznaczony do stosowania u dzieci i młodzieży w wieku poniżej 18 lat.
Fulvestrant Sandoz a inne leki
Należy powiedzieć lekarzowi lub farmaceucie o wszystkich lekach przyjmowanych przez pacjentkę obecnie lub ostatnio, a także o lekach, które pacjentka planuje stosować.
W szczególności należy powiedzieć lekarzowi o stosowaniu leków przeciwzakrzepowych (leków zapobiegających powstawaniu zakrzepów krwi).
Ciąża i karmienie piersią
Jeśli kobieta jest w ciąży lub karmi piersią, przypuszcza, że może być w ciąży lub gdy planuje mieć dziecko, powinna przed zastosowaniem tego leku poradzić się lekarza.
Leku Fulvestrant Sandoz nie wolno stosować w ciąży. Pacjentki w wieku rozrodczym powinny stosować skuteczne metody antykoncepcji w trakcie leczenia i przez 2 lata po przyjęciu ostatniej dawki.
Podczas stosowania leku Fulvestrant Sandoz nie wolno karmić piersią.
Prowadzenie pojazdów i obsługiwanie maszyn
Wpływ leku Fulvestrant Sandoz na zdolność prowadzenia pojazdów lub obsługiwania maszyn nie jest spodziewany. Jeśli jednak leczenie powoduje u pacjentki zmęczenie, nie powinna podejmować tych czynności.
Fulvestrant Sandoz zawiera etanol, alkohol benzylowy i benzoesan benzylu
Ten lek zawiera 1000 mg alkoholu (etanolu 96%) na dawkę, co jest równoważne 100 mg/ml (10% w/v). Ilość alkoholu w dawce tego leku jest równoważna mniej niż 24 ml piwa lub 10 ml wina. Mała ilość alkoholu w tym leku nie będzie powodowała zauważalnych skutków.
Ten lek zawiera 1000 mg alkoholu benzylowego na dawkę, co odpowiada 100 mg/ml. Alkohol benzylowy może wywoływać reakcje alergiczne.
Podawanie alkoholu benzylowego małym dzieciom wiąże się z ryzykiem ciężkich działań niepożądanych, w tym zaburzeń oddychania (tzw. ”gasping syndrome”).
Nie podawać noworodkom (do 4. tygodnia życia) bez zalecenia lekarza.
Nie podawać małym dzieciom (w wieku poniżej 3 lat) dłużej niż przez tydzień bez zalecenia lekarza lub farmaceuty.
Pacjentki z chorobami wątroby lub nerek powinny skontaktować się z lekarzem przed zastosowaniem leku, gdyż duża ilość alkoholu benzylowego może gromadzić się w ich organizmie i powodować działania niepożądane (tzw. kwasicę metaboliczną).
Ten lek zawiera 1500 mg benzoesanu benzylu na dawkę, co odpowiada 150 mg/ml. Benzoesan benzylu może zwiększyć ryzyko żółtaczki (zażółcenie skóry i białkówek oczu) u noworodków (do 4. tygodnia życia).
Jak stosować Fulvestrant Sandoz
Ten lek należy zawsze stosować zgodnie z zaleceniami lekarza lub farmaceuty. W razie wątpliwości należy zwrócić się do lekarza lub farmaceuty.
Zalecaną dawką leku fulwestrantu jest 500 mg (dwa wstrzyknięcia po 250 mg), podawanych raz na miesiąc oraz dodatkowa dawka 500 mg podana po 2 tygodniach od pierwszej dawki.
Fulvestrant Sandoz podawany jest przez lekarza lub pielęgniarkę w powolnym wstrzyknięciu domięśniowym, po jednym w każdy pośladek.
W razie jakichkolwiek dalszych wątpliwości związanych ze stosowaniem tego leku należy zwrócić się do lekarza, farmaceuty lub pielęgniarki.
Możliwe działania niepożądane
reakcje uczuleniowe (nadwrażliwości), w tym obrzęk twarzy, warg, języka i (lub) gardła, mogące być objawami reakcji anafilaktycznych
zakrzep z zatorami (zwiększone ryzyko powstawania zakrzepów krwi)*
zapalenie wątroby
niewydolność wątroby
Należy zgłosić lekarzowi, farmaceucie lub pielęgniarce wystąpienie któregokolwiek z poniższych działań niepożądanych:
Bardzo częste działania niepożądane (mogą występować częściej niż u 1 na 10 osób)
odczyn w miejscu wstrzyknięcia, np. ból i (lub) zapalenie;
nieprawidłowa aktywność enzymów wątrobowych (wykrywana w badaniach krwi)*
nudności
osłabienie, zmęczenie*
ból stawów i bóle kostno-szkieletowe
uderzenia gorąca
wysypka skórna
reakcje alergiczne (nadwrażliwości), w tym obrzęk twarzy, warg, języka i (lub) gardła
Wszystkie pozostałe działania niepożądane
Częste działania niepożądane (mogą występować rzadziej niż u 1 na 10 osób)
ból głowy
wymioty, biegunka lub utrata apetytu*
zakażenia dróg moczowych
ból pleców*
zwiększenie stężenia bilirubiny (barwnik żółci wytwarzany w wątrobie)
zakrzep z zatorami (zwiększone ryzyko powstawania zakrzepów krwi)*
zmniejszona liczba płytek krwi (małopłytkowość)
krwawienie z pochwy
ból w dolnej części pleców, promieniujący do jednej nogi (rwa kulszowa)
nagłe osłabienie, drętwienie, mrowienie lub utrata ruchomości w nodze (zwłaszcza z jednej strony ciała), nagłe trudności w chodzeniu lub utrzymaniu równowagi (neuropatia obwodowa)
Niezbyt częste działania niepożądane (mogą występować rzadziej niż u 1 na 100 osób):
gęsta, biaława wydzielina z pochwy i drożdżyca (zakażenie)
powstanie siniaka i krwawienie w miejscu wstrzyknięcia leku
zwiększenie aktywności enzymu wątrobowego gamma-GT (wykrywane w badaniu krwi)
zapalenie wątroby
niewydolność wątroby
drętwienie, mrowienie i ból
reakcje anafilaktyczne
* działania niepożądane, w których powstaniu dokładna rola leku Fulvestrant Sandoz nie jest ustalona ze względu na chorobę podstawową
Zgłaszanie działań niepożądanych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione w ulotce, należy powiedzieć o tym lekarzowi, farmaceucie lub pielęgniarce. Działania niepożądane można zgłaszać bezpośrednio do Departamentu Monitorowania Niepożądanych Działań Produktów Leczniczych Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych: Al. Jerozolimskie 181 C, 02 - 222 Warszawa
tel.: + 48 22 49 21 301/faks: + 48 22 49 21 309/strona internetowa: https://smz.ezdrowie.gov.pl Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Dzięki zgłaszaniu działań niepożądanych można będzie zgromadzić więcej informacji na temat bezpieczeństwa stosowania leku.
Jak przechowywać Fulvestrant Sandoz
Lek przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Nie stosować tego leku po upływie terminu ważności zamieszczonego na pudełku tekturowym lub etykiecie ampułko-strzykawki po: EXP. Termin ważności oznacza ostatni dzień podanego miesiąca.
Ten lek nie wymaga żadnych szczególnych warunków przechowywania.
Fachowy personel jest odpowiedzialny za prawidłowe przechowywanie, sposób użycia i usuwanie opakowania po zużytym leku Fulvestrant Sandoz.
Nie stosować leku, jeśli zauważy się jakiekolwiek oznaki uszkodzenia ampułko-strzykawki lub zepsucia jej zawartości w postaci np. zmętnienia roztworu, pływajacych w nim cząstek lub zmiany zabarwienia.
Leków nie należy wyrzucać do kanalizacji ani domowych pojemników na odpadki. Należy zapytać farmaceutę, jak usunąć leki, których się już nie używa. Takie postępowanie pomoże chronić środowisko.
Zawartość opakowania i inne informacje Co zawiera Fulvestrant Sandoz
Substancją czynną jest fulwestrant.
Jedna ampułko-strzykawka zawiera 250 mg fulwestrantu w 5 ml roztworu (50 mg/ml).
Pozostałe składniki to: etanol (96%), alkohol benzylowy, benzylu benzoesan i olej rycynowy.
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
W razie wystąpienia któregokolwiek z następujących działań niepożądanych konieczna może być natychmiastowa pomoc medyczna:
Jak wygląda Fulvestrant Sandoz i co zawiera opakowanie
Fulvestrant Sandoz jest przezroczystym, bezbarwnym do żółtego, lepkim roztworem do wstrzykiwań w ampułko-strzykawce.
Opakowanie zawiera jedną lub dwie pojedyncze ampułko-strzykawki. Dodatkowo w opakowaniu znajduje się jałowa igła.
Podmiot odpowiedzialny i wytwórca
Podmiot odpowiedzialny
Sandoz GmbH Biochemiestrasse 10
6250 Kundl, Austria
Wytwórca
Lek Pharmaceuticals d.d.
Verovškova 57
1526 Ljubljana, Słowenia
EBEWE Pharma Ges.m.b.H. Nfg.KG Mondseestrasse 11
4866 Unterach, Austria
Fareva Unterach GmbH Mondseestraße 11
4866 Unterach, Austria
W celu uzyskania bardziej szczegółowych informacji na temat leku oraz jego nazw w krajach członkowskich Europejskiego Obszaru Gospodarczego należy zwrócić się do:
Sandoz Polska Sp. z o.o. ul. Domaniewska 50 C 02-672 Warszawa
tel. 22 209 70 00
Data ostatniej aktualizacji ulotki: 01/2022
Logo Sandoz
Informacje przeznaczone wyłącznie dla fachowego personelu medycznego:
Dawkę leku Fulvestrant Sandoz 500 mg (2 x 250 mg/5 ml roztwór do wstrzykiwań) należy podawać przy użyciu dwóch ampułko-strzykawek (patrz punkt 3).
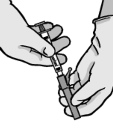
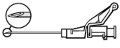
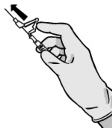
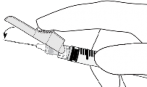
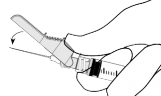
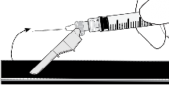
Instrukcja podawania
Ostrzeżenie – przed zastosowaniem nie wyjaławiać w autoklawie igły z systemem osłaniającym. Podczas stosowania leku i usuwania pozostałości unikać kontaktu rąk z igłą.
Strzykawki są dostarczane z igłą z systemem osłaniającym BD SafetyGlide® lub Terumo SurGuard®.
Instrukcja dla igły z systemem osłaniającym BD SafetyGlide®
Dotyczy każdej strzykawki:
| |
| |
| |
| |
|
|
|
| |
osłaniającego igłę. |
|
|
|
UWAGA: Postępuj tak, aby zapewnić bezpieczeństwo sobie i innym. Nasłuchuj kliknięcia i upewnij się wzrokowo, czy końcówka igły jest całkowicie zakryta. | |
Instrukcja dla igły z systemem osłaniającym Terumo SurGuard ®
Dotyczy każdej strzykawki:
| |
| |
|
|
|
|
| |
| |
(aktywować) system osłaniający igłę, stosując jedną z trzech metod: | |
o aktywacja palcem wskazującym |
|
o aktywacja kciukiem |
|
o aktywacja o podłoże |
|
Aktywację potwierdza słyszalne i (lub) wyczuwalne kliknięcie, a można ją również stwierdzić wzrokowo. W razie wątpliwości, czy osłona całkowicie zakryła igłę, należy powtórzyć końcowy etap. | |
Usuwanie
Ampułko-strzykawki przeznaczone są wyłącznie do jednorazowego użycia.
Wszelkie niewykorzystane resztki produktu lub jego odpady należy usunąć zgodnie z lokalnymi przepisami.