Spis treści:
- NAZWA PRODUKTU LECZNICZEGO
- SKŁAD JAKOŚCIOWY I ILOŚCIOWY
- POSTAĆ FARMACEUTYCZNA
- SZCZEGÓŁOWE DANE KLINICZNE
- WŁAŚCIWOŚCI FARMAKOLOGICZNE
- DANE FARMACEUTYCZNE
- PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU
- NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
- DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU I DATA PRZEDŁUŻENIA POZWOLENIA
- DATA ZATWIERDZENIA LUB CZĘŚCIOWEJ ZMIANY TEKSTU CHARAKTERYSTYKI PRODUKTU LECZNICZEGO
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
NAZWA PRODUKTU LECZNICZEGO
SKŁAD JAKOŚCIOWY I ILOŚCIOWY
POSTAĆ FARMACEUTYCZNA
SZCZEGÓŁOWE DANE KLINICZNE
Wskazania do stosowania
w monoterapii do leczenia raka piersi z obecnymi receptorami estrogenowymi, miejscowo zaawansowanego lub z przerzutami, u kobiet po menopauzie:
wcześniej nieleczonych terapią hormonalną lub
z nawrotem choroby podczas lub po zakończeniu leczenia uzupełniającego lekiem z grupy antyestrogenów lub, gdy nastąpiła progresja choroby podczas leczenia lekiem z grupy antyestrogenów;
w skojarzeniu z palbocyklibem w leczeniu miejscowo zaawansowanego lub rozsianego raka piersi z obecnością receptorów hormonalnych (ang. hormone receptor, HR-dodatniego) i bez nadmiernej ekspresji receptora ludzkiego naskórkowego czynnika wzrostu 2 (ang. human epidermal growth factor receptor 2, HER2-ujemnego) u kobiet, które wcześniej otrzymały leczenie hormonalne (patrz punkt 5.1).
Dawkowanie i sposób podawania
Przeciwwskazania
Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania
Interakcje z innymi produktami leczniczymi i inne rodzaje interakcji
Wpływ na płodność, ciążę i laktację
Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn
Działania niepożądane
Przedawkowanie
WŁAŚCIWOŚCI FARMAKOLOGICZNE
Właściwości farmakodynamiczne
Właściwości farmakokinetyczne
Przedkliniczne dane o bezpieczeństwie
DANE FARMACEUTYCZNE
Wykaz substancji pomocniczych
Niezgodności farmaceutyczne
Okres ważności
Specjalne środki ostrożności podczas przechowywania
Rodzaj i zawartość opakowania
Tekturowe pudełko z blistrem zawierającym jedną ampułko-strzykawkę, jedną jałową igłę hipodermiczną z systemem zabezpieczającym (BD SafetyGlide) oraz jedną ulotkę.
Lub
Tekturowe pudełko z dwoma blistrami, z których każdy zawiera jedną ampułko-strzykawkę, dwoma jałowymi igłami hipodermicznymi z systemem zabezpieczającym (BD SafetyGlide) oraz jedną ulotką.
Lub
Tekturowe pudełko z sześcioma blistrami, z których każdy zawiera jedną ampułko-strzykawkę, sześcioma jałowymi igłami hipodermicznymi z systemem zabezpieczającym (BD SafetyGlide) oraz jedną ulotką.
Specjalne środki ostrożności dotyczące usuwania i przygotowania produktu leczniczego do stosowania
Należy wyjąć szklaną ampułkę z blistra i sprawdzić, czy nie jest uszkodzona.
Otworzyć opakowanie zewnętrzne igły z systemem osłaniającym (SafetyGlide).
Przed podaniem roztworów parenteralnych należy dokonać ich wizualnej oceny w celu wykrycia obecności cząstek stałych i zmiany barwy.
Trzymać strzykawkę pionowo.
Drugą ręką chwycić nasadkę, delikatnie odkręcić i zdjąć nasadkę końcówki. W celu zachowania sterylności nie dotykać końcówki strzykawki (patrz Rysunek 1).
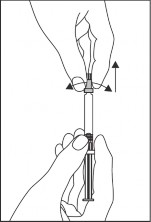
Rysunek 1
Dołączyć igłę z systemem osłaniającym do końcówki Luer-Lock i dokręcić w celu trwałego umocowania (patrz Rysunek 2).
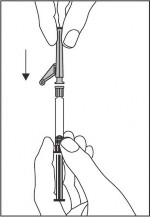
Rysunek 2
Sprawdzić czy igła jest połączona z końcówką Luer-Lock przed przejściem z pozycji pionowej.
Przy dokręcaniu igły należy postępować tak, aby nie uszkodzić jej ostrego końca.
Wypełnioną strzykawkę należy zbliżyć do miejsca podania
Zdjąć osłonkę z igły
Usunąć nadmiar powietrza ze strzykawki
Lek należy podawać domięśniowo, powoli (1-2 minuty/wstrzyknięcie), w pośladek (obszar mięśnia pośladkowego). Dla wygody osoby podającej, ścięcie igły znajduje się na tej samej powierzchni igły co dźwignia systemu osłaniającego igłę (patrz Rysunek 3).
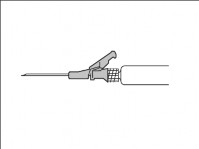
Rysunek 3
Natychmiast po podaniu leku należy uruchomić system osłaniający igłę przez jedno pchnięcie do przodu jego dźwigni (patrz Rysunek 4).
PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU
NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU I DATA PRZEDŁUŻENIA POZWOLENIA
DATA ZATWIERDZENIA LUB CZĘŚCIOWEJ ZMIANY TEKSTU CHARAKTERYSTYKI PRODUKTU LECZNICZEGO
Fulvestrant Stada, 250 mg/ 5 ml, roztwór do wstrzykiwań w ampułko-strzykawce
Jedna ampułko-strzykawka zawiera 250 mg fulwestrantu w 5 ml roztworu. Jeden ml roztworu do wstrzykiwań zawiera 50 mg fulwestrantu.
Substancje pomocnicze o znanym działaniu:
Jeden ml roztworu zawiera 100 mg etanolu (96%), 100 mg alkoholu benzylowego i 150 mg benzylu benzoesanu.
Pełny wykaz substancji pomocniczych, patrz punkt 6.1.
Roztwór do wstrzykiwań w ampułko-strzykawce.
Przejrzysty, bezbarwny do żółtego, niemal wolny od widocznych cząsteczek, oleisty i lepki roztwór.
Stosowanie produktu leczniczego Fulvestrant Stada wskazane jest:
U kobiet przed menopauzą i w okresie okołomenopauzalnym leczenie skojarzone z palbocyklibem należy stosować jednocześnie z agonistą hormonu uwalniającego hormon luteinizujący
(ang. luteinizing hormone releasing hormone, LHRH).
Dawkowanie
Dorosłe pacjentki (także starsze pacjentki)
Zalecana dawka leku to 500 mg, podawana w odstępach jednomiesięcznych z dodatkową dawką 500 mg podaną po upływie 2 tygodni od podania pierwszej dawki.
Gdy fulwestrant jest stosowany w skojarzeniu z palbocyklibem, należy zapoznać się z Charakterystyką Produktu Leczniczego palbocyklibu.
Przed rozpoczęciem leczenia skojarzonego fulwestrantem z palbocyklibem i przez cały czas jego trwania, pacjentki w wieku przed- i okołomenopauzalnym powinny otrzymywać leczenie agonistami LHRH zgodnie z lokalnie przyjętą praktyką kliniczną.
Szczególne grupy pacjentów
Zaburzenia czynności nerek
Nie zaleca się modyfikacji dawki u pacjentek z łagodnymi i umiarkowanymi zaburzeniami czynności nerek (klirens kreatyniny 30 ml/min). Nie badano skuteczności i bezpieczeństwa stosowania produktu u pacjentek z ciężkimi zaburzeniami czynności nerek (klirens kreatyniny < 30 ml/min), dlatego zaleca się ostrożność podczas stosowania w tej grupie pacjentek (patrz punkt 4.4).
Zaburzenia czynności wątroby
Nie zaleca się modyfikacji dawki u pacjentek z zaburzeniami czynności wątroby o nasileniu łagodnym do umiarkowanego. Jednak u tej grupy pacjentek produkt Fulvestrant Stada należy stosować ostrożnie ze względu na możliwość zwiększenia ekspozycji na fulwestrant. Brak danych dotyczących stosowania produktu u pacjentek z ciężkimi zaburzeniami czynności wątroby (patrz punkty 4.3, 4.4
i 5.2).
Dzieci i młodzież
Bezpieczeństwo stosowania i skuteczność działania produktu Fulvestrant Stada u dzieci
i młodzieży w wieku do 18 lat nie zostały ustalone. Aktualne dane przedstawiono w punktach 5.1 i 5.2, ale niemożliwe jest ustalenie zaleceń dotyczących dawkowania.
Sposób podawania
Fulvestrant Stada należy podawać powoli (czas jednego wstrzyknięcia 1-2 minuty), domięśniowo
w dwóch kolejnych wstrzyknięciach po 5 ml, każde w inny pośladek (obszar mięśnia pośladkowego).
Należy zachować ostrożność podczas podawania wstrzyknięcia produktu Fulvestrant Stada w górnoboczną okolicę pośladka ze względu na bliskość nerwu kulszowego.
Pełna instrukcja podawania, patrz punkt 6.6.
Nadwrażliwość na substancję czynną lub na którąkolwiek substancję pomocniczą wymienioną w punkcie 6.1.
Ciąża i karmienie piersią (patrz punkt 4.6).
Ciężkie zaburzenia czynności wątroby (patrz punkty 4.4 i 5.2).
Fulwestrant należy stosować ostrożnie u pacjentek z zaburzeniami czynności wątroby o nasileniu łagodnym do umiarkowanego (patrz punkty 4.2, 4.3 i 5.2).
Fulwestrant należy stosować ostrożnie u pacjentek z ciężkimi zaburzeniami czynności nerek (klirens kreatyniny mniejszy niż 30 ml/min).
Ze względu na domięśniową drogę podania, fulwestrant należy stosować ostrożnie u pacjentek ze skazą krwotoczną, trombocytopenią lub u pacjentek stosujących leki przeciwzakrzepowe.
U pacjentek z zaawansowanym rakiem piersi często występują zaburzenia zatorowo-zakrzepowe. Zaburzenia te obserwowano także u pacjentek w badaniach klinicznych z zastosowaniem fulwestrantu (patrz punkt 4.8). Należy wziąć to pod uwagę przepisując fulwestrant pacjentkom z grupy ryzyka.
W związku ze wstrzyknięciem fulwestrantu zgłaszano reakcje w miejscu wstrzyknięcia takie jak rwa kulszowa, nerwoból, ból neuropatyczny i neuropatia obwodowa.
Należy zachować ostrożność podczas podawania produktu leczniczego fulwestrant w górnoboczną okolicę pośladka ze względu na bliskość nerwu kulszowego (patrz punkty 4.2 i 4.8).
Brak jest danych dotyczących odległych skutków działania fulwestrantu na kości. W związku z mechanizmem działania fulwestrantu istnieje potencjalne ryzyko wystąpienia osteoporozy.
Nie badano skuteczności i bezpieczeństwa stosowania fulwestrantu (podawanego w monoterapii lub w skojarzeniu z palbocyklibem) u pacjentek z masywnymi przerzutami do narządów miąższowych.
Gdy fulwestrant jest stosowany w skojarzeniu z palbocyklibem, należy zapoznać się także z Charakterystyką Produktu Leczniczego palbocyklibu.
Interakcje z testami przeciwciał estradiolu
Ze względu na podobieństwo struktury fulwestrantu i estradiolu, fulwestrant może oddziaływać z testami wykrywającymi poziom estradiolu opartymi na przeciwciałach oraz może powodować fałszywie wysoki poziom estradiolu.
Dzieci i młodzież
Fulvestrant Stada nie jest zalecany do stosowania u dzieci i młodzieży ponieważ nie ustalono bezpieczeństwa ani skuteczności działania u tej grupy pacjentów (patrz punkt 5.1).
Substancje pomocnicze
Etanol 96%
Ten produkt leczniczy zawiera 12,4% objętościowo etanolu (alkohol), tj. 1000 mg w każdej dawce zawierającej 500 mg fulwestrantu, co odpowiada 25 ml piwa lub 10 ml wina na dawkę.
Taka ilość alkoholu prawdopodobnie nie będzie miała wpływu na osoby dorosłe.
Alkohol zawarty w tym produkcie leczniczym może zmieniać działanie innych, stosowanych produktów leczniczych.
Szkodliwe dla osób z chorobą alkoholową.
Alkohol benzylowy
Ten produkt leczniczy zawiera 1000 mg alkoholu benzylowego w każdej dawce zawierającej 500 mg fulwestrantu. Alkohol benzylowy może powodować reakcje alergiczne.
Duże objętości należy podawać z ostrożnością i tylko w razie konieczności, zwłaszcza u pacjentow z zaburzeniami czynności wątroby lub nerek z powodu ryzyka kumulacji i toksyczności (kwasica metaboliczna).
Benzylu benzoesan
Ten produkt leczniczy zawiera 1500 mg benzylu benzoesanu w każdej dawce zawierającej 500 mg fulwestrantu.
Wyniki badania klinicznego nad interakcją z midazolamem (substratem CYP3A4) wykazały, że fulwestrant nie wpływa hamująco na CYP3A4. W przeprowadzonych badaniach klinicznych
nad interakcją z ryfampicyną (lekiem pobudzającym aktywność CYP3A4) i ketokonazolem (lekiem hamującym aktywność CYP3A4), nie stwierdzono istotnej klinicznie zmiany klirensu fulwestrantu. W związku z powyższym nie ma konieczności zmiany dawki fulwestrantu, jeśli jest on stosowany jednocześnie z innymi lekami o działaniu hamującym lub pobudzającym aktywność CYP3A4.
Kobiety w wieku rozrodczym
Pacjentki w wieku rozrodczym powinny stosować skuteczną antykoncepcję w trakcie leczenia fulwestrantem i przez 2 lata po przyjęciu ostatniej dawki.
Ciąża
Fulwestrant jest przeciwwskazany do stosowania w ciąży (patrz punkt 4.3). W badaniach na szczurach i królikach wykazano, że fulwestrant po podaniu pojedynczej dawki domięśniowej przenika
przez łożysko. Badania na zwierzętach wykazały toksyczny wpływ na rozrodczość, w tym
na zwiększenie liczby nieprawidłowości i zgonów płodów (patrz punkt 5.3). Jeśli podczas stosowania produktu Fulvestrant Stada zostanie stwierdzona ciąża, pacjentkę należy niezwłocznie poinformować o potencjalnym ryzyku uszkodzenia płodu i utraty ciąży.
Karmienie piersią
Należy przerwać karmienie piersią w trakcie leczenia fulwestrantem. Fulwestrant przenika do mleka szczurów w okresie laktacji. Nie wiadomo, czy fulwestrant przenika do mleka kobiecego. W związku z możliwością wystąpienia ciężkich działań niepożądanych u karmionego piersią dziecka, którego matka jest leczona fulwestrantem, stosowanie leku w okresie karmienia piersią jest przeciwwskazane (patrz punkt 4.3).
Płodność
Nie badano wpływu stosowania fulwestrantu na płodność u ludzi.
Fulwestrant nie ma wpływu lub ma znikomy wpływ na zdolność prowadzenia pojazdów lub obsługiwania maszyn. Jednak w trakcie stosowania fulwestrantu bardzo często występuje astenia. Pacjenci, u których występuje to działanie niepożądane, powinni zachować szczególną ostrożność podczas prowadzenia pojazdów i obsługiwania maszyn.
Podsumowanie profilu bezpieczeństwa
Monoterapia
W tym punkcie przedstawiono informacje dotyczące wszystkich działań niepożądanych, uzyskane podczas badań klinicznych, stosowania klinicznego po wprowadzeniu do obrotu lub pochodzące ze zgłoszeń spontanicznych. W zbiorczym zbiorze danych dotyczących stosowania fulwestrantu w monoterapii do najczęściej zgłaszanych działań niepożądanych należały odczyny w miejscu
wstrzyknięcia, astenia, nudności i zwiększenie aktywności enzymów wątrobowych (AlAT, AspAT, fosfataza alkaliczna).
Kategorie częstości występowania działań niepożądanych podane w Tabeli 1 zostały zdefiniowane w oparciu o zbiorcze analizy bezpieczeństwa stosowania w grupie terapeutycznej fulwestrantu
w dawce 500 mg w badaniach porównujących fulwestrant w dawce 500 mg z fulwestrantem w dawce 250 mg [CONFIRM (badanie D6997C00002), FINDER 1 (badanie D6997C00004), FINDER 2
(badanie D6997C00006), NEWEST (badanie D6997C00003)] lub tylko z badania FALCON (badanie D699BC00001), w którym porównywano fulwestrant w dawce 500 mg z anastrozolem 1 mg.
W przypadku różnic w częstości występowania między zbiorczą analizą bezpieczeństwa a badaniem FALCON, przedstawiono największą częstość występowania. Częstości wymienione w Tabeli 1 są podane w oparciu o wszystkie zgłoszone działania niepożądane leku, niezależnie od oceny związku przyczynowo-skutkowego przez badacza. Mediana czasu trwania leczenia fulwestrantem w dawce
500 mg dla zbiorczej grupy danych (w tym w badaniach wymienionych wyżej i w badaniu FALCON) wyniosła 6,5 miesiąca.
Tabelaryczne zestawienie działań niepożądanych
Działania niepożądane zostały podane zgodnie z częstością ich występowania oraz z klasyfikacją układów i narządów. Grupy o określonej częstości występowania działań niepożądanych określone są zgodnie z następującą konwencją: Bardzo często (1/10), Często (1/100 do <1/10), Niezbyt często (1/1000 do <1/100). W obrębie każdej grupy o określonej częstości występowania działań niepożądanych są one wymienione według zmniejszającego się nasilenia.
Tabela 1. Działania niepożądane zgłaszane u pacjentek leczonych fulwestrantem w monoterapii
Działania niepożądane podzielone według układów i narządów oraz częstości występowania | ||
Zakażenia i zarażenia pasożytnicze | Często | Zakażenia układu moczowego |
Zaburzenia krwi i układu chłonnego | Często | Zmniejszenie liczby płytek krwie |
Zaburzenia układu immunologicznego | Bardzo często | Reakcje nadwrażliwoście |
Niezbyt często | Reakcje anafilaktyczne | |
Zaburzenia metabolizmu i odżywiania | Często | Anoreksjaa |
Zaburzenia układu nerwowego | Często | Ból głowy |
Zaburzenia naczyniowe | Bardzo często | Uderzenia gorącae |
Często | Żylna choroba zakrzepowo-zatorowaa | |
Zaburzenia żołądka i jelit | Bardzo często | Nudności |
Często | Wymioty, biegunka | |
Zaburzenia wątroby i dróg żółciowych | Bardzo często | Zwiększenie aktywności enzymów wątrobowych (AlAT, AspAT, fosfataza zasadowa)a |
Często | Zwiększenie stężenia bilirubinya | |
Niezbyt często | Niewydolność wątrobyc, f, zapalenie wątrobyf, zwiększenie aktywności gamma- glutamylotranspeptydazy (GGTP)f | |
Zaburzenia skóry i tkanki podskórnej | Bardzo często | Wysypkae |
Zaburzenia mięśniowo-szkieletowe i tkanki łącznej | Bardzo często | Bóle stawów i mięśniowo-szkieletowed |
Często | Ból plecówa | |
Zaburzenia układu rozrodczego i piersi | Często | Krwotok z pochwye |
Niezbyt często | Kandydoza pochwyf, obfite białe upławyf | |
Zaburzenia ogólne i stany w miejscu podania | Bardzo często | Asteniaa, reakcje w miejscu wstrzyknięciab |
Często | Neuropatia obwodowae, rwa kulszowae | |
Niezbyt często | Krwotok z miejsca wstrzyknięciaf, krwiak w miejscu wstrzyknięciaf, nerwobólc, f | |
a Dotyczy działań niepożądanych, dla których dokładny zakres udziału fulwestrantu nie może być określony z powodu istnienia choroby podstawowej.
b Termin reakcje w miejscu wstrzyknięcia nie obejmuje terminów krwotok z miejsca wstrzyknięcia, krwiak w miejscu wstrzyknięcia, rwa kulszowa, nerwoból, neuropatia obwodowa.
c Zdarzenia nie obserwowano podczas dużych badań klinicznych (CONFIRM, FINDER 1, FINDER 2, NEWEST).
Częstość występowania zdarzenia obliczono przyjmując górną granicę 95% przedziału ufności dla estymacji punktowej. Uzyskano wartość 3/560 (gdzie 560 to liczba pacjentów w dużych badaniach klinicznych), co odpowiada kategorii „niezbyt często” dla częstości występowania zdarzeń niepożądanych.
d Obejmuje: ból stawów i rzadziej bóle mięśniowo-szkieletowe, ból mięśni oraz ból kończyny. e Kategoria częstości różni się między danymi ze zbiorczej analizy bezpieczeństwa a badaniem FALCON.
f Tego działania niepożądanego nie obserwowano w badaniu FALCON.
Opis wybranych działań niepożądanych
Podane niżej opisy opierają się na analizie bezpieczeństwa obejmującej 228 pacjentek, które otrzymały przynajmniej jedną (1) dawkę fulwestrantu i 232 pacjentek, które otrzymały przynajmniej jedną (1) dawkę anastrozolu odpowiednio w badaniu fazy 3 FALCON.
Bóle stawów i mięśniowo-szkieletowe
W badaniu FALCON liczba pacjentek zgłaszających działanie niepożądane w postaci bólów stawów i mięśniowo-szkieletowych wynosiła 65 (31,2%) i 48 (24,1%) odpowiednio w grupie fulwestrantu
i anastrozolu. Czterdzieści procent (40%) pacjentek spośród 65 (26/65) z grupy otrzymującej fulwestrant zgłaszało bóle stawów i mięśniowo-szkieletowe w pierwszym miesiącu leczenia, a 66,2% (43/65) pacjentek zgłaszało te bóle w pierwszych 3 miesiącach leczenia. Żadna z pacjentek nie zgłosiła zdarzeń o nasileniu stopnia ≥3 wg CTCAE lub wymagających zmniejszenia dawki, przerwania podawania leku bądź zakończenia leczenia z powodu tych działań niepożądanych.
Leczenie skojarzone z palbocyklibem
Ogólny profil bezpieczeństwa fulwestrantu stosowanego w skojarzeniu z palbocyklibem opiera się
na danych pochodzących od 517 pacjentek z miejscowo zaawansowanym lub rozsianym rakiem piersi z obecnością receptorów hormonalnych (HR-dodatnim) i bez nadmiernej ekspresji receptora ludzkiego naskórkowego czynnika wzrostu 2 (HER2-ujemnym), uczestniczących w randomizowanym badaniu PALOMA3 (patrz punkt 5.1). Najczęstszymi (≥20%) działaniami niepożądanymi dowolnego stopnia nasilenia, zgłaszanymi u pacjentek otrzymujących fulwestrant w skojarzeniu z palbocyklibem były neutropenia, leukopenia, zakażenia, uczucie zmęczenia, nudności, niedokrwistość, zapalenie jamy ustnej, biegunka, małopłytkowość i wymioty. Najczęstszymi (≥2%) działaniami niepożądanymi o nasileniu stopnia ≥3 były neutropenia, leukopenia, zakażenia, niedokrwistość, zwiększenie aktywności AspAT, małopłytkowość i uczucie zmęczenia.
W Tabeli 2 przedstawiono działania niepożądane występujące w badaniu PALOMA3.
Mediana czasu trwania ekspozycji na fulwestrant wyniosła 11,2 miesiąca w grupie otrzymującej fulwestrant w skojarzeniu z palbocyklibem oraz 4,8 miesiąca w grupie otrzymującej fulwestrant w skojarzeniu z placebo.
Mediana czasu trwania ekspozycji na palbocyklib w grupie otrzymującej fulwestrant w skojarzeniu z palbocyklibem wyniosła 10,8 miesiąca.
Tabela 2. Działania niepożądane na podstawie danych z badania PALOMA3 (N=517)
Klasyfikacja układów i narządów Częstość Termin preferowanya | Fulwestrant + Palbocyklib (N=345) | Fulwestrant + placebo (N=172) | ||
Wszystkie stopnie nasilenia n (%) | Nasilenie stopnia ≥ 3 n (%) | Wszystkie stopnie nasilenia n (%) | Nasilenie stopnia ≥ 3 n (%) | |
Zakażenia i zarażenia pasożytnicze | ||||
Bardzo często | ||||
Zakażeniab | 188 (54,5) | 19 (5,5) | 60 (34,9) | 6 (3,5) |
Zaburzenia krwi i układu chłonnego | ||||
Bardzo często | ||||
Neutropeniac | 290 (84,1) | 240 (69,6) | 6 (3,5) | 0 |
Leukopeniad | 207 (60,0) | 132 (38,3) | 9 (5,2) | 1 (0,6) |
Niedokrwistośće | 109 (31,6) | 15 (4,3) | 24 (14,0) | 4 (2,3) |
Trombocytopeniaf | 88 (25,5) | 10 (2,9) | 0 | 0 |
Niezbyt często | ||||
Gorączka neutropeniczna | 3 (0,9) | 3 (0,9) | 0 | 0 |
Zaburzenia metabolizmu i odżywiania | ||||
Bardzo często | ||||
Zmniejszenie apetytu | 60 (17.4) | 4 (1.2) | 18 (10.5) | 1 (0,6) |
Zaburzenia układu nerwowego | ||||
Często | ||||
Zaburzenia smaku | 27 (7.8) | 0 | 6 (3.5) | 0 |
Zaburzenia oka | ||||
Często | ||||
Nasilone łzawienied | 25 (7.2) | 0 | 2 (1,2) | 0 |
Nieostre widzenied | 24 (7.0) | 0 | 3 (1,7) | 0 |
Suchość oka | 15 (4.3) | 0 | 3 (1,7) | 0 |
Zaburzenia układu oddechowego, klatki piersiowej i śródpiersia | ||||
Często | ||||
Krwawienie z nosa | 25 (7.2) | 0 | 4 (2.3) | 0 |
Zaburzenia żołądka i jelit | ||||
Bardzo często | ||||
Nudności | 124 (35.9) | 2 (0.6) | 53 (30.8) | 1 (0,6) |
Zapalenie jamy ustnejg | 104 (30.1) | 3 (0.9) | 24 (14.0) | 0 |
Biegunka | 94 (27.2) | 0 | 35 (20.3) | 2 (1,2) |
Wymioty | 75 (21.7) | 2 (0,6) | 28 (16.3) | 1 (0,6) |
Zaburzenia skóry i tkanki podskórnej | ||||
Bardzo często | ||||
Łysienie | 67 (19.4) | nd | 11 (6,4) | nd |
Wysypkah | 63 (18.3) | 3 (0.9) | 10 (5.8) | 0 |
Często | ||||
Suchość skóry | 28 (8.1) | 0 | 3 (1.7) | 0 |
Zaburzenia ogólne i stany w miejscu podania | ||||
Bardzo często | ||||
Zmęczenie | 152 (44.1) | 9 (2.6) | 54 (31.4) | 2 (1,2) |
Gorączka | 47 (13.6) | 1 (0,3) | 10 (5.8) | 0 |
Często | ||||
Osłabienie | 27 (7.8) | 1 (0.3) | 13 (7.6) | 2 (1.2) |
Badania diagnostyczne | ||||
Często | ||||
Zwiększenie aktywności AspAT | 40 (11.6) | 11 (3.2) | 13 (7.6) | 4 (2.3) |
Zwiększenie aktywności AlAT | 30 (8.7) | 7 (2.0) | 10 (5.8) | 1 (0.6) |
AlAT=aminotransferaza alaninowa; AspAT=aminotransferaza asparaginianowa; N/n=liczba pacjentów; nd = nie dotyczy
a Preferowana terminologia (PT) podana zgodnie z konwencją MedDRA 17.1.
b Zakażenia obejmują wszystkie PT należące do zakażeń i zarażeń pasożytniczych w klasyfikacji układów i narządów.
c Neutropenia obejmuje następujące PT: neutropenię, zmniejszoną liczbę neutrofilów.
d Leukopenia obejmuje następujące PT: leukopenię, zmniejszoną liczbę białych krwinek.
e Niedokrwistość obejmuje następujące PT: niedokrwistość, zmniejszenie stężenia hemoglobiny, zmniejszenie wartości hematokrytu.
f Małopłytkowość obejmuje następujące PT: małopłytkowość, zmniejszoną liczbę płytek krwi.
g Zapalenie jamy ustnej obejmuje następujące PT: aftowe zapalenie jamy ustnej, zapalenie czerwieni warg, zapalenie języka, ból języka, owrzodzenie jamy ustnej, zapalenie błony śluzowej, ból jamy ustnej, uczucie dyskomfortu w jamie ustnej i gardle, ból jamy ustnej i gardła, zapalenie jamy ustnej.
h Wysypka obejmuje następujące PT: wysypkę, wysypkę grudkowo-plamkową, wysypkę ze świądem, wysypkę z rumieniem, wysypkę grudkową, zapalenie skóry, trądzikopodobne zapalenie skóry, toksyczne wykwity skórne.
Opis wybranych działań niepożądanych
Neutropenia
U pacjentek otrzymujących fulwestrant w skojarzeniu z palbocyklibem w badaniu PALOMA3 neutropenię dowolnego stopnia nasilenia zgłaszano u 290 (84,1%) pacjentek, przy czym neutropenię o nasileniu stopnia 3. zgłoszono u 200 (58,0%) pacjentek, a neutropenię o nasileniu stopnia 4 zgłoszono u 40 (11,6%) pacjentek. W grupie otrzymującej fulwestrant w skojarzeniu z placebo (n=172) neutropenię dowolnego stopnia nasilenia zgłaszano u 6 (3,5%) pacjentek. Nie zgłaszano
występowania neutropenii o nasileniu 3 i 4. stopnia w grupie otrzymującej fulwestrant w skojarzeniu z placebo.
U pacjentek otrzymujących fulwestrant w skojarzeniu z palbocyklibem mediana czasu do wystąpienia pierwszego epizodu neutropenii dowolnego stopnia nasilenia wyniosła 15 dni (zakres: 13-512),
a mediana czasu trwania neutropenii stopnia ≥3 wyniosła 16 dni. Gorączkę neutropeniczną zgłoszono u 3 (0,9%) pacjentek otrzymujących fulwestrant w skojarzeniu z palbocyklibem.
Zgłaszanie podejrzewanych działań niepożądanych
Po dopuszczeniu produktu leczniczego do obrotu istotne jest zgłaszanie podejrzewanych działań niepożądanych. Umożliwia to nieprzerwane monitorowanie stosunku korzyści do ryzyka stosowania produktu leczniczego. Osoby należące do fachowego personelu medycznego powinny zgłaszać wszelkie podejrzewane działania niepożądane za pośrednictwem Departamentu Monitorowania Niepożądanych Działań Produktów Leczniczych Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych:
Al. Jerozolimskie 181C, 02-222 Warszawa, tel.: + 48 22 49-21-301, fax: +48 22 49-21-309
Strona internetowa: https://smz.ezdrowie.gov.pl
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Zgłoszono pojedyncze przypadki przedawkowania fulwestrantu u ludzi. W przypadku przedawkowania należy zastosować objawowe leczenie wspomagające. Z badań przeprowadzonych na zwierzętach wynika, że w przypadku stosowania fulwestrantu w większych dawkach należy oczekiwać jedynie objawów związanych z bezpośrednim lub pośrednim działaniem antyestrogenowym (patrz punkt 5.3).
Grupa farmakoterapeutyczna: Leki stosowane w terapii hormonalnej, Antyestrogeny, Kod ATC: L02BA03
Mechanizm działania i wynik działania farmakodynamicznego
Fulwestrant jest kompetycyjnym antagonistą receptora estrogenowego wykazującym powinowactwo do receptora porównywalne z powinowactwem estradiolu. Fulwestrant blokuje troficzne działanie estrogenów nie wykazując nawet częściowego (estrogenopodobnego) działania agonistycznego.
Mechanizm działania polega na zmniejszeniu ilości (down-regulation) białka receptorowego receptora estrogenowego. W badaniach klinicznych u kobiet po menopauzie, z pierwotnym rakiem piersi, stwierdzono, że fulwestrant w porównaniu z placebo znacząco zmniejszał ilość białka receptora estrogenowego w guzach zawierających receptory estrogenowe (ER). Stwierdzono także, że
w znaczącym stopniu zmniejszyła się ekspresja receptora progesteronowego, co potwierdza brak wewnętrznej aktywności estrogenowej.
W przypadku leczenia neoadjuwantowego guzów piersi u kobiet po menopauzie wykazano także, że fulwestrant w dawce 500 mg w większym stopniu ogranicza ekspresję receptora estrogenowego i markera proliferacji Ki67 niż fulwestrant w dawce 250 mg.
Skuteczność kliniczna i bezpieczeństwo w zaawansowanym raku piersi
Monoterapia
Przeprowadzono badanie kliniczne fazy 3. u 736 kobiet po menopauzie z zaawansowanym rakiem piersi, u których doszło do nawrotu w trakcie lub po zakończeniu hormonalnego leczenia uzupełniającego, albo do progresji po leczeniu hormonalnym nowotworu zaawansowanego.
Do badania włączono 423 pacjentki, u których doszło do nawrotu albo do progresji w trakcie leczenia antyestrogenami (podgrupa antyestrogenów) i 313 pacjentek, u których doszło do nawrotu albo
do progresji w trakcie leczenia inhibitorami aromatazy (podgrupa inhibitorów aromatazy). Celem tego badania było porównanie skuteczności i bezpieczeństwa fulwestrantu w dawce 500 mg (n=362)
i w dawce 250 mg (n=374). Pierwszorzędowym punktem końcowym był czas przeżycia wolny
od progresji choroby (PFS), kluczowe drugorzędowe punkty końcowe skuteczności objęły odsetek odpowiedzi obiektywnych (ORR), odsetek korzyści klinicznych (CBR) i przeżycie całkowite (OS). Wyniki badania CONFIRM dotyczące skuteczności leczenia podsumowano w Tabeli 3.
Tabela 3. Podsumowanie wyników dotyczących pierwszorzędowego punktu końcowego oceny skuteczności (PFS) i kluczowych drugorzędowych punktów końcowych oceny skuteczności
w badaniu CONFIRM
Zmienna | Sposób oceny; porównanie leczenia | Fulwestrant 500 mg (N=362) | Fulwestrant 250 mg (N=374) | Porównanie między grupami (fulwestrant 500 mg/fulwestrant 250 mg) | ||
Współczynnik ryzyka | 95% CI | Wartość p | ||||
PFS | Mediana wyznaczona metodą K-M w miesiącach; iloraz ryzyka | |||||
Wszystkie pacjentki | 6,5 | 5,5 | 0,80 | 0,68, 0,94 | 0,006 | |
-Podgrupa AE (n=423) | 8,6 | 5,8 | 0,76 | 0,62, 0,94 | 0,013 | |
-Podgrupa IA (n=313)a | 5,4 | 4,1 | 0,85 | 0,67, 1,08 | 0,195 | |
OSb | Mediana wyznaczona metodą K-M w | |||||
miesiącach; wspólczynnik ryzyka | ||||||
Wszystkie pacjentki | 26,4 | 22,3 | 0,81 | 0,69, 0,96 | 0,016c | |
-Podgrupa AE (n=423) | 30,6 | 23,9 | 0,79 | 0,63, 0,99 | 0,038c | |
-Podgrupa IA (n=313)a | 24,1 | 20,8 | 0,86 | 0,67, 1,11 | 0,241c | |
Zmienna | Sposób oceny; porównanie leczenia | Fulwestrant 500 mg (N=362) | Fulwestrant 250 mg (N=374) | Porównanie między grupami (fulwestrant 500 mg/fulwestrant 250 mg) | ||
Bezwzględna różnica w % | 95% CI | |||||
ORRd | % pacjentek z odpowiedzią obiektywną; Bezwzględna różnica w % | |||||
Wszystkie pacjentki | 13,8 | 14,6 | -0,8 | -5,8, 6,3 | ||
-Podgrupa AE (n=296) | 18,1 | 19,1 | -1,0 | -8,2, 9,3 | ||
-Podgrupa IA (n=205)a | 7,3 | 8,3 | -1,0 | -5,5, 9,8 | ||
CBRe | % pacjentek z korzyścią kliniczną; Bezwzględna różnica w % | |||||
Wszystkie pacjentki | 45,6 | 39,6 | 6,0 | -1,1, 13,3 | ||
-Podgrupa AE (n=423) | 52,4 | 45,1 | 7,3 | -2,2, 16,6 | ||
-Podgrupa IA (n=313)a | 36,2 | 32,3 | 3,9 | -6,1, 15,2 | ||
a Fulwestrant jest wskazany u pacjentek, u których nastąpił nawrót lub progresja choroby podczas leczenia lekami z grupy antyestrogenów. Wyniki w podgrupie inhibitorów aromatazy nie są rozstrzygające.
b OS (przeżycie całkowite) dla końcowej analizy przeżycia przy 75% dojrzałości wyników.
c Nominalna wartość p bez korekty dla testów wielokrotnych między wstępnymi analizami przeżycia całkowitego przy 50% dojrzałości wyników, a zaktualizowanymi analizami przeżycia przy 75% dojrzałości wyników.
d ORR oceniano u pacjentek, które w punkcie wyjściowym zakwalifikowano do grupy podlegającej ocenie odpowiedzi na leczenie (tzn. do grupy pacjentek, u których podczas ocen wyjściowych możliwa była ocena wielkości zmian nowotworowych: 240 pacjentek w grupie leczonej fulwestrantem w dawce 500 mg i 261 pacjentek w grupie leczonej fulwestrantem w dawce
250 mg).
e Pacjentki z najlepszą odpowiedzią obiektywną z odpowiedzi całkowitej, odpowiedzi częściowej lub stabilnej choroby 24 tygodni.
PFS: czas przeżycia wolny od progresji choroby ORR: odsetek odpowiedzi obiektywnych; OR: odpowiedź obiektywna; CBR odsetek korzyści klinicznych; CB: korzyść kliniczna; OS: całkowite przeżycie; K-M: Kaplan-Meier; CI: przedział ufności; AI: inhibitory aromatazy; AE: antyestrogeny.
Przeprowadzono wieloośrodkowe, randomizowane, prowadzone metodą podwójnie ślepej próby, podwójnie pozorowane, badanie fazy 3 porównujące fulwestrant w dawce 500 mg z anastrozolem
1 mg u kobiet po menopauzie z ER-dodatnim i/lub PgR-dodatnim miejscowo zaawansowanym lub przerzutowym rakiem piersi, które wcześniej nie otrzymywały żadnej terapii hormonalnej.
Łącznie 462 pacjentki były sekwencyjnie randomizowane w proporcji 1:1 do grupy otrzymującej fulwestrant w dawce 500 mg lub do grupy otrzymującej anastrozol w dawce 1 mg.
Randomizacja była stratyfikowana według stopnia zaawansowania choroby (miejscowo zaawansowana lub przerzutowa), wcześniejszej chemioterapii z powodu choroby zaawansowanej i obecności mierzalnych zmian.
Pierwszorzędowym punktem końcowym oceny skuteczności w tym badaniu było przeżycie wolne od progresji choroby (PFS) oceniane przez badacza według kryteriów RECIST 1.1 (ang. Response Evaluation Criteria in Solid Tumours; kryteria oceny odpowiedzi w guzach litych). Kluczowe drugorzędowe punkty końcowe oceny skuteczności obejmowały przeżycie całkowite (OS) i odsetek odpowiedzi obiektywnych (ORR).
Mediana wieku pacjentek włączonych do tego badania wyniosła 63 lata (zakres 36-90). U większości pacjentek (87,0%) w punkcie wyjściowym badania występowały przerzuty.
U pięćdziesięciu pięciu procent (55,0%) pacjentek w punkcie wyjściowym badania występowały przerzuty do narządów trzewnych. Łącznie 17,1% pacjentek otrzymało wcześniej chemioterapię z powodu choroby zaawansowanej; u 84,2% pacjentek występowała choroba mierzalna.
W większości predefiniowanych podgrup pacjentek otrzymane wyniki były spójne. W podgrupie pacjentek z chorobą ograniczoną do przerzutów innych niż przerzuty do narządów trzewnych (n=208), HR wyniósł 0,592 (95% CI: 0,419; 0,837) w grupie otrzymującej fulwestrant w porównaniu z grupą leczoną anastrozolem. W podgrupie pacjentek z przerzutami do narządów trzewnych (n=254) HR wyniósł 0,993 (95% CI: 0,740; 1,331) w grupie otrzymującej fulwestrant w porównaniu z grupą leczoną anastrozolem. Wyniki dotyczące skuteczności w badaniu FALCON zostały przedstawione
w Tabeli 4 i na Rycinie 1.
Tabela 4. Podsumowanie wyników dotyczących pierwszorzędowego punktu końcowego oceny skuteczności (PFS) i kluczowych drugorzędowych punktów końcowych oceny skuteczności (ocena badacza, populacja zgodna z zamiarem leczenia) – badanie FALCON
Fulwestrant 500 mg (N=230) | Anastrozol 1 mg (N=232) | |
Czas przeżycia wolny od progresji | ||
Liczba zdarzeń PFS (%) | 143 (62,2%) | 166 (71,6%) |
Współczynnik ryzyka (95% CI) i wartość p dla PFS | HR 0,797 (0,637 - 0,999) p = 0,0486 | |
Mediana PFS [miesiące (95% CI)] | 16,6 (13,8, 21,0) | 13,8 (12,0, 16,6) |
Liczba zdarzeń OS* | 67 (29,1%) | 75 (32,3%) |
Współczynnik ryzyka (95% CI) i wartość p dla OS | HR 0,875 (0,629 - 1,217) p = 0,4277 | |
ORR** | 89 (46,1%) | 88 (44,9%) |
Iloraz szans (95% CI) i wartość p dla ORR | OR 1,074 (0,716 - 1,614) p = 0,7290 | |
Mediana DoR (miesiące) | 20,0 | 13,2 |
CBR | 180 (78,3%) | 172 (74,1%) |
Iloraz szans (95% CI) i wartość p dla CBR | OR 1,253 (0,815 - 1,932) p = 0,3045 | |
*(31% dojrzałość danych) – nieostateczna analiza OS
**u pacjentek z mierzalną chorobą
Rycina 1. Wykres Kaplana-Meiera dla czasu przeżycia wolnego od progresji choroby (ocena badacza, populacja zgodna z zamiarem leczenia) – badanie FALCON
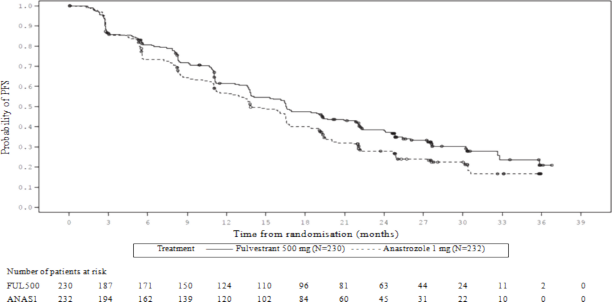
Przeprowadzono dwa badania kliniczne fazy 3, w których udział wzięło 851 kobiet po menopauzie z zaawansowanym rakiem piersi, u których nastąpił nawrót choroby w trakcie lub po zakończeniu hormonalnego leczenia uzupełniającego, lub doszło do progresji choroby po zastosowaniu leczenia hormonalnego choroby w stadium zaawansowanym. U siedemdziesięciu siedmiu procent pacjentek (77%) biorących udział w badaniach występował rak piersi z ekspresją receptora estrogenowego.
W badaniach tych porównywano bezpieczeństwo i skuteczność stosowania fulwestrantu, podawanego w dawce 250 mg raz na miesiąc, i anastrozolu (inhibitora aromatazy) podawanego raz na dobę
w dawce 1 mg. Stwierdzono, że fulwestrant podawany w dawce 250 mg raz na miesiąc jest co najmniej tak skuteczny jak anastrozol, pod względem czasu przeżycia wolnego od progresji choroby, obiektywnej odpowiedzi na leczenie i czasu do zgonu.
Nie stwierdzono istotnej statystycznie różnicy w żadnym z punktów końcowych badania w obu grupach leczenia. Pierwszorzędowym punktem końcowym badania był czas przeżycia wolny
od progresji choroby. Analiza łączna wyników uzyskanych w obu badaniach wykazała, że u 83% pacjentek otrzymujących fulwestrant obserwowano progresję w porównaniu z 85% pacjentek otrzymujących anastrozol. Analiza łączna wyników uzyskanych w obu badaniach wykazała, że współczynnik ryzyka dla porównania fulwestrantu w dawce 250 mg do anastrozolu pod względem czasu przeżycia wolnego od progresji choroby wynosi 0,95 (95% CI 0,82 do 1,10). Obiektywny odsetek odpowiedzi dla fulwestrantu w dawce 250 mg wynosił 19,2% w porównaniu z 16,5%
dla anastrozolu. Mediana czasu do wystąpienia zgonu wynosiła 27,4 miesiąca dla pacjentek leczonych fulwestrantem i 27,6 miesiąca dla pacjentek leczonych anastrozolem. Współczynnik ryzyka
dla porównania fulwestrantu w dawce 250 mg do anastrozolu pod względem czasu do wystąpienia zgonu wynosił 1,01 (95% CI 0,86 do 1,19).
Leczenie skojarzone z palbocyklibem
Przeprowadzono wieloośrodkowe, międzynarodowe, randomizowane, prowadzone metodą podwójnie ślepej próby w grupach równoległych badanie fazy 3 porównujące leczenie fulwestrantem w dawce 500 mg w skojarzeniu z palbocyklibem w dawce 125 mg z leczeniem fulwestrantem w dawce 500 mg w skojarzeniu z placebo u kobiet z miejscowo zaawansowanym rakiem piersi HR-dodatnim i HER2- ujemnym, niekwalifikującym się do leczenia chirurgicznego ani radioterapii z intencją wyleczenia, lub z przerzutowym rakiem piersi, niezależnie od statusu menopauzy, u których doszło do progresji choroby po wcześniejszej terapii hormonalnej w leczeniu (neo) adjuwantowym lub w chorobie rozsianej.
Łącznie 521 kobiet w okresie przed-/około- i pomenopauzalnym, u których doszło do progresji choroby w trakcie lub w ciągu 12 miesięcy od zakończenia uzupełniającej terapii hormonalnej, lub podczas albo w ciągu 1 miesiąca od wcześniejszej terapii hormonalnej z powodu choroby zaawansowanej, zostało zrandomizowanych w stosunku 2:1 do grupy otrzymującej fulwestrant
w skojarzeniu z palbocyklibem lub do grupy otrzymującej fulwestrant w skojarzeniu z placebo. Randomizację stratyfikowano według udokumentowanej wrażliwości na wcześniejszą terapię hormonalną, okresu menopauzy w chwili przystąpienia do badania (okres przed-/okołomenopauzalny w porównaniu z okresem pomenopauzalnym) i obecności przerzutów do narządów miąższowych.
Kobiety w okresie przed-/okołomenopauzalnym otrzymywały agonistę LHRH, goserelinę. Pacjentki z chorobą zaawansowaną/rozsianą, objawową, z zajęciem narządów miąższowych, u których istniało ryzyko wystąpienia w krótkim czasie powikłań zagrażających życiu (w tym pacjentki z masywnymi niekontrolowanymi wysiękami [opłucnowymi, osierdziowymi, otrzewnowymi], zapaleniem naczyń chłonnych płuc i zajęciem ponad 50% wątroby) nie spełniały kryteriów włączenia do tego badania.
Pacjentki kontynuowały przydzielone leczenie do chwili wystąpienia obiektywnej progresji choroby, nasilenia objawów, wystąpienia niemożliwych do zaakceptowania objawów toksyczności, zgonu lub wycofania zgody na udział w badaniu, w zależności od tego, które z tych zdarzeń wystąpiło jako pierwsze.
Zmiana grup leczenia nie była dozwolona.
Pacjentki z grupy otrzymującej fulwestrant w skojarzeniu z palbocyklibem i pacjentki z grupy otrzymującej fulwestrant w skojarzeniu z placebo były dobrze dobrane pod względem wyjściowych danych demograficznych i cech prognostycznych. Mediana wieku pacjentek włączonych do tego badania wyniosła 57 lat (zakres 29, 88). W każdej grupie badanej większość stanowiły kobiety rasy białej, z udokumentowaną wrażliwością na wcześniejszą terapię hormonalną i w okresie pomenopauzalnym.
Około 20% pacjentek stanowiły kobiety w okresie przed-/okołomenopauzalnym. Wszystkie pacjentki otrzymały wcześniej leczenie ogólnoukładowe i większość pacjentek z każdej grupy terapeutycznej była poddana wcześniej chemioterapii z powodu pierwotnego rozpoznania. U ponad połowy (62%) stan sprawności wg ECOG wyniósł 0, u 60% występowały przerzuty do narządów trzewnych, a 60% otrzymało wcześniej więcej niż 1 linię hormonoterapii z powodu pierwotnego rozpoznania.
Pierwszorzędowym punktem końcowym w badaniu było PFS oceniane przez badacza według kryteriów RECIST 1.1. Wspomagające analizy PFS opierały się na niezależnej, centralnej ocenie radiologicznej. Drugorzędowe punkty końcowe obejmowały OR, CBR, czas przeżycia całkowitego (OS), bezpieczeństwo stosowania i czas do pogorszenia (ang. time-to-deterioration, TTD) punktu końcowego dotyczącego bólu.
W badaniu osiągnięto pierwszorzędowy punkt końcowy, uzyskano wydłużenie PFS wg oceny badacza w analizie etapowej przeprowadzonej po wystąpieniu 82% planowanych zdarzeń PFS; wyniki przekroczyły wcześniej określoną granicę skuteczności Haybittle-Peto (α=0,00135), wykazując statystycznie znamienne wydłużenie PFS i klinicznie znaczący efekt leczenia. Bardziej dojrzałą aktualizację danych dotyczących skuteczności przedstawiono w Tabeli 5.
Po obserwacji o medianie czasu trwania wynoszącej 45 miesięcy przeprowadzono końcową analizę OS na podstawie 310 zdarzeń (60% zrandomizowanych pacjentek). Zaobserwowano różnicę w medianie OS wynoszącą 6,9 miesiąca między grupą otrzymującą palbocyklib w skojarzeniu z fulwestrantem a grupą otrzymującą placebo w skojarzeniu z fulwestrantem; ten wynik nie był statystycznie znaczący przy określonym a priori poziomie istotności wynoszącym 0,0235 (test 1- stronny). W grupie leczonej placebo w skojarzeniu z fulwestrantem 15,5% zrandomizowanych pacjentek otrzymało następnie palbocyklib lub inne inhibitory CDK w ramach kolejnych linii leczenia po progresji choroby.
Wyniki dotyczące danych o PFS według oceny badaczy i końcowych danych o OS w badaniu PALOMA3 przedstawiono w Tabeli 5. Odpowiednie wykresy Kaplana-Meiera pokazano na Rycinach 2 i 3.
Tabela 5. Wyniki dotyczące skuteczności – badanie PALOMA3 (ocena badacza, populacja zgodna z zamiarem leczenia)
Aktualizacja analizy (data odcięcia danych: 23 października 2015 r.) | ||
Fulwestrant w skojarzeniu z palbocyklibem (N=347) | Fulwestrant w skojarzeniu z placebo (N=174) | |
Czas przeżycia wolny od progresji | ||
Mediana [miesiące (95% CI)] | 11,2 (9,5, 12,9) | 4,6 (3,5, 5,6) |
Współczynnik ryzyka (95% CI) i wartość p | 0,497 (0,398, 0,620), p <0,000001 | |
Drugorzędowe punkty końcowe | ||
OR [% (95% CI)] | 26,2 (21,7, 31,2) | 13,8 (9,0, 19,8) |
OR (choroba mierzalna) [% (95% CI)] | 33,7 (28,1, 39,7) | 17,4 (11,5, 24,8) |
CBR [% (95% CI)] | 68,0 (62,8, 72,9) | 39,7 (32,3, 47,3) |
Przeżycie całkowite (OS) w analizie końcowej (data ucięcia danych: 13 kwietnia 2018 r.) | ||
Liczba zdarzeń (%) | 201 (57,9) | 109 (62,6) |
Mediana [miesiące (95% CI)] | 34,9 (28,8; 40,0) | 28,0 (23,6; 34,6) |
Współczynnik ryzyka (95% CI) i wartość p† | 0,814 (0,644; 1,029) p=0,0429†* | |
CBR=korzyść kliniczna; CI=przedział ufności; N=liczba pacjentek OR=odpowiedź obiektywna Wyniki dotyczące drugorzędowych punktów końcowych opierają się na potwierdzonych i niepotwierdzonych odpowiedziach według RECIST 1.1.
* Nieistotne statystycznie.
† 1-stronna wartość p w logarytmicznym teście rang ze stratyfikacją uwzględniającą obecność przerzutów do narządów trzewnych i wrażliwość na wcześniejszą terapię hormonalną według randomizacji.
Rycina 2. Wykres Kaplana-Meiera dla czasu przeżycia wolnego od progresji choroby (ocena badacza, populacja zgodna z zamiarem leczenia) – badanie PALOMA3 (data odcięcia danych: 23 października 2015 r.)
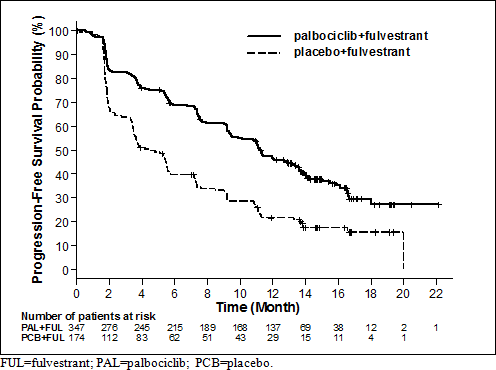
Redukcja ryzyka progresji choroby lub zgonu w grupie otrzymującej fulwestrant w skojarzeniu
z palbocyklibem obserwowano we wszystkich poszczególnych podgrupach pacjentek definiowanych w oparciu o czynniki stratyfikacji i charakterystykę wyjściową. Redukcję ryzyka wykazano u kobiet w okresie przed-/okołomenopauzalnym (HR=0,46 [95% CI: 0,28; 0,75]), u kobiet w okresie
pomenopauzalnym (HR=0,52 [95% CI: 0,40; 0,66]), u pacjentek z lokalizacją przerzutów w narządach miąższowych (HR=0,50 [95% CI: 0,38; 0,65]) i lokalizacją przerzutów poza narządami miąższowymi (HR=0,48 [95% CI: 0,33; 0,71]). Korzyści również obserwowano niezależnie od liczby linii wcześniejszych terapii z powodu choroby rozsianej, niezależnie od tego, czy było to 0 (HR=0,59 [95% CI: 0,37; 0,93]), 1 (HR=0,46 [95% CI: 0,32; 0,64]), 2 (HR=0,48 [95% CI: 0,30; 0,76]) lub ≥3 linie
leczenia (HR=0,59 [95% CI: 0,28; 1,22]).
Rycina 3. Wykres Kaplana-Meiera dla przeżycia całkowitego (populacja zgodna z intencją leczenia) – badanie PALOMA3 (data odcięcia danych: 13 kwietnia 2018 r.)
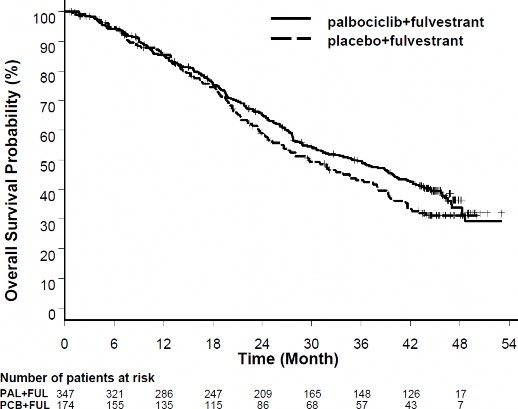
FUL=fulwestrant; PAL=palbocyklib; PCB=placebo
Dodatkowe miary skuteczności (OR i TTR) oceniane w podgrupach pacjentek z zajęciem narządów miąższowych lub bez zostały przedstawione w Tabeli 6.
Tabela 6. Wyniki dotyczące skuteczności u pacjentek z zajęciem narządów miąższowych lub bez, w badaniu PALOMA3 (populacja zgodna z zamiarem leczenia)
Przerzuty do narządów miąższowych | Brak przerzutów do narządów miąższowych | |||
Fulwestrant w skojarzeniu z palbocyklibem (N=206) | Fulwestrant w skojarzeniu z placebo (N=105) | Fulwestrant w skojarzeniu z palbocyklibem (N=141) | Fulwestrant w skojarzeniu z placebo (N=69) | |
OR [% (95% CI)] | 35,0 | 13,3 | 13,5 | 14,5 |
(28,5, 41,9) | (7,5, 21,4) | (8,3, 20,2) | (7,2, 25,0) | |
TTR*, Mediana | 3,8 | 5,4 | 3,7 | 3,6 |
[miesiące (zakres)] | (3,5, 16,7) | (3,5, 16,7) | (1,9, 13,7) | (3,4, 3,7) |
*Wyniki dotyczące odpowiedzi na leczenie na podstawie potwierdzonych i niepotwierdzonych odpowiedzi.
N=liczba pacjentek; CI=przedział ufności; OR= odpowiedź obiektywna; TTR=czas do pierwszej odpowiedzi ze strony guza.
Objawy zgłaszane przez pacjentki były oceniane za pomocą kwestionariusza jakości życia (QLQ)-C30 Europejskiej Organizacji na rzecz Badań i Leczenia Raka (EORTC) i jego modułu dotyczącego raka piersi (EORTC QLQ-BR23). Łącznie 335 pacjentek z grupy otrzymującej fulwestrant w skojarzeniu
z palbocyklibem i 166 pacjentek w grupie otrzymującej fulwestrant w skojarzeniu z placebo wypełniło
kwestionariusz podczas ocen wyjściowych i przynajmniej 1 raz na wizycie po przeprowadzeniu ocen wyjściowych.
Czas do pogorszenia objawów został wcześniej określony jako czas między wynikiem wyjściowym a pierwszym wystąpieniem zwiększenia o ≥10 punktów w wynikach dotyczących objawów bólowych względem oceny wyjściowej. Dołączenie palbocyklibu do leczenia fulwestrantem miało korzystny wpływ na objawy przez istotne wydłużenie czasu do nasilenia objawów bólowych w porównaniu
z leczeniem fulwestrantem w skojarzeniu z placebo (mediana 8,0 miesięcy w porównaniu z 2,8 miesiąca; HR=0,64 [95% CI: 0,49, 0,85]; p<0,001).
Wpływ na endometrium w okresie pomenopauzalnym
Na podstawie wyników badań przedklinicznych nie można sądzić, że fulwestrant wpływa pobudzająco na błonę śluzową macicy po menopauzie (patrz punkt 5.3). W 2-tygodniowym badaniu klinicznym
z udziałem zdrowych ochotniczek po menopauzie leczonych etynyloestradiolem podawanym w dawce 20 mikrogramów na dobę stwierdzono, że w porównaniu z placebo leczenie wstępne fulwestrantem
w dawce 250 mg powoduje istotne osłabienie działania pobudzającego na błonę śluzową macicy. Działanie pobudzające oceniano, mierząc grubość endometrium w badaniu ultrasonograficznym.
Leczenie neoadjuwantowe u pacjentek z rakiem piersi trwające do 16 tygodni, zarówno fulwestrantem w dawce 500, mg jak i fulwestrantem w dawce 250 mg nie spowodowało znaczącej klinicznie zmiany grubości śluzówki macicy, co wskazuje na brak działania agonistycznego. Nie ma dowodów
na niekorzystny wpływ na śluzówkę macicy u badanych pacjentek z rakiem piersi. Brak jest danych dotyczących wpływu na budowę błony śluzowej macicy.
W dwóch krótkotrwałych badaniach klinicznych (trwających 1 i 12 tygodni) przeprowadzonych
u pacjentek w okresie przed menopauzą z łagodnymi schorzeniami ginekologicznymi nie stwierdzono znaczącej różnicy w grubości endometrium (mierzonej ultrasonograficznie) między grupą otrzymującą fulwestrant, a grupą przyjmującą placebo.
Wpływ na kości
Brak jest danych dotyczących odległych skutków działania fulwestrantu na kości. Leczenie neoadjuwantowe u pacjentek z rakiem piersi trwające do 16 tygodni, zarówno fulwestrantem w dawce 500 mg, jak i fulwestrantem w dawce 250 mg nie spowodowało znaczącej klinicznie zmiany
w stężeniach markerów metabolizmu kości w surowicy.
Dzieci i młodzież
Lek Fulvestrant Stada nie jest wskazany do stosowania u dzieci. Europejska Agencja Leków uchyliła obowiązek dołączania wyników badań fulwestrantu we wszystkich podgrupach populacji dzieci
i młodzieży we wskazaniu raka piersi (stosowanie u dzieci i młodzieży, patrz punkt 4.2).
W otwartym badaniu klinicznym fazy 2 oceniano bezpieczeństwo i skuteczność stosowania oraz parametry farmakokinetyczne fulwestrantu u 30 dziewcząt w wieku od 1 do 8 lat z przedwczesnym dojrzewaniem płciowym (ang. Progressive Precocious Puberty) związanym z zespołem McCune Albrighta (MAS). Dzieci otrzymywały domięśniowo fulwestrant w dawce 4 mg/kg masy ciała co miesiąc. To 12-miesięczne badanie pozwoliło na ocenę wielu punktów końcowych istotnych
dla leczenia MAS i wykazało zmniejszenie częstości krwawień z dróg rodnych oraz zmniejszenie wskaźnika zaawansowania wieku kostnego.
W stanie stacjonarnym wartości minimalnych stężeń fulwestrantu ocenione w tym badaniu u dzieci odpowiadały wartościom stwierdzanym u pacjentów dorosłych (patrz punkt 5.2). To małe badanie nie ujawniło żadnych nowych doniesień dotyczących bezpieczeństwa stosowania, ale dane z 5-letniej obserwacji nie są jeszcze dostępne.
Wchłanianie
Po podaniu fulwestrantu w postaci roztworu do wstrzykiwań domięśniowych o długotrwałym działaniu fulwestrant jest powoli wchłaniany i osiąga maksymalne stężenie w osoczu (Cmax) po mniej więcej 5 dniach. Podawanie fulwestrantu w dawce 500 mg powoduje osiąganie stałych lub
w przybliżeniu stałych wartości ekspozycji przez pierwszy miesiąc stosowania (średnie wartości stężeń odpowiednio: AUC 475 [33,4%] ng•dni/ml, Cmax 25,1 [35,3%] ng/ml, Cmin 16,3 [25,9%] ng/ml). W stanie stacjonarnym wartości stężeń fulwestrantu w osoczu mieszczą się w stosunkowo wąskim zakresie, dla którego stężenie maksymalne jest do 3 razy większe niż stężenie minimalne. Po podaniu domięśniowym w zakresie dawek od 50 do 500 mg, ekspozycja jest w przybliżeniu proporcjonalnie zależna od dawki.
Dystrybucja
Fulwestrant podlega rozległej i szybkiej dystrybucji w tkankach. Duża pozorna objętość dystrybucji w stanie stacjonarnym (Vdss) (wynosząca około 3 do 5 l/kg) sugeruje, że lek znajduje się głównie
w przestrzeni pozanaczyniowej. Fulwestrant w dużym stopniu (99%) wiąże się z białkami osocza. Fulwestrant wiąże się przede wszystkim z frakcjami lipoprotein o bardzo małej (VLDL), małej (LDL) i dużej gęstości (HDL). Nie badano interakcji dotyczących kompetycyjnego mechanizmu wiązania
z białkami. Nie określono roli wiązania z globuliną wiążącą hormony płciowe (SHBG).
Metabolizm
Metabolizm fulwestrantu nie został w pełni poznany i zachodzi na drodze wielu możliwych przemian biologicznych, w sposób podobny jak w przypadku endogennych steroidów. Wykryte metabolity (włączając 17-keton, sulfoniany, 3-siarczan, 3- i 17-glukuroniany) mają mniejszą niż fulwestrant lub porównywalną z nim aktywność antyestrogenową. W badaniach z wykorzystaniem ludzkich komórek wątroby i rekombinowanych ludzkich enzymów wątrobowych stwierdzono, że CYP3A4 jest jedynym izoenzymem cytochromu P450 biorącym udział w procesie oksydacji fulwestrantu, natomiast
w warunkach in vivo główną rolę wydają się pełnić enzymy nienależące do grupy cytochromu P450. Na podstawie badań in vitro można sądzić, że fulwestrant nie wpływa hamująco na izoenzymy układu cytochromu CYP450.
Eliminacja
Fulwestrant jest wydalany głównie w postaci zmetabolizowanej. Fulwestrant jest wydalany przede wszystkim z kałem, mniej niż 1% jest wydalany w moczu. Fulwestrant ma duży klirens
11±1,7 ml/min/kg, co może świadczyć o dużym udziale wątroby w wydalaniu leku. Końcowy okres półtrwania (t0,5) po podaniu domięśniowym zależy przede wszystkim od szybkości wchłaniania
i oszacowano, iż wynosi 50 dni.
Szczególne grupy pacjentów
Z analizy farmakokinetyki populacyjnej przeprowadzonej na danych z badań fazy 3 wynika, że nie ma różnic w profilu farmakokinetycznym fulwestrantu stosowanego u pacjentek z różnych grup wiekowych (pacjentki w wieku 33 do 89 lat), o różnej masie ciała (40-127 kg) lub u pacjentek różnych ras.
Zaburzenia czynności nerek
Łagodne i umiarkowane zaburzenia czynności nerek nie wpływają w klinicznie istotny sposób na farmakokinetykę fulwestrantu.
Zaburzenia czynności wątroby
Farmakokinetykę fulwestrantu oceniono w badaniu klinicznym u kobiet z łagodnymi
do umiarkowanych zaburzeniami czynności wątroby (grupa A i B według skali Childa-Pugha) po podaniu pojedynczej dawki produktu. W badaniu stosowano dużą dawkę produktu o krótkim działaniu podawaną w postaci wstrzyknięcia domięśniowego. W grupie kobiet z zaburzeniami czynności wątroby obserwowano mniej więcej 2,5-krotne zwiększenie AUC w porównaniu
do wartości uzyskanych w grupie zdrowych uczestników badania. Oczekuje się, że takie zwiększenie ekspozycji u pacjentek otrzymujących fulwestrant będzie dobrze tolerowane. Nie badano kobiet
z ciężkimi zaburzeniami wątroby (grupa C według skali Childa-Pugha).
Dzieci i młodzież
Farmakokinetykę fulwestrantu oceniono w badaniu klinicznym przeprowadzonym wśród 30 dziewcząt z przedwczesnym dojrzewaniem płciowym związanym z zespołem McCune Albrighta (patrz punkt 5.1). Pacjentki w wieku od 1 do 8 lat otrzymywały fulwestrant domięśniowo w dawce 4 mg/kg masy ciała co miesiąc. Średnia geometryczna (standardowe odchylenie) wartości minimalnych stężeń fulwestrantu w osoczu w stanie stacjonarnym (Cmin, ss) i powierzchnia pola pod krzywą w stanie stacjonarnym (AUCss) wynosiły odpowiednio: 4,2 (0,9) ng/ml i 3680 (1020) ng*hr/ml. Pomimo iż zebrane dane są ograniczone, wartości minimalnych stężeń fulwestrantu w stanie stacjonarnym
w osoczu u dzieci wydają się odpowiadać wartościom stwierdzanym u pacjentów dorosłych.
Fulwestrant wykazuje niewielką toksyczność ostrą.
Fulwestrant był dobrze tolerowany przez wszystkie gatunki zwierząt, którym w badaniach podawano dawki wielokrotne. Reakcje obserwowane w miejscu wstrzyknięcia, tj. zapalenie mięśni i ziarniniaki, wynikały z działania substancji pomocniczych leku. Jednakże w badaniach przeprowadzonych
na królikach zaobserwowano, że zapalenie mięśni było bardziej nasilone w miejscu podania fulwestrantu niż w miejscu podania próbki kontrolnej, która zawierała sól fizjologiczną. Badania przeprowadzone na szczurach i psach wykazały, że po podaniu wielokrotnych dawek fulwestrantu
w postaci wstrzyknięcia domięśniowego występują objawy związane z działaniem antyestrogenowym leku. Przede wszystkim obserwowano wpływ na żeński układ rozrodczy oraz na te narządy, które są wrażliwe na działanie hormonów u obu płci. U niektórych psów, które przyjmowały lek przewlekle (12 miesięcy), obserwowano zapalenie tętnic obejmujące różne tkanki.
W badaniach na psach, gdy fulwestrant był podawany doustnie i dożylnie, stwierdzono, że wpływa on na układ sercowo-naczyniowy (niewielkie uniesienie odcinka ST w badaniu EKG [podanie doustne], zahamowanie zatokowe u jednego psa [podanie dożylne]). Reakcje te wystąpiły, gdy stężenia leku stwierdzane u zwierząt były wielokrotnie większe niż stwierdzone u ludzi (Cmax >15 razy). Należy zatem uznać, że ma to niewielkie znaczenie dla bezpieczeństwa ludzi przy zastosowaniu dawek terapeutycznych.
Fulwestrant nie wykazywał potencjalnego działania genotoksycznego.
Wpływ fulwestrantu na reprodukcję i działanie uszkadzające na zarodek/płód, gdy był on podawany w dawkach zbliżonych do dawek terapeutycznych, wynika z jego działania antyestrogenowego.
Fulwestrant podawany szczurom powodował odwracalne zmniejszenie płodności samic i zmniejszone przeżycie zarodków, a także dystocję i zwiększoną częstość występowania zaburzeń u płodu, w tym patologiczne zgięcie śródstopia. U samic królików, którym podawano fulwestrant, występowały poronienia. Obserwowano zwiększoną masę łożyska i obumieranie zarodków po zagnieżdżeniu.
Stwierdzono zwiększoną częstość występowania nieprawidłowości u płodów królików (w tym wsteczne przesunięcie obręczy miednicy i 27. kręgu przedkrzyżowego).
W dwuletnim badaniu działania rakotwórczego u szczurów (domięśniowe podawanie fulwestrantu) wykazano zwiększoną częstość występowania łagodnych ziarniszczaków w jajniku u samic szczurów po podaniu dużych dawek, 10 mg/szczur/15 dni oraz zwiększoną częstość występowania nowotworów z komórek Leydiga w jądrach u samców. Podczas dwuletniego badania rakotwórczości u myszy
po podaniu dawek 150 mg/kg/dobę i 500 mg/kg/dobę (doustnie, codziennie) stwierdzono zwiększoną częstość występowania nowotworów sznura płciowego i zrębu jajnika (zarówno łagodnych, jak
i złośliwych).
Wyniki ekspozycji układowej (AUC), obserwowane po podaniu największej dawki
bez obserwowanego działania (NOEL), były u szczurów w przybliżeniu 1,5-krotnością oczekiwanej ekspozycji u kobiet i 0,8-krotnością ekspozycji u mężczyzn, a u myszy w przybliżeniu 0,8-krotnością oczekiwanej ekspozycji zarówno u kobiet, jak i u mężczyzn. Indukcja takich nowotworów jest
związana z farmakologicznymi zaburzeniami hormonalnego sprzężenia zwrotnego dla stężenia gonadotropin, spowodowanymi przez antyestrogeny u zwierząt czynnych rozrodczo. W związku z tym wyniki tych badań nie są uznane za odpowiednie do zalecenia stosowania fulwestrantu w leczeniu zaawansowanego raka piersi u kobiet po menopauzie.
Ocena ryzyka dla środowiska
Badania oceny ryzyka dla środowiska wykazały, że fulwestrant może potencjalnie powodować działania niepożądane w środowisku wodnym (patrz punkt 6.6).
Etanol 96% Alkohol benzylowy Benzylu benzoesan
Olej rycynowy oczyszczony
Nie mieszać produktu leczniczego z innymi produktami leczniczymi, ponieważ nie wykonywano badań dotyczących zgodności.
4 lata
Przechowywać i przewozić w stanie schłodzonym (2°C - 8°C).
Przechowywać ampułko-strzykawkę w oryginalnym opakowaniu w celu ochrony przed światłem.
Należy ograniczyć przechowywanie produktu w temperaturze innej niż zakres 2°C - 8°C. Należy unikać przechowywania w temperaturze wyższej niż 30°C i nie przekraczać okresu 28 dni ze średnią temperaturą przechowywania poniżej 25°C (ale powyżej zakresu 2°C - 8°C). Jeśli zakres temperatur zostanie przekroczony, należy natychmiast zastosować zalecane warunki przechowywania (przechowywać i transportować w lodówce 2°C - 8°C). Przekroczenie właściwej temperatury przechowywania może mieć skumulowany wpływ na jakość produktu, a 28-dniowy okres nie może być przekroczony w ciągu 48 miesięcy ważności produktu Fulvestrant Stada (patrz punkt 6.3).
Ekspozycja na temperaturę poniżej 2°C nie powoduje uszkodzenia produktu, pod warunkiem, że nie jest on przechowywany w temperaturze poniżej -20°C.
Zestaw zawierający ampułko-strzykawkę składa się z: ampułko-strzykawki z bezbarwnego szkła typu I, z plastikową nasadką końcówki, z tłokiem z polipropylenu zakończonym bromobutylowym korkiem i ogranicznikiem, zawierającej 5 ml roztworu do wstrzykiwań.
Fulvestrant Stada dostępny jest w trzech wielkościach opakowań:
Nie wszystkie wielkości opakowań muszą znajdować się w obrocie.
Sposób postępowania i utylizacji musi zbyć spójny ze sposobem postępowania i utylizacji innych preparatów przeciwnowotworowych i zgodny z lokalnymi wymogami. Kobiety wchodzące w skład personelu będące w ciąży nie powinny dotykać ani podawać produktu Fulvestrant Stada 250 mg/5 ml, roztwór do wstrzykiwań w ampułko-strzykawce.
Instrukcja podawania
Należy podawać wstrzyknięcie zgodnie z lokalnymi wytycznymi dotyczącymi wykonywania wstrzyknięć domięśniowych o dużej objętości.
UWAGA: Należy zachować ostrożność, jeśli produkt Fulvestrant Stada jest podawany w górnoboczną okolicę pośladka ze względu na bliskość nerwu kulszowego (patrz punkt 4.4).
Ostrzeżenia: Nie należy umieszczać w autoklawie igły z systemem osłaniającym (BD SafetyGlide Shielding Hypodermic Needle) przed jej zastosowaniem.
Podczas stosowania leku i usuwania pozostałości należy unikać kontaktu rąk z igłą. Dotyczy obu strzykawek:
UWAGA: Aktywuj system w bezpiecznej odległości od siebie i innych osób. Po usłyszeniu kliknięcia potwierdź wizualnie, czy końcówka igły jest całkowicie ukryta.
Rysunek 4
Usuwanie leku:
Ampułko-strzykawki są przeznaczone wyłącznie do jednorazowego użycia.
Ten produkt leczniczy może stanowić zagrożenie dla środowiska wodnego. Wszelkie niewykorzystane resztki produktu leczniczego lub jego odpady należy usunąć zgodnie z lokalnymi przepisami
(patrz punkt 5.3).
STADA Arzneimittel AG Stadastrasse 2-18
61118 Bad Vilbel, Niemcy
25713
Data wydania pierwszego pozwolenia na dopuszczenie do obrotu: 21.01.2020
07/2022











